
- •Методические рекомендации к лабораторно-практическим занятиям по общей химии
- •Методические рекомендации к лабораторно-практическим занятиям по общей химии
- •Правила техники безопасности при работе студентов в лабораторных практикумах сгму
- •Контрольные вопросы и задачи
- •Лабораторная работа
- •Контрольные вопросы и задачи
- •Контрольные вопросы и задачи
- •Контрольные вопросы и задачи
- •Контрольные вопросы и задачи
- •Контрольные вопросы и задачи
- •Контрольные вопросы и задачи
- •Контрольные вопросы и задачи
- •Контрольные вопросы и задачи
- •Лабораторная работа
- •Контрольные вопросы и задачи
- •Контрольные вопросы и задачи
- •Лабораторная работа
- •Указания для выполнения и оформления работы (иономер эв- 74)
- •III. Установка температуры раствора
- •V. Окончание работы.
- •Контрольные вопросы и задачи
- •1. Классификация методов количественного анализа
- •2. Теоретические основы титриметрического анализа
- •3. Сущность и основные понятия титриметрического анализа
- •4. Классификация методов титриметрического анализа
- •5. Приготовление рабочих растворов
- •Контрольные вопросы и задачи
- •Контрольные вопросы и задачи
- •Контрольные вопросы и задачи
- •Контрольные вопросы и задачи
- •Контрольные вопросы и задачи
- •Контрольные вопросы и задачи
- •Контрольные вопросы и задачи
- •Лабораторная работа
- •Контрольные вопросы и задачи
- •Список рекомендованной литературы
- •Айвазова Елена Анатольевна
Контрольные вопросы и задачи
Как изменяется степень заполнения адсорбента адсорбтивом с повышением температуры при химической адсорбции?
Приведите эмпирические уравнения адсорбции Фрейндлиха.
В чем сущность ионообменной адсорбции? Какие вещества называются катионитами и анионитами.
Какие вещества называются поверхностно-активными и инактивными?
Почему гидрофобные вещества лучше адсорбируют поверхностно-активные вещества из водных растворов, а гидрофильные — из углеводородных. В чем заключаются особенности адсорбции твердыми адсорбентами различных веществ из растворов?
Во сколько раз поверхностная активность уксусной кислоты больше или меньше поверхностной активности масляной кислоты при условии равенства концентраций из разбавленных водных растворов? (Правило Дюкло-Траубе).
В раствор объемом 60 мл некоторого вещества с концентрацией 0.440 моль/л поместили твёрдый адсорбент массой 3 г. После достижения адсорбционного равновесия концентрация вещества снизилась до 0.350 моль/л. Вычислите величину адсорбции (a =
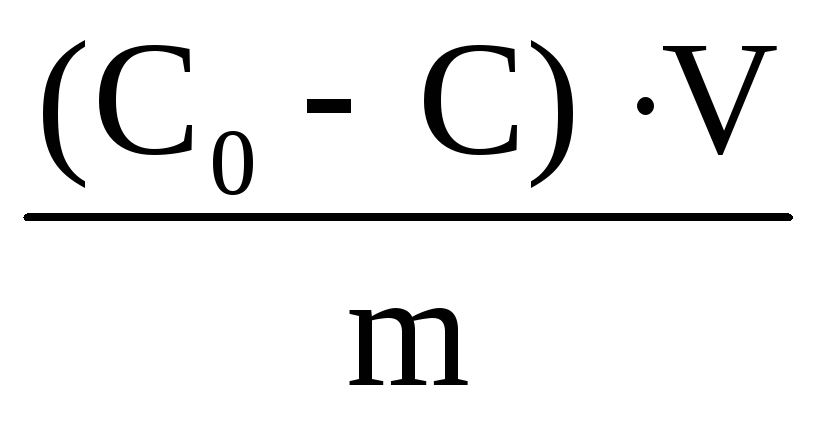 ).
).
Занятие 20. коллоидные растворы и их свойства. получение и очистка золей
Цель занятия:
Научиться получать коллоидные растворы, эмульсии; ознакомиться с методом диализа; научиться определять заряд коллоидной частицы методом электрофореза.
Содержание занятия:
Обсуждение теоретических вопросов и решение задач.
Выполнение лабораторных работ.
Вопросы, предлагаемые для обсуждения на занятии:
Биологическое значение дисперсных систем.
Классификация дисперсных систем по размеру частиц, агрегатному состоянию фаз. Понятие о лиофильных и лиофобных системах.
Свойства дисперсных систем.
Условия, методы получения и очистки коллоидных растворов.
Строение мицеллы. Понятие о межфазном (электротермодинамическом) и электрокинетическом потенциалах.
Электроосмос. Электрофорез.
Способы определения заряда коллоидных частиц.
Лабораторная работа 1. Получение золя берлинской лазури методом диспергирования (пептизации).
В пробирку к 5 мл 2% раствора FeCl3 приливают 1 мл насыщенного раствора К4[Fe(CN)6]. Осадок фильтруют через бумажный фильтр. Через некоторое время воронку с фильтром и осадком переносят в чистую пробирку и к осадку на фильтре добавляют раствор щавелевой кислоты (С = 0.05 моль/л).
Наблюдают изменение цвета фильтрата от жёлто-зелёного до синего.
При оформлении работы составьте уравнение реакции получения берлинской лазури, уравнение диссоциации пептизатора-щавелевой кислоты, напишите формулу мицеллы золя берлинской лазури, указажите его окраску.
Лабораторная работа 2. Получение золя гексацианоферрата(II) меди методом конденсации (реакция двойного обмена).
В колбу отмеряют цилиндром 20 мл 0,1% раствора K4[Fe(CN)6] и добавляют из бюретки 1 мл 1% раствора CuSO4. Получают золь, окрашенный в коричнево-красный цвет.
При оформлении работы составить уравнение реакции получения гексацианоферрата(II) меди, указать окраску золя и составить формулу мицеллы при избытке CuSO4 и при избытке K4[Fe(CN)6].
Лабораторная работа 3. Получение золя гидроксида железа (III) методом конденсации (реакция гидролиза).
В колбу с надписью «Fe(OH)3» цилиндром отмеряют 50 мл дистиллированной воды, нагревают ее до кипения и в кипящую воду быстро, но по частям, приливают 10 мл 2% раствора FeCl3. Золь приобретает красно-бурый цвет. При оформлении работы составить уравнения реакций гидролиза FeCl3,формулу мицеллы и указать окраску золя.
Лабораторная работа 4. Очистка коллоидных растворов при помощи диализа.
Диализу подвергают золь гидроксида железа (III), полученный в предыдущей работе. Работу ставят, руководствуясь приведенной ниже схемой. Через 10 мин часть воды, омывающей пергамент, сливают через резиновую трубочку в чистую пробирку. По окраске этой воды делают вывод, проходят ли коллоидные частицы через мембрану, а затем в этой же пробе проверяют наличие Clˉ-анионов, перешедших в воду из золя (реакция с AgNO3).
При оформлении работы привести подробный рисунок диализатора, указать окраску воды, результат пробы на Clˉ-ион и объяснить их.
Лабораторная работа 5. Получение золя канифоли методом конденсации (метод замены растворителя).
Раствор канифоли и пипетки для него стоят на отдельном столе. В колбу отмеряют цилиндром 20 мл дистиллированной воды, нагревают ее до появления пара, приливают 1 мл 1%-го спиртового раствора канифоли и наблюдают образование опалесцирующего коллоидного раствора.
Лабораторная работа 6. Получение разбавленной эмульсии.
В градуированную пробирку (пипеткой не пользоваться!) наливают 6 мл дистиллированной воды и 2 мл 1%-го спиртового раствора касторового масла, встряхивают и наблюдают образование эмульсии. При оформлении работы привести методику получения эмульсии, указать тип эмульсии (масло/вода или вода/масло), дисперсную фазу и дисперсную среду.
Лабораторная работа 7. Определение знака заряда коллоидных частиц методом электрофореза.
U-образную трубку при помощи пипетки заполняют на 3/4 коллоидным раствором берлинской лазури. В каждое отверстие трубки добавляют по две капли глицерина и раствор перемешивают легким покачиванием. В оба колена на раствор из капельной пипетки, прижав ее к стеклу, наливают раствор KCl высотой 0.7–1 см. Затем в отверстия трубок осторожно опускают электроды так, чтобы они соприкасались только с электролитом. Электроды соединены с источником постоянного тока, цепь замыкают при помощи переключателя. Через 7–10 мин, отключив прибор, отмечают результат работы — усиление (сгущение) окраски у одного из электродов. Зная заряд электрода, делают вывод о знаке заряда коллоидных частиц. При оформлении работы приведите подробный рисунок прибора, время электрофореза, результат опыта и вывод о знаке заряда коллоидных частиц.
