
- •Домашнее задание №1
- •Тема 1.1: “Пересчёт состава и методика расчёта критических (псевдокритических) параметров газовых углеводородных смесей”. Состав природных газов
- •Задача №1
- •Задача №1.2
- •Методика расчёта критических (псевдокритических) параметров углеводородных смесей
- •Задача №2
- •Контрольные вопросы
Домашнее задание №1
Тема 1.1: “Пересчёт состава и методика расчёта критических (псевдокритических) параметров газовых углеводородных смесей”. Состав природных газов
Углеводородные природные газы имеют в своем составе следующие компоненты: углеводородные, инертные, кислые и различные примеси, (включая пары воды, ртути и минеральные соли).
Углеводородные компоненты подразделяются на алканы или углеводороды метанового ряда с общей формулой СnН2n+2, циклоалканы или нафтеновые углеводороды СnН2n, арены или ароматические углеводороды СnН2n-6. Инертные компоненты, входящие в состав природных газов, это азот, гелий и другие редкоземельные газы.
Диоксид углерода и сероводород – кислые компоненты в составе природного газа, на большинстве месторождений природного газа сероводород отсутствует.
В зависимости от содержания углеводородных компонентов природные газы подразделяются на:
1. Газы, добываемые из чисто газовых месторождений. Содержание метана в газе таких месторождений достигает 9899% по объему (см. таблицу 1.1).
2. Газы, добываемые из газоконденсатных месторождений. Среднее содержание 7590% по объему. Из таблицы видно, что Астраханское месторождений содержит метан 47,48%, но в пересчете только на углеводородную часть содержание метана составит около 8085%.
3. Газы, добываемые вместе с нефтью, иногда называемые попутными газами. Они содержат метан, как видно из таблицы 1.1, в среднем 3550% по объему.
Таблица 1.1
|
Месторождение |
Состав газа, % объем |
Относительная плотность | ||||||||
|
СН4 |
С2Н6 |
С3Н8 |
С4Н10 |
С5Н12+ |
СО2 |
Н2S |
N2+R |
| ||
|
Газовые месторождения | ||||||||||
|
Северо-Ставропольское |
98,90 |
0,29 |
0,16 |
0,05 |
|
0,10 |
|
0,40 |
0,56 | |
|
Медвежье |
98,78 |
0,10 |
0,02 |
|
|
0,10 |
|
1,00 |
0,56 | |
|
Уренгойское |
99,05 |
0,06 |
0,01 |
|
|
0,08 |
|
0,80 |
0,56 | |
|
Ямбургское |
98,60 |
0,06 |
0,01 |
|
|
0,19 |
|
1,14 |
0,56 | |
|
Заполярное |
98,78 |
0,07 |
0,01 |
0,01 |
0,01 |
0,13 |
|
1,00 |
0,561 | |
|
Газоконденсатные месторождения | ||||||||||
|
Оренбургское |
84,00 |
5,00 |
1,60 |
0,70 |
1,80 |
0,90 |
2,10 |
3,90 |
0,692 | |
|
Вуктыльское |
74,80 |
8,70 |
3,90 |
1,80 |
6,40 |
0,10 |
|
4,30 |
0,728 | |
|
Уренгойское БУ10 |
86,99 |
5,01 |
2,48 |
1,03 |
3,75 |
0,35 |
|
0,38 |
0,704 | |
|
Астраханское |
47,48 |
1,92 |
0,93 |
0,66 |
3,08 |
21,55 |
22,50 |
1,98 |
1,063 | |
|
Газы, входящие в состав пластовой нефти | ||||||||||
|
Ромашкинское |
46,5 |
18,1 |
16,7 |
7,6 |
4,0 |
0,6 |
|
6,5 |
1,033 | |
|
Туймазинское D1+D2 |
40,4 |
19,2 |
18,5 |
6,6 |
3,0 |
|
|
12,3 |
1,125 | |
|
Самотлорское, Б-10 |
68,6 |
5,5 |
10,8 |
8,2 |
3,7 |
0,4 |
|
2,8 |
1,083 | |
|
Усть-Балыкское,Б-10 |
77,9 |
3,0 |
6,8 |
5,4 |
3,6 |
0,5 |
|
2,8 |
0,960 | |
Состав газовых углеводородных смесей выражается в массовых, молярных и объёмных единицах. Последний компонент С5Н12+В или С6Н14+В включает все высококипящие углеводороды, которые имеются в газе в незначительном количестве. Все элементы характеризуются атомной массой. За единицу атомной массы принята специальная единица, равная 1/12 массе атома углерода (углеродная единица). Масса атома, выраженная в углеродных единицах, называется относительной атомной массой. По аналогии с относительной атомной массой для элементов и веществ используют понятие относительной молекулярной массы, которая равна массе молекулы вещества, выраженная в углеродных единицах. Для перехода к единицам измерения массы в граммах и килограммах используют понятия моль и киломоль. Моль (г/моль) или киломоль (кг/кмоль) вещества – это количества вещества в граммах или килограммах, численно равное относительной молекулярной массе этого вещества. Эта масса называется молярной или молекулярной массой газа. Объёмные и молярные единицы для газа численно равны, так как 1 кмоль газа занимает объём, равный 22,41 м3 при нормальных условиях, т.е. при температуре 273 К и давлении 0,1013 МПа или 24,04 м3 при стандартных условиях, т.е. при температуре 293 К и давлении 0,1013 МПа. Это положение основано на законе Авогадро, согласно которому в равных объемах различных газов при одинаковых температурах и давлениях содержится одинаковое число молекул (при Р=0,1013 МПа и Т=273,16 0К – число Авогадро, равное 6,02∙1023 1/моль).
Для природного газа, являющегося смесью углеводородных и неуглеводородных компонентов, вводится понятие кажущаяся молярная масса Мк, значение которой определяется по формуле:
 ,
кг/кмоль (1.1)
,
кг/кмоль (1.1)
где Мi – молярная масса i-го компонента, кг/кмоль; xi молярная масса i-го компонента в смеси; к – число компонентов в смеси.
Если xi дано в мольных процентах, формула имеет вид:
 (1.2)
(1.2)
Иногда используют единицы измерения г/моль. Часто слово “кажущаяся” опускается и для природного газа это значение называют молярная (а иногда молекулярная) масса газа.
Введём следующие обозначения:
 –молярный процент
или мольная доля i-го
компонента газа;
–молярный процент
или мольная доля i-го
компонента газа;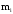 –массовый процент
или массовая доля i-го
компонента газа;
–массовый процент
или массовая доля i-го
компонента газа;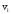 –объёмный процент
или объёмная доля i-го
компонента газа;
–объёмный процент
или объёмная доля i-го
компонента газа; –плотность i-го
компонента газа, кг/м3;
–плотность i-го
компонента газа, кг/м3; –относительная
плотность i-го
компонента газа;
–относительная
плотность i-го
компонента газа; –плотность смеси
газов;
–плотность смеси
газов; –относительная
плотность смеси газов;
–относительная
плотность смеси газов;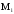 –молекулярная
масса i-го
компонента газа,
–молекулярная
масса i-го
компонента газа,
 ;
;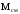 –средняя
(кажущаяся) молекулярная масса смеси
газов,
–средняя
(кажущаяся) молекулярная масса смеси
газов,
 .
.
