
Лабораторный практикум по молекулярной физике
.pdfравенство, будем интегрировать уравнение (1) методом разделения переменных. Для этого запишем его в виде:
|
dT |
|
= − |
q1 |
|
dτ . |
(2) |
|
|
|
c01m0 + cT mT |
||||
|
T − Tср |
|
|
||||
Введем обозначение: |
|
|
|
|
|
|
|
k 1 = |
|
|
q1 |
. |
|
(3) |
|
c 01 m |
0 + c T m T |
|
|||||
|
|
|
|
|
|||
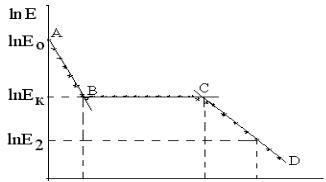
Величина k1 имеет в СИ следующую единицу измерения: [k1] = [q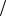 cm] = 1 с-1.
cm] = 1 с-1.
k1 характеризует скорость изменения температуры охлаждаемой системы и называется темпом охлаждения.
Для решения дифференциального уравнения (2) необходимо задать начальное условие: Т = Т0 при τ = 0.
Проинтегрировав правую и левую части уравнения (2), получим:
ln(T – T ср)= - k1τ + ln C, |
(4) |
где С – константа интегрирования. Найдем ее из начально-
го условия: C = T0 – T ср при τ = 0.
Тогда выражение (4) можно записать следующим образом:
ln(T - Tср) = ln(T0 – T ср) - k1τ, |
(5) |
или: |
|
T -Tср = (T0 - Tср )× e −k1τ . |
(6) |
Такой темп охлаждения сохранится до тех пор, пока температура олова не достигнет температуры кристаллизации Тk = Тnл. Эта температура не будет изменяться до тех пор, пока не произойдет полная кристаллизация олова, хотя тепло продолжает отдаваться в окружающую среду.
50
После окончания кристаллизации температура олова с тиглем начинает опять уменьшаться, причем снова по экспоненциальному закону регулярного режима:
T - Tср = (Tk - Tср )× e |
−k2 |
( τ−τk ) |
, |
(7) |
||||
|
|
|
||||||
где |
|
|
|
|
|
|
|
|
k 2 |
= |
|
q 2 |
|
|
, |
|
(8) |
c 02 m 0 |
|
|
|
|
||||
|
|
+ c T m T |
|
|
||||
Тk – температура кристаллизации олова, k2 – темп охлаждения твердого олова с тиглем, с02 – удельная теплоемкость твердого олова.
Кривая зависимости температуры от времени при охлаждении олова имеет вид, показанный на рис. 1.
Т, К
τ, с
Рисунок 2 - Кривая охлаждения олова Здесь участок АВ соответствует охлаждению жид-
кого олова, ВС – участок кристаллизации олова, СД – охлаждение твердого олова.
Вблизи точки В наблюдается небольшой минимум температуры, а вблизи точки С – переходный участок, где темп охлаждения меньше k2 . Нарушение регулярного ре-
51

жима охлаждения вблизи точки В связано с возникновением так называемого метастабильного состояния (переохлажденное состояние жидкости, когда температура жидкости опускается ниже температуры кристаллизации Тк, а кристаллизация ещё не наступает), которое зависит от чистоты исследуемого вещества.
Количество тепла, выделенное при кристаллизации олова, равно:
Q = l m0 , |
(9) |
где l - удельная теплота плавления, численно равная теплоте кристаллизации.
2.2. Вывод формулы для определения λ
Можно записать, что тепло, выделенное при кристаллизации, равно количеству теплоты, отданному телом за время кристаллизации в окружающую среду:
Q = q(Tk - Tср)(tk - tн), |
(10) |
где q = (q1 +q2)/2– средняя скорость теплоотдачи в окружающую среду, tн и tk – моменты времени, соответствующие началу и концу кристаллизации олова.
Приравнивая правые части формул (9) и (10), полу-
чим:
lm0 = q(Tk - Tср)×(tk - tн).
Отсюда: |
q(Tк − Тcp )(t k − t н ) |
|
|
|
l = |
. |
(11) |
||
|
||||
|
mo |
|
||
Выражение для q получим, используя формулы (3) и (8): |
||||
q1 |
= k1(c01m0 + cT mT), |
(12) |
||
q2 |
= k1(c02m0 + cT mT). |
(13) |
||
Следовательно, |
|
|
|
|
q= 1 [k1 (c01m0 + cT mT )+ k2 (c02 m0 + cT mT )] .
2
52

Окончательно выражение для λ получится в виде:
λ = (Tk − Tср )(τ k − τ н ) [k1 (c01m0 + cT mT )+ k2 (c02 m0 + cT mT )]. (14)
2m0
k1, k2, τн, τk находятся из графика, построенного по экспериментальным данным, аналогичного рис. 2.
Для этого запишем уравнение (5) для момента времени τн:
ln(Tk - Tср) = ln(T0 – T ср) - k1τн. (15)
Отсюда получим:
k 1 = |
ln (T 0 − T ср )− ln (T k − Tср ) . |
(16) |
||
τ н |
|
|
|
|
|
|
|
|
|
Аналогично, записав (5) для моментов времени τk |
и τ2, бу- |
|||
дем иметь: ln(Tk – T ср) = ln(T0 |
- Tср) – k 2 τk , |
|
||
ln(T2 - Tср ) = ln(T0 |
– T ср) – k 2 τ2. |
|
||
Вычтя из первого уравнения второе, получим следующую формулу для k2,:
k2 = ln(Tk − Tср )− ln(T2 − Tср ). (17)
τ2 − τk
Вкачестве измерителя температуры в данной лабора-
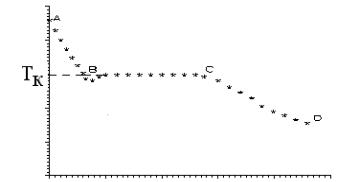
торной работе используется термоэлектрический термометр (принцип его действия – см. лабораторная работа №2). Термо-э.д.с. пропорциональна разности температур “ горячего“ Т и “ холодного” Тср спаев, поэтому кривую охлаждения олова можно построить в переменных E и τ. Если эту же кривую построить в полулогарифмических координатах ln E и τ (рис. 3), то участки АВ и СД станут прямолинейными, что позволит более точно определить моменты начала τн и конца τк кристаллизации.
Таким образом, для определения темпов охлаждения k1 и k2 необходимо построить зависимость E(τ) в полулогарифмических координатах (рис.3). Моменты времени τн и τк соответствуют точкам пересечения прямых АВ и СД с линией кристаллизации ВС.
53
0 |
τн |
τк |
τ2 |
τ, c |
Рисунок 3- Кривая охлаждения олова в полулогарифмическом масштабе
С учетом того, что термо-э.д.с в первом приближении пропорциональна разности температур, при которых находятся концы спаев термопары, формулы (16) и (17) для вычисления k1 и k2 примут вид:
k1 |
= |
ln E0 − ln Ek |
= |
ln(E0 / Ek ) |
, |
(16а) |
|||||
|
τ н |
|
|
||||||||
|
|
|
|
|
|
τ н |
|
||||
k2 |
= |
ln Ek |
− ln E2 |
|
= |
ln(Ek / E2 ) |
. |
(17а) |
|||
τ 2 |
− τ k |
|
|
||||||||
|
|
|
|
|
|
τ 2 − τ k |
|
||||
2.3. Вывод формулы для изменения энтропии при кристаллизации
Энтропия, являющаяся функцией состояния, характеризует вероятность микросостояния физической системы и определяется выражением
54
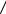
S = k×ln w, |
(18) |
которое называется формулой Больцмана. |
|
Здесь k – постоянная Больцмана, |
w - термодинамическая |
вероятность (или статистический вес), т.е. число микросостояний, посредством которых реализуется данное макросостояние.
Термодинамическая вероятность, а, следовательно, и энтропия, являются функциями параметров состояния системы. В частности, при плавлении и кристаллизации вещества энтропия его должна изменяться.
Методы измерения энтропии при тепловых взаимодействиях основаны на измерении приведенного количества тепла.
Приведенное количество тепла есть отношение элементарного количества тепла, которым обменивается система, к абсолютной температуре Т, при которой происходит этот
обмен. Итак, |
|
dS = δ Q T . |
(19) |
Полное изменение энтропии при обратимом переходе системы из состояния А в В определяется путем интегрирования выражения (19):
Β |
δQ |
|
|
Α∫ |
T |
. |
(20) |
S B − S A = |
|
В частности, изменение энтропии при кристаллизации (так же, как и при плавлении), определяется формулой:
S B - S A |
= DS = l × m . |
(21) |
|
Tk |
|
Так как энтропию в некотором смысле можно считать мерой беспорядка в системе, то при кристаллизации энтропия олова уменьшается, что соответствует переходу системы в более упорядоченное состояние.
55
3.Описание установки
3.1.Принадлежности: тигель с оловом, печь, измерительная термопара, секундомер, цифровой вольтметр.
3.2.Установка (рис.4) состоит из укрепленного на конце штанги тигля с оловом, который можно помещать в электрическую печь и отводить в сторону от печи после того, как олово расплавится.
Один спай термопары находится в глицерине при комнатной температуре, а “ горячий“ спай её помещается в расплавленное олово в тигле.
Термопара подключена к универсальному цифровому вольтметру для измерения термоэлектродвижущей силы (термо-э.д.с) в цепи термопары. Показания вольтметра пропорциональны разности температур спаев термопары:
E=α(T– Тср), |
(22) |
где α - постоянная термопары.
56
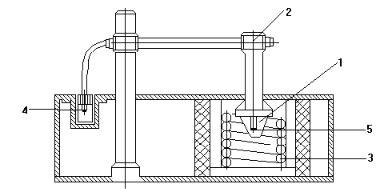
1 - тигель с оловом, 2 - штатив, 3 - нагреватель, 4 - сосуд с глицерином, 5 - измерительная термопара, 6 - изоляционный блок, 7 - корпус.
Рисунок 4-Установка для определения удельной теплоты плавления олова
4. Порядок выполнения работы
4.1. Записать необходимые для расчетов данные в тетрадь:
с01 = 267,9 Дж/(кг×К) - удельная теплоемкость жидкого олова, соответствующая температуре 2400С;
с02 = 246,6 Дж/(кг×К) - удельная теплоемкость твердого олова, соответствующая температуре 2300С;
сТ, mТ и m0 – удельная теплоемкость фарфорового тигля, массы тигля и олова (приведены на табличке возле установки);
Тк = 231,90С – температура кристаллизации олова.
Тср - температура воздуха по показанию контрольного термометра, висящего на стене в лаборатории.
4.2. Поместить тигель с оловом в держателе над печью так, чтобы тигель входил в центральное отверстие муфельной печи.
57
4.3.Включить установку в сеть и повернуть ручку регулировки напряжения.
4.4.Пока олово нагревается, подготовить таблицу для записи результатов эксперимента, предусмотрев в ней следующие колонки:
∙номер по порядку,
∙время в секундах,
∙термо-э.д.с. в милливольтах,
∙логарифм термо-э.д.с.
Всего в таблице необходимо предусмотреть 50 − 100 строк в зависимости от того, через какие интервалы времени будут производиться измерения.
4.5. Следить за плавлением олова в тигле и после того, как оно расплавится, поместить в олово “ горячий“ спай термопары. После достижения показания вольтметра 20 мВ выключить печь и отвести держатель с тиглем в сторону от нагревателя, расположив его над столом на высоте 15 ÷ 20 см.
4.6.Включить секундомер и сразу же начать запись показаний вольтметра через каждые 10÷20 сек. Измерения производить до тех пор, пока показания вольтметра на достигнут значения, в два раза меньшего по сравнению со значением термо-э.д.с, соответствующим температуре кристаллизации.
4.7.Построить кривую охлаждения в переменных
Е= f(τ).
4.8.Построить этот же график в полуогарифмиче-
ских координатах: lnE = f(τ) и определить по нему значения времени, соответствующие началу τн и концу τк процесса кристаллизации, а также значение lnЕк, соответствующее температуре кристаллизации.
58
4.9.По наклону участков AB и СД полулогарифмического графика определить темпы охлаждения k1 и k2, используя формулы (16а) и(17а).
4.10.Используя табличное значение температуры плавления олова и измеренную температуру окружающей среды в лаборатории, с помощью формулы (14) найти удельную теплоту плавления олова.
4.11.По формуле (21) вычислить изменение энтропии олова при кристаллизации.
4.12.Оценить абсолютную и относительную погрешности определения удельной теплоты плавления олова
исравнить полученное значение λ с его табличным значением из справочника.
5. Контрольные вопросы
5.1.Расскажите о фазовых переходах первого рода. Начертите диаграмму состояний и объясните её.
5.2.Что называется удельной теплотой плавления?
5.3.В каких фазах находится вещество при кристаллизации и как изменяется при этом его внутренняя энергия? Какая часть ее (кинетическая или потенциальная) при этом изменяется?
5.4.Как изменяется энтропия тела при кристаллиза-
ции?
5.5.Чем можно объяснить наличие переходных участков на кривой охлаждения вблизи точек В и С на рис. 1?
5.6.Какие погрешности возникают при измерениях? Объясните их причины.
5.7.Какие упрощающие предположения сделаны при выводе формулы (14), и как они скажутся на точности полученного результата?
5.8.Как улучшить данную работу, чтобы уменьшить погрешности измерений?
59
