
- •ОГЛАВЛЕНИЕ
- •1. Способы получения
- •1.1. Способы получения алкилгалогенидов
- •а) галогенирование алканов
- •б) аллильное хлорирование алкенов
- •г) гидрогалогенирование алкенов
- •д) гидрогалогенирование сопряженных диенов
- •е) замещение гидроксильной группы в спиртах на галоген
- •1.2. Способы получения винил- и арилгалогенидов
- •1.3. Способы получения дигалогенпроизводных
- •2. Химические свойства
- •2.1. Реакции нуклеофильного замещения (SN) в алкилгалогенидах
- •А) Механизм мономолекулярного нуклеофильного замещения (SN1)
- •Б) Механизм бимолекулярного нуклеофильного замещения (SN2)
- •2.2. Особенности нуклеофильного замещения галогена в арилгалогенидах
- •А) Нуклеофильное замещение в неактивированных арилгалогенидах
- •Б) Нуклеофильное замещение в активированных арилгалогенидах
- •2.3. Реакция дегидрогалогенирования
- •2.4. Восстановление галогенпроизводных
- •2.5. Реакции галогенпроизводных с металлами
- •3. Задачи и упражнения
- •СПИРТЫ
- •1. Способы получения
- •1.1. Гидратация алкенов
- •1.2. Гидролиз галогенпроизводных
- •1.3. Восстановление карбонильных соединений
- •1.4. Получение спиртов реакцией Гриньяра
- •1.5. Получение диолов и триолов
- •2. Химические свойства
- •2.1. Кислотно-основные свойства
- •2.2. Реакции спиртов с разрывом связи О-Н
- •2.2.1. Алкилирование спиртов
- •2.2.2. Ацилирование спиртов
- •2.3. Реакции спиртов с разрывом связи С-О
- •2.3.1. Замещение гидроксильной группы на галоген
- •2.3.2. Образование простых эфиров (межмолекулярная дегидратация)
- •2.3.3. Внутримолекулярная дегидратация спиртов до алкенов
- •2.4. Окисление и дегидрирование спиртов
- •3. Задачи и упражнения
- •ФЕНОЛЫ
- •1. Способы получения
- •1.1. Щелочной гидролиз арилгалогенидов
- •1.2. Щелочное плавление солей ароматических сульфокислот
- •1.3. «Кумольный» метод получения фенола
- •2. Химические свойства
- •2.1. Кислотно-основные свойства фенолов
- •2.2. Фенолы как нуклеофилы
- •2.2.1. Алкилирование и ацилирование фенолов по атому кислорода
- •2.2.2. Реакции электрофильного замещения
- •3. Задачи и упражнения
- •АЛЬДЕГИДЫ И КЕТОНЫ
- •1. Способы получения
- •1.1. Окисление алкенов
- •а) озонолиз алкенов
- •б) окисление алкенов в присутствии хлорида палладия
- •1.2. Гидратация алкинов
- •1.3. Получение ароматических альдегидов и кетонов ацилированием аренов
- •1.4. Гидролиз геминальных дигалогенидов
- •1.5. Окисление и дегидрирование спиртов
- •1.6. Получение альдегидов и кетонов из карбоновых кислот и их производных
- •а) восстановление ацилгалогенидов до альдегидов (реакция Розенмунда)
- •б) пиролиз кальциевых солей карбоновых кислот
- •в) синтез кетонов реакцией Гриньяра из нитрилов карбоновых кислот
- •2. Химические свойства
- •2.1. Кислотно-основные свойства и кето-енольная таутомерия
- •2.2. Реакции нуклеофильного присоединения
- •а) Реакции с О-нуклеофилами
- •б) Реакции с S-нуклеофилами
- •в) Реакции с N-нуклеофилами
- •г) Реакции с С-нуклеофилами
- •2.3. Реакции енолизующихся альдегидов и кетонов с галогенами
- •2.4. Окисление и восстановление альдегидов и кетонов
- •2.4.1. Окисление альдегидов и кетонов
- •2.4.2. Восстановление альдегидов и кетонов
- •2.4.3. Реакция Канниццаро
- •3. Задачи и упражнения
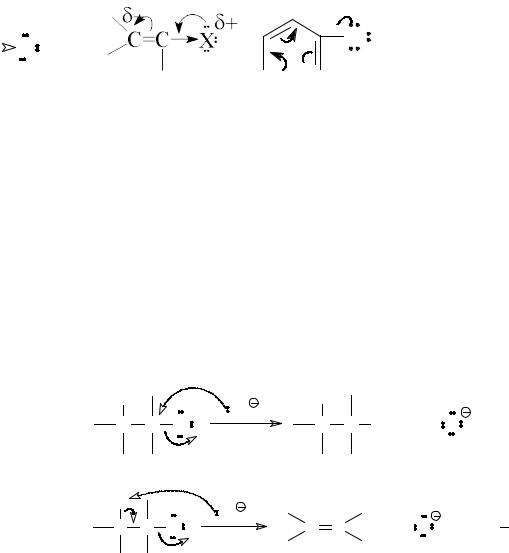
2. Химические свойства
Для галогенпроизводных как соединений, имеющих полярную связь углерод-галоген, характерны реакции с гетеролитическим разрывом этой связи. При этом атом галогена уносит с собой оба электрона связи, т.е. уходит как анион. В зависимости от строения галогенпроизводного этот разрыв связи может протекать легче или труднее. Для алкилгалогенидов, в которых атом галогена связан с sp3-гибридизированным атомом углерода, этот процесс происходит значительно легче, чем для винилили арилгалогенидов, у которых атом галогена не просто связан с sp2-гибридизированным атомом углерода σ-связью, но и участвует в p-π-сопряжении.
Rδ+ Xδ−
δ− 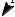
 X δ+
X δ+
δ−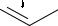
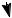 δ−
δ−
На место уходящего атома галогена может присоединиться частица, которая за счет своей пары электронов образует новую σ- связь. Так осуществится замещение атома галогена на нуклеофил, т.е. нуклеофильное замещение (SN). Кроме того, уход атома галогена в виде аниона может сопровождаться отрывом протона от соседнего атома углерода. В этом случае произойдет отщепление, или элиминирование (Е), галогеноводорода с образованием двойной связи. Обе реакции – и нуклеофильное замещение, и элиминирование – происходят параллельно, т.е. являются конкурирующими процессами, поскольку одна и та же частица может в первом случае выступать как нуклеофил, а во втором случае – как основание.
|
H |
Y |
H |
|
|
|
нуклеофильное |
C C X |
C C Y |
+ |
X |
||
|
||||||
замещение (SN) |
|
|
|
|
|
|
элиминирование (Е) |
H |
Y |
|
|
|
|
C C X |
C C + |
X |
+ H Y |
|||
|
2.1. Реакции нуклеофильного замещения (SN) в алкилгалогенидах
11
http://mitht.ru/e-library

В реакциях нуклеофильного замещения галогенпроизводные выполняют роль реагента, алкилирующего нуклеофильную частицу. В зависимости от того, несет ли нуклеофильная частица заряд или нет, схемы такого алкилирования могут выглядеть по-разному, например:
CH3CH2 Cl |
+ |
Na OH |
CH3CH2 |
OH + |
Na Cl |
|||
CH3 |
|
|
H |
|
CH |
H |
|
|
CH3 C Br |
|
O |
|
3 |
|
Br |
||
+ |
H |
CH |
C O |
+ |
||||
CH3 |
|
|
3 |
CH |
H |
|
|
|
|
|
|
|
|
|
|||
|
|
|
|
|
3 |
|
|
|
В первом случае при взаимодействии этилхлорида с водным раствором едкого натра (щелочной гидролиз) произошло этилирование гидроксид-аниона. Атом кислорода в нуклеофильной частице в процессе реакции выступил донором неподеленной пары электронов и потерял заряд. Во втором случае при взаимодействии трет-бутилбромида с водой (нейтральный гидролиз) произошло алкилирование воды как нуклеофила. Теперь уже нейтральный атом кислорода выступил в качестве донора неподеленной пары электронов и приобрел положительный заряд.
Описанный выше гидролиз галогенопроизводных является одним из примеров многочисленных реакций нуклеофильного замещения. В результате гидролиза галогенопроизводных образуются спирты, а в результате реакций с другими нуклеофилами – разнообразные функциональные производные углеводородов. Ниже приведены еще некоторые примеры реакций нуклеофильного замещения:
•алкилирование алкоголятов – синтез простых эфиров по Вильямсону
CH Cl |
+ CH O Na |
CH2OCH3 |
2 |
3 |
|
бензилхлорид |
метилат натрия |
бензилметиловый эфир |
•алкилирование карбоксилат-анионов (солей карбоновых кис-
лот) – синтез сложных эфиров
12
http://mitht.ru/e-library
аллилйодид ацетат калия |
аллилацетат |
•замещение атома галогена на галоген (реакция Финкельштей-
на)
CH3CH2Br + I
 CH3CH2I + Br
CH3CH2I + Br
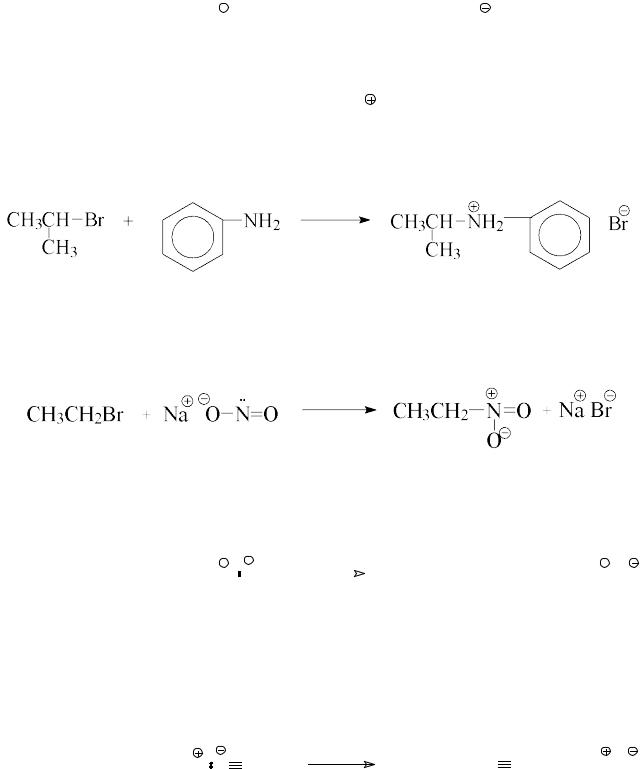
• алкилирование аммиака или аминов
CH3I + NH3  CH3NH3 I
CH3NH3 I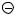
йодид метиламмония
анилин |
бромид изопропилфениламмония |
• алкилирование нитрит-аниона – синтез нитросоединений
нитроэтан
•алкилирование цианид-аниона – синтез нитрилов карбоновых кислот
CH2=CHCH2CH2Cl + Na |
|
|
|
|
|
|
|
|
CH2=CHCH2CH2C |
|
|
N + Na |
|
|
Cl |
|
|
C |
|
|
N |
|
|
|
|
|
|||||
|
|
|
|
|
|
|
|
|
|||||||
|
|
|
|
|
|
|
|||||||||
|
|
|
|
|
|
||||||||||
|
|
|
|
|
|
|
|||||||||
4-хлор-1-бутен |
нитрил 4-пентеновой кислоты |
||||||||||||||
• алкилирование ацетиленидов
CH3CH2CH2Br + Na C CCH3 |
CH3CH2CH2C CCH3 + Na Br |
13
http://mitht.ru/e-library

Нуклеофильное замещение в алкилгалогенидах может происходить по двум альтернативным механизмам:
•с последовательными процессами разрыва связи углеродгалоген и образования новой связи с нуклеофилом (мономолекулярное нуклеофильное замещение, или SN1)
•с одновременным (синхронным) разрывом связи углеродгалоген и образованием новой связи с нуклеофилом (бимолекулярное нуклеофильное замещение, или SN2).
А) Механизм мономолекулярного нуклеофильного замещения (SN1)
Этот механизм представляет собой последовательность двух стадий, отличающихся константами скорости. На первой стадии полярная связь углерод-галоген субстрата медленно подвергается гетеролизу с образованием карбокатиона и галогенид-аниона.
Rδ+ X δ− |
R + X |
На второй стадии образовавшийся карбокатион очень быстро образует с нуклеофилом ковалентную связь по донорноакцепторному механизму: карбокатион предоставляет вакантную орбиталь, а нуклеофил – пару электронов.
R




 +
+ 







 Y
Y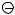
 R Y
R Y
Так как первая стадия протекает значительно медленнее, чем вторая, скорость реакции замещения определяется скоростью пер-
вой стадии, которая зависит только от концентрации галогенопроизводного как единственного участника этой стадии. Такой процесс нуклеофильного замещения называют мономолекулярным и обозначают SN1.
По этому механизму реагируют галогенпроизводные, которые могут образовать устойчивые карбокатионы. Поэтому среди насыщенных галогенпроизводных этот механизм характерен, прежде всего, для третичных галогенидов, поскольку третичные карбокатионы являются более устойчивыми, чем вторичные или первичные. Так, например, следующие карбокатионы можно расположить в ряд по убыванию их устойчивости:
14
http://mitht.ru/e-library
CH3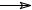 C
C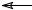 CH3 > CH3
CH3 > CH3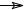 CH
CH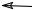 CH3 > CH3
CH3 > CH3 CH2 > CH3
CH2 > CH3
CH3
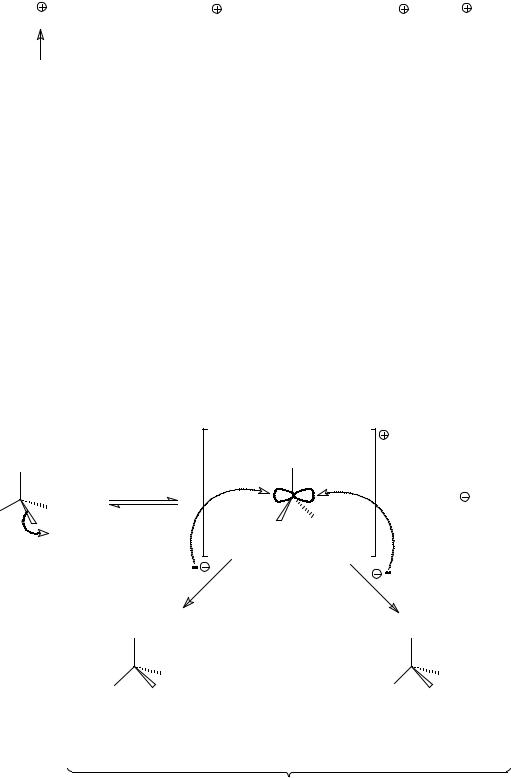
Если атом галогена соединен с асимметрическим атомом углерода хиральной молекулы, то мономолекулярное нуклеофильное замещение приводит к рацемизации по данному асимметрическому атому, поскольку образующийся карбокатион как плоская в области заряженного атома углерода (sp2-гибридизация) частица может присоединить нуклеофил с одинаковой вероятностью с каждой из сторон от этой плоскости с образованием двух энантиомеров (на схеме показана вакантная р-орбиталь, симметричная относительно плоскости карбокатиона).
Например, при щелочном гидролизе (S)-2,3-диметил-3- хлорпентана образуется смесь равных количеств энантиомерных спиртов, т.е. рацемический спирт.
|
CH(CH ) |
|
CH(CH3)2 |
|
|
3 2 |
|
|
|
CH3CH2 |
CH3 |
CH3CH2 |
CH3 |
+ Cl |
|
Cl |
|
||
(S)-2,3-диметил-3- |
|
|
|
|
хлорпентан |
HO |
|
OH |
|
|
|
CH(CH3)2 |
|
CH(CH3)2 |
|
HO |
CH3 |
|
CH3 |
|
CH2CH3 |
CH3CH2 OH |
||
|
(R)-2,3-диметил-3- |
(S)-2,3-диметил-3- |
||
|
|
пентанол |
|
пентанол |
рацемат
Кроме третичных галогенпроизводных, по механизму SN1 могут реагировать также аллил- и бензилгалогениды, которые образуют устойчивые карбокатионы, стабилизированные за счет сопряжения.
15
http://mitht.ru/e-library
