
- •Федеральное агентство по образованию
- •Оглавление
- •Введение
- •Механизм взаимодействия металла с металлоидом и условия, необходимые для протекания процесса
- •Механизм процесса
- •Перемещение ионов под действием электрического поля
- •Характер перемещения ионов в идеальной кристаллической решетке
- •Перемещение ионов в неидеальной кристаллической решетке
- •Перемещение катионов при наличии вакансий в катионной подрешетке
- •Перемещение катионов при возможности их нахождения в междоузлиях
- •Образование тепловых дефектов кристаллической решетки
- •Общие положения
- •Возникновение точечных структурных дефектов кристаллической решетки в результате теплового движения
- •Возникновение точечных структурных дефектов при переходе ионов в междоузлие
- •Переход катиона из узла в междоузлие
- •Переход аниона из узла в междоузлие
- •Возникновение дефектов в результате перехода ионов из объема на поверхность или с поверхности в объем
- •Переход ионов из узлов в объеме кристалла в узлы над его поверхностью
- •Переход ионов из узлов на поверхности кристалла в его объем (в междоузлия)
- •Возникновение тепловых электронных дефектов
- •Константы равновесия процессов образования тепловых дефектов
- •Константа равновесия образования дефектов по Френкелю в катионной подрешетке
- •Константы равновесия образования других тепловых дефектов
- •Расчет равновесной концентрации тепловых дефектов
- •Типы структурной разупорядоченности кристаллов
- •Распространенность различных типов разупорядоченности
- •Образование дефектов нестехиометрии
- •Точечные структурные дефекты, обусловленные отклонением состава от стехиометрического
- •Тип «Френкель»
- •Тип «Шоттки»
- •Условия и механизм образования нестехиометрической фазы
- •Связь между давлением газообразного металлоида и составом равновесной твердой фазы
- •Механизм и равновесие возникновения недостатка металлоида (избытка металла)
- •Тип «Френкель»
- •Тип «Шоттки»
- •Механизм и равновесие возникновения избытка металлоида (недостатка металла)
- •Зависимости концентраций дефектов от давления металлоида в газовой фазе
- •Общие положения
- •Соотношение между константами равновесия процессов возникновения недостатка и избытка металлоида
- •Расчет равновесных концентраций дефектов при заданном давлении металлоида
- •Составление и решение системы уравнений
- •Приближенный метод построения зависимостей концентраций дефектов от давления металлоида Выбор системы координат для построения зависимостей
- •Построение приближенных зависимостей для кристалла с типом разупорядоченности «Френкель»
- •Расчет концентраций тепловых дефектов и значения
- •Определение концентраций дефектов при ≠
- •Построение диаграммы
- •Построение приближенных зависимостей для кристалла с типом разупорядоченности «Шоттки»
- •Расчет концентраций тепловых дефектов и значения
- •Определение концентраций дефектов при ≠
- •Построение диаграммы
- •Анализ характера зависимостей концентрации дефектов от давления металлоида в газовой фазе
- •Влияние примесей на равновесие дефектов в кристалле
- •Примеси, оказывающие наибольшее влияние на равновесие дефектов
- •Примеси замещения с зарядом катионов, превышающим заряд катионов матрицы
- •Примеси замещения с зарядом катионов меньшим, чем заряд катионов матрицы
- •Механизм и закономерности процесса образования твердого продукта (теория Карла Вагнера)
- •Механизм и условия протекания процесса
- •Электрическая схема процесса
- •Соотношения, определяющие силу тока
- •Уравнения скорости образования твердого продукта
- •Зависимость константы скорости от давления металлоида
- •Возможные лимитирующие стадии процесса
- •Константа скорости реакции при лимитирующем переносе заряда ионами Решение в общем виде
- •Константа скорости реакции при лимитирующем переносе заряда электронами
- •Анализ ожидаемых закономерностей процесса с помощью теории Вагнера
- •Характеристика образующегося продукта
- •Направление роста ZnO
- •Влияние давления кислорода на скорость реакции (на величину константы скорости)
- •Влияние примесей на скорость реакции (на величину константы скорости)
- •Закономерности протекания реакций с участием металла, имеющего несколько устойчивых степеней окисления
- •Характер образующейся оболочки
- •Закономерности образования многослойной оболочки
- •Соотношения между толщиной слоев
Соотношение между константами равновесия процессов возникновения недостатка и избытка металлоида
Константы равновесия процессов возникновения избытка металла (недостатка металлоида) KФ(Ме) и KШ(Ме) связывают с давлением металлоида равновесные концентрации электронов проводимости и межузельных катионов либо вакансий анионов, а константы равновесия процессов возникновения избытка металлоида (недостатка металла) KФ(Х) и KШ(Х) – концентрации дырок и вакансий катионов. Но концентрации электронов проводимости и дырок, межузельных катионов и вакансий катионов, вакансий анионов и вакансий катионов попарно связаны между собой константами равновесия тепловой разупорядоченности (константами равновесия типа произведений растворимости) – соответственно Kи, KФ и KШ. Следовательно, должны существовать выражения, связывающие между собой константы равновесия процессов возникновения избытка металла и процессов возникновения избытка металлоида и включающие константы равновесия тепловой разупорядоченности. То, что константы равновесия процессов образования дефектов нестехиометрии должны быть связаны между собой, подсказывает и простая логика: обе эти константы описывают один и тот же обратимый процесс обмена металлоидом между твердой и газовой фазами, и отличаются они только тем, какое направление перехода металлоида выбрано в качестве прямой реакции.
Найдем выражения, связывающие константы, для кристалла Ме2Х3 º 2Ме3+·3Х2-.
Равновесия в кристалле с типом разупорядоченности «Френкель» описываются константами
KФ(Ме)
=
![]() (e–)3
(e–)3![]() ;
;
KФ(Х)
=
 ;
;
KФ
=
![]()
![]() ;
;
Kи = (e–)(е+).
Выразим в первом уравнении концентрацию электронов проводимости через концентрацию дырок, а концентрацию межузельных катионов через концентрацию вакансий катионов:
KФ(Ме)
=
![]()

![]() .
.
После преобразования полученного выражения получаем:
 =
=![]() .
.
Но выражение, стоящее в левой части равенства, – это не что иное, как KФ(Х), следовательно,
KФ(Х)
=![]() .
.
Теперь найдем соотношения между константами равновесия образования дефектов нестехиометрии в кристалле типа «Шоттки»:
KШ(Ме)
=
![]() (e–)2
(e–)2![]() ;
;
KШ(Х)
=
 ;
;
KШ
=![]()
![]() ;
;
Kи = (e–)(е+).
Выразим в первом уравнении концентрацию электронов проводимости через концентрацию дырок, а концентрацию вакансий анионов через концентрацию вакансий катионов и затем преобразуем полученное выражение:
KШ(Ме)
=
![]()

 ,
,
 =
= .
.
Теперь возведем левую и правую части равенства в степень 3/2, чтобы получить концентрацию вакансий катиона в первой степени:
 =
= .
.
Левая часть этого равенства - это выражение KШ(Ме), следовательно,
KШ(Ме)
= .
.
Расчет равновесных концентраций дефектов при заданном давлении металлоида
Составление и решение системы уравнений
Методику
расчета равновесных концентраций
дефектов при заданном давлении металлоида
![]() (подразумевается
(подразумевается
![]() ≤
≤![]() ≤
≤![]() )
и известных значениях всех констант
равновесия рассмотрим на примере
кристалла Ме2Х3,
тип разупорядоченности «Френкель». В
таком
кристалле присутствуют 4 вида дефектов:
точечные структурные дефекты
)
и известных значениях всех констант
равновесия рассмотрим на примере
кристалла Ме2Х3,
тип разупорядоченности «Френкель». В
таком
кристалле присутствуют 4 вида дефектов:
точечные структурные дефекты
![]() и
и
![]() и электронные дефекты e–
и e+.
Для определения концентраций этих
дефектов (т. е. расчета 4 неизвестных
величин) необходимы 4 уравнения,
связывающие равновесные концентрации
дефектов между собой и с давлением
металлоида.
и электронные дефекты e–
и e+.
Для определения концентраций этих
дефектов (т. е. расчета 4 неизвестных
величин) необходимы 4 уравнения,
связывающие равновесные концентрации
дефектов между собой и с давлением
металлоида.
Два из этих уравнений – это уравнения типа произведения растворимости, связывающие попарно равновесные концентрации дефектов между собой:
0
D
![]() +
+
![]() ,
,
![]()
![]() =
KФ, (I)
=
KФ, (I)
0 D e– + e+, (e–)(e+) = Kи. (II)
Третье уравнение – это уравнение, описывающее равновесие массообмена кристалла и газовой фазы (обратимого перехода металлоида из одной фазы в другую) и связывающее концентрации двух дефектов (одного точечного структурного и одного электронного) с давлением металлоида в газовой фазе. При этом можно использовать либо уравнение, описывающее уход металлоида из кристалла, либо уравнение, описывающее переход металлоида из газовой фазы в кристалл, но не оба вместе, так как на самом деле эти уравнения представляют собой два варианта записи одного и того же обратимого процесса. Соответственно обозначаем варианты третьего уравнения как IIIa и IIIб:
0
D
![]() ↑
+ 3e–
+
↑
+ 3e–
+
![]() , (e–)3
, (e–)3![]() =KФ(Ме)
=KФ(Ме)![]() ,
(IIIа)
,
(IIIа)
![]() ↓
D
3e+
+
↓
D
3e+
+
![]() ,(е+)3
,(е+)3![]() =KФ(Х)
=KФ(Х)![]() .
(IIIб)
.
(IIIб)
Необходимо еще одно уравнение, связывающее между собой равновесные концентрации дефектов; этим уравнением будет математическое описание одного из обязательных условий равновесия – отсутствие в кристалле некомпенсированных электрических зарядов (условия электронейтральности кристалла). Поскольку в идеальном кристалле заряды катионов и анионов взаимно компенсируются, условие электронейтральности относится к зарядам дефектов и формулируется следующим образом: в равновесном кристалле сумма зарядов всех положительно заряженных дефектов равна сумме зарядов всех отрицательно заряженных дефектов.
Составим уравнение, описывающее условие электронейтральности кристалла («уравнение электронейтральности») в самом общем виде, с учетом всех возможных дефектов, а не только характерных для какого-то одного типа разупорядоченности.
Пусть
в единице объема кристалла содержится
![]() электронов
проводимости,
электронов
проводимости,![]() дырок,
дырок,![]() вакансий катиона,
вакансий катиона,![]() катионов
в междоузлиях,
катионов
в междоузлиях,![]() вакансий
аниона,
вакансий
аниона,![]() анионов
в междоузлиях. При этом положительный
заряд всех дырок равен их числу
анионов
в междоузлиях. При этом положительный
заряд всех дырок равен их числу![]() (величина заряда дырки равна единице),
положительный заряд всех катионов в
междоузлиях равенzMe
(величина заряда дырки равна единице),
положительный заряд всех катионов в
междоузлиях равенzMe![]() (каждый межузельный катион несетzMe
положительных зарядов), а положительный
заряд всех вакансий аниона равен zХ
(каждый межузельный катион несетzMe
положительных зарядов), а положительный
заряд всех вакансий аниона равен zХ![]() (каждая вакансия аниона несетzХ
положительных зарядов). В результате
суммарный положительный заряд всех
положительно заряженных дефектов в
единице объема равен
(каждая вакансия аниона несетzХ
положительных зарядов). В результате
суммарный положительный заряд всех
положительно заряженных дефектов в
единице объема равен
![]() +
zMe
+
zMe![]() +
zХ
+
zХ![]() ;
;
очевидно, суммарный отрицательный заряд в единице объема равен
![]() +
zMe
+
zMe![]() +zХ
+zХ![]() ,
,
и в равновесном кристалле выполняется условие
![]() +
zMe
+
zMe![]() +
zХ
+
zХ![]() =
=![]() +zMe
+zMe![]() +zХ
+zХ![]() .
(63)
.
(63)
Уравнение
(63) связывает между собой числа дефектов
в единице объема кристалла, а не их
концентрации. Но поскольку концентрация
дефекта – это отношение числа дефектов
данного вида в единице объема кристалла
к сумме чисел катионных и анионных узлов
в единице объема (см. п. 2.4.1), для перехода
к концентрациям достаточно почленно
разделить левую и правую части равенства
на
![]() =
=![]() +
+![]() :
:
![]() +
zMe
+
zMe +zХ
+zХ![]() =
=![]() +zMe
+zMe +zХ
+zХ![]() ,
,
откуда
(е+)+zMe(![]() )+zХ(
)+zХ(![]() )
= (e–)+zMe(
)
= (e–)+zMe(![]() )+zХ(
)+zХ(![]() ).
(64)
).
(64)
Применительно
к кристаллу
Ме2Х3
типа «Френкель», в котором
![]() ,
,
![]() ,
e–
и e+
уравнение электронейтральности принимает
вид
,
e–
и e+
уравнение электронейтральности принимает
вид
(е+)+3![]() =
(e–)+3
=
(e–)+3![]() .
(IV)
.
(IV)
Теперь
рассмотрим последовательность расчета
равновесных концентраций дефектов при
заданном давлении металлоида
![]() .
.
Поскольку
при избытке металла целесообразно
использовать уравнение (IIIа),
а при избытке металлоида – уравнение
(IIIб),
а избыток металла или металлоида
определяется тем, меньше или больше
![]() ,
чем
,
чем
![]() ,
расчет необходимо начать с определения
величины
,
расчет необходимо начать с определения
величины![]() .
.
Расчет
![]()
При
![]() =
=
![]() дефекты только тепловые, и их концентрации
определяются соотношениями, рассмотренными
в п. 2.4.3:
дефекты только тепловые, и их концентрации
определяются соотношениями, рассмотренными
в п. 2.4.3:
![]() т
=
т
=
![]() т
=
т
=
![]() ,
,
(e–)т
= (е+)т
=
![]() .
.
Поэтому
![]() можно найти из уравнения(IIIа)
или (IIIб)
как давление металлоида
можно найти из уравнения(IIIа)
или (IIIб)
как давление металлоида
![]() ,
при котором концентрации дефектов имеют
эти значения.
,
при котором концентрации дефектов имеют
эти значения.
Воспользуемся уравнением (IIIа):
(e–)3![]() =KФ(Ме)
=KФ(Ме)![]() ;
;
при
![]() =
=![]() получаем:
получаем:
(![]() )3
)3![]() =KФ(Ме)
(
=KФ(Ме)
(![]() )–3/4;
)–3/4;
(![]() )3/4
=
)3/4
=
![]() ;
;
![]() =
=
 =
=
 .
.
С тем же успехом можно использовать уравнение (IIIб):
(е+)3![]() =KФ(Х)
=KФ(Х)![]() ;
;
при
![]() =
=![]() получаем:
получаем:
(![]() )3
)3![]() =KФ(Х)
(
=KФ(Х)
(![]() )3/4;
)3/4;
(![]() )3/4
=
)3/4
=
![]() ;
;
![]() =
=
 =
=
 .
.
Методика
расчета
![]() для кристаллов с типом разупорядоченности
«Шоттки» и различающимся числом катионов
и анионов несколько отличается от
описанной выше. Рассмотрим ее на примере
кристалла того же состава.
для кристаллов с типом разупорядоченности
«Шоттки» и различающимся числом катионов
и анионов несколько отличается от
описанной выше. Рассмотрим ее на примере
кристалла того же состава.
Концентрации
тепловых
дефектов
при
![]() =
=
![]() определяются соотношениями, также
рассмотренными в п. 2.4.3:
определяются соотношениями, также
рассмотренными в п. 2.4.3:
![]() =
[(3/2)2KШ]1/5,
=
[(3/2)2KШ]1/5,
![]() =
[(2/3)3KШ]1/5,
=
[(2/3)3KШ]1/5,
(e–)
= (е+)
=
![]() .
.
Подставим концентрации тепловых дефектов в уравнение, описывающее зависимость концентрации дефектов от давления металлоида при избытке металла:
(e–)2![]() =KШ(Ме)
=KШ(Ме)![]() ,
,
Kи[(3/2)2KШ]1/5
= KШ(Ме)
(![]() )–1/2,
)–1/2,
(![]() )1/2
=
)1/2
=
![]() ,
,
![]() =
=
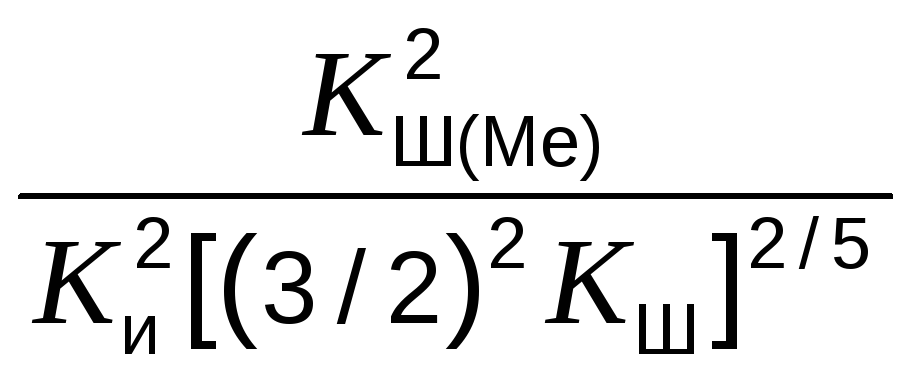 .
.
При использовании уравнения для избытка металлоида:
(е+)3![]() =KШ(Х)
=KШ(Х)![]() ,
,
![]() =
KШ(Х)(
=
KШ(Х)(![]() )3/4,
)3/4,
(![]() )3/4
=
)3/4
=
![]() ,
,
![]() =
=
 .Расчет
концентрации дефектов при
.Расчет
концентрации дефектов при
![]() ≠
≠![]()
Рассчитываем
концентрацию дефектов в кристалле Ме2Х3
типа «Френкель» при
![]() <
<
![]() .
.
Система уравнений:
![]()
![]() =
KФ,
(I)
=
KФ,
(I)
(e–)(e+) = Kи, (II)
(e–)3![]() =KФ(Ме)
=KФ(Ме)![]() ,
(IIIа)
,
(IIIа)
(е+)
+
3![]() =
(e–)
+
3
=
(e–)
+
3![]() .
(IV)
.
(IV)
Алгоритм
решения: с помощью уравнений (I)
– (IIIа)
последовательно выражаем через
концентрацию одного из дефектов
концентрации всех остальных и подставляем
в уравнение (IV);
в результате получаем уравнение с одной
неизвестной концентрацией и находим
ее, а далее последовательно находим все
другие концентрации. Целесообразно все
концентрации выражать через концентрацию
точечного структурного дефекта, входящую
в уравнение (III)
– независимо от формулы соединения и
типа разупорядоченности, эта концентрация
в уравнении (III)
имеет степень, равную 1, что облегчает
преобразования. В нашем случае это
![]() .
.
С помощью уравнения (I) выражаем концентрацию вакансий катиона:
![]() =
KФ
=
KФ![]() .
.
С помощью уравнения (IIIа) выражаем концентрацию электронов проводимости:
(e–)
=
![]()
и с помощью уравнения (II) – концентрацию дырок:
(е+)
=
![]() =
= .
.
Подставляем в уравнение (IV):
 +
3
+
3![]() =
=![]() +
3KФ
+
3KФ![]() .
.
Перенесем
все члены этого равенства в левую сторону
и расположим в порядке убывания степени
![]() :
:
3![]() +
+ –
–![]() –
3KФ
–
3KФ![]() = 0.
= 0.
При
известных значениях KФ,
Kи,
KФ(Ме)
и заданном
![]() это уравнение имеет единственный
действительный положительный корень,
удовлетворяющий физическому смыслу.
Как правило, для отыскания этого корня
приходится использовать численные
методы, хотя в некоторых случаях удается
найти аналитическое решение. В частности,
если все члены полученного уравнения
умножить на
это уравнение имеет единственный
действительный положительный корень,
удовлетворяющий физическому смыслу.
Как правило, для отыскания этого корня
приходится использовать численные
методы, хотя в некоторых случаях удается
найти аналитическое решение. В частности,
если все члены полученного уравнения
умножить на![]() ,
получим:
,
получим:
3![]() +
+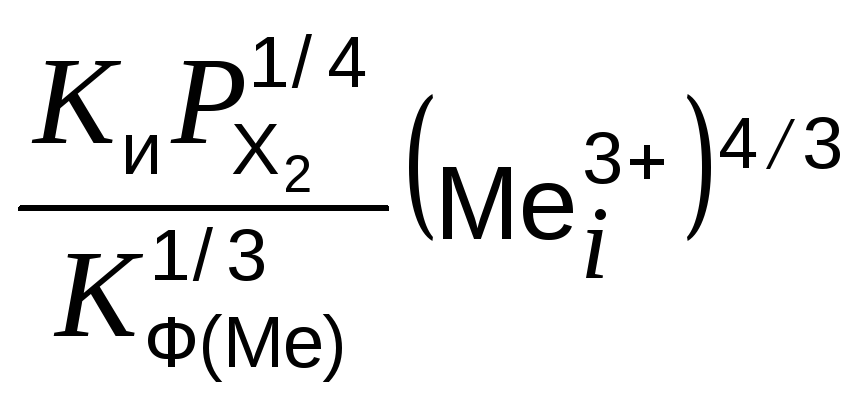 –
–![]() –
3KФ
=
0,
–
3KФ
=
0,
и
если обозначить
![]() =y,
то уравнение превратится в кубическое
типа
=y,
то уравнение превратится в кубическое
типа
ay3 + by2 + cy + q = 0,
корни которого находятся по известным формулам.
После
определения
![]() расчет концентраций всех остальных
дефектов не вызывает никаких сложностей.
расчет концентраций всех остальных
дефектов не вызывает никаких сложностей.
Обычно
представляет интерес не определение
концентраций дефектов при одном заданном
давлении металлоида, а построение
зависимостей этих концентраций от
![]() в интервале от
в интервале от
![]() до
до
![]() .
Для построения зависимостей необходимо
достаточно большое число точек (иногда
десятки, не менее 5 точек при
.
Для построения зависимостей необходимо
достаточно большое число точек (иногда
десятки, не менее 5 точек при
![]() <
<
![]() и столько же при
и столько же при
![]() >
>
![]() ),
и даже при использовании компьютера
расчеты требуют больших затрат времени
и труда. Поэтому для построения
зависимостей используют приближенный
метод, не требующий никаких сложных
вычислений.
),
и даже при использовании компьютера
расчеты требуют больших затрат времени
и труда. Поэтому для построения
зависимостей используют приближенный
метод, не требующий никаких сложных
вычислений.
