
- •I. Понятие иммунная система
- •II. Клетки иммунной системы
- •III. Виды иммунных реакций
- •Поверхностные барьеры
- •Гуморальные и биохимические факторы
- •Система комплемента
- •Фагоциты
- •Вспомогательные клетки
- •Распознавание антигенов
- •Иммунный ответ
- •Нейтрализация
- •Фагоцитоз
- •Т-киллеры
- •Запоминание контакта с антигенами
Введение
Под иммунитетом понимают совокупность биологических явлений, направленных на сохранение внутренней среды и защиту организма от инфекционных и других генетически чужеродных для него агентов. Существуют следующие виды инфекционного иммунитета:
антибактериальный
антитоксический
противовирусный
противогрибковый
антипротозойный
Инфекционный иммунитет может быть стерильным (возбудителя в организме нет) и нестерильным (возбудитель в организме). Врожденный иммунитет имеется с рождения, он может быть видовым и индивидуальным. Видовой иммунитет – невосприимчивость одного вида животного или человека к микроорганизмам, вызывающим заболевание у других видов. Он генетически детерминирован у человека как биологического вида. Видовой иммунитет всегда активен. Индивидуальный иммунитет пассивный (плацентарный иммунитет). Неспецифические факторы защиты следующие: кожа и слизистые оболочки, лимфатические узлы, лизоцим и другие ферменты полости рта и ЖКТ, нормальная микрофлора, воспаление, фагоцитирующие клетки, естественные киллеры, система комплемента, интерфероны. Фагоцитоз.
I. Понятие иммунная система
Иммунная система представляет собой совокупность всех лимфоидных органов и скоплений лимфоидных клеток организма. Лимфоидные органы подразделяются на центральные – тимус, костный мозг, сумка Фабрициуса ( у птиц) и ее аналог у животных - пейеровы бляшки; периферические – селезенка, лимфатические узлы, солитарные фолликулы, кровь и другие. Главный компонент ее – лимфоциты. Выделяют два основных класса лимфоцитов: В-лимфоциты и Т-лимфоциты. Т-клетки участвуют в клеточном иммунитете, регуляции активности В-клеток, гиперчувствительности замедленного типа. Различают следующие субпопуляции Т-лимфоцитов: Т- хелперы (запрограммированы индуцировать размножение и дифференцировку клеток других типов), супрессорные Т-клетки, Т-киллеры (секрктируют цитотоксические димфокины). Основная функция В- лимфоцитов заключается в том, что в ответ на антиген они способны размножаться и дифференцироваться в плазматические клетки, продуцирующие антитела. В – лимфоциты разделяются на две субпопуляции: 15 В1 и В2. В – клетки это долгоживущие В – лимфоциты, произошедшие из зрелых В – клеток в результате стимуляции антигеном при участии Т-лимфоцитов.
Иммунный ответ – это цепь последовательных сложных кооперативных процессов, идущих в иммунной системе в ответ на действие антигена в организме. Различают первичный и вторичный иммунный ответ, каждый из которых состоит из двух фаз: индуктивной и продуктивной. Далее иммунный ответ возможен в виде одного из трех вариантов: клеточный, гуморальный и иммунологическая толерантность. Антигены по происхождению: естественные, искусственные и синтетические; по химической природе: белки, углеводы (декстран), нуклеиновые кислоты, конъюгированные антигены, полипептиды, липиды; по генетическому отношению: аутоантиген, изоантигены, аллоантиген, ксеноантигены. Антитела – это белки, синтезирующиеся под влиянием антигена.
II. Клетки иммунной системы
Иммунокомпетентные клетки — это клетки, входящие в состав иммунной системы. Все эти клетки происходят из единой родоначальной стволовой клетки красного костного мозга. Все клетки делятся на 2 типа: гранулоциты (зернистые) и агранулоциты (незернистые).
К гранулоцитам относят:
нейтрофилы
эозинофилы
базофилы
К агранулоцитам:
макрофаги
лимфоциты (B, T)
Нейтрофильные
гранулоциты
или нейтрофилы,
сегментоядерные
нейтрофилы,
нейтрофильные
лейкоциты —
подвид гранулоцитарных
лейкоцитов,
названный нейтрофилами за то, что при
окраске
по Романовскому
они интенсивно окрашиваются как кислым
красителем эозином,
так и основными красителями, в отличие
от эозинофилов,
окрашиваемых только эозином, и от
базофилов,
окрашиваемых только основными
красителями.
Зрелые нейтрофилы имеют сегментированное ядро, то есть относятся к полиморфноядерным лейкоцитам, или полиморфонуклеарам. Они являются классическими фагоцитами: имеют адгезивность, подвижность, способность к хемостаксису, а так же способность захватывать частицы (например, бактерии).
Зрелые сегментоядерные нейтрофилы в норме являются основным видом лейкоцитов, циркулирующих в крови человека, составляя от 47% до 72% общего количества лейкоцитов крови. Ещё 1—5% в норме составляют юные, функционально незрелые нейтрофилы, имеющие палочкообразное сплошное ядро и не имеющие характерной для зрелых нейтрофилов сегментации ядра — так называемые палочкоядерные нейтрофилы.
Нейтрофилы способны к активному амёбоидному движению, к экстравазации (эмиграции за пределы кровеносных сосудов), и к хемотаксису (преимущественному движению в направлении мест воспаления или повреждения тканей).
Нейтрофилы способны к фагоцитозу, причём являются микрофагами, то есть способны поглощать лишь относительно небольшие чужеродные частицы или клетки. После фагоцитирования чужеродных частиц нейтрофилы обычно погибают, высвобождая большое количество биологически активных веществ, повреждающих бактерии и грибы, усиливающих воспаление и хемотаксис иммунных клеток в очаг. Нейтрофилы содержат большое количество миелопероксидазы, фермента, который способен окислять анион хлора до гипохлорита — сильного антибактериального агента. Миелопероксидаза как гем-содержащий белок имеет зеленоватый цвет, что определяет зеленоватый оттенок самих нейтрофилов, цвет гноя и некоторых других выделений, богатых нейтрофилами. Погибшие нейтрофилы вместе с клеточным детритом из разрушенных воспалением тканей и гноеродными микроорганизмами, послужившими причиной воспаления, формируют массу, известную как гной.
Повышение доли нейтрофилов в крови называется относительным нейтрофилёзом, или относительным нейтрофильным лейкоцитозом. Повышение абсолютного числа нейтрофилов в крови называется абсолютным нейтрофилёзом. Снижение доли нейтрофилов в крови называется относительной нейтропенией. Снижение абсолютного числа нейтрофилов в крови обозначается как абсолютная нейтропения.
Нейтрофилы играют очень важную роль в защите организма от бактериальных и грибковых инфекций, и сравнительно меньшую — в защите от вирусных инфекций. В противоопухолевой или антигельминтной защите нейтрофилы практически не играют роли.
Нейтрофильный ответ (инфильтрация очага воспаления нейтрофилами, повышение числа нейтрофилов в крови, сдвиг лейкоцитарной формулы влево с увеличением доли «юных» форм, указывающий на усиление продукции нейтрофилов костным мозгом) — самый первый ответ на бактериальные и многие другие инфекции. Нейтрофильный ответ при острых воспалениях и инфекциях всегда предшествует более специфическому лимфоцитарному. При хронических воспалениях и инфекциях роль нейтрофилов незначительна и преобладает лимфоцитарный ответ (инфильтрация очага воспаления лимфоцитами, абсолютный или относительный лимфоцитоз в крови).
Эозинофильные
гранулоциты
или эозинофилы,
сегментоядерные
эозинофилы,
эозинофильные
лейкоциты
— подвид гранулоцитарных
лейкоцитов
крови.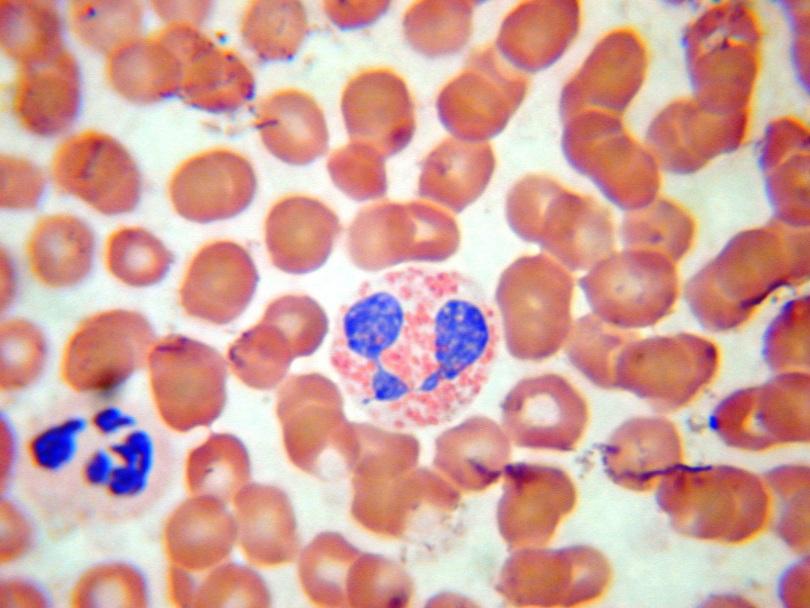
Эозинофилы названы так потому, что при окраске по Романовскому интенсивно окрашиваются кислым красителем эозином и не окрашиваются основными красителями, в отличие от базофилов (окрашиваются только основными красителями) и от нейтрофилов (поглощают оба типа красителей). Так же отличительным признаком эозинофила является двудольчатое ядро (у нейтрофила оно имеет 4-5 долей, а у базофила не сегментировано).
Эозинофилы способны к активному амебоидному движению, к экстравазации (проникновению за пределы стенок кровеносных сосудов) и к хемотаксису (преимущественному движению в направлении очага воспаления или повреждения ткани).
Эозинофилы, как и нейтрофилы, способны к фагоцитозу, причём являются микрофагами, то есть способны, в отличие от макрофагов, поглощать лишь относительно мелкие чужеродные частицы или клетки. Однако, эозинофил не является "классическим" фагоцитом, его главная роль не в фагоцитозе. Главнейшее их свойство - экспрессия Fc-рецепторов, специфичных для Ig E. Физиологически это проявляется в мощных цитотоксических, а не фагоцитарных, свойствах эозинофилов, и их активном участии в противопаразитарном иммунитете. Однако, повышенная продукция антител класса E может привести к аллергической реакции немедленного типа (анафилактический шок), что является главным механизмом всех аллергий такого типа.
Также эозинофилы способны поглощать и связывать гистамин и ряд других медиаторов аллергии и воспаления. Они также обладают способностью при необходимости высвобождать эти вещества, подобно базофилам. То есть эозинофилы способны играть как про-аллергическую, так и защитную анти-аллергическую роль. Процентное содержание эозинофилов в крови увеличивается при аллергических состояниях.
Эозинофилы менее многочисленны, чем нейтрофилы. Большая часть эозинофилов недолго остаётся в крови и, попадая в ткани, длительное время находится там.
Нормальным уровнем для человека считается 120—350 эозинофилов на микролитр.
Базофильные
гранулоциты
или базофилы,
сегментоядерные
базофилы,
базофильные
лейкоциты —
подвид гранулоцитарных
лейкоцитов.
Содержат базофильное S-образное ядро,
зачастую не видимое из-за перекрытия
цитоплазмы гранулами гистамина и прочих
аллергомедиаторов. Базофилы названы
так за то, что при окраске
по Романовскому
интенсивно поглощают основной
краситель и не окрашиваются кислым
эозином,
в отличие и от эозинофилов,
окрашиваемых только эозином, и от
нейтрофилов,
поглощающих оба красителя.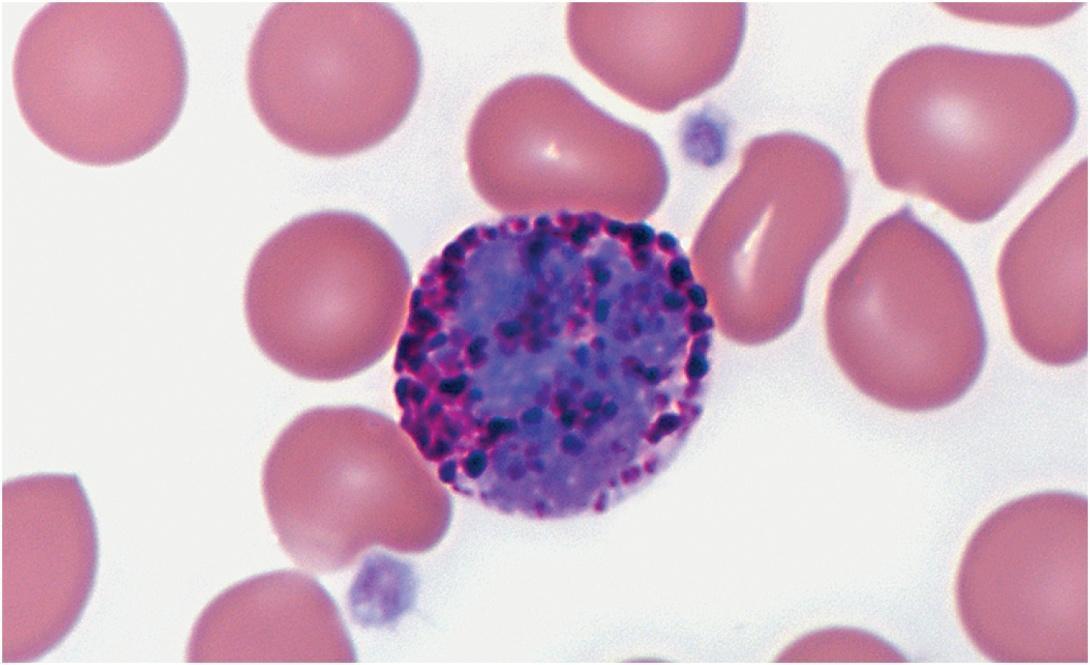
Базофилы — очень крупные гранулоциты: они крупнее и нейтрофилов, и эозинофилов. Гранулы базофилов содержат большое количество гистамина, серотонина, лейкотриенов, простагландинов и других медиаторов аллергии и воспаления.
Базофилы принимают активное участие в развитии аллергических реакций немедленного типа (реакции анафилактического шока). Существует заблуждение, что базофилы являются предшественниками лаброцитов. Тучные клетки очень похожи на базофилов. Обе клетки имеют грануляцию, содержат гистамин и гепарин. Обе клетки также выделяют гистамин при связывании с иммуноглобулином Е. Это сходство заставило многих предположить, что тучные клетки и есть базофилы в тканях. Кроме того, они имеют общий предшественник в костном мозге. Тем не менее базофилы покидают костный мозг уже зрелым, в то время как тучные клетки циркулируют в незрелом виде, только со временем попадают в ткани. Благодаря базофилам яды насекомых или животных сразу блокируются в тканях и не распространяются по всему телу. Также базофилы регулируют свертываемость крови при помощи гепарина. Однако исходное утверждение всё же верно: базофилы являются прямыми родственниками и аналогами тканевых лаброцитов, или тучных клеток. Подобно тканевым лаброцитам, базофилы несут на поверхности иммуноглобулин E и способны к дегрануляции (высвобождению содержимого гранул во внешнюю среду) или аутолизу (растворению, лизису клетки) при контакте с антигеном-аллергеном. При дегрануляции или лизисе базофила высвобождается большое количество гистамина, серотонина, лейкотриенов, простагландинов и других биологически активных веществ. Это и обусловливает наблюдаемые проявления аллергии и воспаления при воздействии аллергенов.
Базофилы способны к экстравазации (эмиграции за пределы кровеносных сосудов), причём могут жить вне кровеносного русла, становясь резидентными тканевыми лаброцитами (тучными клетками).
Базофилы
обладают способностью к хемотаксису
и фагоцитозу.
Кроме того, по всей видимости, фагоцитоз
не является для базофилов ни основной,
ни естественной (осуществляемой в
естественных физиологических условиях)
активностью. Единственная их функция
- мгновенная дегрануляция, ведущая к
усилению кровотока, увеличению
проницаемости сосудов. росту притока
жидкости и прочих гранулоцитов. Другими
словами, главная функция базофилов
заключается в мобилизации остальных
гранулоцитов в очаг воспаления.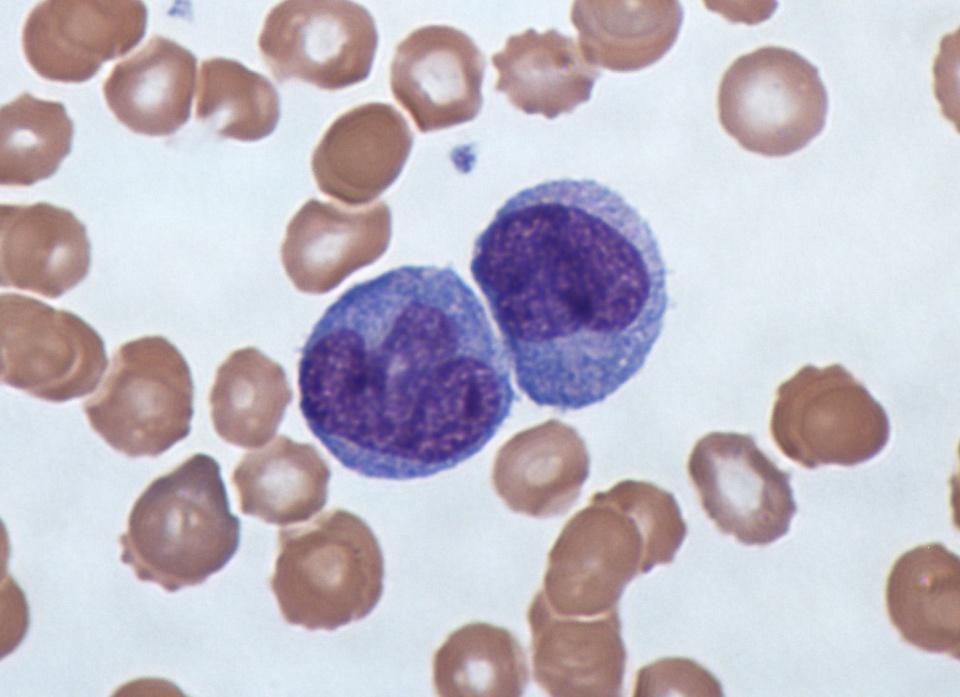
Моноцит - крупный зрелый одноядерный лейкоцит группы агранулоцитов диаметром 18—20 мкм с эксцентрично расположенным полиморфным ядром, имеющим рыхлую хроматиновую сеть, и азурофильной зернистостью в цитоплазме. Как и лимфоциты, моноциты имеют несегментированное ядро. Моноцит — наиболее активный фагоцит периферической крови. Клетка овальной формы с крупным бобовидным, богатым хроматином ядром (что позволяет отличать их от лимфоцитов, имеющих округлое тёмное ядро) и большим количеством цитоплазмы, в которой имеется множество лизосом.
Помимо крови, эти клетки всегда присутствуют в больших количествах в лимфатических узлах, стенках альвеол и синусах печени, селезенки и костного мозга.
Моноциты находятся в крови 2-3 дня, затем они выходят в окружающие ткани, где, достигнув зрелости, превращаются в тканевые макрофаги — гистиоциты. Моноциты также являются предшественниками клеток Лангерганса, клеток микроглии и других клеток, способных к переработке и представлению антигена.
Моноциты обладают выраженной фагоцитарной функцией. Это самые крупные клетки периферической крови, они являются макрофагами, то есть могут поглощать относительно крупные частицы и клетки или большое количество мелких частиц и как правило не погибают после фагоцитирования (возможна гибель моноцитов при наличии у фагоцитированного материала каких-либо цитотоксических для моноцита свойств). Этим они отличаются от микрофагов — нейтрофилов и эозинофилов, способных поглощать лишь относительно небольшие частицы и как правило погибающих после фагоцитирования.
Моноциты способны фагоцитировать микробов в кислой среде, когда нейтрофилы неактивны. Фагоцитируя микробов, погибших лейкоцитов, поврежденные клетки тканей, моноциты очищают место воспаления и подготавливают его для регенерации. Эти клетки образуют отграничивающий вал вокруг неразрушаемых инородных тел.
Активированные моноциты и тканевые макрофаги:
осуществляют противоопухолевый, противовирусный, противомикробный и противопаразитарный иммунитет, производяцитотоксины,интерлейкин(ИЛ-1),фактор некроза опухоли(ФНО),интерферон
участвуют в регуляции гемопоэза(кроветворения)
принимают участие в формировании специфического иммунного ответа организма.
Моноциты, выходя из кровяного русла, становятся макрофагами, которые наряду с нейтрофилами являются главными «профессиональными фагоцитами». Макрофаги, однако, значительно больше по размерам и дольше живут, чем нейтрофилы. Клетки-предшественницы макрофагов — моноциты, выйдя из костного мозга, в течение нескольких суток циркулируют в крови, а затем мигрируют в ткани и растут там. В это время в них увеличивается содержание лизосом и митохондрий. Вблизи воспалительного очага они могут размножаться делением.
Моноциты способны, эмигрировав в ткани, превращаться в резидентные тканевые макрофаги. Моноциты также способны, подобно другим макрофагам, выполнять процессинг антигенов и представлять антигены Т-лимфоцитам для распознавания и обучения, то есть являются антигенпрезентирующими клетками иммунной системы.
Макрофаги — это большие клетки, активно разрушающие бактерии. Макрофаги в больших количествах накапливаются в очагах воспаления. По сравнению с нейтрофилами моноциты более активны в отношении вирусов, чем бактерий, и не разрушаются во время реакции с чужеродным антигеном, поэтому в очагах воспаления вызванного вирусами гной не формируется. Также моноциты накапливаются в очагах хронического воспаления.
Моноциты секретируют растворимые цитокины, оказывающие воздействие на функционирование других звеньев иммунной системы. Цитокины, секретируемые моноцитами, называют монокинами.
Моноциты синтезируют отдельные компоненты системы комплемента. Они распознают антиген и переводят его в иммуногенную форму (презентация антигена).
Моноциты
продуцируют как факторы,
усиливающие свертывание крови
(тромбоксаны,
тромбопластины),
так и факторы, стимулирующие фибринолиз
(активаторы
плазминогена).
В отличие от В-
и Т-лимфоцитов,
макрофаги и моноциты не способны к
специфическому распознаванию антигена.
T-лимфоциты, или Т-клетки — лимфоциты, развивающиеся у млекопитающих в тимусе из предшественников — претимоцитов, поступающих в него из красного костного мозга. В тимусе T-лимфоциты дифференцируются, приобретая Т-клеточные рецепторы (TCR) и различные ко-рецепторы (поверхностные маркеры). Играют важную роль в приобретённом иммунном ответе. Обеспечивают распознавание и уничтожение клеток, несущих чужеродные антигены, усиливают действие моноцитов, NK-клеток, а также принимают участие в переключении изотипов иммуноглобулинов (в начале иммунного ответа B-клетки синтезируют IgM, позже переключаются на продукцию IgG, IgE, IgA).
Типы Т-лимфоцитов:
Т-клеточные рецепторыявляются основными поверхностными белковыми комплексами Т-лимфоцитов, ответственными за распознавание процессированных антигенов, связанных с молекуламиглавного комплекса гистосовместимостина поверхностиантигенпрезентирующих клеток. Т-клеточный рецептор связан с другим полипептидным мембранным комплексом,CD3. В функции CD3 комплекса входит передача сигналов в клетку, а так же стабилизация Т-клеточного рецептора на поверхности мембраны. Т-клеточный рецептор может ассоциироваться с другими поверхностными белками, TCRкорецепторами. В зависимости откорецептораи выполняемых функций различают два основных типа Т клеток.
Т-хелперы
Т-хелперы- Т-лимфоциты, главной функцией которых является усиление адаптивного иммунного ответа. Активируют Т-киллеры,B-лимфоциты,моноциты, NK-клетки при прямом контакте, а также гуморально, выделяяцитокины. Основным признаком Т-хелперов служит наличие на поверхности клетки молекулыкорецептораCD4. Т-хелперы распознают антигены при взаимодействии их Т-клеточного рецептора с антигеном, связанным с молекулами главного комплекса гистосовместимости II класса.
Т-киллеры
Т-киллеры, цитотоксические T-лимфоциты, CTL - Т-лимфоциты, главной функцией которых является уничтожение повреждённых клеток собственного организма. Мишени Т-киллеров — это клетки, поражённые внутриклеточными паразитами (к которым относятся вирусы и некоторые виды бактерий), опухолевые клетки. Т-киллеры являются главным компонентом антивирусного иммунитета. Основным признаком Т-киллеров служит наличие на поверхности клетки молекулыкорецептораCD8. Т-киллеры распознают антигены при взаимодействии их Т-клеточного рецептора с антигеном, связанным с молекулами главного комплекса гистосовместимости I класса.
Т-хелперы и Т-киллеры образуют группу эффекторных Т-лимфоцитов, непосредственно ответственных за иммунный ответ. В то же время существует другая группа клеток, регуляторные Т-лимфоциты, функция которых заключается в регулировании активности эффекторных Т-лимфоцитов. Модулируя силу и продолжительность иммунного ответа через регуляцию активности Т-эффекторных клеток, регуляторные Т-клетки поддерживают толерантность к собственным антигенам организма и предотвращают развитие аутоиммунных заболеваний. Существуют несколько механизмов супрессии: прямой, при непосредственном контакте между клетками, и дистантный, осуществляющийся на расстоянии — например, через растворимые цитокины.
γδ Т-лимфоциты
γδ
Т-лимфоциты представляют собой небольшую
популяцию клеток с видоизмененным
Т-клеточным рецептором. В отличие от
большинства других Т-клеток, рецептор
которых образован двумя α и β субъеденицами,
Т-клеточный рецептор γδ лимфоцитов
образован γ и δ субъеденицами. Данные
субъеденицы не взаимодействуют с
пептиднымиантигенами презентированными MHC
комплексами. Предполагается, что γδ
Т-лимфоциты участвуют в узнаваниилипидныхантигенов.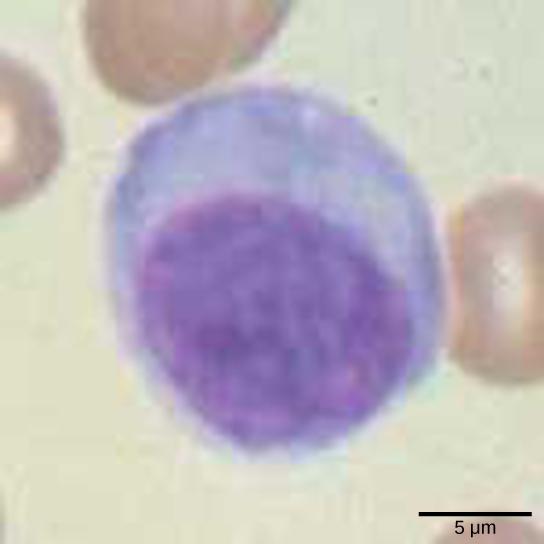
B-лимфоциты (B-клетки, от bursa fabricii птиц, где впервые были обнаружены) — функциональный тип лимфоцитов, играющих важную роль в обеспечении гуморального иммунитета. При контакте с антигеном или стимуляции со стороны T-клеток некоторые B-лимфоциты трансформируются в плазматические клетки, способные к продукции антител. Другие активированные B-лимфоциты превращаются в B-клетки памяти. Помимо продукции антител, В-клетки выполняют множество других функций: выступают в качестве антигенпрезентирующих клеток, продуцируют цитокины и экзосомы.
У эмбрионов человека и других млекопитающих B-лимфоциты образуются в печени и костном мозге из стволовых клеток, а у взрослых млекопитающих — только в костном мозге. Дифференцировка В-лимфоцитов проходит в несколько этапов, каждый из которых характеризуется присутствием определённых белковых маркеров и степенью генетической перестройки генов иммуноглобулинов.
Различают следующие типы зрелых В-лимфоцитов:
Собственно В-клетки (ещё называемые «наивными» В-лимфоцитами) — неактивированные В-лимфоциты, не контактировавшие с антигеном. Не содержат тельца Голла, вцитоплазмерассеянымонорибосомы. Полиспецифичны и имеют слабое сродство к многим антигенам.
В-клетки памяти — активированые В-лимфоциты, вновь перешедшие в стадию малых лимфоцитов в результате кооперации с Т-клетками. Являются долгоживущим клоном В-клеток, обеспечивают быстрый иммунный ответи выработку большого количества иммуноглобулинов при повторном введении того же антигена. Названы клетками памяти, так как позволяют иммунной системе «помнить» антиген на протяжении многих лет после прекращения его действия. В-клетки памяти обеспечивают долговременный иммунитет.
Плазматические клетки — являются последним этапом дифференцировки активированных антигеном В-клеток. В отличие от остальных В-клеток несут мало мембранных антител и способны секретировать растворимые антитела. Являются большими клетками с эксцентрично расположенным ядром и развитым синтетическим аппаратом - шероховатый эндоплазматический ретикулумзанимает почти всю цитоплазму, также развит иаппарат Гольджи. Являются короткоживущими клетками (2-3 дня) и быстро элиминируются при отсутствии антигена, вызвавшего иммунный ответ.
Характерной
особенностью В-клеток является наличие
поверхностных мембраносвязанных
антител, относящихся к классам IgM и IgD.
В комплексе с другими поверхностными
молекулами иммуноглобулины формируют
антигенраспознающий рецептивный
комплекс, ответственный за узнавание
антигена. Также на поверхности
В-лимфоцитов расположены антигены МНС
класса II,
важные для взаимодействия с Т-клетками,
также на некоторых клонах В-лимфоцитов
присутствует маркер CD5,
общий с Т-клетками. Рецепторы компонентов
комплемента
C3b (Cr1, CD35) и C3d (Cr2, CD21) играют определённую
роль в активации В-клеток. Следует
отметить, что маркеры CD19,
CD20 и CD22 используются для идентификации
В-лимфоцитов. Также на поверхности
В-лимфоцитов обнаружены Fc
рецепторы.
Натуральные киллеры - большие гранулярные лимфоциты, обладающие цитотоксичностью против опухолевых клеток и клеток, зараженных вирусами. В настоящее время NK-клетки рассматривают как отдельный класс лимфоцитов. NK выполняют цитотоксические и цитокин-продуцирующие функции. NK являются одним из важнейших компонентов клеточного врождённого иммунитета. NK формируются в результате дифференцировки лимфобластов (общих предшественников всех лимфоцитов). Они не имеют Т-клеточных рецепторов, CD3 или поверхностных иммуноглобулинов, но обычно несут на своей поверхности маркеры CD16 и CD56 у людей или NK1.1/NK1.2 у некоторых линий мышей. Около 80 % NK несут CD8.
Эти клетки были названы естественными киллерами, поскольку, по ранним представлениям, они не требовали активации для уничтожения клеток, не несущих маркеров главного комплекса гистосовместимости I типа.
Основная функция NK — уничтожение клеток организма, не несущих на своей поверхности MHC1 и таким образом недоступных для действия основного компонента противовирусного иммунитета — Т-киллеров. Уменьшение количества MHC1 на поверхности клетки может быть следствием трансформации клетки в раковую или действием вирусов, таких как папилломавирус и ВИЧ.
Макрофаги, нейтрофилы, эозинофилы, базофилы и натуральные киллеры обеспечивают прохождение врождённого иммунного ответа, который является неспецифичным.
