
Khimia / Химия / ХИМИЯ НОВЫЕ ЛАБЫ / лаба 14 / Опыт 3,4
.docОпыт №3. Активизирующие свойства хлора на коррозию.
Поместили в две пробирки по кусочку алюминия и по 10 капель 0.5 н. раствора сульфата меди и по 3 капли 0.2 н. раствора серной кислоты. В одну из пробирок добавили 3 капли 3%-ного раствора хлорида натрия.
1 пробирка: Al+CuSO4+H2SO4+NaCl
2 пробирка: Al+CuSO4+H2SO4
Наблюдали контактное выделение меди на поверхности алюминия в виде черноватого налета и в следствии этого обесцвечивание раствора.
2Al+3CuSO4=Al2(SO4)3+3Cu
A
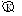 l│H2SO4│Al2O3
l│H2SO4│Al2O3
Также наблюдали образование пузырьков водорода.
A: Al-3e=Al3+ K: 2H++2e=H2, Cu2++2e=Cu
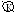

Al│H2SO4, NaCl│CuSO4
Ионы, разрушающие защитные пленки металлов и тем самым способствующие коррозии, называют активаторами коррозии. В данном опыте активатором коррозии является ион хлора. Из этого следует, что в первой пробирке процессы протекают интенсивнее, т.к. присутствуют ионы хлора.
Опыт №4. Коррозия в результате различного доступа кислорода к поверхности металла (атмосферная коррозия).
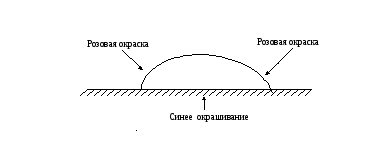
Очистили стальную пластину наждачной бумагой. На чистую поверхность нанесли каплю специального реактива – ферроксилиндикатора (состоящий из фенолфталеина ( индикатор на гидроксильные ионы) и красной кровяной соли (индикатор на ионы двухвалентного железа – синее окрашивание)). Через 10 минут наблюдали появление синей окраски (свидетельствует о наличии Fe2+) в центре капли и розовой (свидетельствует о наличии OH-) по окружности.
F
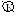 e│H2O,
O2│FeO
e│H2O,
O2│FeO
A: Fe-2e=Fe2+
K: O2+H2O+4e=4OH-
Из-за различного доступа кислорода к поверхности металла возникают участки с различными потенциалами, т.е. образуется гальванопара. Катодные участки с наиболее положительным потенциалом возникают возле краев капли, куда легче проникает кислород. Анодные участки с наиболее отрицательным потенциалом возникают в центре капли, защищенные каплей электролита.
Fe2++2OH-=Fe(OH)2
4Fe(OH)2+O2+2H2O=4Fe(OH)3
Fe(OH)3=FeO(OH)+H2O
