
Release Final
.pdf
атомної маси ядра) – 2, 10, 18, 36. Магічні числа для кластерів: 2, 18, 40. Електронні магічні числа відповідають випадку, коли верхній енергетичний рівень структури (нанокластера) повністю заповнений.
Теорія молекулярних орбіталей для кластерів атомів.
Альтернативна (моделі желе) модель, що використовується для розрахунків властивостей кластерів, розглядає їх як молекули і використовує для обчислень існуючі теорії молекулярних орбіталей, такі як теорія функціоналів густини.
Коли молекула складається з багатьох атомів і містить багато електронів, задача стає досить складною, і для її рішення використовуються багато наближених методів. Теорія функціоналів густини є одним з таких підходів.
Структуру з найменшою енергією можна знайти обчислювальними методами, що і визначає рівноважну геометрію молекули. Такі методи молекулярних орбіталей з деякими змінами можуть бути використані і для металічних наночастинок.
У теорії МО передбачається, що електронні хвильові функції окремих атомів комбінуються, утворюючи молекулярні хвильові функції (або, як їх ще називають, молекулярні орбіталі). Ці орбіталі, які тепер делокалізовані навколо всієї молекули, заселяються всіма доступними електронами усіх атомів, що входять до складу молекули. В дійсності ж молекулярні орбіталі утворюються тільки з хвильових функцій електронів найдальших від ядра оболонок (валентних електронів), тобто з тих, які істотно перекриваються при зближенні атомів одна з одною. Електронні орбіталі внутрішніх оболонок приблизно збігаються з атомними орбиталями ізольованих атомів.
Для одноелектронної молекули рівняння Шредінгера може бути вирішено аналітично, що дає набір молекулярних хвильових функцій , які описують молекулярні орбіталі і залежать від квантового числа , яке задає момент імпульсу відносно осі, що проходить через ядра. За аналогією з класифікацією атомних орбіталей (АО) через значення моменту імпульсу l: s, р, d і т. д., МО можна класифікувати як , ,  у відповідності до значення = 0, 1, 2. Дуже просто, -МО утворюється при перекриванні (насправді як лінійна комбінація) АО паралельних до осі зв'язку, а -МО утворюється при перекриванні АО перпендикулярних до осі зв'язку.
у відповідності до значення = 0, 1, 2. Дуже просто, -МО утворюється при перекриванні (насправді як лінійна комбінація) АО паралельних до осі зв'язку, а -МО утворюється при перекриванні АО перпендикулярних до осі зв'язку.
Опис молекулярних орбіталей і діаграма енергетичних рівнів іона Н+2:
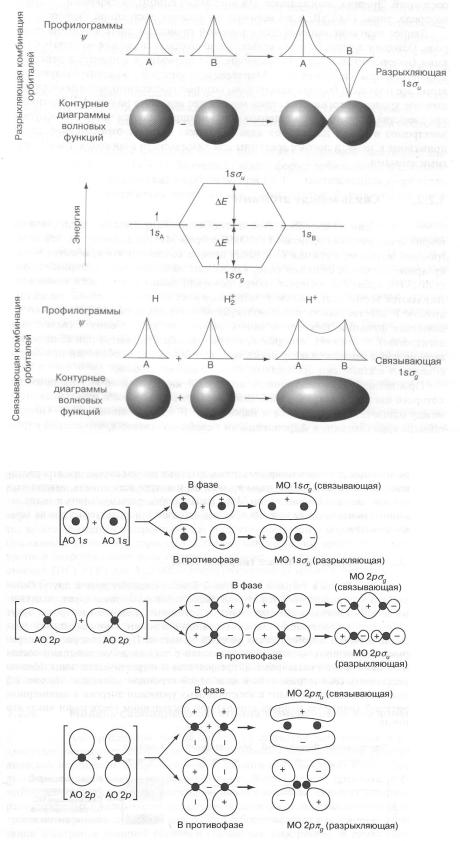
Утворення молекулярних орбіталей у виді лінійної комбінації атомних орбіталей; знаки «+» и «—» показують знаки (фази) хвильових функцій:
Діаграма електронних рівнів енергії все більш довгого ланцюжка атомів, що показує перетворення молекулярних орбіталей в енергетичні зони одновимірного кристалла:
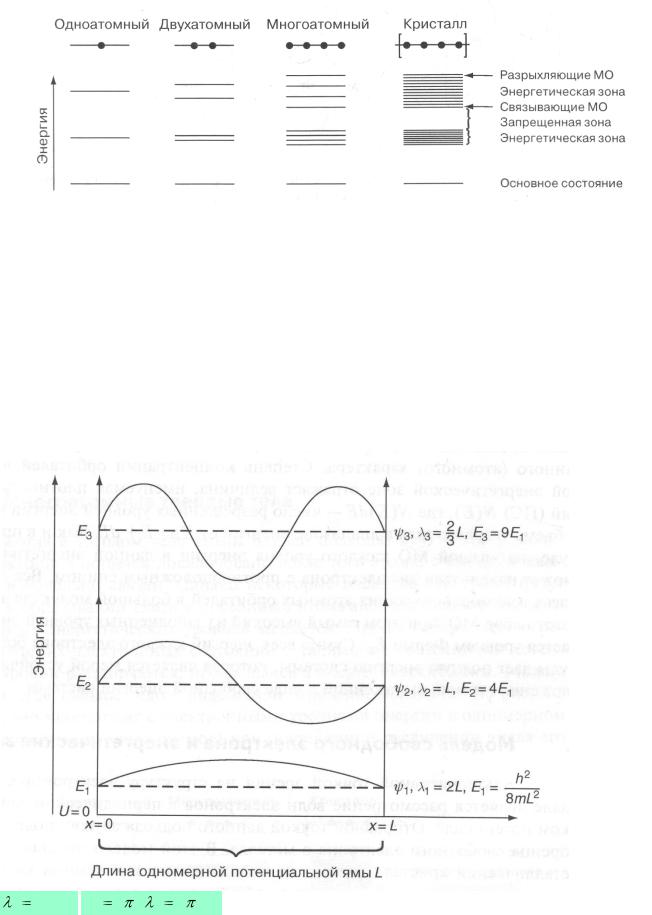
Сума всіх енергій кожного електрона великої молекули дає повну енергію системи, яка є мірою стійкості розташування атомів, що виражена у вигляді вільної енергії системи.
Подивіться також З1.djvu.
(92) (60) Модель вільного електрона і енергетичні зони. Зонна діаграма кластерів з малої кількості атомів.
Під час відповіді на це питання, будь ласка, ознайомтесь також з попереднім в частині молекулярних орбіталей (МО).
Альтернативною точкою зору на структуру електронних зон в кристалі є розгляд хвиль електронів в періодичному кристалічному потенціалі. Відправною точкою даного підходу служить модель вільного електрона в металі (модель Друде-Лоренца).
Діаграма рівнів енергії, на якій показані деякі допустимі хвильові функції електрона, обмеженого в одномірній потенціальній ямі:
n 2L / n, kn 2 / n n / L.
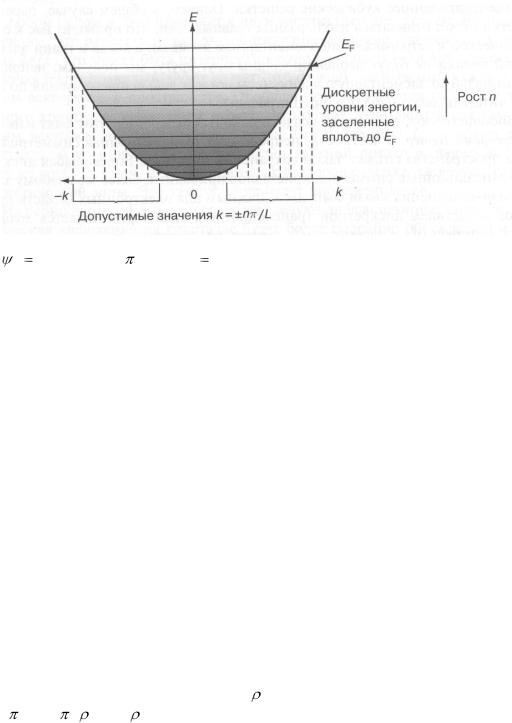
Схематична версія квадратичної залежності між допустимими електронними хвильовими векторами і їх енергією для електронів, обмежених у одновимірній потенціальній ямі. Затінені області енергій зображують ті рівні, які зайняті електронами:
|
|
|
|
|
n2 h2 |
. |
|
n |
(2 / L)1/ 2 sin(n x / L), |
|
En |
||||
|
|
|
|
||||
|
|
|
|
|
8mL2 |
|
|
|
|
|
|
||||
|
У моделі вільних |
електронів показано, що енергії електронних станів залежать від 1/L2, |
|||||
де |
L - характерний розмір |
системи. Відстань між сусідніми рівнями також змінюється |
|||||
пропорційно 1/L2.
Основний ефект, внесений цими змінами в об'ємні електронні структури, полягає у зміні повної енергії, а отже, нехтуючи ентропійних фактором, і в зміні термодинамічної стабільності систем з нанометровими характерними розмірами в порівнянні із звичайними об'ємними кристалами. Цей ефект може мати безліч наслідків. Може змінитися найбільш стабільна форма даного матеріалу. Наприклад, дрібні наночастинки або нанометрові шари можуть прийняти кристалічну структуру, яка відрізняється від звичайного об'ємного матеріалу. Так, про деякі метали, що звичайно перебувають у формі гексагональної щільно упакованої атомної структури, повідомляється, що в обмежених системах типу металевих мультишарів вони приймають гранецентровану структуру. Прийняття нової кристалографічної структури при зменшенні характерного розміру до якогось критичного значення викликано відповідною зміною густини електронних станів і часто супроводжується зниженням повної енергії системи.
Зменшення розмірів системи може змінити хімічну реактивність, яка є функцією структури та заселеності найбільш високих електронних рівнів енергії. Відповідно можуть змінюватися електричні, теплові, оптичні та магнітні властивості, також залежні від розташування самих верхніх заселених електронних рівнів енергії.
І відношення площі поверхні до об'єму (S/V), і питома площа поверхні (м2/г) системи обернено пропорційні розміру частинки і тому стають надзвичайно великими, коли діаметр частинок виявляється меншим 100 нм. Для ізольованої сферичної частинки радіусом r,
виготовленої з матеріалу густиною , площа поверхні на одиницю маси матеріалу дорівнює
4 r2/(4/3 r3 ) = 3/r .
Якщо атом знаходиться на поверхні, то очевидно, що кількість атомів-сусідів менша, ніж у такого ж атома в об'ємі, а значить, у нього буде інше зв'язування (що призводить до відомих понять поверхневого натягу та поверхневої енергії) і інша електронна структура.
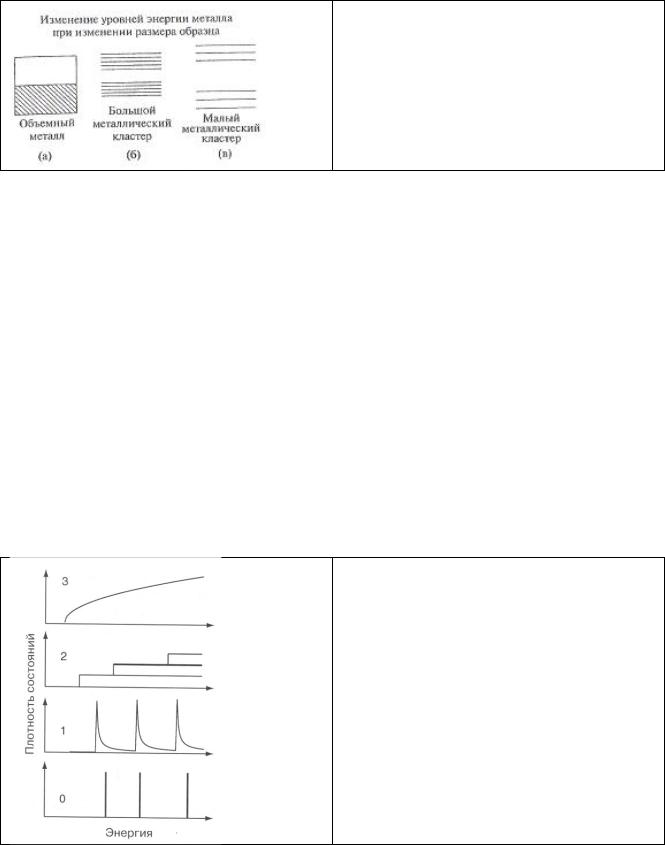
Приклад зміни рівнів енергії металу при зменшенні кількості атомів: (а) – валентна зона об’ємного металу; (б) – у великому кластері із 100 атомів виникає заборонена зона; (в) – маленький кластер, що складається з трьох атомів.
Коли частка металу зменшується в розмірах до декількох сотень атомів, густина станів у зоні провідності - верхній зоні, яка містить електрони, радикально змінюється. Безперервна густина станів у зоні замінюється набором дискретних рівнів, інтервали між якими можуть опинитися більше, ніж теплова енергія кВт, що приводить до утворення щілини.
Зрештою, можна зменшити кластер до розмірів, при яких відстань між протилежними гранями наблизиться до довжини хвилі електрона. У такому випадку енергетичні рівні можуть бути отримані шляхом розгляду квантової задачі про частку в потенційному ящику. Це називається квантовим розмірним ефектом.
(115) Густина електронних станів в наноструктурах.
Показано, що у випадку об'ємного матеріалу густини станів повинна бути пропорційна Е1/2. Однак густина станів сильно змінюється при зменшенні розмірів системи, оскільки в цьому випадку також відбувається і зменшення ступенів свободи простору хвильових векторів. Проста теорія, для випадків чисто три-, дво- і одномірних систем, дає густину станів, пропорційну kn-2, де n - розмірність системи, тому для параболічних зон густина станів пропорційна Е(n-2)/2. В разі квазімалорозмірних систем, таких як квантові ями або квантові дроти, в яких через квантові обмеження утворюється набір підзон, густина станів пропорційна Е(n-2)/2 для кожної з підзон в окремо, як показано на рис. 3.14. В разі квантових точок, квантово обмежених у всіх трьох вимірах, не існує неперервного розподілу станів, і тому залежність густини станів приймає вигляд спектра дискретних значень енергії, показаний на нижньому рис. 3.14. Він схожий на спектр випромінювання окремого атома.
Рис. 3.14. Густина електронних станів об'ємного напівпровідника (3D), квантової ями (2D), квантового дроту (1D) і квантової точки (0D).
Багато оптичних та електронних властивостей наноструктур залежать від густини станів, отже, вони також сильно залежать від обмежень розмірів.
Читайте також shark007.narod.ru
(63) Як змінюються оптичні спектри поглинання при зменшенні розмірів наночастинок?
Презентація 01.ppt слайди 42. 43 Презентація 05 pp28-30 Презентація 06.ppt слайди 19 20 21 Лекция Лозовского №3, слайд 19
(80) Визначення магнітного моменту в досліді Штерна-Герлаха.
Опыт Штерна-Герлаха, экспериментально подтвердивший, что атомы обладают магнитным моментом, проекция которого на направление внешнего магнитного поля принимает лишь определённые значения (пространственно квантована). Осуществлен в 1922 О. Штерном и немецким физиком В. Герлахом (W. Gerlach), которые исследовали прохождение пучка атомов Ag (а затем и др. элементов) в сильно неоднородном магнитном поле (см. рис.) с целью проверки теоретически полученной формулы пространств. квантования проекции mz на направление Z магнитного момента атома mo: mz=mom (т =0±1,...).
На атом, обладающий магнитным моментом и движущийся в неоднородном вдоль Z магнитном поле Н, действует сила F= mzдН/дZ, которая отклоняет его от первоначального направления движения. Если проекция магнитного момента атома могла бы изменяться непрерывно, то на пластинке П наблюдалась бы размытая широкая полоса. Однако в Ш.— Г. о. было обнаружено расщепление пучка атомов на 2 компоненты, симметрично смещенные относительно первичного направления распространения на величину D — на пластинке появлялись две узкие полосы. Это указывало на то, что проекция магнитного момента атома mz на направление поля Н принимает только два отличающиеся знаком значения ±mo, т. е. mo ориентируется вдоль Н и в противоположном направлении. Величина магнитного момента атома mо, измеренная в опыте по смещению D, оказалась равной магнетону Бора.
(82) (83) (84) Сили Ван дер Ваальса. Потенціал Ленарда-Джонса. Конденсація Бозе.
Презентація 06.ppt слайди 26-29.
(110)Типи напівпровідників.
Презентація 03.ppt слайди 2-8 16 17 http://shark007.narod.ru/3/b3v2.htm
(111)(112) (113) Квантові ями, дроти, точки.
Презентація 03.ppt слайди 19-25
(114) Надгратки.
Презентація 03.ppt слайди 26 27 Лекции Лозовского
(117) (119) Електрично наведені точки та дроти. Модуляційне легування.
Презентація 03.ppt слайди 43 44 Презентація 05.ppt слайди 1-6
(121) (122) (123) (124) (125). Резонансне тунелювання. Ефект зарядки. Кулонівська блокада. Балістичне перенесення носіїв. Ефект Ааронова-Бома.
Презентація 05.ppt слайди 15-23
Ефект Ааронова-Бома – чисто квантовий ефект взаємодії електричного поля з зарядами в областях простору, де напруженість електричного поля дорівнює нулю. Ефект виникає внаслідок того, що кванова механіка оперує узагальненим потенціалом електромагнітного

поля, що може не дорівнювати нулеві, навіть якщо звична нам напруженість поля в цій точці таки нуль.
(120) Квантовий ефект Холла.
Презентація 05.ppt слайди 7-9 http://shark007.narod.ru/16/b16v2.htm
(126) (127) Всерединозонне, міжзонне поглинання в напівпровідникових наноструктурах.
Презентація 05.ppt слайди 24-30
(128) Процеси світловипромінювання в наноструктурах.
Презентація 05.ppt слайди -20, 31-36
(129)Фононне горло в квантових точках.
Презентація 05.ppt слайди 24, 37-39
(130)(131) Квантово-обмежений еффект Штарка. Нелінійні ефекти.
Презентація 05.ppt слайди 40-43
(56)Які основні властивості наноматеріалів?
Презентація 01.ppt слайди 5, 33,
(57)В чому проявляються квантово-розмірні ефекти в наноматеріалах?
Презентація 01.ppt слайди 27, 44 Презентація 03.ppt слайди 18, 31 Презентація 05.ppt слайди 8-10
(93) Рівняння Холла-Петча.
Багато властивостей є безперервною функцією розмірів системи. Рівняння Холла-Петча визначає межу текучості матеріалу як функцію середнього розміру зерна <d>:
k d |
1/ 2 |
, |
де k і 0 - константи. |
0 |
Хімія наночастинок. Отримання наночастинок.
(9) (10) (65) Фотофрагментація. Кулонівський вибух.
Презентація 06.ppt слайди 22-24
З1.djvu – 91+ стр.
(14) (15) (16) (17) Синтез наночастинок: високочастотний індукційний нагрів, термоліз. Імпульсний лазерний метод отримання наночастинок. Хімічні методи синтезу наночастинок.
Презентація 06.ppt слайди 32-36 Презентація 02.ppt слайди 23, 33-41
З1.djvu – 96+ стр.
(69) Навести приклади не вуглецевих шароподібних молекул.
L04-NM-Evtukh-1.ppt слайди 21
Возможно ли существование шарообразных молекул из других атомов, например, кремния или азота? Исследователи в Японии сумели создать корзинообразные структуры из кремния.
Однако в отличие от углерода один лишь кремний не может образовывать замкнутые структуры. Исследователи показали, что кремний может формировать замкнутую структуру вокруг атома вольфрама в виде гексагональной клетки.
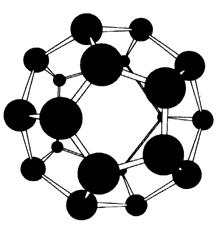
Потенциальными применениями таких структур являются компоненты квантовых компьютеров, химические катализаторы и новые сверхпроводники. Существуетмножество предсказанных на основе вычислений молекулярных орбиталей стабильных замкнутых структур из других атомов. Например, методом функционала плотности показано, что кластер N20 должен быть стабильными иметь додекаэдрическую структуру, показанную на
рис. 17.10. Вычисления также показали, что этот кластер будет очень мощным взрывчатым веществом, примерно в 3 раза мощнее наиболее энергоемких современных материалов. Однако синтез N20 может оказаться очень сложным.
Рис. 17.10. Предсказанная структура молекулы N20, вычисленная на основе теории функционала плотности
(96) (97) Нанотехнології. Процеси зверху-вниз та знизу-вверх. Подрібнення матеріалів.
Презентація 02.ppt слайди 2-3, 13
+ будь ласка, скористайтесь матеріалами з хімії наноматеріалів, там все толково.
Презентація 02_2013_sposobi_poluchenia_o.ppt
(6) (61) (94) Хімічні властивості наночастинок. Реакційна здатність металів при зменшенні розмірів кластерів.
Презентація 01.ppt слайди 37.38 Презентація 06.ppt слайди 12.13
З1.djvu – 85стр.
Фізика наночастинок. Оптичні, електричні властивості.
(4) (58) Геометрична структура нанокластерів.
Презентація 01.ppt слайди 28. 34.35 Презентація 06.ppt слайди 6-8
З1.djvu – 80стр.
(5) (59) Електронна структура нанокластерів.
Презентація 01.ppt слайди 27.28.30.31.44.
Презентація 06.ppt слайди 9-11
З1.djvu – 83стр.
(7)Магнітні кластери.
Презентація 01.ppt слайди 28. 34.35 Презентація 06.ppt слайди 6-8
З1.djvu – 87стр.
(8)Оптичні властивості напівпровідникових наночастинок.
Презентація 01.ppt слайди 42. 43 Презентація 06.ppt слайди 19 20 21
З1.djvu – 90стр.
(11)Кластери інертних газів.
Презентація 06.ppt слайди 25 26
З1.djvu – 93стр.
(12)Надтекучі кластери.
Презентація 06.ppt слайди 27 28 29
З1.djvu – 94стр.
(13)Молекулярні кластери.
Презентація 06.ppt слайди 30 31
З1.djvu – 95стр.
(76) Описати електричні властивості наночастинок.
Презентація 05 слайди 58+ Презентація 02 слайди 46 Презентація 01 слайди 47
(88) Залежність коеф-ту поглинання світла металевими частинками від довжини світла.
Презентація 01.ppt слайд 42
(95) Оптичні властивості наночастинок.
Презентація 01.ppt слайди 42. 43 Презентація 06.ppt слайди 19 20 21
(50) (173) (186) Металічні нанокластери в складі скла.
08. L05-NM-Evtukh-1.ppt слайди 26-29 З1.djvu с. 136-139
Тонкі плівки, пористі матеріали. Літографія та напилення.
(98) Літографія.
Презентація 02.ppt слайди 6,7,8.9.10.11 Презентація 03.ppt слайди 36
(99) М’яка літографія.
Презентація 02.ppt слайди 9,10
(100)Методи осадження з газової фази.
Презентація 02.ppt слайди 14 15 16 19
(101)(102) (103) Плазмове осадження. Тліючий розряд постійного струму. Магнетронне напилення. Вакуумне дугове напилення.
Презентація 02.ppt слайди 20-22
(104) (105) Молекулярно-променева епітаксія (МПЕ). Метал-органічна газо фазова епітаксія (МОГФЕ).
Презентація 02.ppt слайди 25-31 Презентація 03.ppt слайди 35 http://shark007.narod.ru/1/b1v3.htm
(106)Колоїдні методики.
Презентація 02.ppt слайди 35-37 Презентація 03.ppt слайди 48
(107)Методи шаблонного росту наноматеріалів.
Презентація 02.ppt слайди 42-44
(116) Вирощування на краю відколу.
Презентація 03.ppt слайди 37 38
(108) (118) Самоорганізація. Самозбирання, використання в синтезі наночастинок.
Презентація 02.ppt слайди 45 48-50 Презентація 03.ppt слайди 49 - 61
(51) (71) (72) (174) (196) Пористий кремній. Властивості. Технології формування.
Нанохімія Гринь
08. L05-NM-Evtukh-1.ppt слайди 30+
Наноструктуровані матеріали.
(41)(164) (194) Об’ємні наноструктуровані матеріали.
08. L05-NM-Evtukh-1.ppt слайди 2
З1.djvu с. 124
(42)(43) (44) (165) (166) (167) Розупорядкована твердотільна структура. Метод компактування. Охолодження розплаву спінінгуванням. Газова атомізація.
08. L05-NM-Evtukh-1.ppt слайди 3-7 З1.djvu с. 124-126
(45)(46) (169) Механічні властивості наноструктурованих матеріалів. Механізми розрушення полікристалічних матеріалів.
08. L05-NM-Evtukh-1.ppt слайди 8-13
Лекція 01 слайд 39
З1.djvu с. 127-129
(47) (170) Наноструктуровані багатошарові матеріали.
08. L05-NM-Evtukh-1.ppt слайди 14-16
