
Сборник методичек по физике - УГНТУ / Гусманова10
.pdfМинистерство образования и науки Российской Федерации
Государственное образовательное учреждение высшего профессионального образования
«УФИМСКИЙ ГОСУДАРСТВЕННЫЙ НЕФТЯНОЙ
ТЕХНИЧЕСКИЙ УНИВЕРСИТЕТ»
Кафедра физики
ТЕПЛОЕМКОСТЬ ИДЕАЛЬНОГО ГАЗА.
МЕТОД КЛЕМАНА-ДЕЗОРМА ДЛЯ
ОПРЕДЕЛЕНИЯ ОТНОШЕНИЯ CP/CV
Учебно-методическое пособие к лабораторным работам
по молекулярной физике
2-1
УФА 2010
Учебно-методическое пособие предназначено для студентов всех форм обучения и содержит краткие сведения по теории и описание порядка выполнения лабораторной работы по разделу “Молекулярная физика”.
Составители: Гусманова Г.М., доц., канд. хим. наук Сафиуллина А.Г., доц., канд. хим. наук
Рецензент |
Лейберт Б.М., доц., канд. техн. наук |
Уфимский государственный нефтяной технический университет, 2010

ЛАБОРАТОРНАЯ РАБОТА 2-1
"Теплоемкость идеального газа. Метод Клемана-Дезорма для
определения отношения Cp/Cv"
Цель работы: изучить молекулярно-кинетическую теорию теплоемкости,
определить отношение теплоемкости воздуха при постоянном давлении к теплоемкости при постоянном объеме.
Приборы и принадлежности: стеклянный баллон, U-образный манометр,
вакуумный насос.
ТЕОРИЯ МЕТОДА Внутренняя энергия представляет собой энергию всех видов
внутренних движений в теле (системе) и энергию взаимодействия всех частиц (атомов, молекул, ионов и т. д.), входящих в тело (систему). При вычислении изменения внутренней энергии учитывают ту ее часть, которая не остается постоянной в исследуемых процессах. Под внутренней энергией газа понимают кинетическую энергию движения молекул газа и потенциальную взаимодействия молекул между собой.
Идеальным газом называется газ, взаимодействиями между молекулами которого можно пренебречь. Таким образом, потенциальная энергия взаимодействия молекул идеального газа не учитывается.
Числом степеней свободы i называется число независимых координат
(уравнений), с помощью которых можно однозначно определить положение молекулы (тела) в пространстве. Для одноатомной молекулы i = 3, для двухатомной - i= 5, для трехатомной (и далее многоатомной) - i = 6.
Внутренней энергией идеального газа называется сумма кинетических энергий беспорядочного движения всех его молекул, которая равна:
U i m RT
2 M

где i - число степеней свободы, т — масса газа, М - молярная масса,
R = 8,31 Дж/(моль-К) - универсальная газовая постоянная, Т -
термодинамическая температура.
Внутренняя энергия является функцией состояния, т.е. не зависит от вида перехода из одного состояния в другое (процесса), а зависит лишь от параметров начального и конечного состояний системы.
V 2
Работа газа равна A pdV
V 1
где р - давление, dV- бесконечно малое изменение объема.
Теплота и работа не являются функциями состояния, т.е. зависят от вида перехода из одного состояния в другое (процесса).
Первое начало термодинамики является законом сохранения энергии для тепловых процессов: количество теплоты, переданное системе,
расходуется на приращение внутренней энергии системы и совершение системой работы:
dQ = dU+dA
Иногда имеются отличия в записи малых величин теплоты, работы и приращения внутренней энергии, которые отражают зависимость теплоты
δQ и работы δА от вида перехода из одного состояния в другое (процесса), а
изменения внутренней энергии dU - только от начального и конечного состояний системы.
Теплоемкостью называется величина, равная количеству теплоты,
которое требуется передать телу, чтобы изменить его температуру на единицу (на 1К - в СИ). Единицей измерения теплоемкости является 1 Дж/К.
C dQdT
Удельной теплоемкостью называется величина, равная количеству теплоты, которое требуется передать единице массы m (1кг - в СИ) газа,
чтобы изменить его температуру на единицу (на 1К - в СИ), т. е.

теплоемкость единицы массы вещества. Единицей измерения удельной теплоемкости является 1 Дж/(кгК).
c C dQ m mdT
Молярной теплоемкостью называется величина, равная количеству теплоты, которое требуется передать единице количества вещества v (l молю в СИ), чтобы изменить его температуру на единицу (на 1К - в СИ), т. е.
теплоемкость 1 моля вещества. Единицей измерения молярной теплоемкости является 1 Дж/(моль-К).
Nm C dQ
dT
Процесс, происходящий без теплообмена с окружающей средой,
называется адиабатическим. В этом случае dQ=0, следовательно, первое начало термодинамики для него принимает вид
dU = - dA.
При этом работа совершается газом за счет убыли его внутренней энергии.
В адиабатическом процессе все термодинамические параметры р, V и Т меняются. Их можно связать уравнением Пуассона:
pVγ=const
или соотношениями TVγ-1=const, Tp(1-γ)/γ=const
где γ- показатель адиабаты, равный Cp i 2 , - уравнениями
Cv i
адиабатического процесса.
В адиабатном процессе работу можно рассчитать по формуле:
V 2 |
V 2 |
pV |
|
pV |
|
V |
|
1 |
|
||
A |
pdV |
1 |
|
dV |
1 1 |
|
[1 ( |
1 |
) |
|
] |
V |
|
1 |
|
|
|||||||
V 1 |
V 1 |
|
|
V |
|
|
|
||||
|
|
|
|
|
|
|
|
2 |
|
|
|
По первому началу термодинамики при постоянном объеме dA = О, и
вся подводимая системе теплота идет на увеличение его внутренней энергии,
т.е. dQ= dU. Поэтому молярная теплоемкость при постоянном объеме равна
Nv ( dQ )v dU i R
dT dT 2
По первому началу термодинамики при постоянном давлении вся подводимая системе теплота идет на увеличение его внутренней энергии и совершение работы, т.е. dQ = dU + dA. Поэтому молярная теплоемкость при постоянном давлении равна
Np ( |
dQ |
) p |
dU pdV |
Cv R |
i 2 |
R |
dT |
dT |
|
||||
|
|
2 |
|
|||
Или Cp=Cv+R.Этоуравнение называется уравнением Майера.
Молярная теплоемкость при постоянной температуре Ст равна:
NT dQdT
Молярная теплоемкость в адиабатном процессе Сад равна:
dQ
Naa dT 0
Таким образом, в молекулярно-кинетической теории теплоемкость принимает различные значения в зависимости от типа процесса.
ОПИСАНИЕ МЕТОДА Метод Клемана-Дезорма по определению отношения теплоемкостей
базируется на измерении давления газа в одном и том же сосуде,
последовательно проходящего через три состояния: из первого во второе газ переходит адиабатически, из второго в третье - изохорически (рис. 1).
p
1
p1
3'
|
|
3 |
||
h2' |
|
3'' |
||
|
|
|
h2" |
|
p 2 |
|
|
|
|
|
|
|
|
|
2' |
2 |
2'' |
||
0  V
V
V1 |
V2 |
Рис. 1. Зависимость давления газа Р от объема V для изучаемой массы газа
Рассмотрим это более подробно.
В стеклянный баллон нагнетается воздух до давления Р1 которое превышает атмосферное давление Р0 на величину Р', то есть
Р1=Р0+Р' и Р'«Р0.
После установления термодинамического равновесия с окружающей средой температура газа в баллоне будет Т1. Таким образом, начальное состояние газа определяется параметрами Р1, V1, T1. Затем баллон на короткое время соединяют с атмосферой, при этом давление в баллоне падает до значения Р2, равного атмосферному: Р2 = Ро .
Этот процесс расширения газа происходит достаточно быстро, поэтому теплообменом с окружающей средой через стенки баллона можно пренебречь и считать процесс адиабатическим. Воздух в баллоне перейдет в состояние 2 с параметрами P2, V2, Т2 , причем V2 > V1 и Т2 < Т1. При адиабатическом расширении часть воздуха выходит в атмосферу, поэтому необходимо иметь в виду, что V1 - это объем воздуха в состоянии 1,
несколько меньший объема баллона.
Связь между состояниями 1 и 2 определяется уравнением Пуассона:

|
|
p1V1 |
p2V2 |
, |
(1) |
||
с другой стороны, по уравнению состояния идеального газа |
|
||||||
. |
|
p1V1 |
|
p2V2 |
|
|
(2) |
|
|
|
|
||||
|
T1 |
T2 |
|
||||
|
|
|
|
||||
|
Подставив отношение V1/V2 |
из (2) в (1), получим зависимость между |
|||||
давлением и температурой газа в этих состояниях: |
|
||||||
( |
p1 |
) 1 ( |
T1 |
) |
(3) |
|
|
||||
|
p2 |
. |
|||
|
|
T2 |
|
||
В дальнейшем, после закрытия клапана, воздух в баллоне изохорически нагревается до температуры окружающей среды Т1 а давление повысится до значения Р3, которое превысит атмосферное Р0 на небольшую величину Р",
то есть воздух переходит в состояние 3 с параметрами P3,V2,T1, при этом
Р3= Р0 + Р" и Р" « Р0.
Связь.между состояниями 2 и 3 находим из уравнения изохорического
|
p2 |
|
p3 |
|
|
процесса: |
T2 |
(4) |
|||
|
|||||
|
|
T1 |
|||
Из формул (3) и (4) с учетом того, что Р1 = Р0 + Р', а Р3 = Р0 + Р", получаем
( |
p0 p' |
) 1 ( |
p0 p" |
) |
|||||
|
|
|
|
|
|||||
|
p0 |
, |
|||||||
|
p0 |
||||||||
|
(1 |
p' |
) 1 (1 |
|
p" |
) |
|||
|
|
|
|||||||
|
|
p0 |
. |
||||||
|
|
|
p0 |
||||||
Так как Р"«Р0 и Р'« Р0, то, разлагая оба двучлена в ряд и ограничиваясь членами первого порядка, получаем
1 ( 1) p' 1 p" |
, |
|
p0 |
p0 |
|
откуда
|
|
p' |
(5) |
|
p' p" |
||||
|
|
Измеряя давление водяным манометром и учитывая, что давление р столба жидкости пропорционально плотности жидкости ρ и высоте столба жидкости в манометре h, давление в сосуде перед открытием клапана Р' и давление,
установившееся при тепловом равновесии, после закрытия клапана Р" можно выразить следующим образом:
p'=pgh1 |
p"=pgh2 , |
(6) |
где g - ускорение свободного падения.
Подставляя уравнение (6) в уравнение (5), получим расчетную формулу для определения:
|
|
h1 |
|
|
|
|
. |
h1 h2 |
. |
(7) |
|||
|
||||||
|
|
|
||||
Однако практически невозможно добиться, чтобы длительность открывания клапана τ в точности совпала бы со временем его адиабатического расширения, которое рассматривается в работе. Этот процесс всегда быстропротекающий в реальных условиях, поэтому
длительность открывания клапана необходимо выбрать предельно
малой (τ = 0). Если перекрыть баллон раньше, чем давление упадет до атмосферного, то получим завышенное значение Р" (или h2),
соответствующее отрезку 2'-3' (см.рис.1). Наоборот, при запаздывании получается заниженное значение h2", соответствующее отрезку 2"- 3".
Поэтому найдем h2 графически, как в момент сразу после открытия
клапана, продолжив прямую до пересечения с осью ординат. Давление р
со |
временем |
t |
в |
откачиваемом |
сосуде |
падает, |
поэтому |
p-(p+dp)=Apdt, где А - константа. Так как давление р столба жидкости
пропорционально плотности жидкости ρ и высоте столба жидкости в

манометре h p= ρ gh , то, сократив нa ρg и интегрируя h от h2 до h2", a t от 0 до
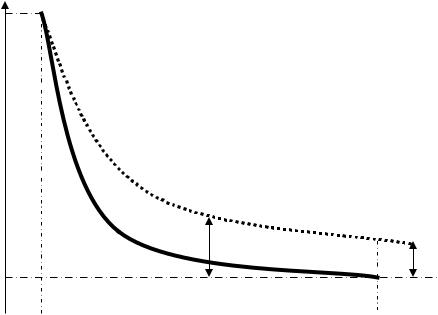
τ, получим: ln h2"= ln h2-Аτ. Поэтому чтобы рассчитать точное значение длительности открывания клапана τ строят график зависимости ln h2" от τ. На рис. 2 представлен график зависимости ln h2" от τ. Графическое определение величины h2 показано на рис. 2 (см. п.5 главы "Порядок выполнения работы").
ln h2"
ln h2
ln h2
0
τ, с
Рис. 2. Графическое определение величины h2
ОПИСАНИЕ УСТАНОВКИ
Одно колено жидкостного (водяного) манометра открыто, а другое соединено с сосудом, поэтому, когда сосуд соединен с атмосферой, уровни
К
Н
Б
М
Рис. 3. Схема экспериментальной установки
