
- •А.М.Сыркин, н.Е.Максимова, л.Г.Сергеева химия воды
- •Утверждено Редакционно-издательским советом угнту
- •2. Строение молекул воды
- •3. Структура воды
- •4. Физические свойства воды
- •5. Изотопный состав воды
- •6. Химические свойства воды
- •7. Строение водных растворов
- •8. Структура воды на твердых поверхностях
- •9. Характеристика природных вод
- •10. Химический состав природных вод
- •Изменение содержания отдельных ионов от солесодержания в воде [1, 2]
- •11. Воды нефтяных и газовых месторождений
- •Классификация природных вод в.А. Сулина [1] по типам
- •12. Сточные воды
- •13. Значение воды в нефтяной промышленности
- •14. Показатели качества и химический анализ воды
- •15. Отложение солей при добыче нефти
- •16. Основные методы очистки воды
- •17. Очистка сточных вод
- •18. Лабораторные работы
- •18.1. Лабораторная работа «Методы определения жесткости»
- •18.2. Лабораторная работа «Методы умягчения воды»
- •18.3. Лабораторная работа «Качественный анализ химического состава воды»
- •Описание качественных реакций на ионы
- •18.4. Лабораторная работа «Химиический анализ состава пластовой воды»
- •19. Задачи и упражнения
- •Задачи для самостоятельного решения
- •Варианты заданий самостоятельной работы
- •Редактор л.А.Маркешина
18.3. Лабораторная работа «Качественный анализ химического состава воды»
Цель работы. Изучение качественных реакций на ионы Ca2+, Mg2+, SO42–,
Cl–, CO32–, S2– и открытие их в пробе.
Описание качественных реакций на ионы
Обнаружение Ca2+
а) к 1-2 каплям раствора CaCl2 добавьте 1-2 капли раствора (NH4)2C2O4. Наблюдайте помутнение раствора вследствие образования Са2С2О4;
б) на предметном стекле поместите каплю раствора CaCl2 и добавьте каплю 2 н раствора H2SO4; слегка упарьте до появления каемки по краям капли. Образовавшиеся кристаллы рассмотрите в микроскоп. Сделайте выводы. Сравните с рис. 12;
Рис.12.Кристаллы
CaSO4∙2H2O,
образующиеся
из
разбавленных
растворов
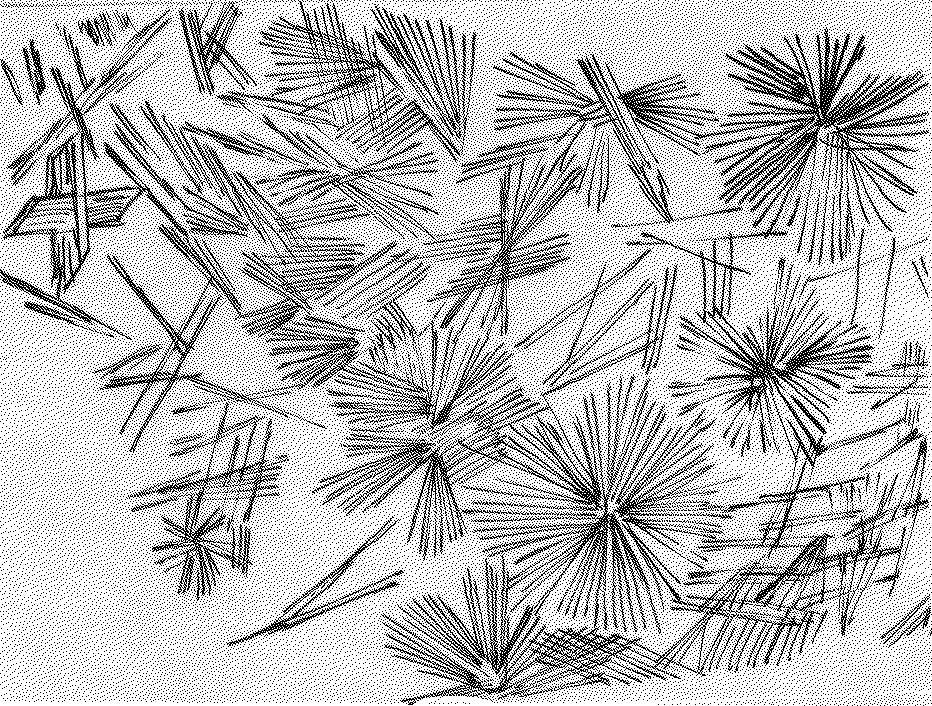
в) к 1-2 каплям раствора соли кальция СаCl2 добавьте по капле раствор NH4OH и NH4Cl, нагрейте и осадите примерно равным объёмом насыщенного раствора K4[Fe(CN)6]. Проверьте растворимость осадка в 2 н уксусной кислоте.
Обнаружение Mg2
а) к капле раствора MgCl2 или MgSO4 добавьте каплю 5%-го аммиачного раствора оксихинолина. Наблюдайте образование зеленоватого осадка оксихинолината магния;
б) к одной капле раствора MgCl2 добавьте I каплю NH4Cl и кристаллик Na2HPO4. Наблюдайте образование характерного кристаллического осадка MgNH4PO4. Рассмотрите кристаллы в микроскоп. Сравните с рис. 13.
Рис. 13. Кристаллы
MgNH4PO4∙6H2O,
образующиеся при быстрой кристаллизации
Обнаружение Cl– К капле NaCl добавьте 1 каплю раствора AgNO3. Наблюдайте образование осадка.
Обнаружение SO42– К 1 капле Na2SO4 добавьте 1 каплю раствора BaCl2. Что наблюдается?
Обнаружение CО32 –К 1 капле Na2CO3 добавьте каплю концентрированной HCl. Какой газ выделяется?
Обнаружение S2– К 1 капле раствора сульфида натрия добавить 1 каплю соли свинца. Объясните наблюдаемое явление.
Выполнение работы. Используя соответствующие реактивы, проделайте качественные реакции на ионы Са2+, Mg2+, SO42_, CO32_, S2_, Cl_. Все реакции выполняйте на часовых или предметных стеклах. Запишите уравнения в молекулярном и ионном виде. Составьте таблицу по форме:
|
Изучаемые ионы |
Используемые реактивы |
Цвет и структура осадков | |||||
|
|
|
|
|
|
| ||
|
Ca2+ |
|
|
|
|
|
|
|
|
Mg2+ |
|
|
|
|
|
|
|
|
SO42– |
|
|
|
|
|
|
|
|
CO32– |
|
|
|
|
|
|
|
|
S2– |
|
|
|
|
|
|
|
|
Cl– |
|
|
|
|
|
|
|
В соответствующую клеточку впишите формулу вещества, отметьте цвет и структуру осадка (плотный, рыхлый, мелкокристаллический, хлопьевидный и т.д.).
