
- •Занятие 2. Биохимия твердых тканей зуба
- •2. Состав и функции дентина. Особенности биохимии дентина. Неорганические и органические компоненты дентина. Белки дентина: коллаген 1 типа, фосфосиалопротеины, фосфорин. Несовершенный дентиногенез.
- •3. Вода – 13%.
- •3. Биохимия цемента. Виды цемента: бесклеточный (первичный) и клеточный (вторичный), их состав и функции. Органический матрикс цемента - коллагены I, II, III, V, XII и XIV типов.
- •4. Состав и функции пульпы. Коллагеновые и неколлагеновые (остеопонтин, остеонектин, интегрины, амелогенины, щелочная фосфатаза и другие) белки пульпы.
Занятие 2. Биохимия твердых тканей зуба
1. Состав и функции эмали. Особенности биохимии зубной эмали. Неорганические компоненты эмали. Минеральные вещества эмали: кристаллы апатитов и другие. Структура кристалла гидроксиапатита, соотношение кальций/фосфор. Органические компоненты эмали. Особенность аминокислотного состава белков эмали. Белки эмали (амелогенины, энамелины, тафтелины и КСБЭ (кальций связывающие белки эмали). Несовершенный амелогенез.
Эмаль покрывает коронку зуба. Это самая плотная и твердая ткань организма, которая по твердости подобна кварцу. Функция эмали заключается в защите дентина и пульпы зуба от внешних повреждающих факторов, избирательная проницаемость.
Особенностью эмали является то обстоятельство, что сразу после ее формирования она утрачивает клетки - главные носители жизни. Зрелая эмаль становится объектом воздействия различных факторов. Не имея своих клеток, она поддерживает нормальное состояние в течениедлительного времени. Эмаль отличается еще и тем, что это самая твердая ткань. По шкале твердости она приближается к кварцу.
Соотношение кальция к фосфору 2:1 или 33,6-39,4 и 16,1-18,0%
Неорганические компоненты эмали
В молочных зубах неорганический компонент эмали составляет примерно 80%, а в зрелой эмали – 96 – 97%.
Зрелая эмаль включает следующие компоненты:
1. неорганические компоненты – 96 – 97%;
2. органические компоненты – 0,4 – 0,8%;
3. вода.
Вода эмали бывает двух видов:
1. свободная вода – это вода, которая испаряется при высушивании зубов;
2. связанная, или кристаллическая, вода – это вода, которая составляет гидратную оболочку кристаллов апатитов.
Структурной единицей эмали являются кристаллы апатитов, образующие эмалевые призмы. Чем четче границы кристаллов, тем больше степень минерализации эмали. Из кристаллов образуются эмалевые призмы. Кристаллы ориентированы перпендикулярно к поверхности эмали. Формирование и ориентация кристаллов эмали зависит от характера питания, но процентное соотношение кальция, фосфора и карбонатов является постоянной величиной. Содержание стронция и свинца в эмали сильно колеблется, так как зависит от их содержания в почве.
М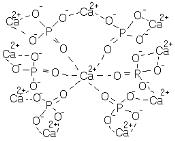 инеральные
вещества распределены в эмали неравномерно:
в поверхностных слоях преобладают
кальций, фтор, фосфаты, а в глубоких
слоях – натрий и магний. Равномерно
распределены стронций, медь, алюминий
и калий.
инеральные
вещества распределены в эмали неравномерно:
в поверхностных слоях преобладают
кальций, фтор, фосфаты, а в глубоких
слоях – натрий и магний. Равномерно
распределены стронций, медь, алюминий
и калий.
Минеральные вещества эмали:
1. кристаллы апатитов:
o гидроксиапатит – 75 %;
o карбонатапатит – 19%;
o хлорапатит – 4,4%;
o фторапатит – 0,66%;
2. другие минеральные вещества – примерно 2%.
Кристаллы эмали в 10 раз больше кристаллов дентина и костей.
К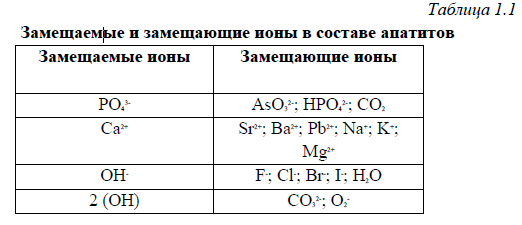 ристаллы
гидроксиапатита создают в эмали эффект
молекулярного сита, через которое в
эмалевую жидкость проходят ионы и
небольшие органические молекулы.
Эмалевая жидкость, или эмалевый ликвор,
- это жидкость внутри эмали. Поскольку
эмаль обладает проницаемостью, то
возможны изоморфные замещения всех
компонентов гидроксиапатитов.
ристаллы
гидроксиапатита создают в эмали эффект
молекулярного сита, через которое в
эмалевую жидкость проходят ионы и
небольшие органические молекулы.
Эмалевая жидкость, или эмалевый ликвор,
- это жидкость внутри эмали. Поскольку
эмаль обладает проницаемостью, то
возможны изоморфные замещения всех
компонентов гидроксиапатитов.
В норме эмаль находится в состоянии динамического равновесия между медленно протекающими процессами де- и реминерализации. В этих случаях свободные места в кристаллической решетке гидроксиапатитов занимают ионы, находящиеся в избытке. Так, за счет изоморфного замещения кальция гидроксиапатитов на хром, бром, магний величина коэффициента Са/Р уменьшается, что способствует развитию кариеса.
Образование карбонатапатитов Са10(РО4)5(СО3)(ОН)2 делает эмаль хрупкой и повышает кариесовосприимчивость.
При взаимодействии гидроксифторапатитов с ионами фтора образуются гидроксифторапатиты и фторапатиты:
Са10(РО4)6(ОН)2 + F- → Ca10(PO4)6F(OH) + OH-;
Ca10(PO4)6F(OH) + F- → Ca10(PO4)6F2 + OH-
В результате образования гидроксифторапатитов и фторапатитов повышается плотность кристаллической решетки эмали, уменьшается пространство между кристаллами эмали и уменьшается ее проницаемость. Это способствует повышению устойчивости эмали к неблагоприятным факторам внешней среды, например, к снижению рН.
Если в эмаль попадает фтор в высоких концентрациях, что обычно обусловлено его избыточным содержанием в воде, почве, то образуется фторид кальция CaF2, который практически не растворяется в воде и при значениях рН ротовой жидкости более 7,0 исчезает с поверхности зубов. При этом вместе с фтором эмаль теряет и кальций, что приводит к разрушению апатитов и возникновению о о .
При дефиците в организме кальция и фосфатов, который, может быть, при недостатке этих компонентов в продуктах питания или при нарушении их всасывания в кишечнике, активируются реакции изоморфного замещения. При этом кариесогенными элементами считаются селен, кадмий, марганец, свинец.
При поступлении в организм продуктов, обогащенных солями кальция, ускоряется выведение из организма стронция. Возможность изоморфного вытеснения чужеродного иона из апатита с помощью кальция используется при проведении реминерализующей терапии эмали.
К сильным кариесостатикам относятся фтор и фосфор, к средним – молибден, бор, медь, ванадий, литий, алюминий.
В направлении от поверхности эмали к эмалево-дентинной границе количество неорганических компонентов уменьшается.
Органические компоненты эмали
Органические вещества эмали располагаются между кристаллами апатитов в виде пучков, спиралей и пластинок. С возрастом в наружном слое эмали повышается содержание белка, и это приводит к снижению кариесорезистентности твердых тканей зуба.
Органический матрикс эмали включает небольшое количество углеводов, липидов и белков.
В живых организмах минерализация тканей, в том числе и эмали, осуществляется только на белковых матрицах. Для инициации роста кристаллов используются белки с небольшой молекулярной массой. Энамелобласты синтезируют высокомолекулярные гликофосфопротеины, которые в дальнейшем подвергаются частичному протеолизу, и образуются низкомолекулярные белки, которые могут связывать кальций и фосфаты.
Особенностью аминокислотного состава белков эмали является наличие большого количества таких аминокислот как серин, глутамат, аспартат и лизин, способных связывать кальций и фосфаты.
Большую часть белков эмали составляют амелогенины (90%), примерно 10% белков эмали приходится на энамелины, тафтелины и КСБЭ (кальций связывающие белки эмали).
● Амелогенины являются гликофосфопротеинами, содержащими 75% неорганических фосфатов. Эти белки характеризуются высоким содержанием пролина, глутамина, гистидина и лейцина.
● Энамелины – это гликофосфопротеины, связанный с минеральными компонентами эмали.
● Тафтелины – это гликофосфопротеины, участвующий в образовании центров кристаллизации на начальных стадиях минерализации эмали.
На эмбриональном этапе развития эмали соотношение амелогенинов к энамелину составляет 9:1, в то время как в зрелой эмали оно одинаковое – 1:1
Амелогенины играют ведущую роль в формировании и минерализации матрицы эмали, но быстро разрушаются.
В состав энамелинов и тафтелинов входят фосфорилированные остатки аминокислот, которые связывают кальций и фосфаты. Это приводит к образованию первичного кристалла, или первичной ячейки гидроксиапатита:
Белок – Сер-(СН2ОН) + АТФ → Белок-Сер-(СН2ОРО3Н2) + АДФ
(фермент - протеинкиназа).
Далее к фосфорилированным остаткам серина в составе белков присоединяются катионы кальция, а к ним – опять остатки фосфорной кислоты и кальция, то есть имеет место чередование «фосфат – кальций – фосфат- …». Это является первичным кристаллом.
Кроме серина, остатки лизина в белках могут присоединять фосфат по аминогруппе. В этом случае после реакции дефосфорилирования фосфаты могут использоваться для образования апатитов.
● Кальцийсвязывающие белки эмали (КСБЭ) содержат остатки гамма-карбоксиглутамата, к которому присоединяется кальций. Это необходимо для образования внутри- и межцепочечных кальциевых мостиков в белковой матрице, благодаря которым обеспечивается их правильная ориентация в матрице. Таким образом, белковая сетка эмали представляет собой трехмерную матрицу для минерализации.
Функции матрицы:
1. образование каркаса для связывания кальций-связывающих белков;
2. формирование трехмерной структуры для минерализации с помощью КСБЭ;
3. формирование центров кристаллизации с помощью КСБЭ, фосфолипидов и цитрата;
4. обеспечение ориентации, упорядоченности, регулярности и прочности образованной структуры.
Сетка, сформированная кальцием и КСБЭ, фиксируется на волокнах амелогенинов, что приводит к постепенной упорядоченной кристаллизации гидроксиапатитов и отложению новых кристаллов гидроксиапатитов.
Транспорт минеральных компонентов к эмали осуществляется в двух направлениях:
1. Пульпа → Дентин → Эмаль;
2. Слюна → Эмаль.
Перемещение ионов определяется величиной осмотического давления.
Несовершенный амелогенез
Несовершенный амелогенез – это наследственная дисплазия эмали зубов. Нарушение развития тканей зуба приводит к появлению различных дефектов. Причины:
1. локальные факторы: местное воспаление, травмы временных зубов;
2. системные повреждения: данные повреждения охватывают ряд зубов. Они возникают при инфекционных заболеваниях, а также при нарушениях метаболизма как у беременных женщин, так и у детей после рождения;
3. наследственные факторы: они характеризуются недоразвитием зубов и передаются из поколения в поколение.
Наследственные факторы несовершенного амелогенеза могут быть вызваны мутациями в генах белков эмали, нарушениями посттрансляционных модификаций, уменьшением синтеза и секреции амелобластами (энамелобластами) фосфолипидов и цитрата.
Кроме того, причинами несовершенного амелогенеза являются дефицит кальция и фосфатов, прием антибиотиков – ингибиторов биосинтеза белков. Так, в результате приема тетрациклина беременными женщинами и детьми раннего возраста нарушается минерализация эмали: она становится очень тонкой и даже практически отсутствует. Зубы становятся меньших размеров, серого и коричневого цвета (тет ик ино е б ).
Еще одним заболеванием, характеризующимся нарушением образования и структуры эмали, является флюороз зубов. Его причиной является избыток фтора. В больших дозах фтор угнетает пролиферацию амелобластов, биосинтез белков эмали, нарушает образование фосфосерина, так как может связываться с оксиметильной группой серина (-СН2ОН) и тем самым препятствовать ее фосфорилированию, что приводит к нарушению образования первичных кристаллов и минерализации эмали.
Кроме того, фтор ингибирует активность сериновых протеаз – ферментов, участвующих в реакциях частичного протеолиза высокомолекулярных белков эмали. Частичный протеолиз высокомолекулярных белков эмали необходим для формирования ограниченной матрицы и центров инициации минерализации.
Два вида гипоминерализации:
1) легкая форма, характеризующаяся наличием меловидных пятен на поверхности эмали;
2) тяжелая форма, характеризующаяся наличием темных пигментных пятен, которые возникают в результате того, что ионы железа и пищевые пигменты связываются с белками эмали, и в этих местах она окрашивается в желто-коричневый цвет.
Гипоксия плода также негативно сказывается на амелогенезе, так как в результате гипоксии уменьшается количество АТФ – источника фосфата для реакций фосфорилирования белков эмали. Это приводит к тому, что уменьшается связывание кальция с белками эмали, и нарушается ее минерализация.
