
- •Предисловие
- •1.1. Структура наполненных полимерных покрытий
- •1.2. Взаимодействие поверхности пигментов с компонентами пленкообразующих систем
- •1.3. Влияние пигментов на структуру и свойства лакокрасочных покрытий
- •2. Основы технологии производства пигментированных лакокрасочных материалов
- •2.1. Принципы выбора пигментов
- •2.3. Основы процесса диспергирования пигментов
- •2.4. Стабилизация пигментных дисперсий
- •3. Способы производства пигментированных лакокрасочных материалов
- •3.1. Пигментирование однофазных органорастворимых пленкообразующих систем
- •3.2. Пигментирование однофазных водоразбавляемых пленкообразующих систем
- •3.3. Пигментирование однофазных нелетучих пленкообразующих систем
- •3.4. Пигментирование двухфазных систем
- •3.5. Порошковые краски
- •3.6. Фляшинг-процесс
- •4. Основное оборудование для получения пигментированных лакокрасочных материалов
- •4.1. Диссольверы
- •4.2. Трехвалковые мельницы
- •4.3. Бисерные мельницы
- •4.6. Ультразвуковые диспергаторы и магнитная обработка при диспергировании пигментов
- •Заключение
- •Литература
- •Содержание
Значение Kд находят из уравнения aKд = ln a0 −t ln at .
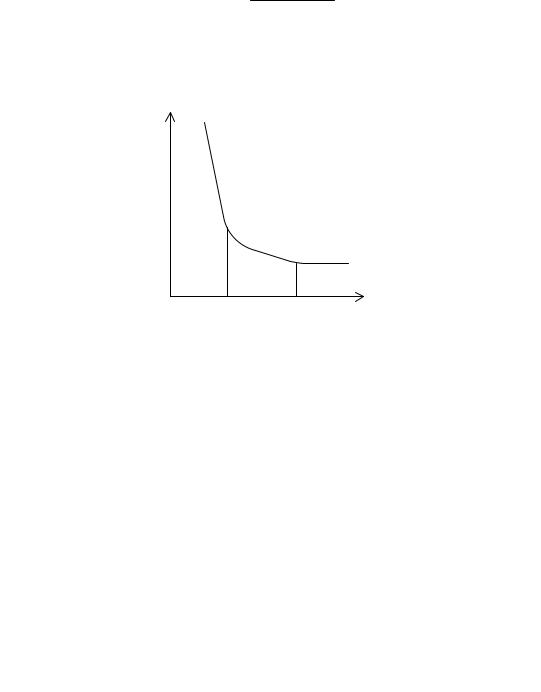
Процесс диспергирования протекает в две стадии (рис. 2.3). Каждая стадия характеризуется собственным коэффициентом скорости, причем Kд1 >> Kд2.
lna
I
II
Рис. 2.3. Изменение размера пигментных агрегатов а во время диспергирования
Для значительной продолжительности диспергирования (время стремится к бесконечности) уравнение дает конечное «нулевое» решение, что не соответствует действительности. В пределе диспергирование должно заканчиваться полным разрушением агрегатов до первичных частиц, свойственных данному пигменту. Практически в полидисперсных системах остаются наиболее прочные агрегаты и флокулы ранее уже диспергированных частиц. При этом устанавливается определенное адсорбционно-дисперсионное равновесие.
Малая эффективность второй стадии диспергирования очевидна, поэтому целесообразно прерывать процесс после завершения первой стадии. Если нужно получить более высокую дисперсность, то продолжать диспергирование следует в другом, более энергонапряжен- номоборудованииивизмененнойповерхностно-активнойсреде.
2.4. СТАБИЛИЗАЦИЯ ПИГМЕНТНЫХ ДИСПЕРСИЙ
Высокодисперсные суспензии термодинамически неустойчивы и склонны к самопроизвольному укрупнению частиц. При
63

хранении красок, получении и отверждении покрытий возникают скопления – сгустки пигментных частиц и участки покрытий, свободные от пигментов. Скопления мелких частиц оптически проявляют свойства крупных, при этом снижаются укрывистость, красящая способность, блеск, изменяется оттенок покрытий. Идет непроизводительная затрата пигментов, готовых лакокрасочных материалов и энергии.
Коллоидные частицы пигментов размером 0,1–0,5 мкм подвержены броуновскому движению. Сталкиваясь между собой под влиянием сил притяжения, они коагулируют, образуя агрегаты. Достигнув определенного размера, под влиянием силы тяжести агрегаты оседают, образуя плотный осадок – коагулят. Частицы, имеющие адсорбционные оболочки, могут слипаться своими оболочками – флокулировать. Флокуляция является частным случаем коагуляции, когда частицы дисперсной фазы образуют хлопья, соединяясь через прослойки – «мостики» межфазного адсорбционносольватного слоя.
Стремление дисперсной системы снизить запас поверхностной энергии вызывает самопроизвольный процесс укрупнения частиц путем агрегации. Это явление названо агрегативной неустойчивостью, в отличие от неустойчивости, обусловленной гравитационным разделением фаз путем осаждения частиц, коя зо-
вется кинетической, или седиментационной, неустойчивостью.
Разновидностью кинетической неустойчивости является процесс, противоположный осаждению, – всплывание, или миграция пигментов в слое краски. Этот процесс подобен флотации. Несмоченные частицы или флокулы выносятся на поверхность пузырьками паров растворителей или воздуха, что так же, как и седиментация, ведет к расслоению красок.
2.4.1. Агрегативная устойчивость дисперсных систем
Теоретически скорость быстрой коагуляции может быть определена по уравнению
−∂∂Nt = 8πdN1 0D ,
где N0, N – первоначальное число частиц в единице объема суспензии и через промежуток времени τ соответственно; d – диаметр частиц; D – коэффициент диффузии, равный
64

D = −6πkTdη,
здесь k – постоянная Больцмана; Т – абсолютная температура; η – вязкость среды.
Подставляя значение коэффициента диффузии в уравнение для времени, за которое число частиц уменьшится вдвое, получим:
t1/2 = 4kTN3η 0 .
Для реального пигментированного лакокрасочного материала при комнатной температуре уменьшение числа частиц вдвое в соответствии с этим уравнением произойдет за время от 15 мин до 2,5 ч. Практически коагуляция протекает гораздо медленнее, так как не каждое соударение приводит к слипанию частиц. Чтобы произошло слипание, частицы должны преодолеть определенный энергетический барьер.
В полидисперсных системах коагуляция протекает быстрее, при этом мелкие частицы исчезают значительно скорее. Частицы, имеющие форму листков, коагулируют с такой же скоростью, как и сферические; а иглообразные значительно быстрее.
Пока нет универсальной количественной теории агрегативной устойчивости, но определены факторы стабилизации дисперсных систем в соответствии с теориями:
–теория Дерягина – Ландау – Фервея – Овербека (теория ДЛФО) – равновесия сил притяжения и отталкивания частиц при наличии на их поверхности двойного электрического слоя;
–теория П. А. Ребиндера – наличия структурно-механического барьера, создаваемого на частицах толстыми, прочными и упругими адсорбционно-сольватными слоями;
–теория энтропийного и энтальпийного отталкивания частиц при перекрытии рыхлых адсорбционно-сольватных слоев с подвижными цепями и петлями полимеров.
Теория ДЛФО. Между частицами одновременно действуют ван-дер-ваальсовы силы притяжения и силы отталкивания, создаваемые при наложении двойных электрических слоев поверхности частиц. Потенциальную энергию дальнодействующих сил притяжения приближенно описывает уравнение (знак «–» обозначает энергию притяжения):
65
U A = 12Adh ,
где A – постоянная Гамакера, определяющая энергию дисперсионных взаимодействий (≈10–20 Дж); d – диаметр частиц; h – расстояние между поверхностями частиц.
Неорганические пигменты, как правило, собственных электрических зарядов не имеют. Они их приобретают при адсорбции веществ, способных к диссоциации на ионы. Потенциальную энергию электрических сил отталкивания, действующих на расстоянии до 100 нм, обозначим UR. Полная потенциальная энергия взаимодействия между частицами равна:
UT = UA +UR.
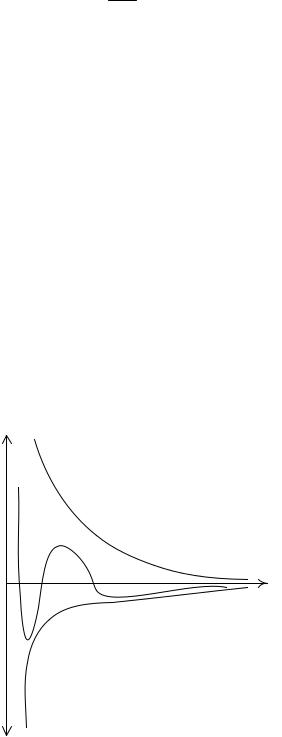
Энергия отталкивания UR уменьшается с увеличением расстояния между частицами более медленно, чем энергия притяжения UА. Как видно из рис. 2.4, при самом малом расстоянии между частицами силы отталкивания, называемые силами Борна, резко возрастают. Частицы могут соединиться при сближении, если их потенциальная энергия UА превосходит значение Uмакс на суммарной кривой, т. е. для взаимодействия необходима энергия активации.
UR
h
UA
Рис. 2.4. Зависимость потенциальной энергии U от расстояния между поверхностями частиц h: 1 – первичный минимум Uмин1 (коагуляция); 2 – вторичный минимум Uмин2 (флокуляция); 3 – энергетический барьер Uмакс
66
Единственным источником для преодоления этого энергетического барьера является тепловая энергия. Чем выше температура, тем
больше частиц будет соединяться. Если Uмакс (точка 3 на рис. 2.4) значительнобольшетепловойэнергии, дисперсиябудетустойчивой.
Результирующая действия сил притяжения и отталкивания (кривая U на рис. 2.4) имеет два минимума – две потенциальные ямы. Uмин1 при очень малом расстоянии между частицами определяет коагуляционное соединение частиц. Uмин2 проявляется при несколько большем расстоянии между центрами частиц. Если Uмин2 > kT, то частицы также соединяются, но это соединение может быть не непосредственным, а через прослойку окружающей среды, например адсорбированной жидкости, т. е. происходит флокуляция. Для редиспергирования коагуляционных контактов требуется затрата большого количества энергии. В этом случае образующиеся осадки могут быть практически необратимыми вследствие возникновения молекулярного взаимодействия между контактирующими поверхностями частиц. При флокуляции частицы хлопьевидного объемистого осадка связаны слабыми силами, и он легко редиспергируется при перемешивании.
Приближенно величина UR равна:
= εr2ψ2
UR Rc ,
где ε – диэлектрическая проницаемость среды; r – радиус частиц; ψ – поверхностный потенциал двойного электрического слоя (из-за крайней трудности его определения в качестве первого приближения обычно принимают ς – потенциал поверхности); Rc – расстояние между центрами частиц.
Согласно теории ДЛФО, для придания дисперсиям достаточной устойчивости необходимо, чтобы энергия отталкивания была не менее 15kT.
Экспериментально доказано, что при r < 0,5 мкм и ε < 5 (в эмалях с неполярными органическими растворителями) стабилизация за счет электрического отталкивания практически не имеет места. Начиная с ε > 40 этот фактор становится заметным и для водных систем (ε = 81) может вносить заметный вклад или даже быть определяющим фактором стабилизации при условии содержания в системе электролитов в количестве, не превышающем порога коагуляции. Поэтому пигменты, предназначаемые для водоразбавляемых красок, не должны содержать растворимых
67
веществ, особенно ионов поливалентных металлов, свыше определенного жестко регламентированного количества.
Для неорганических пигментов, не имеющих собственного электрического заряда в неполярных средах, стабилизация за счет наложения двойных электрических слоев практически не имеет места.
Теория структурно-механического барьера. Представление о структурно-механическом барьере как о наиболее мощном и универсальном факторе, ослабляющем взаимодействие между частицами, особенно в высоконаполненных суспензиях в неполярных средах, растворах, не содержащих ионизируемых групп, и расплавах олигомеров и полимеров, ввел Ребиндер.
Адсорбционные слои на поверхности твердых частиц оказывают не только стерическое препятствие к сближению частиц до расстояния эффективного действия сил притяжения между частицами, но одновременно снижают запас поверхностной энергии, образуя новую поверхность раздела фаз с незначительной энергией взаимодействия 20–30 мДж, характерной для групп СН2 и СН3. При большой толщине адсорбционно-сольватный слой, взаимодействуя с активными центрами твердой поверхности, полностью компенсирует ее силовое поле. Структурно-механический барьер эффективен, когда адсорбционный слой обладает высокой структурной вязкостью, упругостью и прочно связан с твердой поверхностью. Стабилизирующее действие возрастает по мере адсорбционного насыщения твердой поверхности и достигает максимума вблизи ее полного насыщения. В этом случае энергия столкновения двух частиц со сплошными адсорбционно-сольватными слоями условно может быть приравнена к эластичному удару сферических тел и определяется модулем упругости слоя.
Расчеты энергии притяжения между частицами показывают, что с уменьшением размера частиц и расстояния между ними снижается и необходимая толщина адсорбционного слоя, препятствующего сближению частиц. Для частиц с r = 0,5 мкм она должна быть не менее 10 нм, для частиц с r = 0,1 мкм достаточно слоя толщиной 5 нм.
Энтропийное отталкивание. Механизм энтропийной стабилизации основан на том, что большие молекулы пленкообразователей, закрепленные одним концом или частью сегментов на поверхности пигмента, сохраняют подвижность своих углеводородных цепей, которые имеют возможность принимать любую пространст-
68
венную конформацию, отвечающую минимальному энергетическому уровню. Сближение адсорбционных слоев двух частиц, а тем более их перекрывание уменьшает возможность реализации многих пространственных конформаций молекул, отвечающих минимуму энергии, т. е. приводит систему к снижению конформационной энтропии. В соответствии со вторым законом термодинамики без подвода энергии извне такой процесс сближения не может осуществиться, что равносильно наличию определенного энергетического барьера, препятствующего сближению частиц с рыхлыми ад- сорбционно-сольватными оболочками.
Энтальпийное отталкивание. При сближении частиц пиг-
ментов и перекрывании сольватных слоев повышается концентрация молекул пленкообразователя в зоне перекрывания, что приводит к осмотическому переносу растворителя из объема дисперсионной среды в межчастичное пространство, повышению давления в этой области и расклинивающему действию, т. е. расталкиванию частиц. При этом в «хорошем» растворителе величина энтальпийного отталкивания положительна, в «плохом» – отрицательна. Следовательно, в «хороших» растворителях адсорбционные слои отталкивают друг друга, а в «плохих» – притягивают. Однако избыток очень «хорошего» растворителя может вызвать десорбцию пленкообразователя, снижение величин концентрации пленкообразователя в адсорбционном слое и уменьшение толщины этого слоя за счет десорбции пленкообразователя с твердой поверхности.
Энтропийное и энтальпийное отталкивание вероятно только при соблюдении условия h < 2δ. В ином случае значения URS и URH будут нулевыми, т. е. в разбавленных суспензиях, и для низкомолекулярных пленкообразователей и ПАВ этот фактор не имеет места. Для большинства органорастворимых и водорастворимых красочных систем, содержащих неионогенные ПАВ, при высоком ОСП этот механизм стабилизации весьма вероятен.
Энергия взаимодействия адсорбционных слоев GR связана с изменением энтропии и энтальпии системы известным уравнением:
GR = HR – T SR.
При этом знак и значение GR зависят от соотношения энтальпии и энтропии. Если значение GR отрицательно, флокуляция частиц усиливается; если эта величина равна нулю, флокуляция происходит так же, как и в отсутствие адсорбционного слоя (т. е. наступает коагуляция). При положительном значении GR
69
частицы защищены от флокуляции. Величина GR положительна
вследующих случаях:
1)когда энтропия и энтальпия отрицательны с большим значением энтропийного члена; энтропийная стабилизация проявляется при снижении числа конформационных изменений цепей полимера в адсорбционном слое;
2)когда обе величины положительны, но доминирует энтальпийный фактор, – будет иметь место энтальпийная стабилизация;
3)когда HR положительна, а SR отрицательна, и, следовательно, оба члена способствуют стабильности.
Энергия энтропийных сил отталкивания между адсорбционными слоями на частицах составляет приблизительно 40kT, что значительно больше минимальной энергии 15kT, которая, согласно теории ДЛФО, может придать дисперсным частицам агрегативную устойчивость.
Таким образом, существующие теории стабилизации дисперсий основаны на взаимодействии адсорбционных слоев, но требования к строению этих слоев различны. Электрические силы отталкивания возникают при адсорбции ионов низкомолекулярных веществ, ПАВ, олигомеров и полиэлектролитов, способных к диссоциации. Электрические силы отталкивания оказывают стабилизирующее действие преимущественно в полярных дисперсионных средах, например в водоразбавляемых красках.
Для формирования структурно-механического барьера необходимы адсорбционно-активные молекулы с молекулярной массой, приближающейся к критической, при которой изменяется конформационное состояние олигомеров и полимеров, и в количестве, достаточном для покрытия поверхности диспергированных пигментов. При отсутствии прочной связи с активными центрами твердой поверхности такие слои могут быть нарушены, что вызывает дестабилизацию дисперсий.
Для энтропийного отталкивания нужны также большие молекулы, способные прочно закрепляться хотя бы одним сегментом на твердой поверхности, а свободными цепями – хвостами или петлями быть направленными в окружающую дисперсионную среду.
Алкидные, эпоксидные и другие олигомеры с молекулярной массой менее 1000 лишь на несколько часов задерживают флокуляцию. Надежную стабилизацию обеспечивают полярные олигомеры с молекулярной массой 2000–5000. Большие полимерные молекулы могут быть неэффективны, так как они обычно сверну-
70
ты в клубки и глобулы, прочно связанные внутримолекулярными связями, и лишь налипают на твердые частицы, не образуя с ними хемосорбционных связей.
2.4.2. Кинетическая (седиментационная) устойчивость пигментных дисперсий
Осаждение частиц, агрегатов и флокул пигментов в эмалях и красках под влиянием силы тяжести описывается законом Стокса:
v = 2r2 gΔρ, 9η
где v – скорость осаждения; r – радиус частиц; g – ускорение силы тяжести; Δρ – разница плотностей пигмента и среды; η – вязкость системы.
Неагрегированные частицы пигментов размером до 0,3 мкм, подверженные тепловому броуновскому движению, теоретически не должны осаждаться. С ростом размера частиц скорость осаждения увеличивается в квадратичной зависимости. Крупные частицы, оседая, захватывают мелкие. Повышение вязкости уменьшает скорость осаждения частиц, чем обычно и пользуются. Вводя в красочные системы структурирующие добавки (аэросил или бентонит в количестве 0,5–2,0% или органические загустители), которые придают системам тиксотропность, увеличивают вязкость в состоянии покоя в сотни раз и тем самым снижают во столько же раз скорость расслоения красок. Однако полностью устранить расслоение невозможно, поэтому стремятся получить слабофлокулированные рыхлые осадки, легко редиспергируемые при перемешивании. Всплывание частиц устраняют, повышая их смачиваемость модифицированием поверхности.
2.4.3. Флокуляция дисперсий
В дисперсиях частицы пигментов с образовавшимися на их поверхности адсорбционно-сольватными слоями могут соединяться между собой как за счет сил дальнодействия твердых поверхностей, перекрывающих тонкие адсорбционные слои, так и в результате взаимодействия между молекулами наружных поверхностей адсорбционных слоев соседних частиц. В первом случае медленно образуются плотные, трудно редиспергируемые осадки, по свойствам близкие к коагуляционным, во втором – рыхлые, объемистые, легко редиспергируемые при перемешивании.
71
Кроме того, при смешении однопигментных паст, например диоксида титана и органических пигментов, иногда происходит выпадение в осадок одного или обоих пигментов. Это явление называют софлокуляцией. Причина – наличие на поверхности частиц несмоченных активных участков, склонных к взаимному насыщению.
Причины флокуляции. Флокуляция может происходить при диспергировании пигментов в случаях:
–неполного смачивания пигментов;
–несоответствия акцепторно-донорных свойств пленкообразователя и пигмента;
–диспергирования пигментов в смесях двух пленкообразователей, придающих при адсорбции частицам разные электрические заряды;
–высокой влажности пигментов (более 0,5–2,0%) при диспергировании в неполярных средах.
Основной причиной труднообратимой флокуляции хорошо диспергированных пигментных паст является недостаточная толщина или малая прочность адсорбционно-сольватных слоев. Тонкие слои либо формируются из низкомолекулярных ПАВ и растворителей, молекулы которых ориентированы вертикально к твердой поверхности, либо при низкой концентрации больших молекул в растворах они ориентируются в адсорбционносольватном слое, развернувшись вдоль твердой поверхности. Чаще же причиной флокуляции является разрушение или утоньшение ранее сформированных толстых слоев, состоящих из клубков, глобул и вторичных надмолекулярных структур, слабо связанных между собой и с твердой поверхностью.
Сильная флокуляция с выпадением пигментов («пигментный шок») происходит:
1) при перераспределении – отсасывании растворителей из сольватных слоев пигментных «тощих» паст, диспергированных в разбавленных (до 15–20%) растворах, при введении в них концентрированных (55–60%) растворов тех же пленкообразователей;
2) добавлении в пигментные пасты больших порций хороших растворителей, способных хотя бы временно и частично нарушить адсорбционный слой;
3) перераспределении ПАВ между пигментом и пленкообразователем в случае введения новых компонент, особенно в водоразбавляемых латексных красках;
72
4)разведении теплых пигментных паст большим количеством холодного (структурированного) лака;
5)высокой скорости испарения основного растворителя в процессах окраски распылением и высокотемпературного отверждения;
6)механическом перемешивании с большими скоростями сдвига, способными разрушать не только тиксотропные структуры, но и сами слои.
Иной вид флокуляции может иметь место при взаимодействии наружных поверхностей адсорбционных слоев. В случае избытка ПАВ могут формироваться вторичные слои с обратной ориентацией, которые взаимодействуют между собой полярными группами. Большие молекулы и надмолекулярные структуры, завязанные в адсорбционных слоях, могут взаимодействовать своими полярными группами и неполярными цепями со слоями соседних частиц.
Присутствие в разбавленной системе больших молекул полиэлектролитов с разными функциональными группами и развернутыми цепями приводит также к сильной флокуляции.
Обратимая флокуляция может быть полезной. Физическое взаимодействие наружных поверхностей межфазных оболочек пигментов между собой создает легкообратимые структуры и способствует стабилизации дисперсий. Такая слабая флокуляция является желательной. При ней незначительно снижается дисперсность, укрывистость и красящая способность пигментов, но красочные системы получают и положительные технологические свойства. Тиксотропность слабофлокулированных систем улучшает розлив, устраняет натеки. Относительно быстро образующиеся при хранении таких систем объемистые рыхлые осадки легко редиспергируются при перемешивании. Красочные системы с предельно дефлокулированными частицами с замкнутыми адсорбционными слоями характеризуются наивысшими значениями укрывистости и красящей способности, но, не обладая тиксотропностью, при нанесении дают натеки, частицы оседают медленно и образуют плотные осадки.
Оценка степени флокуляции. Степень флокуляции пигмен-
тов оценивают по изменению дисперсности и зависящих от нее свойств пигментов в красках или покрытиях, а также по объему и структуре выпадающих осадков. Измерения дисперсности проводят в свежеизготовленных красках или покрытиях и через опреде-
73
ленные промежутки времени (несколько минут или часов в случаях быстрой флокуляции, суток и месяцев в случаях медленной).
Более специфичными методами оценки флокуляции являются бумажная хроматография и рассеяние ИК-света. Бумажная хроматография основана на измерении скорости миграции пигментов при поднятии краски по вертикально подвешенной бумажной полоске или по растеканию капли краски на бумажном фильтре. По характеру распределения пигментов, окрашивающих бумагу, и скорости продвижения красочного фронта можно дифференцированно оценивать степень флокуляции.
Интересен метод оценки степени флокуляции белых пигментов в сухих пленках на стекле по изменению наблюдаемого через пленку цвета вольфрамовой нити лампы накаливания. В случае нефлокулированной системы цвет спирали красный, слабофлокулированной – сиреневый, флокулированной – голубой, сильнофлокулированной – белый. На этом же принципе различного рассеяния ИК-света частицами разного размера основан спектрофотометрический метод. Рассеяние ИК-света (2500 нм) в направлении, обратном потоку падающего света, для нефлокулированного диоксида титана составляет 7%, для флокулированного – 25%.
74
