
- •4. Понятие о терпенах. Классификация. Закономерности образования (биосинтез) и распространение в растениях
- •Классификация
- •Строение молекул
- •Биосинтез
- •Ациклические монотерпены
- •Моноциклические монотерпены
- •Бициклические монотерпены
- •Сесквитерпены
- •Ароматические соединения
- •Значение эфирных масел для растений
- •Накопление эфирных масел
- •Заготовка
- •Хранение
- •Исследование и стандартизация эфирных масел
- •Классификация антраценпроизводных
- •5. Стимулирующее и регенерирующее действие.
- •4. Реакции с солями тяжелых металлов.
- •1. Реакции осаждения.
- •2. Цветные реакции.
- •1. Извлечение алкалоидов из растительного сырья (см. Выше)
- •2. Очистка полученных извлечений (от смолы, пигментов, жиров, пектин. В-в) (см. Выше)
- •3. Разделение полученной суммы и выделение индивидуальных соединений.
- •4. Собственно количественное определение содержания выделенных и очищенных алкалоидов.
Исследование и стандартизация эфирных масел
Эфирные масла представляют собой смеси душистых веществ, относящихся к различным классам органических соединений, преимущественно к терпеноидам, реже ароматическим или алифатическим соединениям.
Эфирные масла получают обычно из растительного сырья путем дистилляции с водой или водяным паром, а также экстракцией органическими растворителями, прессованием и другими способами.
Описание. Бесцветные или окрашенные прозрачные жидкости, чаще желтоватого цвета, со специфическим запахом и вкусом. Как правило, эфирные масла легче воды.
Под влиянием воздуха и света многие эфирные масла, постепенно окисляясь, изменяют запах и цвет (темнеют). Некоторые эфирные масла при хранении загустевают.
Растворимость. Масла растворимы, очень мало растворимы или практически нерастворимы в воде; легко растворимы или растворимы в спирте, эфире и других органических растворителях.
В спирте различной концентрации (указанной в соответствующей нормативно-технической документации) растворимость определяют следующим образом: в мерный цилиндр вместимостью 10 мл наливают 1 мл масла и постепенно приливают из бюретки при тщательном взбалтывании по 0,1 мл спирта определенной концентрации при 20°С до полного растворения масла.
Подлинность.
Цвет и прозрачность определяют, поместив 10 мл масла в цилиндр из прозрачного бесцветного стекла диаметром 2 - 3 см, наблюдая в проходящем свете.
Запах определяют, нанося около 0,1 мл (2 капли) масла на полоску фильтровальной бумаги длиной 12 см и шириной 5 см так, чтобы масло не смачивало края бумаги, и сравнивают запах испытуемого образца через каждые 15 мин, с запахом контрольного образца, нанесенного таким же образом на фильтровальную бумагу. В течение 1 ч запах должен быть одинаков с запахом контрольного образца.
Вкус определяют, прикладывая к языку полоску фильтровальной бумаги с нанесенной на нее каплей масла, или смешивают 1 каплю эфирного масла с 1 г сахарной пудры и пробуют на язык.
Посторонние примеси.
Спирт. 2 - 3 капли эфирного масла наносят на воду, налитую на часовое стекло, и наблюдают на черном фоне; не должно быть заметного помутнения вокруг масла. 1 мл масла наливают в пробирку, закрывают ее рыхлым комочком ваты, в середину которого помещен кристаллик фуксина, л подогревают до кипения; не должно быть фиолетово-розового окрашивания ваты.
Жирные и минеральные масла. 1мл эфирного масла взбалтывают в пробирке с 10 мл спирта; не должно наблюдаться помутнения и капель жирного масла.
Вода. Содержание воды определяют методом дистилляции.
Числовые показатели.
Температуру затвердевания определяют по методике как и жиры, при этом высота слоя масла должна быть не менее 5 см.
Плотность определяют с помощью пикнометра.
Угол вращения плоскости поляризации определяют в поляриметре.
Показатель преломления определяют рефрактометром.
Кислотное число определяют в навеске 1,5 - 2 г масла, взятой с погрешностью ±0,01 г и растворенной в 5 мл нейтрализованного спирта.
Понятие о гликозидах, их классификация. Физические и химические свойства.
Гликозиды – природные соединения, производные циклических сахаров, которые в процессе гидролиза распадаются на продукты, среди которых всегда есть сахаристое вещество и вещество неуглеводной природы - агликон.
В состав гликозидов входят гексозы, пентозы, уроновые кислоты. Образование гликозидной связи происходит за счет полуацетальных гидроксилдьных групп моносахаридов, поэтому их называют гликозидными гидроксилами.
Классификация гликозидов.
По углеводной части молекулы:
Монозиды – углеводный компонент содержит 1 моносахарид;
Биозиды – 2 моносахарида;
Триозиды – 3 моносахарида;
Тетразиды – 4 моносахарида;
Олигозиды – 5 и более сахаров.
По характеру гликозидной связи:
Соединение сахара и агликона происходит за счет полуацетального гидроксила циклической формы сахара и водорода гидроксильных групп.
О-гликозиды – присоединение идет через атом кислорода. Это наиболее многочисленная группа гликозидов, они легко подвергаются гидролизу.
S – гликозиды – присоединение идет через атом серы. Тиогликозиды очень устойчивы к кислотному гидролизу, но легко подвергаются ферментативному и щелочному гидролизу. S- гликозиды обычно имеют сложный агликон, который при гидролизе распадается на компоненты, в числе которых всегда имеется серосодержащее эфирное масло.
Серосодержащие эфирные масла раздражающе действуют на слизистые оболочки и кожу. Благодаря этому свойству растения, содержащие свободные серосодержащие эфирные масла (лук, чеснок) или тиогликозиды (горчица сарептская), издавна используются для получения лекарственных средств, оказывающих местное раздражающее или отвлекающее действие.
Обезжиренный жмых семян горчицы используют для изготовления горчичников. Семена горчицы сарептской содержат тиогликозид синигрин. В присутствии воды при температуре 30 - 40С под влиянием фермента мирозина отщепляется аллилизотиоцианат, называемый горчичным эфирным маслом.
N- гликозиды – присоединение идёт через атом азотаю Вырабатываются плесенями, грибами.
С- гликозиды – присоединение идёт через атом углерода. Этот вид гликозидов отличается большой устойчивостью к гидролизу, они содержатся в растениях семейств розоцветных, бобовых, капустных.
3. По характеру агликона:.
По характеру агликона классифицируются в основном О-гликозиды.
Алкилгликозиды – агликонами являются алифатические углеводороды и их производные, это, например, элеутерозид из элеутерококка колючего.
Цианогенные гликозиды – агликон содержит цианогенную или нитрильную группу (-СN). Наиболее характерны для растений семейства розоцветные подсемейства сливовых. Локализуются в семенах. В медицинской практике применяются горькоминдальная вода, которую получают из хмыха семян горького миндаля перегонкой с водяным паром. Амигдалин, содержащийся в семенах миндаля, под влиянием фермента - глюкозидазы расщепляется на 2 молекулы глюкозы, бензальдегид и синильную кислоту. Горькоминдальная вода применяется в каплях и в микстуре в качестве успокоительного и обезболивающего средства.
Амигдалин + 2 Н2О + - глюкозидаза 2 С6Н12О6 + С6Н5СНО + НСN
глюкоза бензальдегид цианистый
водород
Заготовка, сушка и хранение гликозидного сырья.
Собирают сырьё после 10-11 часов, когда полностью обсохнет роса. Собирают в небольшую по объему, хорошо проветриваемую тару (корзины). Сырьё укладывают рыхло, не утрамбовывают. От момента сбора до сушки должно пройти не более 2-х часов.
Сушку сырья проводят с учетом активности ферментов. Обычно гликозидное сырьё сушат при 50 – 60ºС – это сушка с частичной денатурацией ферментов. Иногда сырьё выдерживают при 70 – 80ºС в течение часа (происходит полная денатурация ферментов), а затем досушивают воздушно-теневым способом.
Хранят сырьё при температуре воздуха 12 -15ºС и влажности воздуха 30 -40%. Хранят чаще в тюках из ткани, тканевых мешках, ящиках из листовой древесины. Фасуют в бумажные пакеты. Срок годности от 2 до 5 лет.
Понятие о горечах, их классификация. Физические и химические свойства. Особенности заготовки, сушки, хранения сырья. Оценка качества сырья, методы анализа. Пути использования сырья, медицинское применение.
Горечи (Amara) – растительные, главным образом, безазотистые вещества, возбуждающие аппетит и улучшающие пищеварение.
По своему горькому вкусу и способности стимулировать деятельность желез слюны, желчи, панкреатического и желудочного сока горечи сходны с эфирными маслами. Разница заключается в том, что горечи повышают секрецию этих желез медленно, но более устойчиво и сильно.
Классификация ЛРС, содержащего горечи, и его заготовка. В растениях горечи могут встречаться вместе с эфирными маслами – такие горечи принято относить к группе «ароматических горечей» (Amara aromatica), в отличие от «чистых горечей» (Amara pura) и «слизевидных горечей» (Amara mucilaginosa), присутствующих вместе со слизистыми веществами и другими полисахаридами. В большинстве случаев агликоны молекул горечей относят к монотерпеноидам, называемым иридоидами, реже – к сесквитерпеноидам, валепотриатам и другим соединениям.
Кроме того, есть вещества, обладающие горьким вкусом, которые содержат в своих молекулах азот и относятся к группе терпеноидных алкалоидов (например, хинин, стрихнин). Последние не рассматриваются как истинные горечи, а будут изучаться вместе с другими алкалоидами в конце курса. Основанием для этого служит их высокая токсичность и существенно иной характер фармакологического действия на организм.
Относительно распространения горечей в растительном мире и подготовки ЛРС, следует сказать, что горечи-иридоиды являются важным хемосистематическим признаком. Они локализуются в клеточном соке различных органов. Часто встречаются в растениях семейств Вахтовые, Горечавковые, Норичниковые, Мареновые,Подорожниковые, Яснотковые и др.
Лекарственные растения и лекарственное растительное сырье, содержащие горечи, подразделяют, по крайней мере, на три подгруппы:
а) горько-ароматическое (или горько-пряное) сырье, содержащее как горечи, так и эфирные масла, которое сушат при температуре 30-45ºС (корневища аира при температуре не выше 40ºС);
б) сырье, содержащее чистые горечи, сушку которого осуществляют при температуре 40-60ºС;
в) сырье, где горечи присутствуют вместе со слизями; его сушат при температуре 40-60ºС. В последней подгруппе: цетрария исландская, подорожник большой, содержащий иридоидный гликозид аукубин.
По химической природе горечи относятся к терпеноидам. Часть из них является монотерпеноидами (С5Н8)2, часть – сесквитерпеноидами (С5Н8)3, встречаются также ди- и тритерпеноидные горечи. Все горечи, в особенности тритерпеноидные, сильно окислены и содержат в молекуле гидрокси-, карбокси-, эпокси-, эфирные и сложноэфирные или лактонные группировки.
Кроме того, только немногие горечи присутствуют в растениях в свободном, агликоновом состоянии; большинство горечей находится в клетках и тканях растений в гликозилированной форме, т.е. имеют кроме терпеноидного агликона еще и присоединенную углеводную цепочку, которая под действием ферментов в кислой среде (кислых гидролаз, или даже просто под действием низких рН) отщепляется от агликона.
ЛРС, содержащее горечи-иридоиды, сушат как гликозидное сырье, т.е. при температуре 50-60ºС. ЛРС, содержащее сесквитерпеновые горечи, сушат как эфиромасличное сырье, т.е. при температуре 30-40ºС (не выше 45ºС) на проветриваемых чердаках, под навесами и т.д. Для оценки качества сырья органолептические показатели практически не используются. Кроме того, для оценки качества ЛРС теперь обычно используют сопутствующие вещества: эфирные масла, ксантоны, флавоноиды или просто экстрактивные вещества. Например, в траве золототысячника зонтичного определяют не горечи, а ксантоны; в траве полыни горькой и корнях одуванчика – экстрактивные вещества, в корнях аира болотного – эфирные масла, а в листьях вахты трехлистной – сумму флавоноидов. Для сохранения горечей при выделении из ЛРС его предварительно обрабатывают раствором Са(ОН)2 или СаСО3 – для нейтрализации кислот и ферментов.
Классификация, физико-химические свойства горечей и извлечение их из ЛРС. Монотерпеновые горькие гликозиды являются иридоидными гликозидами. Иридоиды – группа циклопентан-пирановых монотерпенов, название которых происходит от муравьев Iridomyrmex. Горечи – производные иридоидов подразделяют, по крайней мере, на:
а) собственно иридоиды (например, логанин);
б) секо-иридоиды – иридоиды с раскрытым кольцом циклопентана (например, секологанин, сверозид).
В отдельные группы выделяют:
- сесквитерпеноидные горечи, представленные преимущественно лактонами гвайянового ряда (например, артабсин, ахиллин);
- иридоиды в семействе Валериановых, которые представлены валепотриатами (например, валерозидат).
Горечи, производные иридоидов, представляют собой бесцветные кристаллические или аморфные вещества с температурой плавления 50-300ºС, хорошо растворимые в воде и низших спиртах. Однако встречаются иридоиды, плохо растворимые в воде и лучше – в этилацетате.
Понятие о сердечных гликозидах, их классификация. Особенности структуры агликона и сахарного компонента. Особенности заготовки, сушки, хранения сырья. Пути использования сырья, медицинское применение.
Сердечными гликозидами называют гликозиды, которые являются производными циклопентанапергидрофенантрена, содержащие в положении 17 ненасыщенное пятичленное или шестичленное лактонное кольцо и оказывающие кардиотоническое действие.
+Своё название они получили благодаря специфическому действию на сердце. Кардиотонические гликозиды увеличивают силу и уменьшают частоту сердечных сокращений, улучшают тканевой обмен сердечной мышцы. Препараты, содержащие кардиотонические гликозиды, применяют при сердечной недостаточности и нарушениях ритма сердца: пороках сердца вследствие перенесенного ревматизма, частых атак ангин; дистрофии миокарда; тахикардии, острой сердечной недостаточности, возникающей при обширных травмах, инфекционных заболеваниях и др. Отличия в действии препаратов заключаются в скорости наступления эффекта, продолжительности действия, в способности к кумуляции и в побочных эффектах. Противопоказания: брадикардия, атриовентрикулярная блокада различной степени; необходима осторожность при стенокардии и инфаркте миокарда.
Сердечными гликозидами называют гликозиды растительного происхождения, агликоны которых являются стероидами – производными циклопентанпергидрофенантрена, содержащие в положении С-17 ненасыщенное лактонное кольцо и обладающие в связи с этим избирательным действием на сердечную мышцу. Разрыв или изомеризация лактонного кольца ведет к полной потере биологической активности.
Общая структура сердечных гликозидов имеет следующий вид:
На биологическую активность сердечных гликозидов оказывает влияние не только строение агликона, но и природа углеводного остатка. В большинстве случаев углеводный компонент присоединяется к агликону по месту расположения спиртового гидроксила в положении С-3, построен линейно и может содержать от одного до пяти моносахаров. Чаще всего это дезоксисахара: дигитоксоза, ацетилдигитоксоза, цимароза и др. Наиболее сильное, но кратковременное действие оказывают монозиды; с удлинением углеводной цепи действие становится более мягким и длительным. Специфическим действием на миокард обладает только агликон.
Молекулы сердечных гликозидов состоят из агликона и углеводной части.
Специфическим действием на сердце обладает только агликон, сахара на сердце не действуют, но в сочетании с агликоном обусловливают растворимость гликозидов в воде и способствуют накоплению фермента АТФ-азы.

В основе агликона сердечных гликозидов лежит стероидное ядро циклопентанпергидрофенантрена, в котором:
Кольца А/В могут иметь как цис-, так и транс сочленение;
Кольца В/С имеют транс положение – присущее всем природным стероидам;
Кольца С/D имеют цис - сочленение.
В стероидном ядре имеются постоянные заместители:
В 17 положении стероидного ядра у сердечных гликозидов всегда присоединяется 5-ти или 6-ти членное ненасыщенное лактонное кольцо. Присутствие лактонного кольца отличает сердечные гликозиды от всех остальных природных стероидов. Именно наличие ненасыщенного лактонного кольца в молекуле сердечных гликозидов обусловливает специфическое действие этой группы веществ на сердце. Отсутствие, разрыв или изомеризация лактонного кольца приводитк полной потере активности сердечных гликозидов.
В 3 и 14 положениях присутствуют гидроксильные (-ОН ) группы;
В 13 положении находится метильная (-СН3 ) группа.
Природные агликоны сердечных гликозидов могут иметь переменные заместители:
В 10 положении могут быть метильная (-СН3 ), оксиметильная (-СН2ОН), альдегидная (-СНО), или карбоксильная (-СООН) группы. Наличие в 10 положении альдегидной группы приводит к возрастанию гидрофильности и увеличению активности сердечных гликозидов при одновременном повышении токсичности;
В 1,2,5,11,12,15 и 16положениях могут присутствовать гидроксильные (-ОН) группы. Её наличие в 16 положении приводит к снижению активности сердечного гликозида. Гидроксилы в 16 положении могут быть ацилированы муравьиной, уксусной, изовалериановой кислотами, что увеличивает токсичность сердечных гликозидов.
Важное значение имеет ориентация функциональных групп относительно плоскости молекулы. Наибольшей активностью обладают сердечные гликозиды у которых имеется -ориентация лактонного кольца и других заместителей.
Свободные агликоны сердечных гликозидов плохо удерживаются миокардом. Поэтому их действие проявляется очень короткое время и они более токсичны по сравнению с гликозидами.
Все сердечные гликозиды являются О-гликозидами. В составе сердечных гликозидов обнаружено более 30 моносахаров. Среди них встречаются широко распространенные в растениях сахара: глюкоза, галактоза, арабиноза и другие, а так же специфические углеводы: рамноза, цимароза, дигитоксоза.
Дезоксисахара всегда присоединяются непосредственно к агликону. Если в состав углеводной части молекулы входит глюкоза, то она всегда находится в конце цепи.
+Углеводная часть может содержать от 1 до 5 моносахаров. Количество моносахаридных остатков в цепи имеет важное значение для силы, быстроты и продолжительности действия сердечных гликозидов. С возрастанием количества сахаров в углеводной части молекулы действие сердечных гликозидов становится более мягким и продолжительным.
Таким образом, сердечные гликозиды состоят из трёх основных частей:
стероидный цикл;
лактонное кольцо;
углеводная часть.
В качестве лекарственного сырья, содержащего сердечные гликозиды, заготавливают:
Листья – Digitalis purpurea, D. grandiflora, D. lanata, Convallaria majalis;
Траву - Convallaria majalis, Adonis vernalis, Erysimum canescens;
Цветки - Convallaria majalis;
Семена – Strophantus Kombe, S. gratus.
+Заготовку сырья, содержащего сердечные гликозиды, проводят по правилам сбора гликозидного сырья. Сразу же после сбора, сырьё необходимо немедленно в течение не менее чем 3-х часов доставить к месту сушки. Сушка искусственная при температуре 50 – 60 С, при этой температуре происходит инактивация ферментов и предотвращается ферментативный гидролиз сердечных гликозидов. Исключение может составить сырьё ландыша майского и горицвета (адониса) весеннего, ферменты которых обладают малой активностью. Поэтому для этих видов сырья допускается воздушно-теневая сушка при условии хорошей вентиляции или искусственная сушка при 49 -50С. Траву желтушника раскидистого перерабатывают в свежем виде.
Все виды сырья, содержащего сердечные гликозиды, хранят по списку Б, а семена строфанта Комбе по списку А, в плотно укупоренной таре при 10 - 15С. Еа этикетках тары обязательно указывается количество единиц действия в 1 г сырья, год сбора и дата анализа.
Физические и химические свойства сердечных гликозидов. Оценка качества сырья, методы анализа. Пути использования сырья, медицинское применение.
Физико-химические свойства сердечных гликозидов
Сердечные гликозиды в основном представляют собой кристаллические (реже аморфные) вещества, бесцветные или белые, горького вкуса, без запаха. Имеют фиксированную точку плавления (100-2700С), оптически активны.
Сердечные гликозиды мало растворимы в органических растворителях (нерастворимы в петролейном и диэтиловом эфире), но растворимы в смеси хлороформ-спирт, в водных растворах этилового или метилового спирта. Растворимость в воде повышается с увеличением длины углеводной цепи.
Агликоны сердечных гликозидов хорошо растворимы в органических растворителях.
В зависимости от степени растворимости в воде или липидах сердечные гликозиды разделяют на следующие группы:
1. Полярные (гидрофильные) гликозиды (группа строфанта). В положении С-10 находится альдегидная группа. К этой группе относятся кардиогликозиды строфанта, ландыша майского, адониса весеннего и желтушника раскидистого. Их агликонами являются строфантидин и его аналоги, имеющие в своей структуре четыре гидрофильные группы, придающие агликону достаточно выраженные гидрофильные свойства, а метильная группа только одна (в положении С-13).


К-строфантидин
Полярные гликозиды хорошо растворяются в воде, но плохо в липидах. В связи с этим они плохо всасываются слизистой оболочкой желудочно-кишечного тракта (применяются преимущественно парэнтерально, вводятся внутривенно), но легко выводятся через почки. Кардиотонический эффект развивается уже через 5-10 мин. Высокая скорость наступления эффекта объясняется тем, что полярные сердечные гликозиды мало связываются с белками плазмы крови и быстро распределяются в организме. Не кумулируют и обладают наименьшей длительностью действия (до 24 ч). «Препараты скорой помощи».
2. Неполярные (липофильные) сердечные гликозиды (группа наперстянки. В положении С-10 находится метильная группа. К этой группе относятся гликозиды наперстянок пурпуровой и крупноцветковой. Агликоном является дигитоксигенин, содержащий только две свободные гидрофильные группы. Липофильность обусловлена дополнительной метильной группой в положении 10.
Дигитоксигенин
Эта группа сердечных гликозидов плохо растворима в воде и хорошо – в липидах, поэтому обладает высокой всасываемостью в кишечнике (применяют преимущественно перорально). Кардиотонический эффект наступает через 2-4 ч после приема. Неполярные сердечные гликозиды активно связываются с белками плазмы крови и плохо фильтруются через почки. Все это приводит к высокой степени кумуляции в организме и максимальной продолжительности действия (до 10-14 дней).
3. Относительно полярные гликозиды – промежуточные соединения между полярной и неполярной группами. К ним относятся гликозиды наперстянки шерстистой. Агликон дигоксигенин имеет три свободные гидрофильные группы (имеется дополнительная ОН-группа в положении 12). Эти вещества относительно хорошо растворимы как в липидах, так и в воде, поэтому достаточно хорошо всасываются при приеме внутрь, но и хорошо выводятся через почки. Способны связываться с белками плазмы крови (но значительно менее активно, чем неполярные гликозиды), следовательно, умеренно кумулировать и действовать до 5-7 дней. Препараты относительно полярных сердечных гликозидов могут применяться как парэнтерально, так и перорально.
Сердечные гликозиды способны к кислотному, щелочному и ферментативному гидролизу. При кислотном и щелочном гидролизе сразу происходит глубокое расщепление гликозида до агликона и сахара. При ферментативном гидролизе происходит ступенчатое отщепление моносахаров и из первичных гликозидов образуются вторичные гликозиды с более короткой углеводной цепью. Например, первичный гликозид наперстянки пурпурной – пурпуреагликозид А содержит углеводную цепь, состоящую из трех молекул дигитоксозы и одной терминальной молекулы глюкозы.


При отщеплении молекулы глюкозы в результате ферментативного гидролиза пурпуреагликозида А образуется достаточно устойчивое соединение дигитоксин, используемое в качестве лечебного препарата.
Следует отметить, что деструкция углеводного компонента сердечных гликозидов легко протекает в естественных условиях, например, при заготовке и первичной переработке сырья, когда собранное сырье согревается и содержащиеся в нем ферменты активизируются. В то же время образование вторичных и даже третичных гликозидов – далеко не всегда желаемый процесс и для его ограничения сушку сырья, содержащего сердечные гликозиды, проводят не позднее, чем через 1 час после сбора сырья, при температуре 50-70оС. Хранят сырье при температуре не выше 150С, в отдельном помещении, под замком (содержит сильно действующие и ядовитые вещества).
Качественный анализ сердечных гликозидов.
Для обнаружения в сырье сердечных гликозидов используются три группы цветных реакций: на углеводный компонент, на стероидное ядро и на лактонный цикл.
1. Реакции на углеводный компонент. Реакции, как правило, проводят после кислотного гидролиза сердечных гликозидов. Наличие образовавшихся «нормальных» моносахаров определяют с помощью реактива Фелинга или реакцией серебряного зеркала. Дезоксисахара дают положительную реакцию Келлер-Килиани: спиртовой раствор сахара в ледяной уксусной кислоте, содержащей следовые количества сульфата железа (III), при наслаивании на концентрированную серную кислоту приобретает ярко-голубой или сине-зеленый цвет.
2. Реакции на стероидный цикл. В их основе лежит способность стероидного ядра к дегидратации под действием кислотных реагентов с образованием окрашенных комплексных соединений.
Реакция Либермана-Бурхарда: сухой остаток очищенного извлечения гликозида растворяют в 1 мл уксусного ангидрида, прибавляют 2-3 капли концентрированной серной кислоты (50:1) – развивается красно-розовое окрашивание, переходящее в зеленое, а затем в синее.
3. Реакции на пятичленное лактонное кольцо (для карденолидов). Основаны на способности лактонного кольца окисляться полинитросоединениями в щелочной среде с образованием окрашенных продуктов.
Реакция Легаля – с нитропруссидом натрия (при добавлении гидроксида натрия) развивается красное окрашивание;
Реакция Балье – с пикриновой кислотой в щелочной среде развивается оранжевое окрашивание;
Реакция Раймонда – с мета-динитробензолом развивается фиолетовое окрашивание.
На шестичленное лактонное кольцо буфадиенолидов до сих пор не найдено специфических реактивов, однако для них характерна в у/ф спектре полоса поглощения при 300 нм.
![]()
Количественное определение сердечных гликозидов.
С целью количественного определения сердечных гликозидов в сырье после очистки суммы сердечных гликозидов или выделения индивидуальных веществ используют физико-химические методы: спектрофотометрические, полярографические, титриметрические. Существенным недостатком вышеперечисленных методов является то обстоятельство, что оценка проводится, как правило, по одному из компонентов молекулы гликозида (стероидному циклу, лактонному кольцу, углеводному компоненту), и не учитывается целостность всего соединения, как необходимое условие для проявления стандартной биологической активности. В процессе переработки сырья, его хранения, при выделении индивидуальных соединений химическая структура гликозидов претерпевает изменения: происходит частичное разрушение лактонного цикла, варьирует длина углеводной цепи и т.д. Следовательно, различные молекулы сердечных гликозидов, содержащиеся в препарате, будут обладать и различной силой фармакологического эффекта. По этой причине дозировать лекарственные формы, содержащие сердечные гликозиды, основываясь только на данных о содержании сердечных гликозидов, полученных физико-химические методами, не представляется возможным.
Для препаратов растительного сырья и препаратов, содержащих сердечные гликозиды, обязательным является биологическое тестирование.
В основу биологического метода контроля положено токсическое действие сердечных гликозидов на организм животного, в результате которого наступает систолическая остановка сердца. Биологическая стандартизация проводится на лягушках. Активность оценивают по сравнению со стандартным препаратом (очищенным спиртовым экстрактом суммы гликозидов или индивидуальным кристаллическим гликозидом) и выражают в лягушачьих единицах действия (ЛЕД). Устанавливают наименьшие дозы стандартного образца и исследуемого препарата, вызывающие систолическую остановку сердца подопытных животных; затем рассчитывают содержание ЛЕД в 1 г исследуемого средства (в одной таблетке, в 1 мл). Одна единица действия (ЛЕД) соответствует наименьшей дозе препарата, вызывающей систолическую остановку сердца стандартной лягушки в течение 1 часа, если испытывают сырье и препараты наперстянки, ландыша и горицвета; или 2 часов, если испытывают сырье и препараты строфанта и желтушника.
В НД на лекарственное растительное сырье, содержащее гликозиды, обязательно указывается валор. Валор сырья - это количество ЛЕД в 1 г лекарственного растительного сырья.
Понятие о сапонинах, их классификация. Пути использования сырья, медицинское применение.
Сапонины — это группа биологически активных веществ, по химическому строению являющихся гликозидами, но обладающих рядом характерных свойств. Их водные растворы или извлечения из сырья при встряхивании образуют стойкую пену, почему их и назвали сапонинами от латинского слова sapo — мыло. Кроме того, они обладают гемолитической активностью, т.е., растворяют эритроциты (красные кровяные тельца). Агликон у сапонинов называется сапогенином. По структуре сапогенинов сапонины разделяются на две подгруппы: стероидные и тритерпеновые
Стероидные сапонины.Сапогенины этих сапонинов являются производными циклопентанпергидрофенантрена, как и агликоны кардиотонических гликозидов. Однако стероидные сапонины не оказывают кардиотонического действия, так как не имеют лактонного кольца при С17 и ряда других функциональных групп.
Сапогенины всех стероидных сапонинов имеют:
у С3 кольца А – гидроксильную (-ОН) группу;
в положении 16-17 — спирокетальную группировку за счет окисления боковой цепи;
в положении 5-6 — двойную связь (-CH=CH-);
в положениях С10и C13— метильные (-СН3) группы
Диосгенин
Углеводная часть молекулы стероидных сапонинов присоединяется в положении С3агликона и может содержать от 1 до 9 моносахаридов (глюкоза, галактоза, рамноза, галактуроновая кислота и др.). Моносахариды могут образовывать как линейные, так и разветвленные цепи. Например, стероидный сапонин диосцин (диоскорея ниппонская –Dioscoreanipponica, якорцы стелющиеся –Tribulusterrestris) состоит из агликона диосгенина, к которому присоединяется разветвленная триоза
Стероидные сапонины встречаются редко, преимущественно в растениях тропического климата. В семействах диоскорейных, норичниковых, спаржевых, амариллисовых стероидные сапонины часто встречаются совместно с кардиотоническими гликозидами (наперстянка, ландыш и др.).
Тритерпеновые сапонины имеют общую формулу (С5Н8)6 и, в зависимости от количества колец в структуре агликона, делятся на пентациклические и тетрациклические.
а) Тетрациклические — содержат в структуре агликона 4 кольца и подразделяются на производные даммарана (даммарандиол), циклоартана (циклоартенол), зуфана. В основе этой группы лежит даммаран. Производные даммарана легко окисляются с образованием гетероциклов (панаксдиол и панакстриол). Соединения подобного строения обнаружены в женьшене (Panaxginseng), заманихе высокой (Oplopanaxelatus), березе (Betulaspp.).
б) Пентациклические — содержат в структуре агликона 5 колец. Среди этой группы выделяют производные урсана (альфа-амирин), олеанана (бета-амирин), лупана (лупеол), гопана. С медицинской точки зрения, наиболее важными являются производные урсана и олеанана, которые отличаются друг от друга расположением заместителей – метильных (-СН3) групп в положениях 19 и 20 кольца Е.
Альфа-амирин лежит в основе различных соединений, которые найдены в ортосифоне тычиночном, или почечном чае (Orthosiphonstamineus), лапчатке прямостоячей (Potentillaerecta) и других. Наиболее важным представителем является кислота урсоловая (28-карбокси-альфа-амирин). Кислота урсоловая обнаружена во многих растениях (бруснике -Vacciniumvitis-idaea, клюкве болотной -Oxycoccuspalustrisи др.), причем встречается как в виде гликозидов, так и свободного агликона.
Бета-амирин лежит в основе следующих соединений:
кислота олеаноловая (28-карбокси-бета-амирин). Кислота олеаноловая и ее производные являются агликонами сапонинов аралии высокой (Araliaelata), синюхи голубой (Polemoniumcaeruleum), конского каштана (Aesculushippocastanum), первоцвета весеннего (Primulaveris), календулы лекарственной (Calendulaofficinalis), патринии средней (Patriniaintermedia) и др.
кислота глицирретиновая (11-оксо-29-карбокси-бета-амирин). Кислота глицирретиновая является агликоном кислоты глицирризиновой (в С3положении присоединяется углеводная цепь из двух молекул глюкуроновой кислоты). Кислота глицирризиновая содержится в солодке голой (Glycyrrhizaglabra) и солодке уральской (G.uralensis).
Углеводная часть тритерпеновых сапонинов может присоединяться к агликону в различных положениях:в С3 положении за счет гидроксильной (-ОН) группы;
в С28 положении за счет карбоксильной (-СООН) группы (при этом связь агликона с сахаром называется ацилгликозидной);
с сапогенином могут быть связаны две углеводные цепи (за счет гидроксильной группы в С3 положении и карбоксильной группы в С28положении). В этом случае сапонины относятся к дигликозидам.
Тритерпеновые сапонины могут быть нейтральными и кислыми. Кислотные свойства обусловлены наличием карбоксильных групп сапогенина и углеводной части молекулы. Гидроксильные группы могут быть ацилированы уксусной, тиглиновой, пропионовой, ангеликовой и другими кислотами.
Углеводная часть тритерпеновых сапонизидов может содержать от 1 до 11 моносахаридов (глюкоза, галактоза, рамноза, арабиноза, фруктоза, глюкуроновая и галактуроновая кислоты). Она может быть линейной и разветвленной (например, у аралозидов — сапонинов аралии высокой). Разветвление углеводной цепи происходит от первого сахарного остатка, связанного с агликоном.
Пути использования сырья, содержащего сапонины
Лекарственное растительное сырье, содержащее сапонины, используется для получения разнообразных лекарственных форм и препаратов.
I.Экстемпоральные лекарственные формы(отпускают без рецепта врача, приказ МЗСР РФ № 587 от 13.09.05).
1. Настои:
листья почечного чая;
трава астрагала шерстистоцветкового.
2. Отвары:
корневища с корнями синюхи голубой;
корни солодки.
3. Порошок корней солодки сложный.
4. Сборы:
сбор отхаркивающий № 2;
сбор «Арфазетин» (входят корни аралии или корневища с корнями заманихи);
сборы мочегонные, противоязвенные и т.д.
II.Экстракционные (галеновые) препараты.
1. Настойки:
женьшеня, биомассы женьшеня;
заманихи;
аралии.
2. Экстракты:
сухой экстракт корней солодки;
густой экстракт корней солодки (входит в состав грудного эликсира).
III.Препараты, содержащие сумму сапонинов.
1. «Сапарал» — сумма аммонийных солей аралозидов.
2. «Полиспонин» — сумма сапонинов диоскореи ниппонской.
3. «Трибуспонин» — сумма сапонинов якорцев стелющихся.
IV.Препараты индивидуальных сапонинов.
1. «Глицирам» — аммонийная соль глицирризиновой кислоты.
2. «Глидеринина мазь» (глидеринин выделен из экстракта корней солодки).
V.Полусинтетические препараты.
1. «Кортизон» (гормон коры надпочечников) — получают на основе стероидного сапогенина диосгенина.
VI.Комплексные препараты.
1. «Амтерсол» (сироп, в состав входит экстракт корней солодки).
2. Грудной эликсир.
3. Настойка биоженьшеня с витаминами и минеральными солями.
4. «Сафинор» (в состав входит сапарал).
VII.Препараты на основе других групп биологически активных веществ.
1. «Ликвиритон» — спазмолитическое, противовоспалительное, антацидное средство.
2. «Флакарбин» — спазмолитическое, противовоспалительное, капилляроукрепляющее средство.
Оба препарата получены на основе флавоноидов корней солодки. Применяются при язвенной болезни желудка и двенадцатиперстной кишки, а также при гиперацидных гастритах.
Сапонины используют также в пищевой промышленности, в технике (для изготовления огнетушителей), в парфюмерии (как мягкие моющие средства).
Медицинское применение сырья и препаратов, содержащих сапонины
Сапонины обладают широким спектром фармакологического действия.
1. Гипохолестеринемическоеипротивосклеротическоедействие. Сапонины обладают способностью снижать уровень холестерина в крови, что приводит к снижению склеротических изменений в кровеносных сосудах, уменьшению их ломкости и т.д. Действие характерно для стероидных сапонинов диоскореи ниппонской и якорцев стелющихся.
2. Тонизирующее,стимулирующее,адаптогенноедействие. Характерно для сапонинов женьшеня, заманихи высокой, аралии высокой. Их препараты применяют при переутомлении, усталости, гипотонии, как иммуномодуляторы.
3. Отхаркивающеедействие. Сапонины повышают секрецию желез верхних дыхательных путей. Это ведет к разжижению мокроты, что облегчает ее эвакуацию. Такое действие характерно для сапонинов солодки и синюхи голубой.
4. Диуретическоедействие характерно для сырья почечного чая и астрагала шерстистоцветкового, которые применяются при отеках сердечного происхождения.
5. Легкое слабительное действие характерно для корней солодки.
6. Кортикотропноедействие (подобное действию кортизона и других гормонов коркового слоя надпочечников). Регулируется водно-солевой обмен, проявляется противовоспалительное и антиаллергическое действие. Характерно для сырья солодки, применяют при астме, экземе, дерматитах.
7. Седативноедействие характерно для сырья синюхи голубой.
8. Гипотензивноедействие при начальных стадиях сердечно-сосудистой недостаточности проявляют биологически активные вещества астрагала шерстистоцветкового.
9. Противоязвенное действие проявляется у сбора, в состав которого входит сырье синюхи голубой и сушеницы топяной.
Физические, химические и биологические свойства сапонинов. Оценка качества сырья, методы анализа.
Физические свойства.Сапонины — бесцветные или желтоватые аморфные вещества. В кристаллическом состоянии выделены гликозиды, имеющие в углеводной цепи до 4 моносахаридов. Оптически активны.
Гликозиды растворимы в воде. Растворимость увеличивается с возрастанием количества моносахаридов в углеводной цепи. В разведенных (60-70 %) спиртах растворяются на холоду; в более крепких (80-90 %) спиртах — только при нагревании, а при охлаждении выпадают в осадок. Нерастворимы в органических растворителях (ацетон, хлороформ, бензол).
Свободные сапогенины не растворяются в воде и хорошо растворимы в органических растворителях.
В зависимости от рН водных извлечений сапонины делят на:
нейтральные — стероидные и тетрациклические тритерпеновые сапонины;
кислые — пентациклические тритерпеновые сапонины. Их кислотность обусловлена наличием карбоксильных (-СООН) групп в структуре агликона или присутствием уроновых кислот в углеводной цепи.
Специфическим свойством сапонинов является их способность снижать поверхностное натяжение жидкостей (воды) и давать при встряхивании стойкую обильную пену. Такая поверхностная активность связана с наличием в молекулах сапонинов одновременно как гидрофильного, так и липофильного остатков.
Химические свойства обусловлены структурой агликона, наличием отдельных функциональных групп, а также присутствием гликозидной связи.
Сапонины гидролизуются под влиянием ферментов и кислот. Производные кислот олеаноловой и глицирретиновой гидролизуются под воздействием щелочей.
При взаимодействии с кислотными реагентами (сурьмы (III) хлорид, сурьмы (V) хлорид, железа (III) хлорид, кислота серная концентрированная и др.) образуют окрашенные продукты.
Кислые сапонины образуют нерастворимые комплексы с солями тяжелых металлов (Ва, Рb,Cu).
Сапонины способны образовывать комплексы с белками, стеринами, липидами, фенольными соединениями. В составе комплексов сапонины не обладают гемолитической и поверхностной активностью.
Сапонины, имеющие в своей основе стероидное ядро, вступают в специфическую реакцию Либермана–Бурхарда.
Биологические свойства. Сапонины обладают гемолитической активностью. Они способны растворять липидную часть оболочки эритроцитов. В результате этого оболочка из полупроницаемой становится проницаемой. Гемоглобин свободно поступает в плазму крови и растворяется в ней. Образуется красный прозрачный раствор — «лаковая» кровь.
Гемолитической активностью обладают только гликозиды. В связи с этим сапонины не применяются для внутривенного введения, т.к. вызывают анемию. При приеме внутрь, после гидролиза в желудочно-кишечном тракте до агликонов, сапонины теряют гемолитическую активность.
Гемолиз эритроцитов вызывают не все сапонины. Этим свойством не обладают сапонины солодки.
Сапонины токсичны для холоднокровных животных (рыбы, лягушки, круглые черви). Они нарушают функцию жабр, которые являются не только органом дыхания, но и регулятором солевого осмотического давления в организме. Сапонины парализуют или вызывают гибель холоднокровных животных даже в больших разведениях (1:1 000000).
Агликоны сапонинов для холоднокровных животных не токсичны.
Оценка качества сырья, содержащего сапонины. Методы анализа
Наличие сапонинов в лекарственном растительном сырье можно установить при помощи качественных реакций, которые проводят непосредственно с сырьем или с водным извлечением из него.
Качественные реакции на сапонины основаны на их физических, химических и биологических свойствах.
Государственная фармакопея XI издания (вып. 2) рекомендует использовать качественные реакции для подтверждения подлинности для трех видов сырья.
1. Корневища с корнями синюхи голубой. С водным извлечением проводят реакцию пенообразования, основанную на способности сапонинов снижать поверхностное натяжение жидкости (воды) и давать в отваре стойкую обильную пену после встряхивания.
2. Корни аралии маньчжурской (а. высокой). Метанольное извлечение хроматографируют в тонком закрепленном слое силикагеля (на пластинках «Силуфол») в системе растворителей хлороформ-метанол-вода (61:32:7). В качестве свидетеля используют раствор сапарала. Хроматограмму проявляют 20 % раствором кислоты серной и нагревают в сушильном шкафу (t= 105 °C) в течение 10 мин. Появляются пятна вишневого цвета.
3. Корни женьшеня.
а) Реакция с порошком корней женьшеня (на гликозиды). При нанесении кислоты серной концентрированной на порошок корней женьшеня через 1-2 минуты появляется кирпично-красное окрашивание, переходящее в красно-фиолетовое, а затем — в фиолетовое.
б) Наличие панаксозидов доказывают при помощи разделения извлечения из корней женьшеня в тонком слое силикагеля и последующего проявления полученной хроматограммы раствором кислоты фосфорно-вольфрамовой при нагревании. Панаксозиды проявляются в виде розовых пятен.
Общих методов количественного определения сапонинов в лекарственном растительном сырье нет. Чаще всего используют методы:
1. Потенциометрическийметод. Метод основан на определении изменения электродвижущей силы (ЭДС) в результате титрования. Метод используется для определения суммы аралозидов в корнях аралии маньчжурской (а. высокой).
Этапы определения:
подготовительный;
экстракция аралозидов метиловым спиртом и их кислотный гидролиз;
очистка от сопутствующих веществ — осаждение кислоты олеаноловой в результате смены растворителя (разбавление спиртового извлечения водой и охлаждение);
растворение кислоты олеаноловой в горячей смеси метилового и изобутилового спиртов (1:1,5);
количественное определение — титрование раствором натрия гидроксида (0,1 моль/л) в смеси метилового спирта и бензола:
Точку эквивалентности определяют потенциометрически.
2. Спектрофотометрическийметод. Метод основан на способности сапонинов и их окрашенных комплексов поглощать монохроматический свет при определенной длине волны. Метод предложен для определения содержания сапонинов в следующих видах сырья:
а) корневища с корнями диоскореи ниппонской. Проводят кислотный гидролиз сапонинов с последующим проведением реакции свободного агликона (диосгенин) с реактивом (пара-диметиламинобензальдегид). Образуется окрашенный комплекс;
б) корни солодки. Проводят осаждение кислоты глицирризиновой концентрированным раствором аммиака. Осадок растворяют и определяют оптическую плотность полученного раствора.
3. Гравиметрическийметод — определение экстрактивных веществ. Метод основан на определении сухого остатка после высушивания суммы веществ, извлеченных из сырья соответствующим экстрагентом. Метод предложен для оценки качества сырья женьшеня, почечного чая, синюхи голубой, солодки.
В сырье астрагала шерстистоцветкового и заманихи высокой количественное содержание биологически активных веществ не определяют.
14. Понятие о простых фенольных соединениях (гликозидах), их классификация. Физические и химические свойства. Особенности заготовки, сушки, хранения сырья. Оценка качества сырья, методы анализа. Пути использования сырья, медицинское применение
Простые фенольные соединения - вещества растительного происхождения, содержащие одно ароматическое кольцо с одной или несколькими свободными или связанными гидроксильными группами.
Классификация простых фенольных соединений (ПФС).
С6-ряд


С6-С2-ряд – фенилэтаноиды

Физико-химические свойства ПФС.
В растениях чаще встречаются в виде гликозидов или сложных эфиров. Наиболее широко распространены фенологликозиды (гидроксильная группа связана с сахаром).
Бесцветные кристаллические вещества, хорошо растворимы в воде, этиловом и метиловом спиртах и этилацетате, водных растворах гидрокарбоната и ацетата натрия; нерастворимы в этиловом эфире и хлороформе. Агликоны плохо растворимы в воде, но хорошо растворимы в эфире, бензоле, хлороформе и этилацетате. Все фенологликозиды оптически активны, обладают фиксированной точкой плавления, индивидуальными УФ- и видимыми спектрами. Способны к кислотному и ферментативному гидролизу.
Легко окисляются, особенно в щелочной среде, образуя хиноидные соединения. Обладают кислотными свойствами, образуют со щелочами растворимые в воде окрашенные соли (феноляты).
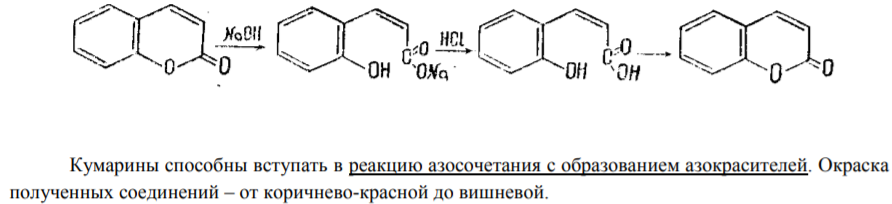
Фенольные гликозиды, имеющие свободную гидроксильную группу, вступают во все реакции, характерные для фенолов: с железоаммонийными квасцами, солями тяжелых металлов, реакцию диазотирования и т.д. С солями диазония образуют азокрасители, от оранжевого до вишнево-красного цвета. В случае, если гидроксил гликозилирован, реакции проводят после кислотного или ферментативного гидролиза.
Особенности заготовки, сушки, хранения сырья.
Заготовку сырья брусники и толокнянки проводят в два срока — ранней весной до цветения и осенью с начала созревания плодов до появления снежного покрова. Сушка воздушно-теневая или искусственная при температуре не более 50-60 °С в тонком слое. Повторная заготовка на одних и тех же зарослях возможна через 5-6 лет.
Сырье родиолы розовой (золотой корень) заготавливают в фазы конца цветения и плодоношения. Сушат при температуре 50-60 °С. Повторная заготовка на одних и тех же зарослях возможна через 10-15 лет.
Сырье щитовника мужского (Rhizomata Filicis maris) собирают осенью, не моют, сушат в тени или в сушилках при температуре не более 40 °С. Повторная заготовка на одних и тех же зарослях возможна через 20 лет.
Сырье хлопчатника — кору корней (Cortex radicum Gossypii) — заготавливают после сбора урожая хлопка.
Хранят сырье по общему списку в сухом, хорошо проветриваемом помещении. Срок годности — 3 года. Корневища папоротника мужского хранят 1 год.
Оценка качества сырья, методы анализа.
Качественные реакции.
1. На арбутин:
1.1.С сульфатом закисного железа. К водному извлечению прибавляют кристаллик сульфата закисного железа, развивается сначала сиреневый, затем темно-фиолетовый цвет и образуется темно-фиолетовый осадок.
1.2. С фосфорномолибденовокислым натрием. К водному извлечению прибавляют 4 мл р-ра аммиака и 1 мл 10% раствор фосфорно-молибденовокислого натрия в хлористоводородной кислоте; развивается синее окрашивание.
2. На салидрозид: После ТСХ в у/ф свете (254 нм) наблюдается фиолетовое пятно розавина; после обработки анисового альдегида р-ром уксуснокислым, при нагревании, видно красно-коричневое пятно салидрозида.
Количественное определение.
1) Гравиметрический метод (флороглюциды в корневищах папоротника мужского). Этапы: извлечение флороглюцидов диэтиловым эфиром в аппарате Сокслета, очистка методом смены растворителей, отгонка эфира, высушивание сухого остатка до постоянной массы.
2) Спектрофотометрический метод: арбутин в листьях брусники и толокнянки. Этапы: извлечение 70%-ным этанолом; очистка на хроматографической колонке, заполненной алюминия оксидом; определение оптической плотности раствора (при длине волны 285 нм); расчет содержания с использованием удельного показателя поглощения арбутина.
3) Метод ВЭЖХ: салидрозид и розавин в корневищах и корнях родиолы розовой.
Пути использования сырья, медицинское применение
Из лекарственного растительного сырья, содержащего фенологликозиды, получают:
1. Экстемпоральные лекарственные формы:
- отвары (сырье брусники, толокнянки, родиолы розовой);
- сборы (сырье брусники, толокнянки, родиолы розовой).
2. Экстракционные (галеновые) препараты:
экстракты:
- жидкий экстракт (корневища и корни родиолы розовой);
- густой эфирный экстракт (корневища папоротника мужского).
3. Новогаленовые препараты:
«Родаскон» из сырья родиолы розовой.
4. Препараты индивидуальных веществ:
3 % линимент госсипола и глазные капли — 0,1 % раствор госсипола в 0,07 % растворе натрия тетрабората (кора корней хлопчатника).
Сырье, содержащее простые фенольные соединения, обладает широким спектром фармакологического действия.
1. Антимикробное, противовоспалительное, диуретическое (мочегонное) действие характерно для сырья брусники и толокнянки. Оно обусловлено наличием в сырье арбутина. Применяют лекарственные формы из сырья брусники и толокнянки для лечения воспалительных заболеваний почек, мочевого пузыря (циститы, уретриты, пиелиты) и мочевыводящих путей.
2. Противовирусное действие характерно для фенольных соединений коры корней хлопчатника. «Госсипол» применяют при лечении опоясывающего лишая, простого герпеса, псориаза (линимент); при герпетическом кератите (глазные капли).
3. Адаптогенное, стимулирующее и тонизирующее действие оказывают препараты корневищ и корней родиолы розовой. Применяют для лечения больных неврозами, гипотонией, вегето-сосудистой дистонией, шизофренией.
4. Антигельминтное (противоглистное) действие оказывают препараты корневищ папоротника мужского. Применяют экстракт мужского папоротника густой при инвазиях ленточными паразитами. При его использовании через 30-40 минут назначают только солевые слабительные средства, способствующие изгнанию паразита из желудочно-кишечного тракта.
15. Понятие о кумаринах и хромонах, их классификация. Роль для жизни растений. Физические и химические свойства. Оценка качества сырья, методы анализа. Пути использования сырья, медицинское применение.
Кумарины
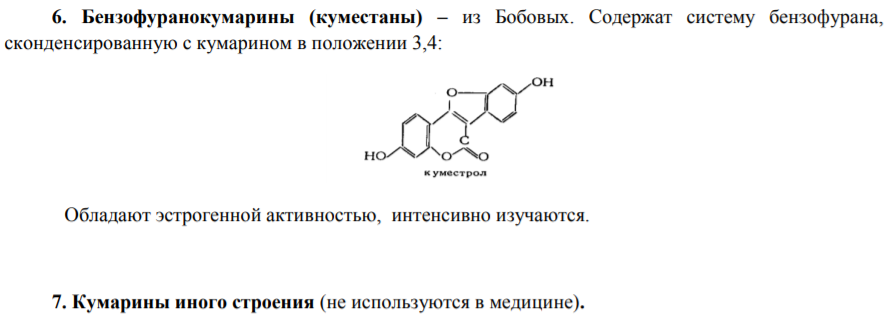
Кумаринами называются природные фенольные гетероциклические соединения, в основе которых лежит конденсированная система бензольного ядра с альфа-пироновым - 9,10-бензо-альфа-пирон.
Кумарин можно рассматривать как ненасыщенный ароматический лактон цис-ортооксикоричной кислоты:

Кумарины довольно часто встречаются в высших растениях, реже - в низших, совсем не обнаружены в водорослях, незначительно представлены в папоротникообразных и голосеменных. Практически все известные кумарины выделены из покрытосеменных. В этой группе особенно высоким содержанием кумаринов отличаются семейства Apiaceae, Rutaceae, Fabaceae, Hippocastanaceae и некоторые другие.
Кумарины локализуются в различных органах растений, чаще и больше всего в корнях, коре, плодах, меньше - в стеблях и листьях. Содержание этих соединений в разных растениях колеблется от 0,5 до 2 (10) %, причем встречаются до 10 разных кумаринов в одном растении. В природе чаще всего встречаются наиболее простые производные кумаринов. Основное количество соединений этой группы в растениях найдено в свободном состоянии, т.е. в виде агликонов, и лишь незначительное число - в виде гликозидов. Углеводная часть кумариновых гликозидов чаще всего представлена D-глюкозой, присоединенной у С-6, С-7 или С-8 кумаринового ядра.
Роль в жизни растений: Кумарины обладают разносторонней биологической активностью. Они участвуют в регуляции роста растений, защищают их от избыточного солнечного облучения, вирусных заболеваний.


Физико-химические свойства кумаринов.
Выделенные в индивидуальном виде кумарины представляют собой бесцветные или слегка желтоватые кристаллические вещества, хорошо растворимые в органических растворителях (этиловом спирте, хлороформе, диэтиловом эфире и т.д.), жирах и жирных маслах; в воде нерастворимы или малорастворимы. Гликозиды кумаринов растворимы в воде и нерастворимы в органических растворителях.
Особенностью кумаринов является их легкая растворимость (особенно при нагревании) в водных растворах щелочей за счет образования солей оксикоричной кислоты.
При нагревании до 100оС кумарины способны к сублимации (возгонке) и обнаруживаются в виде игольчатых кристаллов.
Многие кумарины имеют характерную флуоресценцию в ультрафиолетовой части спектра; в щелочной среде она усиливается, в кислой – менее интенсивна.
Характерным свойством всех групп кумаринов является их специфическое отношение к щелочи. При действии горячей разбавленной щелочи (10%) они медленно гидролизуются, при этом происходит обратимый разрыв лактонного кольца с образованием растворов желтого цвета (соли цисортогидроксикоричной кислоты – кумаринаты). При подкислении щелочных растворов (10% НCl) или при насыщении углекислым газом кумарины переходят в исходное состояние, и образовавшийся кумарин выпадает в осадок. Это свойство использует при качественном анализе кумаринов (лактонная проба).
Качественный анализ кумаринов.
Для обнаружения кумаринов в растительном сырье используют их лактонные свойства, способность флуоресцировать в ультрафиолетовом свете, давать окрашенные растворы с диазосоединениями, способность к микросублимации, а также применяют хроматографический анализ с последующим проявлением хроматограмм диазореактивом или просмотром при УФосвещении.
Количественное определение кумаринов.
При количественном определении кумаринов учитывается то или иное специфическое свойство оцениваемого кумарина.
1. Наличие нескольких полос высокой интенсивности в интервале длин волн 220-320 нм позволяет использовать для количественного определения кумаринов УФ-спектрофотометрию (трава донника лекарственного, корневища и корни вздутоплодника сибирского).
2. Хроматоспектрофотометрический метод: количественной оценке кумаринов предшествует их разделение на хроматографических колонках или в тонком слое сорбента (плоды амми большой, псоралеи костянковой, листья инжира).
3. Полярографический метод (в плодах пастернака). Восстановление кумаринов на ртутнокапельном электроде в альфа-пироновом кольце по месту двойной связи в положении 3-4.
Дополнительные методы:
4. Способность кумаринов давать устойчивые красно-оранжевые и красно-пурпуровые растворы с диазотированным сульфаниламидом в щелочной среде используется в колориметрических методах определения кумаринов.
5. Специфическая реакция кумаринов со щелочами лежит в основе метода нейтрализации (обратное титрование), который применяется для определения как суммы кумаринов, так и индивидуальных компонентов.
6. Способность лактонного кольца кумарина к обратимому размыканию и смыканию в зависимости от рН среды, сопровождающемуся выпадением осадка, используется в гравиметрическом методе определения суммы кумаринов в растительном сырье.
Пути использования сырья, медицинское применение.
1. Экстемпоральные лекарственные формы:
— настой травы донника;
— успокоительный сбор (трава донника).
2. Экстракционные препараты:
— «Эскузан ликвидум» (Германия) — водно-спиртовой экстракт семян конского каштана (по 20 мл);
— «Эскузан» — водно-спиртовой экстракт семян конского каштана, выпускается в виде драже.
3. Препараты, получаемые на химико-фармацевтических заводах.
3.1. Препараты, содержащие сумму веществ:
— «Эсфлазид» — сумма сапонинов и кумаринов (из семян) и флавоноидов (из листьев) конского каштана (табл. 0,1 N 30);
— «Бероксан» — смесь ксантотоксина и бергаптена из плодов пастернака посевного (табл. 0,02 N 50; 0,25 % и 0,5 % растворы по 50 мл).
— «Аммифурин» — смесь бергаптена, ксантотоксина и изопимпинеллина из сырья амми большой (табл.0,02 N 100; 0,3 % раствор по 50 мл);
— «Псоберан» — смесь фурокумаринов псоралена и бергаптена, выделенных из листьев инжира (табл.0,01 N 50; 0,1 % раствор по 50 мл).
— «Фловерин» — смесь пиранокумаринов (дигидросамидина и виснадина) из корневищ и корней вздутоплодника сибирского (табл. 0,05 N 100).
3.2. Комплексные препараты:
— «Сафинор» — входят: фловерин, сапарал, рибоксин и калия оротат (табл.0,65 N 50).
Природные производные кумарина обладают многосторонней биологической активностью.
1. Сырье, содержащее простые кумарины, обладает мягчительным действием. Траву донника используют в виде припарок, способствующих вскрытию и рассасыванию нарывов. Также она входит в состав успокоительных сборов, проявляет успокаивающее, противосудорожное и антикоагулянтное действие. Трава донника обладает противовоспалительным, венотонизирующим, анальгезирующим, фибринолитическим и спазмолитическим действием.
2. Сырье, содержащее гидроксикумарины, обладает антикоагулянтным действием, гидроксикумарины препятствуют свертываемости крови, оказывают венотонизирующее и Р-витаминное действие. Для профилактики и лечения тромбозов, тромбофлебитов, тромбоэмболии, геморроя назначают препараты «Эсфлазид», «Эскузан ликвидум», «Эскузан».
3. Фотосенсибилизирующее (антилейкодермическое) действие. Фурокумарины обладают способностью повышать чувствительность кожи к действию УФ-лучей, стимулировать образование пигмента меланина (т.е. способствовать восстановлению пигментации кожи и волос).
4. Коронарорасширяющее и спазмолитическое действие. Характерно для пиранокумаринов и некоторых фурокумаринов, на основе которых созданы препараты:
— «Фловерин» — применяют при неспецифических ангиоспазмах и эндартериитах различной этиологии;
— «Сафинор» — применяют при ишемической болезни сердца, инфаркте миокарда, тяжелых заболеваниях и нагрузках, которые сопровождаются астеноневротическими реакциями и вегетативной дистонией; для лечения алкоголизма и абстинентных состояний.
Хромоны
Как к кумаринам, так и к флавоноидам по химической структуре близка группа веществ растительного происхождения, называемая хромонами. Хромоны – природные фенольные соединения, получающиеся в результате конденсации гамма-пиронового и бензольного колец, производные бензо-гамма-пирона. Известно около 50 производных хромона, преимущественно в растениях из сем. Myrtaceae, Apiaceae.
Классификация

Из числа известных производных хромонов медицинское значение пока имеют только фуранохромоны - келлин и виснагин, содержащиеся в плодах амми зубной. Они оказывают спазмолитическое действие при спазмах гладкой мускулатуры (назначают при бронхиальной астме, спазмах ЖКТ, стенокардии)

Физико-химические свойства.
Хромоны - белые или желтоватые кристаллические вещества, без запаха, с горьким вкусом, в воде нерастворимы, хорошо растворимы в органических растворителях (этиловом спирте, хлороформе, диэтиловом эфире и т.д.). Гликозиды растворимы в водно-спиртовых растворах и воде.
Характерна желтая, желто-зеленая, голубая, коричневая флуоресценция в УФ-свете. Ее интенсивность усиливается при действии паров аммиака или спиртовых растворов щелочей. В отличие от кумаринов, она усиливается и при обработке серной кислотой.
Кроме того, в отличие от кумаринов, при реакции со щелочью у хромонов происходит необратимое раскрытие гамма-пиронового кольца (кумарины при подкислении р-ра регенерируют).
При реакции азосочетания в растворах хромоны дают желтую окраску, а не красную, как кумарины. От кумаринов хромоны отличаются и по спектрам поглощения.
Качественные реакции.
С 0,1% р-ром уранилацетата хромоны образуют окрашенные р-ры или желтый осадок. С конц. кислотами (серной, хлористоводородной, ортофосфорной) образуют оксониевые соли лимонножелтого цвета. С конц. щелочами – пурпурно-красное окрашивание.
Количественное определение – фотоколориметрический и хроматоспектрофотометрический методы.
Пути использования сырья, медицинское применение
Из сырья виснаги морковевидной на фармацевтических заводах получают препараты, расширяющие коронарные сосуды сердца и бронхи, а также расслабляющие мышечную ткань органов брюшной полости и мускулатуру мочеточников:
— «Келлин» используется как спазмолитическое и седативное средство при стенокардии и бронхиальной астме;
— «Ависан» — препарат, содержащий сумму фуранохромонов, пиранокумаринов и флавоноидов виснаги морковевидной. Является эффективным спазмолитическим средством при спазмах мочеточников, почечных коликах и выведении почечных камней.
Келлин в настоящее время как самостоятельное средство почти не применяется. Он используется главным образом в составе комплексных препаратов «Викалин» и «Марелин». «Викалин» применяется при язве желудка, двенадцатиперстной кишки и гиперацидных гастритах. «Марелин» как спазмолитическое и противовоспалительное, а также способствующее отхождению почечных конкрементов средство применяется при почечных коликах, для профилактики рецидивов после операционного удаления камней и их самопроизвольных отхождений.
16. Понятие о лигнанах, их классификация. Физические и химические свойства. Закономерности образования, накопления и распространения в растениях. Пути использования сырья, медицинское применение



Физико-химические свойства.
Бесцветные или слегка окрашенные твердые кристаллические вещества. Оптически активны. Хорошо растворимы в спирте, водно-спиртовых смесях, хлороформе, бензоле, эфире, жирных и эфирных маслах; нерастворимы в воде и не перегоняются с водяным паром (кроме гликозидов), что вызывает трудности при их выделении из сырья. В УФ свете - голубая или желтая флуоресценция. Избирательно поглощают свет при длине 275-280, 220-230 нм.
Лигнаны довольно широко распространены в растительном мире. Особенно часто встречаются в растениях семейств сложноцветных (Asteraceae), аралиевых (Araliaceae), барбарисовых (Berberidaceae), березовых (Betulaceae), буковых (Fagaceae), гречишных (Polygonaceae), норичниковых (Scrophulariaceae), рутовых (Rutaceae), сосновых (Pinaceae), лимонниковых (Schisandraceae).
Лигнаны накапливаются во всех органах и тканях растений. Максимальное накопление лигнанов наблюдается преимущественно в период плодоношения в семенах и плодах лимонника, а также в подземных частях — корневищах и корнях элеутерококка, корневищах с корнями подофилла.
Пути использования сырья, медицинское применение
1. Экстемпоральные лекарственные формы:
отвары (плоды и семена лимонника, корневища и корни элеутерококка);
тонизирующие и гипогликемические сборы (корневища и корни элеутерококка);
сок свежих плодов лимонника;
порошок семян лимонника.
2. Экстракционные (галеновые) препараты:
настойка (1:5) (плоды и семена лимонника);
жидкий и сухой экстракты (корневища и корни элеутерококка).
3. Суммарные (готовые) препараты:
«Подофиллин» (корневища с корнями подофилла);
«Карсил», «Легалон», «Силегон», «Силимар», «Силибор», «Силимарин» (сумма флаволигнанов из плодов расторопши пятнистой).
Лигнаны обладают рядом ценных фармакологических свойств:
1. Тонизирующее, стимулирующее и адаптогенное действие. Характерно для препаратов элеутерококка и лимонника, которые являются аналогами женьшеня. Препараты элеутерококка понижают уровень сахара в крови, повышают содержание гемоглобина, нормализуют кровяное давление, усиливают остроту зрения.
2. Слабительное, желчегонное, цитостатическое действие. Характерно для препаратов подофилла. «Подофиллин» (смола, содержащая смесь лигнанов подофилла) обладает выраженным слабительным действием при хронических запорах и желчегонным эффектом, усиливает выделение желчи. Применяется также при папилломатозах гортани, папилломах мочевого пузыря. Блокирует деление клеток злокачественных образований на стадии метафазы.
3. Антигеморрагическое действие. Кунжутное масло, содержащее лигнаны, используется для лечения тромбопении и геморрагических диатезов.
4. Гепатопротекторное действие. Характерно для препаратов из плодов расторопши пятнистой, обусловлено флаволигнанами. Применяются при токсических поражениях печени, остром и хроническом гепатите, циррозе печени, нарушении липидного обмена, жировой дистрофии печени.
17. Понятие об антраценпроизводных, их классификация. Закономерности образования, локализации и распространения в растениях. Роль для жизни растений. Пути использования сырья, медицинское применение.
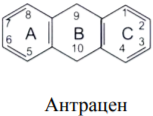
Антраценпроизводными называют группу природных соединений, в основе которых лежит ядро антрацена различной степени окисленности по кольцу В.
Производные антрацена широко распространены в природе, известно более 200 соединений. Они обнаружены в высших растениях, лишайниках, некоторых низших грибах, плесени, а также найдены в некоторых насекомых и морских организмах. Около половины известных антраценпроизводных выделено из высших растений. Наиболее богаты антраценпроизводными виды семейств Rhamnaceae, Polygonaceae, Hypericaceae, Liliaceae, Fabaceae, Rubiaceae, и др.
Антраценпроизводные в растениях встречаются как в свободном виде (в виде агликонов), так и в сочетании с углеводным компонентом, т.е. в виде гликозидов, и в этом случае они называются антрагликозидами. Углеводный компонент может быть представлен глюкозой, рамнозой, ксилозой, арабинозой. Большинство антрагликозидов – О-гликозиды; при этом углеводный компонент может быть присоединен к агликону в - и -положениях. Обнаружены С-гликозиды (в сырье алоэ, сенны).
Антрагликозиды в растениях содержатся в клеточном соке в растворенном состоянии, агликоны – в виде кристаллических включений (в сердцевинных лучах, паренхиме коры).
Встречаются, в основном, в коре, древесине, подземных органах. Содержание – от 2 до 6%. С возрастом их количество увеличивается, причем в старых растениях преобладают окисленные формы, в молодых – восстановленные. Больше восстановленных форм весной, к осени они переходят в окисленные. Более фармакологически ценны окисленные формы; восстановленные формы вызывают тошноту, рвоту, колики. В живых растениях и в свежезаготовленном сырье антраценпроизводные находятся, как правило, в восстановленной форме, а в высушенном – преимущественно в окисленной.
