
- •Запасы углеводородного сырья
- •Лекция № 3 Прямая перегонка нефти
- •Углеводородный состав нефти
- •Лекция № 4 Углеводородный состав нефти (продолжение) Парафиновые углеводороды нефти.
- •Нафтеновые углеводороды нефти.
- •Ароматические углеводороды нефти.
- •Углеводороды: гибридного или смешанного строения.
- •Кислородные соединения нефти.
- •Сернистые соединения нефти
- •Азотистые соединения нефти
- •Практика № 1 Смолисто - асфальтеновые вещества нефти.
- •Уголь Твердые горючие ископаемые
- •Подготовка твердых горючих ископаемых веществ к переработке
- •Подготовка угля к обогащению
- •3. Дробление - процесс разрушения кусков материала под воздействием внешних сил для получения продукта заданной крупности.
- •Завершающие стадии обогащения угля.
- •Переработка твердых горючих ископаемых.
- •Твердый остаток (полукокс)
К невосполнимым источникам эн-ии относятся 3 вида: природные УВ-газы, жидкие нефти, тв. горючие орг. в-ва (нефтебитумы, горные сланцы, каменные угли). Сырые энергоносители после очистки и предварит. подготовки перерабатываются в основном в топливо (≈85-90%), масла и спец. продукты. И только в 20-м веке нефтеприродный газ стал источником орг. сырья.
В наст. вр. весь орг. синтез базируется на ископаемом сырье (камен. уголь, нефть, природный газ). В процессах их физического, термического и каталитического расщепления (крекинг, пиролиз, риформинг, конверсия, коксование) получают 5 главных групп исходных в-в для синтеза многих орг. соед-й: 1) парафины (от СН4-С15-С40) 2) олефины (С2Н4, С3Н6, С4Н8, С5Н10) 3) ароматические УВ (бензол, толуол, ксилолы, нафталин) 4) ацетилен (С2Н2) 5) синтез-газ СО+Н2. Первичная переработка этих 5 групп исх. в-в в др. продукты есть основная фун-я отрасли орг. синтеза. А выделение этих 5 групп из ископаемого сырья – есть фун-я отрасли производства УВ-сырья. УВ-сырье в осн. используется как топливо, поэтому его кол-во учитывается в условных единицах 1 т.у.т. = 7*106 ккал = 29,274*106. Ориентировочные данные о записях ископаемого топлива в ед. 1,05*1018 кДж. Мировые запасы природного УВ-газа оцениваются в 142 триллиона кубометров (115 млрд тонн). 18% мировых запасов газа нах. в России, 15% от мир. добычи газа тоже в России. Ежегодное мировое потребление газа 1800 млрд м3, в т.ч. в России 850 млрд м3. Из общих мировых запасов ≈55 трлн м3 приходится на страны СНГ. Ближ. Восток – 45 трлн м3, Американ. континент трлн м3, Американ. континент – 15 трлн м3, Азия и Тихий океан – 10 трлн м3, Африка – 10 трлн м3, Запад. Европа - трлн м3. Страны экспортеры газа (400 млрд м3 уходит в год): Россия – 38%, Канада – 14%, Туркмения – 9%, Нидерланды – 8%, Алжир – 8%, Индонезия – 7%, Норвегия – 6%. Страны импортеры (в млрд м3): Украина – 72, США – 60, Германия – 55, Япония – 40, Италия – 30, Франция, Беларусь – 15. Месторождения УВ-газа в России располагаются: 1) северные районы западн. Сибири (Оренгойское и Медвежье) 2) Заполярное на Ямале 3) Оренбургская обл. 4) Астраханские месторож-я 5) Башкирия 6) Дагестан 7) Урало-Поволжье. В России гигантом газ. промыш-сти явл. Газпром, кот. обладает разведданными запасами ≈50 млн м3. Доля осн. регионов в общей добыче газе Газпрома: Тюменская обл. – 8,6%, Оренбургская – 5,6%, Астраханская обл. – 2%. Большинство УВ-газов сод. в кач-ве примесей (1-5%) не УВ-газы: N2 и CO2, сероводород H2S, сероуглеродные COS и CS2, а также сероорганические RSH (R-орг. радикал). Месторожд-я, богатые азотом: Удмуртия (Чутырское, Киенгопское) – 70-76%, Узбекистан (Учкыр) – 12-54%. Содерж-е H2S обычно бывает до 3-х %, газ Оренбургского месторож-я сод. 1,3-4,5% H2S, а во Франции (Лак) – 15%. Некот. газы. газоконденсатных (г/к) месторожд-й Астраханской обл. имеют сод-е 1,6-14% H2S. CO2 обычно бывает от 0,1 до 7%. Ar и He в некот. американ. месторожд-ях достигает до 7%, а в российских – 0,02-0,05%. УВ-газ добывается в виде метан-этановой смеси, не содержащей конденсата (менее 10 мл на м3), метан-этан-пропановой смеси с примесями бутана и конденсата (20 мл на м3 и более, до 400). Газ исп-ся как бытовое, печное моторное топливо и для различных нужд нефтехимии, производства этилена, Н2, синтез-газа, биосинтеза кормового белка из СН4+С2Н4.
Газ. Главным источником С1-С5 явл. природные и попутные (нефтяные) газы. Газ г/к-месторождений, а также нефтезаводские газы от процессов переработки нефтепродуктов в присут-ии Н2, напр. риформинг. Природными наз. газы из чисто газовых месторождений. Состав их – насыщ. УВ, в осн. сост. из СН4 – 80-99%. Но газы некот. мест-й (Пермской, Оренбуржской, Куйбышевской, Дагестана, Узбекистана сод. только СН4 31-80%). Сод-е С2Н6 достигает 12%, N2 – 10%, но масторож-е Пермской, Саратовской, Оренбургской, Куйбышевской, Узбекистана (Учкыр), сод. имеет в своем составе от 12 до 54% N2. А газ Астраханской обл. сод. 23% H2S и 25% СО2. Другие газы. Некот. газовые месторожд-я с высоким пластовым давл-ем отлич. тем, что в газе сод. значительное кол-во жидких УВ. При снижении давл-я эти жидкие УВ конденсир. и могут быть отделены от газа. Это явл-е получило назв-е ретраградной конденсации, а жидк., выделенная из газа при добыче, наз. конденсатом, кот. сод. УВ от С5Н12 до С20Н42 и выполняет в большинстве случ-ев от 40 до 350 °С. Конденсаты содержат бензиновые и керасиновые фракции, а газ г/к-месторожд-й по составу близок к природному газу. В процессе эксплуатации г/к-месторожд-й пластовое давл-е снижается и в рез-тате конденсации часть конденсата высаживается из газа, оставаясь в пласте. При этом в 1-ую оч. снижаетсся сод-е тяжелых УВ. С целью увеличения степени извлечения конденсата необх-мо поддерж. пластовое давл-е путем возврата части газа в пласт – сайклинг-процесс. Он весьма заманчив для повыш-я отбора конденсата, но дороговат (надо строить технологич. установку, дожимную компрессорную высок. давл-я, надо бурить нагнетательные скважины, поэтому неизбежна консервация добычи газа в среднем на 10-15 лет. За это время конденсата в пласте остается столько, что его добыча станов. невыгодной). Для удешевления сайклинг-процессов прим. т.н. частичный сайклинг-процесс. В этом случ-е при циркуляции в пласт возвращается только часть. При частичном сайкл.-пр. давл-е в пласте постепенно сниж., что приводит поток к частичному выд-ю в пласте жидк. конденсата. В процессе непрерыв. циркуляции сухого газа поры пласта с выпавшим конденсатом как бы промыв. газом, в рез-тате чего жидк. УВ испаряются и уносятся общим потоком газа. Конденсатов некот. месторож-й сод. 40% нафтеновых УВ (алициклич. УВ), что делает эти конденсаты ценным сырьем для нефтехимии. Березанское месторож-е (Краснодар. к.), Очакское (Туркмения), а также есть конденсаты, сод. пром. УВ (Березанское, Майкопское). Парафино-нафтеновые – Оренгойское мест-е (Запад. Сибирь). Все эти конденсаты – прекрасное сырье производства нефтехим. полупродуктов. Попутные нефтяные газы. Попутными наз. газы, выд. вместе с нефтью при ее добыче из нефтяных скважин. Попутный нефт. газ сост. из насыщ. УВ С1-С5 и некот. кол-ва инертных газов. Наиболее ценными явл. С2-С5-сырье для нефтехимии. Часть газа отделяется в сепараторах, а др. остается растворенной в нефти и отдел. при ее стабилизации, т.е. от гонки летучих компонентов при нагревании газостабилизации. Природн. газ выгодно исп. как источник СН4. К нему близок газ г/к-месторождений. Нефтяные камни (Азербайджан) сод. С3 и более 54 г/м3, а Герасимовское месторож-е (Оренбург. обл.) – 13304 г/м3. С2Н6 - значит-но содержание от 160 до 425 г/м3 (Коми, Урало-Поволжье, Восточ. Украина). Н2S 219 г/м3 – много (Щелкановское мест-е (Башкирия)). Нефтезаводские газы. В них сод. насыщ. и ненасыщ. УВ – С1-С4. Кроме того, в состав могут вх. Н2, Н2S, небольшое кол-во органич. соед-ний S. Осн. источником газа явл. процессы деструктивной переработки нефти (термич., каt крекинг и риформинг). Поэтому, наряду с насыщ. УВ сод. много олефинов и некот. кол-во водорода. Газ каt риформинга богат H2 (до 60% об.) и сод. только насыщ. УВ. Такое различие в составе газов услож. их переработку.
Требования к кач-ву товарных газов. Потребитель газов нах. на большом расстоянии от места добычи газов, поэтому обеспечение бесперебойной подачи газа потребителям явл. определяющим при разработке качественных показателей. Условием этого является: 1) газ не должен вызывать коррозию трубопроводов, арматуры и приборов. 2) продукт должен оставаться в однофазном сост-ии. 3) не должен вызывать осложнений у потребителей при исп-ии. Для ряда процессов недопустимо наличие в газе H2O, CO, CO2, H2S, NH3 и др. реакционных примесей. Первичная подготовка газа к переработке. Сырой газ из скважин поступает на установку комплексов подготовки газа, где происходит отделение механич. примесей и осушка газа. Далее поступает на установку по выделению из него вредных примесей (сернистых соед-ний) и нежелательных примесей (N2, CO2, влага), и отделение газового конденсата (УВ от пропана и выше), получение He из сухого газа. Из конденсата на установке стабилизации выделяют широкую фракцию легких УВ С2-С5 и газовый бензил. В осн. группу процессов очистки и переработки входят стадии: 1) сепарация конденсата – отделение жидк. фазы, выполнимой газом из скважины 2) сепарация капельной жидк-и 3) отделение вредн. примесей (H2S и CO2) 4) глубокая сушка газа от влаги до температуры точки росы (т.р.) – 30 и ниже. 5) отбензинивание газа (удаление из него УВ от пропана и выше) 6) извлечения гелия. H2S обычно перерабатывается на месте с получ-ем элементар. S.
Продуктами переработки и нефтяных газов явл.: 1) товарный природный газ, направляемый по газопроводам в кач-ве газового, промыш. и бытового топлива 2) ШФЛУ (широк. фракция легких УВ) 3) Сжиженный газ – концентрат УВ в С3-С4, выделенный из ШФЛУ 4) газовый конденсат 5) гелий 6) одорант (в осн. этилмеркаптан) – сильно пахнущее в-во. Влага в газах. Нефтяные и природные газы, добываемые из недр Земли, насыщены водяными парами, содерж-е кот. опр. давл-ем, темпер. и хим. составом газа. Каждому знач-ю температуры и давления соответствует макс. возможное содержание водяных паров. Влагосодержание, соответствующее полному насыщению газа водяными парами, наз. РАВНОВЕСНЫМ. Если понизить температуру газа, содержащего максимально возможное количество водяных паров, оставив давление неизменным, то часть водяных паров сконденсируется. Температура, при кот. водяные пары, содержащиеся в газе конденсир. наз. точкой росы газа по влаге при данном давлении. С увеличением плотности газа и содержания солей величина влагосодержания уменьшится. На равновесие влагосодержания влияет наличие в газе С3Н8 и более тяж. УВ (H2S, CO2, N2 – влияют)
В присут. H2S и CO2 влагосодерж-е увелич., а в пр. N2 – уменьш. Сод-е в нефтяных и природных газах водян. паров регламентируется, т.к. они могут конденсироваться в технологич. системах, в рез-тате чего будут создаваться усл-я для обр-я гидратов (тв. кристаллич. в-в), кот. закупоривают пространство трубопроводов и затрудняют нормальное усл-е эксплуатации объектов добычи, переработки и транспортировки газов.
ГАЗОВЫЕ ГИДРАТЫ (г.г.). Гидраты представляют собой соед-я - включения, кот. могут существовать в стабильном состоянии, не являясь хим. соед-ем. Гидраты – тв. р-ры, где р-лем явл. молекулы H2O, образующие с пом. водородных связей объёмный каркас гидрата, в полостях кот. нах. молекулы газов (CH4, C2H6, пропан, бутан, N2, H2S, CO2, Ar), способных образовывать гидраты. Кристаллогидраты обр. на поверхности раздела фаз газ-вода. Свободная вода после обр-я гидратов продолжает переходить в гидратное сост-е только при перемешивании фаз и при наличии соотв. т/д усл-й. При отсутствии перемешивания диффузия через тв.плёнку гидратов становится затруднительной и дальнейший рост гидратов прекращается. Усл-е обр-я гидратов зависит от сод-я минеральных солей в H2O (кот. нах. в газе) – с увелич-ем их сод-я температура начала гидратообр-я понижается. По внеш. виду г. напомин. лед или лёгкий спрессованный снег.
Для опр-я равновесных
усл-й обр-я гидратов в природных газах
широко исп-ся НОМОГРАММА;
зная
плотность газа и его давление можно
опр. температуру гидратообр-я. Молекулы
газа связ. с молекулами H2O
в каркасе вандер-вальсовыми связями.
Газ в тв. сост-ии (гидратах), минуя жидк.
сост-е, переходит в газообр. и таит в
себе огромную силу; если его сразу
выпустить на волю, то он может вызвать
экологич. катастрофу. На Земле около
половины углерода, связ. в орг. и неорг.
соед-ях, сод. в виде гидратов CH4.
Гидраты обл.
высоким электрич. сопротивл-ем, хорошо
проводят звук и практически непроницаемы
для свободных молекул H2O
и газа. У них
очень низкая теплопроводность (для
метано-гидрата 273К в 5 раз ниже чем у
льда). Плотность гидрата CH4
ниже плот. H2O
и льда и составл.
 =900кг/м3.
Гидраты явл.
источником газа, кот. может
составить реальную конкуренцию
традиционн. месторожд-ям газа в силу
неисчерпаемости ресурсов широкого
распр-я не глубокого залегания и
концентрир. сост-я газа.
=900кг/м3.
Гидраты явл.
источником газа, кот. может
составить реальную конкуренцию
традиционн. месторожд-ям газа в силу
неисчерпаемости ресурсов широкого
распр-я не глубокого залегания и
концентрир. сост-я газа.
1 м3 CH4 -гидрата сод. до 300 м3 газа и 0,78 м3 H2O. Хар-но то, что процесс гидратообр-я протек. и в настоящ. время. Залежи гидратов в осн. распр. на шельфах морей и океанов, на морском дне и под ним (≈98%) и только 2% гидратов залегает на суше. Гидраты нах. в шельфовых зонах и прибрежных склонах на небольшой глубине и встреч. практически на любых широтах. Шельф – выровненная обл. подводной окраины материка, примыкающий к суше. Границами шельфа явл. берег моря или океана и т.н. бровка (резкий перегиб морского дна – переход к материковому склону).
Глубина над бровкой обычно 100-200 м или 300-1500 м (Охотское море). Наиболее обширен шельф у северного побережья Австралии. Газ. гидраты были обнаруж. под мёрзлыми породами в север. районах России, Аляски и Канады. По разным данным от 10 до 60% территории России благоприятны для накопления гидратов. На суше в России выявл. гидратопроявления на Янбургском газоконденсатном месторожд-ии (ГКМ), Бованском и в районе алмазной трубки Удачной, на золотоносных (?) Чукотки, Мессояхском месторожд-ии. Наиболее известные на сегодняш. день мест-я метаногидр.: Маллик (Канада), Нанкийское (Япония), Мессояхское (РФ). В Баренцевом и Охотском морях кол-во метана оценивается 1100-1200 трлн. м3. По данным России в Чёрном море 2530 трлн. м3, но, к сожалению, пока нет технологии добычи газов из гидратов.
МЕТОДЫ ПРЕДУПРЕЖДЕНИЯ ГИДРАТООБР-Й: применяются: 1) ингибирование (подача в газ. поток различ в-в, понижающих темпер. гидратообр-я (метанол, гликоли и др. в-ва)). 2) осушка газов осн. на извлечении паров H2O жидк. или тв. поглотителями. 3) процесс низкотемпертур. сепарации (НТС). Ингибирование осн. на том, что ингибитор растворяется в свободной H2O, в рез-те чего сниж. давление паров H2O и темпер. газообр-я. CH3OH имеет высок. давление насыщ. паров, что затрудняет извлечение его из газового потока, услож. его регенерацию и приводит к большим потерям ингибитора.
Поэтому CH3OH прим. обычно в проточных системах (скважинах и магистральных газопроводах для разлож-я и образовавшихся гидратных пробок без последующей его регенерации. Кроме того, CH3OH прим. в пр. низкотемпературной сепарации для предупреждения обр-я гидратов, с целью выделения из него тяжел. УВ и паров H2O. Сущность процессов НДС – в однократной конденсации УВ (?).
В кач-ве ингибитора широко используются гликоли (60-80%)
Практика №4. За рубежом чаще исп-ся ДЭГ, в отечественной практике – ЭГ, т.к. он растворяется в газоконденсат. Ингибитор нужно вводить в потом газа в раскалённом сост-ии. Гликоли можно регенерировать выпоркой H2O из водн. Р-ров гликолей. Степень конденсации каждого УВ зависит от t и р. При давл-ии 3,5 Мпа и темпер – 40 градусов достигается почти полная конденсация C4-C5, а этан конденсируется на 50%, пропан – 79%. Важнейший параметр НТС – исходное давление газа из скважины. Перед сепаратором 2-й ступени вместо конденсатора иногда устанавл. холодильную машину.
В наст.вр. большинство установок НТС не обеспечивают требуемым стандартам степени выделения конденсата и влаги из газа. Причины: 1) Перегрузка сепарацион. оборудования 2) Недостаточная поверхность теплообменников 3) Своевременный ввод холодильных установок. Вместо дросселирования газа через клапан может быть использовано его расширение в турбодетандере – процесс низкотемпературной конденсации. Это позволяет более эф-но исп-ть перепад давл-я газа, при этом достигается более низкая темпер. охлажд-я газа – до -120°.
МЕТОДЫ ОСУШКИ ГАЗА. 1) Абсорбция влаги гироскопическими жидкостями. 2) Адсорбция влаги активир. тв-ми. осушителями. 3) Конденсация влаги за счёт сжатия и/или охлаждения газа. Абсорбция – в кач-ве абсорбентов исп-ют водные р-ры моно- , ди- и триэтиленгликоля. Осушка газа основана на разности парциальных давл-й водяных паров в газе и абсорбенте. Кол-во влаги, кот. можно извлечь из газа абсорбентами – осушителями опр-ся гигроскопическими св-вами осушителя. Температурой и давл-ем опр-ся эффективностью контакта газа и абсорбента, массой циркулирующего осушителя и его вязкостью.
 Температура
кипения, отличающаяся от температуры
кип-я на столько, чтоб (?).
Низкую вязкость в увл-ях эксплуатации
обеспечивающих хороший контакт с газом
в абсорберах, теплообменниках и др.
массообменным оборудованием. Низкую
взаимор-римость с компонентами газа.
Низкую коррозионную активность. Низкую
вспениваемость в усл-ях контакта газовой
смеси. Высшую устойчивость к ок-ям и
термическому разложению. Этим требованиям
отвечают гликоли
ЭГ, ДЭГ и ТЭГ и ПГ, и спирты парафинового
ряда, и смеси гликолей со спиртами или
их эфирами.
Важным
св-вом гликолей явл.
их способность понижать температуру
замерзания в водн. р-рах гликолей как
ингибитов обр-я гидратов при минусовых
температурах.
Температура
кипения, отличающаяся от температуры
кип-я на столько, чтоб (?).
Низкую вязкость в увл-ях эксплуатации
обеспечивающих хороший контакт с газом
в абсорберах, теплообменниках и др.
массообменным оборудованием. Низкую
взаимор-римость с компонентами газа.
Низкую коррозионную активность. Низкую
вспениваемость в усл-ях контакта газовой
смеси. Высшую устойчивость к ок-ям и
термическому разложению. Этим требованиям
отвечают гликоли
ЭГ, ДЭГ и ТЭГ и ПГ, и спирты парафинового
ряда, и смеси гликолей со спиртами или
их эфирами.
Важным
св-вом гликолей явл.
их способность понижать температуру
замерзания в водн. р-рах гликолей как
ингибитов обр-я гидратов при минусовых
температурах.
Влажный газ направляется в нижнюю часть абсорбера 1, а концентрированный гликоль подаётся на верхнюю тарелку абсорбера. С верха абсорбера уходит осушенный газ, с низа – обводненный гликоль. Газ направляется потребителям, а гликоль далее нагревается в рекуперативном теплообменнике 2 и поступает в выветриватель 3, где из него выделяются поглощённые в абсорбере углеводороды. После выветривателя 3 гликоль нагревается в теплообменнике 4 и поступает в десорбер 5. С верха десорбера отводятся пары воды и оставшееся количество газа, с низа – регенерированный гликоль, который после охлаждения в теплообменник 2 и холодильнике 7 поступает в ёмкость 8, оттуда забирается насосом 9 и подаётся в абсорбер 1 (в ёмкость 8 модно подавать свежий гликоль при необходимости восполнения потерь гликоля). Абсорбция осуществляется при низких температурах, десорбция при высоких. Гликоли часто регенерируют под вакуумом во избежание нарушения их химической стабильности, т.к. температура низа десорбера должна быть выше температуры их разложения.
Требования к осушителям: Удовлетворительно осушающую способность в широком интервале концентраций, давления и температур (т.е.обеспечивать достаточное понижение точки росы газа). Р-ры ЭГ имеют более низкую t замерзания, большую степень предотвращения гидратооб-я при одинак. конц-ях, меньшую вязкость при рабочих температурах, осушки и более низкую р-римость в УВ конденсате по сравнению с ДЭГ и ТЭГ. Однако ЭГ имеет недостаток – высокую упругость паров. Напр. при t 20° упругость паров 99%-го р-ра ЭГ в 2,5 раза больше ТЭГ и в 7 раз больше ДЭГ. Поэтому при просушке происходят большие потери ЭГ. Р-римость природного газа в ТЭГ в 25-35% выше, чем у ДЭГ. С этой т. зрения применение ДЭГ предпочтительнее. Следует отметить, что ТЭГ обеспеч. гарантированно по УВ=-20, а также отмечается меньшей летучестью и обечпеч. высокую депрессию, т.р. в процессе осушки газа, легко регенерируется. Снижение т.р. достигаемое при (?). Температуры в абсорбционной колонке, св-в и свойства р-ра осушителя, эффективности контакта, между газом и осущителем (?). Контактирование фаз между колоннами может осущ. (?) (тарельчатая) или непрерывн. Тарельчатые имеют меньшие потери напора, чем насадочные.
Адсорбционные методы извлечения влаги. При необходимости достижения высокой депрессии т.р.по влаге (100-120) и обеспечения глубокой осушки газов (до т.р. -85, -100) исп-ют, как правило, адсорбционные методы извлечения влаги. Адсорбция – процесс конц-я в-в на поверхности или в объёме микропор тв. тела. Осушка газа адсорбентами осн.на способности тв. тел опред. структуры поглащать влагу из газа при сравнит.низких температурах и выдел.её при повыш. t. Адсорбент – бокситы, сост. в осн. из Al2O3, активир. Al2O3 – очищенный боксит, гели – в-ва, сост. из SiO2 или алюмогеля, молекулярная сетка (цеолиты – Na, Ca-силикаты (MeO*SiO2*уH2O)). Для адсорбентов хар-на развитая внутр. поверхность (1 г – 500-800 м2). Развитая внутренняя поверхность создаётся капилляром или крист. решёткой. Она несоизмеримо больше внешней поверхности адсорбента. Адсорбцион. процессы можно проводить периодически в аппаратах с неподвиж. слоем и непрерыв. и непрерыв. аппаратах. с движ. слоем адсорбента. Непрерывные пр. не получили широкого распр-я из-за влажности технологич. оформл-я. На установках с периодич. пр. адсорбции предусм. 3 или 2 адсорбера (в 1-ом проходит абсорбция, 2-ом – десорбция, 3-ем – охлаждение абсорбента). В пр. адсорбцион. осушки все поглащ. из газа компоненты адсорбера с различ. скор-ю. В 1-ую очередь поглащ. пары воды. Адсорбция сопровож. выд-ем тепла. При этом обр-ся адсорбцион. фронт, кот. перемещ. в напр-ии движ-я газа. Когда фронт достигнет последнего по хожу газослоя адсорбента, сод-е влаги в осуш. газе нач. ув-ся, что свидетельствует о насыщении адсорбента парами воды и необходимости прекращения процесса. При проскоке влаги сырой газ напр. в др. адсорбер, где до этого регенерировали осушитель. Ад-я сопровож.выделением тепла. На промышленных установках адсорбент регенерирует продукты и слоя горячим потоком природного или (?). Газ нагрев. до температуры 176-204°, а для цеолитов – 316-370°. При этом разница температур газа на входе и на выходе из десорбера составл. обычно 30°. Объём газа регенерации 5-15% от общей производительности установки осушки. На промышл. устан. сырой газ пропускают через слой адсорбента сверху вниз, а газ регенерации – снизу вверх. Продолж-сть цикла осушки обычно составл.8, 12, 16 или 24 часа. Для обеспеч-я стабильного кач-ва осушки газа адсорбция ёмкость поглотителя исп-ся не полностью – адсорберы переключают с одного цикла на др. до протока влаги. Поглощающая способность адсорбента постепенно снижается, что связ. с закупоркой его транспортных пор высокомолекулярными УВ. Период адсорбента обычно бывает от 2-х до 5 лет.
Имеется ряд схем адсорбцион. осушки газа: 1) Установки с открытыми циклами регенерации адсорбента (газ регенерации проходит через адсорберы, нах. на стадии десорбции влаги, а охлаждения сорбента, после чего газ удаляется из системы регенерации. 2) Установки с закрытым циклом регенерации адсорбента газ регенерации циркулирует в системе по замкнутому контуру.
Капитальные и эксплуатационные затраты по схеме с закрытым циклом выше, чем по схеме с открытым циклом регенерации. Предпочтение отдают от 1-й схеме, т.к. она обеспеч. высокую стабильность и высок. степень осушки газа. При выборе адсорбента исходят из усл-ий его работы и заданной точки росы газа. Силикагель мерки КСМ обеспеч. осушку газа до т.р.= - 55 - -57°, гликозем - -55°, Al2O3 = - 60- -66°. Синтетический цеолит т.р.= - 70 - -75°.
Адсорбцион. метод осушки газа с пом. цеолита считают наиболее перспективным и надёжным при необходимости достижения низкой т.р. газа, и ещё цеолиты могут работать при повыш. температуре
В ряде случаев осушку на ГПЗ исп-ют комбинированную на 1-ой степени адсорбции, на др. ст. – адсорбц. методом. Иногда исп. комбинированный метод адсорбции на 1-ой ступени - с пом. силикагеля или Al2O3, а на 2-й -на цеолитах. Адсорбционные методы гарантируют простоту и надёжность, но для этого необх. большие капитальные и эксплуатацион. затраты. Эф-сть адсорбента сниж. в рез-те его загрязнения ингибиторами, коррозией и др. примесями.
Месторождения газа в Африке. Запасы сост. 14 трлин. м3 (7,5% мир. запас.): 1) у берегов Танзании 900 млрд м3. 2) Мозамбик – 2,8 трлн м3. 3) у берегов Кении и Мадагаскаре. Обнаружены запасы на востоке Африки: Алжир, Египет, Ливия, Нигерия, экваториальная Гвинея, Ангола. Западная Африка ориентир. на нефть, попутный газ, сжигаемый на факелах. Ориентировочные данные о запасах ископаемого топлива в ед. 1,05*106 кДж: табл.
Вредные примеси в газе и методы очистки от них. CO2, H2S, COS, CS2, тиофен, R-S-R, сероорг. соед-я. Снижают активность каt процессов, отравл. каt, вызывают коррозию Me. В присут. CO2 сниж. теплота сгорания газообр. топлива, уменьшается эффективность исп-я магистральных газопроводов из-за этого балласта. Макс. содерж-е H2S в природных газах РФ 23% (Астрахан. газоконденсатное месторождение), а в газах Канады – 75% (Пантер-Ривер). Кроме того, в газах сод. сероорганич. соед-я, кот. даже в небольших кол-вах осложн. добычу, транспортировку и исп-е минеральн. ресурсов газовых месторождений. В газах Оренбургского м-я сероорг.соед-й бывает от 1000 до 2000 мг/м3 и при этом сод-е H2S=16000 мг/м3 (1,8-2%). В РФ допускается наличие H2S не более 22 мг/м3, в США – 5,7 мг/м3, а CO2, общей серы и меркаптанов сод-е устанавл. обычно газотранспортными кампаниями в завис. от требований потребителей (CO2: 1-2%, меркалтан: 1,5-5 мг/м3; общей серы до 228 мг/м3). Применяют абсорбцион. пр. (для очистки). Они подраздел. на: 1) Хемосорбцион. процессы 2) Абсорбционные пр-ы 3) Комбинированные пр. 4) окислительные пр. Окислит. пр. осн. на необратимом превращении поглащ. H2S в элементар. серу. В кач-ве поглотителя исп-ют горячий р-р мышьяковых солей щелочных Me. В отношении CO2 этот пр. явл. обычным сорбционным процессом.Недостатком пр. явл. высокая токсичность применяемого поглотителя.
Хемосорбционные процессы – Пр-ы очистки газа растворителями, представл. собой водные р-ры алканоламинов: моноэтаноламин, диэтаноламин, триэтаноламин, дигликольамин. Эти процессы осн. на хим. р-ии нежелат. соед-й с р-лями. К этой же гр. относятся пр. поташной, щелочной очистки.
1.1. Процесс МЭА. Аминовые пр. обеспеч. тонкую очистку газов от H2S и CO2 при различном давлении, концентрации их в исходном сырье, растворимость углеводородов в этих абсорбентах невелика. Технологическое и аппаратурное оформление отличается простотой и надёжностью: 2RNH2+H2S↔(RNH3)2S, где R=CH2CH2OH; (RNH3)2S+ H2S↔2RNH3HS; CO2+2RNH2+H2O↔(RNH3)2CO3; CO2+2(RNH3)2CO3+H2O↔2RNH3HCO3. Реакции экзотермические. При низкой температуре реакции протекают слева направо, при высокой – справа налево. Основные недостатки процесса: не достигается комплексная очистка газов от CO2, H2S, CS2, RSH и COS, низкая глубина извлечения меркаптанов и некоторых других сераорганических соединений, абсорбенты и продукты взаимодействия их с примесями, содержащимися в сыром газе, нередко обладают повышенной коррозионной активностью.
 Процесс
МЭА-очистки газа. Сырой
газ с температурой 10-40°
подают на нижнюю тарелку абсорбера 1,
кот. орошается МЭЛ и кот. подаётся на
верхнюю и среднюю тарелку абсорбера.
Процесс
МЭА-очистки газа. Сырой
газ с температурой 10-40°
подают на нижнюю тарелку абсорбера 1,
кот. орошается МЭЛ и кот. подаётся на
верхнюю и среднюю тарелку абсорбера.
С верха выходит очищ. газ, а с низа – насыщ. кислыми газами абсорбент, 55-60°, давление 0,2-5,5 Мпа. Очищ. газ после сепаратора 2 направл. к потребителю, а насыщ. сорбент поступает в сепаратор 3, где за счёт дросселирования р-ра из абсорбента выдел. поглощённые УВ (сепарационный газ исп-ся как топливо).
После сепаратора 3 насыщ. абсорбент нагрев. в теплообменнике 6 и поступает в среднюю часть десорбера 7. Темпер. в нижн. части десорбера =115-130°, за счёт нагрева р-ля стекающего с ниж. тарелки.
Рабочее давл-е десорбера 0,15 Мпа. Смесь кислых газов, паров воды и оставшиеся УВ выходят сверху десорбера 7, охлаж. в воздуш. и в водяном холодильниках 8 и 9 и после чего двухфазная смесь поступает в сепаратор 10, где вода отделяется от кислых и УВ-газов. Вода подаётся в кач-ве орошения на верхнюю тарелку десорбера для предотвращения уноса МА с верхних продуктов, а кислые газы направл. на установку по производству S.
Регенерируемый р-р МА после охлаждения в теплообменнике 6 и и холодильниках 4,5 подается подаётся в абсорбер 1 с t=35-40°.
Процесс МЭА имеет ряд недостатков: 1) Обр-е необратимых хим. соед-ий МЭП с COS, CS2 и CO2 2) Большие потери от испарения 3) Не высокая степень извлечения RSH 4) Низкая избирательность к H2S в присут. CO2. 5) Вспениваемость в присут. жидких УВ, ингибиторов коррозии и механич. примесей.
1.2. Процесс ДЭА. В этом пр. исп-ся в кач. р-ля водн. р-р ДЭА в конц-ии 20-25%, 25-27%, 25-30%. Этот пр. широко исп., т.к. он лишён ряда недостатков, присущих МЭА. Он исп-ся для очистки газов, сод. COS и CS2, т.к. обр. соед-я легко гидролизируются при повыш. t с выд-ем H2S и CO2. Степень насыщения р-ра в этом пр. достигает 1-1,13 моль/моль сорбента ДЭА. Также достоинством явл. малые потери об испарения и меньшая вспениваемость. Р-р ДЭА хим. стабилен в усл-ях процесса, легко регенерируется, абсорбция проводится при t на 10-20° выше, чем МЭА. Недостатки: 1) Высокие удельные расходы абсорбента 2) Высокая стоимость ДЭА 3) Для одинак.с МЭА степенью очистки требуются более высокие скорости циркуляции р-ля. Технологич. схемы процессов МЭА и ДЭА одинаковы.
1.3. Процесс Адип. Водный р-р диизопропаноламина (40%). Обеспечивается тонкая очистка газа от H2S до 1,5 мг/м3 в РФ. Этот же сорбент очищают одновременно от CO2, COS и R-S-R. Здесь расход пара на регенерацию р-ра в 2 раза < чем в МЭА пр. и р-римость УВ в сорбенте не велика (до 0,5 об %). Процесс Адип хорошо исп-ся за рубежом для очистки природн. нефтян.газа, и также газов каталитических пр-ов нефтеперераб. заводов.
1.4. Процесс Экснамин. В кач-ве р-ля исп. водн. р-р. дигликольамина (ДГА) NH2-CH2-CH2-O-CH2-CH2-OH.
Он исп-ся в конц-ии 60-65%, обеспечив. высок. извле-е CO2, COS, CS2 и др. и при этом обр. легкорегенерир. соед-е.
Технологич. схема ДГА аналогична установке амидной очистки, однако р-римость УВ в р-ре ДГА выше, чем в р-рах МЭА и ДЭА, и после отделения в сепараторе УВ-газ подают на очистку (повторную).
1.5. Поташная очистка. Очистка от CO2 горяч.р-рами карбоната, активир. различным добавками ДЭА. Методы очистки газа горяч. р-ром поташа 110-115°, осн. на возрастании р-римости солей H2O при увелич. t. Поэтому при очистке м.б. исп. более конц-ные р-ры. Преимуществом р-ра поташа явл. его высокая хим. стойкость и большая избират-сть к H2S. Регенерацию насыщ. р-ра проводят при t 115-120° и пониж. давл-ем.
Практика №5. Важным преимуществом процесса абсорбции явл. значит-е увеличение скор. гидратации CO2 и скор. абсорбции в целом. Эти физико-хим.особенности позволили осуществл. такой пр. очистки, в кот. абсорбция и регенерация проводится при одинак. температурах, причём абсорбция протек. при повыш. давл-ии, а реген-я при давл-ии, близком к атмосферному. Поташная очистка получила широк. распр-е, однако исп-е конц. р-ров поташа приводит к обр-ю кристаллов БИКАРБОНАТА КАЛИЯ, вызывающих износ рабочих колёс насоса. Снижение конц-ии р-ра увелич. расход электроэн-ии на перекачивание больших объёмов р-ра, затруднено получ-е меркаптанов RSH. Вывод: хемосорбцион. пр-ы с прим-ем р-ров аминов для очистки газов с малым сод-ем H2S (<0,05%) и высоким соотношением CO2 и H2S считается нерациональным, т.к. сод-е H2S в газах регенерации 3-5 об%. Получение S из таких газов на типовых установках пр. невозможно, и их приходится сжигать на факелах. Отсюда недостаток загр-я ктмосферы. Также в таком пр. затруднено извлечение RSH. При очистке газов аминами остаточное допустимое сод-е H2S равно 0,001% и CO2 до 0,02%. Такая степень очистки допустима для всех проц-ов переработки газов.
1. ФИЗИЧЕСКИЕ ПРОЦЕССЫ АБСОРБЦИИ. Процессы очистки газов методом физич. аб-ии «нежелательных» соед-ий соверш. органич. р-лями: пропиленкарбонатом, N-метилпирролидоном, диметиловый эфир полиэтиленгликоля и др. Эти абсорбенты, как правило, не пенятся и не коррозируют аппаратуру, многие им. низк. t замерзания. Регенерация физич. абсорбентов протек. без подвода тепла, за счёт снижения давления в сист.
Недостатки: р-ли хорошо поглощают УВ. Эти пр. лучше исп-ть для грубой очистки с последующей МА очисткой.
2.1. Процесс Флюор. Абсорбентт пропиленкарбонат. Хорошо р-ряет H2S, CO2, CS2, RSH и УВ, обладает слабым коррозион. д-ем к Me, имеет низк. давл-е насыщ. паров. В рез-те сод-е чистых компонентов в очищ. газе составл.: CO2-2%, H2S-5,7 мг/м3. Пр. можно исп-ть для очистки природн., нефтян. и технологич. газов с повыш. сод-ем CO2 и низк. отнош.H2S и CO2. Аб-ю проводят в интервалеле t от 0 до -6 при парциальном давл-ии кисл. компонентов в исх. сырье более 0,4 Мпа. Регенерацию абсорбента осущ. без подвода тепла путём ступенчатого снижения давления.
2.2. Пр. Селексол. Абсорбент диметиловый эфир полиэтиленгликоля. Разраб. фирмой Chemical corporation, р-ль не токсичен, хим. стабилен, не пенится, не обл. коррозион. активн-стью, легко разлаг. при биологич. очистке сточных вод, обладает высок. селективностью и обеспеч. избирательное извлечение H2S в присут. CO2 (усл-е при 20° и 0,1 Мпа (1 атм)). Р-римость H2S в 10 раз выше, чем в CO2. Недостаток: сорбент наряду с кисл. компонентами хорошо р-ряет УВ. Он может исп-ся для пр-са очистки сухих газов C1+C2.
2.3. Процесс Пуризол. N – метилпирролидон. Разраб. фирмой Лурги, не токсичен, хорошо р-ряет CO2, RSH и УВ, поглащ. пары H2O, не обл. коррозион. возд-ем, химич. стабилен, легко разлаг. при биологич. очистке сточных вод, обл. высок. селективностью и обеспеч. избир-е извлечение H2S в присут.CO2. Абсорбция кисл. компонентов может осущ. в 2 ступени: грубую и тонкую. В Новочеркасске пуризол был предн. для очистки прир. газа от RSH. Исходный газ сод. RSH 80-250 мг/м3, а после очистки 1-2 мг/м3.
2.4. Ректизол. К физич. пр-сам сорбции относится пр. ректизол – очистка газа от CO2 холодным CH3OH благодаря увеличению р-римости CO2 при низк. t и повыш. давл-ии. Абсорбция метанолом – более выгодн. метод, его можно исп. при t до -60°. Так, при такой t и давл-ии 0,4 МПа в 1 г CH3OH может р-риться 600 см3 CO2.
3. Комбинированные процессы. Р-ры алканоламинов + орг. р-ли (напр.c CH3OH). Они осн. на физич. адсорбции орг. р-лями и химич. взаим-ии с алканоламинами. Их можно исп. для комплексн. очистки газов от CO2, H2S, RSH и COS.
3.1. Процесс Сульфинол: Смесь воды р-ра диизопропаноламина с сульфаланом (циклотетраметиленсульфон): Берут 30% амина и 64% сульфолана и 6% H2O. Хорошо р-ряет CO2, H2S, CS2, RSH, COS и УВ, химич. и термич. стабилен, может быть исп. для комплексной очистки сухих газов от нежелат-х примесей, проводит тонкую очистку газа от CS2 и RSH одновременно. Степень извлечения RSH = 95%. Процесс разраб. фирмой Shell.
ВЫВОД: требования к орг. р-лям, используемых в комбинир.методах: 1) Термохимич. устойчивость в смеси с H2O, аминами и компонентами очищаемого газа 2) Доступность и низк. стоимость 3) Смешиваемость аминов с H2O и продуктами р-ии 4) Низкая теплоёмкость и давл-е насыщ. паров 5) Требуемая вязкость рабочего р-ра 6) Нетоксичность.
ЛЕКЦИЯ № 2
Нефть
Термин «нефть» вкл. в себя жидкие продукты широкого диапазона качества. Сюда входят сверхлегкие нефти (газовый конденсат, нефти с содержанием светлых фракций более 80%), обычные нефти (плотностью 0,80-0,95г/см3) и сверхтяжелые нефти (высоковязкие нефти и природные нефтебитумы).
Мировые запасы оцениваются следующими цифрами (в млрд. т):
Газовый конденсат 1,0-1,5 (извлекаемый - 1,0)
Обычные нефти 220-280 (извлекаемые - 100)
Сверхтяжелые нефти 650-730 (извлекаемые - 350)
В скобках показаны извлекаемые запасы, кот. примерно в 2 раза ниже общих.
Запасы обычной нефти распределены следующим образом (%):
На Ближнем и Среднем Востоке ≈ 60
В южной и Северной Америке ≈ 15
В странах СНГ и Китае - 12
В Африке - 8
В остальных странах - 5
Запасы сверхтяжелых нефтей сосредоточены в основном в Канаде, Венесуэле и на территории СНГ.
В мире разведано («доказанные запасы») около 140 млрд. т. нефти, причем более половины принадлежит пяти странам Персидского залива. В год в мире добывается свыше 3 млрд. тонн нефти, две трети кот. потребляются развитыми странами Запада и Японии. Львиная доля достается США - около 1 млрд. т.
В Старом Свете основные запасы принадлежат Саудовской Аравии – 25 % мировых – около 35 млрд. тонн. Еще примерно по 8-10% (12-15 млрд. т) находится в странах Персидского залива: Иран, Ирак, Кувейт и Объединенных Арабских Эмиратах. В табл. 1 приведены мировые нефтяные запасы.
Табл. 1 – мировые нефтяные запасы по странам
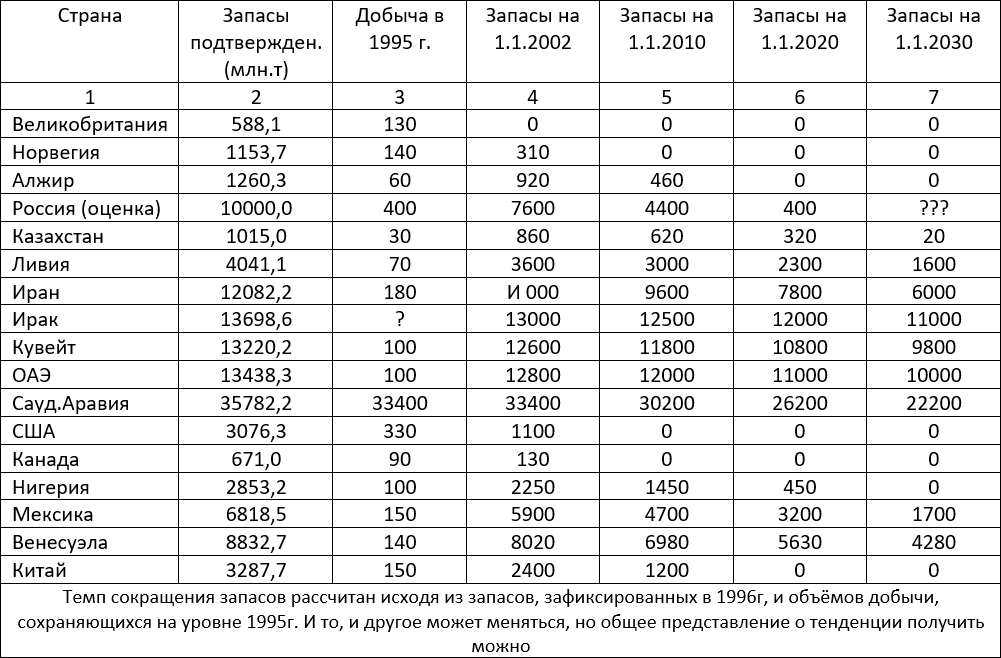
Структура месторождений, как и повсюду, постепенно меняется в худшую сторону, поскольку наиболее богатые и легкодоступные месторождения выработаны более чем на половину. Вновь открываемые содержат тяжелые, трудноизвлекаемые нефти.
Диспропорции между запасами и объемами потребления по нефти и газу вызвали серьезные опасения об истощаемости ресурсов жидких и газообразных УВ.
Компания «Роснефть» – лидер российской нефтяной отрасли. Добычу нефти в России ведут 240 нефтегазовых компаний, из них 11 нефтегазовых холдингов, на кот. приходится 90% всего объёма добычи.
Нефть, получаемую непосредственно из скважин, называют сырой. При выходе из нефтяного пласта содержит частицы горных пород, воду, а также р-ренные в ней соли и газы. Эти примеси вызывают коррозию и серьезные затруднения при транспортировке и переработке нефтяного сырья. Из нефти удаляется вода, механические примеси, соли и тв. УВ, выделяется газ. Газ и наиболее легкие УВ необходимо выделять из состава нефти, т.к. они являются ценными продуктами и могут быть утеряны при ее хранении. Кроме того, наличие газов при транспортировке нефти по трубопроводу может привести к образованию газовых мешков на возвышенных участках трассы.
Простые породы, играющие роль приемников нефти и газа, широко распространены в толще земной коры и носят название коллекторов. Движение нефти по пластам - миграция приводит к накапливанию в каком-либо ограниченном пространстве, образуя промышленную нефтяную залежь. Добывается нефть путем бурения скважин, по кот. она поступает и на поверхность земли, либо самостоятельно под давлением газов, либо выкачивается насосами.
Важнейшими характеристиками сырой нефти явл.: плотность, содержание серы, фракционный состав, а также вязкость, содержание воды, хлористых солей и содержание механических примесей.
Одно из главных свойств непереработанной нефти - её плотность, кот. зависит от содержания тяжелых УВ, таких как парафины и смолы. Для ее выражения используется как относительная плотность, выраженная в г/см3, так и плотность, выраженная в градусах Американского нефтяного института - American Petroleum Institute (API).
Табл. 2 - Относительная плотность различных сортов нефти

Запасы углеводородного сырья
Основная часть нефти добывается на востоке: в Башкирии, Татарстане, в Пермской, Саратовской, Куйбышевской, Оренбургской областях, в Сибири (Тюменской, Иркутской, Томской областях), на Сахалине. Кроме того, нефтяные месторождения имеются в Баку, Грозном, Дагестане, Среднеазиатских государствах, Западной Украине, в Беларуси и др.
Элементный, фракционный и углеводородный составы нефти
В земной коре на различной глубине (до 2 тыс. метров и более) находят жидкий горючий минерал - нефть, кот. по внешнему виду представляет собой маслянистую, чаще всего темную жидкость, флюоресцирующую на свету. Цвет зависит от содержания и строения смолистых веществ, встречаются даже дочти бесцветные нефти.
Нефть - сложная смесь большого числа УВ различной молекулярной массы и химического строения с примесью, иногда очень значительной, сернистых, кислородных, азотистых и смолистых веществ.
Нефть имеет органическое происхождение, являясь продуктом разложения и сложных химических превращений отмерших растительных и животных остатков.
Различные металлы и другие элементы, входящие в состав гетероорганических соединений, а также соли кислых в-в нефти при сгорании превращаются в оксиды и образуют негорючий остаток, кот. и наз. золой. При количественном определении золы необходимо нефть или нефтепродукт отделять от случайных механических примесей, кот. не могут характеризовать химический состав нефти. Содержание золы в нефти очень мало и составляет сотые, реже десятые доли процента. В золе чаще всего встречаются след. элементы: Сa. Mg, Fe, Al, Si, V, Na. Ванадий в золе некот. нефтей явл. преобладающим элементом. Выяснилось, что ванадий присутствует преимущественно в золе сернистых нефтей (Туймазинская, Ишимбаевская).
Часто растворены в нефти газообразные УВ. Главные элементы, из кот. состоят все компоненты нефти, - «С» и «Н». Содержание углерода и водорода в различных нефтях колеблется в сравнительно узких пределах и составляет в среднем: для углерода 83,5 - 87%, для водорода - 11,5 -14%, в то время как в углях находится 5 ─ 8 % водорода. Повышенное соотношение водорода к углероду и объясняет жидкое состояние нефти. Наряду с «С» и «Н» во всех нефтях присутствует сера, кислород и азот, в сумме кот. составляют 2 ─ 3 %. Имеются нефти, кот. целиком состоят из углерода и водорода (например, Пенсильвания, США). Азота в нефтях мало (0,001 - 0,3 %), содержание кислорода от 0,1 ─ 1 до 2 — 3 %. Но по содержанию серы нефти резко отличаются друг от друга. Наиболее сернистые нефти месторождений Оренбургской, Куйбышевской областей, Татарии, Венесуэлы. Максимальное содержание серы - у Мексиканской нефти (3,5 - 5,3 %) и в нефтях месторождений Узбекистана - Хау-Дак, Уч - Кизыл (3,2 - 6,3 %).
В очень малых количествах в нефтях присутствуют металлы (W, Ni, Fe, Mg, Cr, Ti, Co, K, Ca, Na и другие).
Разделение сложных смесей на более простые, на индивидуальные компоненты называется фракционированием. Наиболее распространенные методы фракционирования - перегонка и ректификация. Эти методы и положены в основу заводской переработки нефти. Под фракционным составом нефти или нефтепродукта понимают количественное содержание веществ нефти, выкипающих в определенных температурных пределах.
Если бы при переработке сырой нефти ограничивались её перегонкой или другими физическими методами разделения, сохраняющими неизменным химич. состав нефти, то таким образом не удалось бы удовлетворить мировую потребность в бензине, а его октановое число было бы слишком низким. Поэтому используются химич. методы переработки нефти, в результате кот. природа её компонентов изменяется (термический и каталитический крекинг, риформинг, процессы изомеризации и алкилирования и другие).
