
- •1. Анемии. Определение понятия. Основные лабораторные и клинические признаки.
- •2. Этиопатогенетическая классификация анемий.
- •2. Анемии вследствие кровопотери
- •3. Этиология и патогенез постгеморрагических анемий.
- •I стадия – рефлекторно-сосудистая
- •II стадия- гидремическая
- •III стадия- стадия - регенераторная (или стадия костно-мозговой регенерации)
- •2. Хроническая постгеморрагическая анемия
- •4. Этиология и патогенез внутрисосудистых гемолитических анемий.
- •5. Этиология и патогенез наследственных гемолитических анемий.
- •1. Мембранопатии
- •2. Энзимопатии
- •3. Гемоглобинопатии
- •6. Железодефицитные анемии. Этиология и патогенез.
3. Гемоглобинопатии
ЭТИОЛОГИЯ: связаны с наследственным нарушением синтеза гемоглобина.
-качественные гемоглобинопатии сопровождаются изменением первичной структуры молекулы гемоглобина
-количественные гемоглобинопатии характеризуются нарушением количественного соотношения HbA и HbF в крови из-за недостаточности образования отдельных полипептидных цепей глобина
Наибольшее значение в практическом отношении представляют гемоглобиноз S (серповидноклеточная анемия) и талассемия.
ПАТОГЕНЕЗ:
ГЕМОГЛОБИНОЗ S возникает в связи с наследованием патологического гемоглобина S, в котором гидрофильная глутаминовая кислота замещена на гидрофобный валин.
Это приводит к смене электрического заряда и полимеризации гемоглобина в условиях гипоксии, снижению его растворимости с образованием тактоидов (веретенообразных остроконечных кристаллов), которые растягивают оболочку эритроцитов.
В результате клетки приобретают форму «серпа», теряют пластичность, повышают вязкость крови, замедляют кровоток, вызывают стаз.
Стаз приводит к гипоксемии, еще более повышая уровень «серпления» эритроцитов. Такие эритроциты могут острыми концами повреждать неизмененные клетки, что приводит к внутрисосудистому гемолизу.
ТАЛЕССЕМИЯ связана со снижением или отсутствием синтеза α-, β-, δ- или γ-цепей глобина. Различают α-, β-, δ- и γ-талассемию.
Чаще всего встречается нарушение синтеза β-глобиновых цепей - β-талассемия. В этом случае содержание HbA1 (α2β2) уменьшается, а уровень HbF (α2γ2) и HbA2 (α2δ2) возрастает.
Недостаточный синтез β-цепей приводит к избыточному образованию α-цепей. Лишние α-цепи способствуют появлению нестабильного гемоглобина, который преципитирует и выпадает в эритроците в виде «телец включения», придавая им форму мишеней.
α-цепи вступают в соединение с SH-группами мембраны и повышают ее проницаемость, нарушаются процессы ассимиляции железа и синтеза гемоглобина. Это обусловливает раннюю гибель эритроцитов в результате внутриклеточного гемолиза с развитием гипохромной анемии.
6. Железодефицитные анемии. Этиология и патогенез.
В крови железа в норме 12-32 мкмоль/л, оно связано с транспортным белком плазмы – трансферрином
Общее количество железа в организме - 4-5 г (у мужчин 50 мг/кг, а у женщин - 40 мг/кг), из которого большая часть (около 60 %) содержится в эритроцитах в составе Нb.
Остальное железо входит в состав миоглобина, железосодержащих ферментов, трансферрина, ферритина, гемосидерина.
Органы - депо железа: печень (гепатоциты, макрофаги), костный мозг, селезенка, мышцы.
ЭТИОЛОГИЯ
1. Может наблюдаться врожденный дефицит железа у недоношенного ребенка или ребенка, рожденного от много рожавшей матери и имеющей ЖДА.
2. Алиментарная недостаточность железа встречается у детей, находящихся на искусственном неполноценном вскармливании, а также у взрослых, не получающих полноценное питание, или у строгих вегетарианцев, не использующих специальные пищевые добавки.
3. Повышенное расходование железа при повторных беременностях, быстрорастущем организме (подростки), частые инфекции (железо идет на работу макрофагов)
4. Нарушения всасывания железа при резекции желудка, воспалительных процессах
5. Порочный круг: дефицит железа → атрофия слизистой оболочки желудка и кишечника → нарушение всасывания железа → дефицит железа.
6. Нарушение транспорта железа: наследственное отсутствие трансферрина, нарушение его синтеза в печени при ответе острой фазы или повышенная потеря трансферрина с мочой
ПАТОГЕНЕЗ
Сводится к уменьшению гемоглобинизации эритроцитов.
-Синтез Нb страдает больше, чем пролиферация клеток, и поэтому содержание Нb снижается в большей степени, чем число эритроцитов
-Нt снижается только при тяжелых анемиях
Стадии:
1. Скрытый дефицит железа, не приводит к характерным изменениям крови, но вызывает увеличение всасывания железа в кишечнике
2. Снижение содержания железа в плазме (видимых признаков все еще нет), уменьшается насыщение трансферрина
3. Постоянный дефицит железа и все признаки заболевания, регенераторная способность костного мозга снижена умеренно
4. Тяжелый дефицит железа, угнетение эритропоэза, нарушение регенерации тканей, ослабление функций ферментов, гипоксические поражения тканей
ПРИЗНАКИ:
-выраженная гипохромия (ЦП снижен до 0,5-0,6; MCH и MCHC резко снижены). На 1-й и 2-й стадиях ЖДА может быть нормохромная.
-гипоксия
-многочисленные ферментные расстройства (т.к. железо входит в состав 72 ферментов)-СИДЕРОПЕНИЧЕСКИЙ СИНДРОМ
-резкая мышечная слабость (из-за гипоксии и нарушения обмена миоглобина)
-нарушения течения беременности
СИДЕРОПЕНИЧЕСКИЙ СИНДРОМ: сухость кожи, раннее поседение и выпадение волос, повышенная ломкость и искривление ногтей, их выраженная поперечная исчерченность, воспаление околоногтевого валика, койлонихии - ложкообразные ногти.
Возможно развитие глоссита, эзофагита, охриплости голоса, дисфагии. Из-за нарушения образования коллагена происходит отслойка эпителия от базальной мембраны, образуются паутиноподобные наслоения и пленки в глотке, гортани и пищеводе, гиперемия небных дужек, повышен риск развития опухолей пищевода. Атрофический гастрит, энтерит. Снижение активности ферропротеинов вызывает снижение продукции соляной кислоты что нарушает не только всасывание железа, но и др. веществ.
Склонность к кариесу зубов, наблюдаются извращения вкуса (люди едят всякие гадости типа глины, нюхают ацетон)-из-за нарушения работы рецепторов и вкусовых анализаторов
В мазках периферической крови больных ЖДА встречаются кольцевидные эритроциты, анизохромия.
На фоне выраженного пойкилоцитоза встречаются мишеневидные клетки.
Анизоцитоз с преобладанием микроцитов.
В крови снижены содержание железа (менее 12 мкмоль/л), коэффициент насыщения трансферрина
7. В12-фолиеводефицитные анемии. Этиология и патогенез.
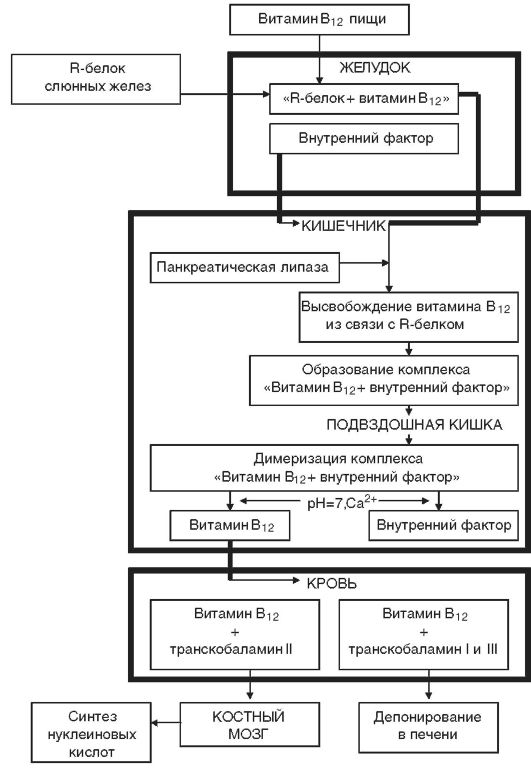
Метаболизм В12 в организме
ЭТИОЛОГИЯ
1. Алиментарные формы заболевания развиваются у лиц, получающих неполноценное питание, у строгих вегетарианцев, в течение многих лет не употребляющих мясной пищи.
2. Нарушение всасывания кобаламина может быть следствием резекции желудка или подвздошной кишки, атрофического гастрита или колита, рака желудка или кишечника, врожденного дефицита в кишечнике В12-связывающих рецепторов. Самая частая причина-иммунное повреждение (IgG) париетальных клеток желудка и связанный с этим дефицит внутреннего фактора Касла.
3. Повышенное расходование витамина при паразитировании широкого лентеца, беременности и лактации.
Запасы витамина В12 в печени достаточно большие, и при полном исключении поступления витамина извне их истощение происходит лишь спустя 2–3 года.
ПАТОГЕНЕЗ
Мегалобласт — родоначальная клетка эритропоэза, отличающаяся аномальной формой и необычно крупными размерами.
Расстройства пищеварения и переход на мегалобластический тип кроветворения обусловливаются резким снижением активности В12-зависимых энзимов, участвующих в метаболизме фолатов (соли фолиевой кислоты), необходимых для синтеза ДНК.
Нарушается синтез ДНК, что приводит к удлинению S-фазы клеточного цикла и патологии деления и созревания эпителиальных клеток ЖКТ и миелокариоцитов. В костном мозге развивается мегалобластоз.
Нарушение кроветворения связано с замедлением темпа мегалобластического эритропоэза в результате удлинения времени митотического цикла и сокращения числа митозов: вместо трех митозов, свойственных нормобластическому эритропоэзу, регистрируется только один. Срок жизни эритроцитов сокращается до 30-40 дней (в норме - 90 дней). Часть клеток погибает на ранних стадиях развития. Распад мегалобластов в костном мозге, наряду с их замедленной дифференциацией, и мегалоцитов в крови приводит к тому, что процессы кроветворения не компенсируют процессы кроверазрушения. Развивается мегалобластическая анемия.
ПРОЯВЛЕНИЯ:
Содержание эритроцитов и гемоглобина в крови может резко снижаться, однако цветовой показатель выше 1 (1,4—1,8) в связи с наличием в крови больших по объему мегалобластов и мегалоцитов, насыщенных гемоглобином.
В мазке крови-мегалобласты (12-15 мкм) и мегалоциты (10-12 мкм)
Анемия проявляется слабостью, быстрой утомляемостью, одышкой, сердцебиением. Выявляется снижение желудочной секреции, атрофический гастрит.
