
1488
.pdf
откуда
cV
cV cV1m1 cV 2m2 . m1 m2
566,6 3 10 3 742 4 10 3 667 Дж/(кгK). 3 10 3 4 10 3
Рассуждая подобным образом, получим формулу для определения удельной теплоемкости смеси при постоянном давлении
cp cp1m1 cp2m2 , m1 m2
где cp1 и cp2 удельные теплоемкости углекислого газа и азота соответственно.
cp1 |
|
i 2 |
R |
|
6 2 8,31 |
755 |
Дж/(кг K). |
|
2M |
2 44 10 3 |
|||||||
|
|
|
|
|
||||
cp2 |
|
i 2 R |
|
5 2 8,31 |
1039 |
Дж/(кг K). |
||
2M |
|
2 28 10 3 |
||||||
|
|
|
|
|
|
|||
cp |
755 3 10 3 1039 4 10 3 |
|
||||||
|
3 10 3 4 10 3 |
917 Дж/(кг K). |
||||||
|
|
|
|
|||||
Ответ: cV 667 Дж/(кг K), cp 917 Дж/(кг K).
Пример 3. Нагревается или охлаждается газ, расширяющийся по закону pV 2 const ?
|
Дано: |
|
|
|
|
Решение: |
|
|
то V2 V1. |
|||
pV 2 const |
Так как по |
условию газ расширяется, |
||||||||||
|
|
Запишем закон |
расширения |
для |
двух произвольно |
|||||||
Как |
изменяется |
|||||||||||
температура газа? |
выбранных состояний газа |
|
p |
|
V 2 |
|
||||||
|
|
p V |
2 |
p V |
2 |
|
|
|
|
|||
|
|
|
|
, откуда |
1 |
|
2 . |
(1) |
||||
|
|
|
|
|
||||||||
|
|
1 1 |
2 2 |
|
|
p |
2 |
|
V 2 |
|
||
|
|
|
|
|
|
|
|
|
|
1 |
|
|
ОпишемкаждоеизсостоянийгазауравнениемКлапейрона– Менделеева:
p1V1 RT1 ;
p2V2 RT2 .
91
Разделив одно из них на другое, получим
p1 |
|
T1 |
V2 . |
(2) |
|
p |
|||||
|
T |
V |
|
||
2 |
|
2 |
1 |
|
Приравнивая правые части уравнений (1) и (2), получим
V 2 |
|
T |
|
V |
|
T |
|
V |
|
2 |
|
1 |
|
2 |
, откуда |
1 |
|
2 . |
|
V |
|||||||||
V 2 |
|
T |
|
|
T |
|
V |
||
1 |
|
2 |
|
1 |
|
2 |
|
1 |
Так как V2 V1, то T1 1, откуда следует, что T1 T2 .
T2
Таким образом, газ в данном процессе охлаждается.
Ответ: газ охлаждается.
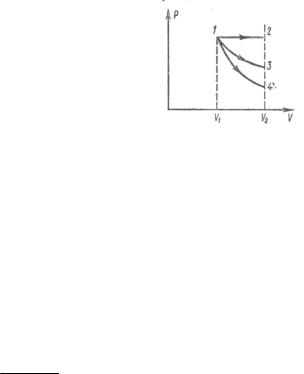
Пример 4. Азот, занимающий при давлении p 105 Па объем V1 10 л, расширяется вдвое.
Определите конечное давление и работу, совершённую газом при следующих процессах: а) изобарном, б) изотермическом, в) адиабатном (см. рисунок).
Дано: |
Решение: |
||
p 10 |
5 |
Па |
Заданное начальное давление позволяет считать газ |
|
идеальным. Рассмотрим графики всех процессов в коор- |
||
V1 10 л |
динатах p , V . Очевидно, что работа будет тем больше, чем |
||
A ? |
|
p ? |
|
|
|
|
выше пройдет кривая, т.е. чем больше давление в течение |
|
|
|
процесса. Исходя из молекулярно-кинетической теории |
|
|
|
давление определяется силой ударов молекул о стенки и |
|
|
|
частотой ударов. |
Согласно |
основному уравнению молекулярно-кинетической теории, |
||
p 2 n m0  2
2  . 3 2
. 3 2
Это уравнение есть следствие того, что сила, действующая на стенку сосуда, определяется (по абсолютному значению) числом ударов, испытываемых стенкой за некоторое время, и силой этих ударов.
При изобарном 1-2 процессе расширение происходит при непрерывном увеличении температуры, что соответствует увеличению силы отдельных ударов, испытываемых стенками сосуда. Частота ударов уменьшается вследствие увеличения объема так, что давление остается постоянным.
При изотермическом 1-3 процессе кинетическая энергия молекул не изменяется, и давление уменьшается только в результате уменьшения числа ударов, испытываемых стенкой.
92
При адиабатном 1-4 процессе кинетическая энергия молекул, отдаваемая движущемуся поршню, не пополняется извне. Поэтому адиабатное расширение происходит при более резком, чем при постоянной температуре, падении давления (уменьшается и частота ударов, и сила ударов).
Работа при изобарном процессе
A12 p1(V2 V1) 1000 Дж.
При изотермическом процессе конечное давление
p p V |
/ V 0,5 105 Па. |
|
|
|
||||||
3 |
1 |
1 |
2 |
|
|
|
|
|
|
|
Работа газа |
|
|
|
|
|
|
|
|
|
|
V2 |
|
|
V2 dV |
|
V |
|
|
|
|
|
A13 pdV p1V1 |
V |
|
2 |
|
|
|
|
|||
p1V1 ln |
|
690 |
Дж. |
|
|
|||||
V |
|
|
||||||||
V1 |
|
|
V1 |
|
1 |
|
|
|
|
|
При адиабатном процессе конечное давление |
|
|
|
|
||||||
|
p |
p (V / V ) . |
|
|
|
|
||||
|
4 |
|
1 |
1 |
2 |
|
|
|
|
|
Азот– двухатомныйгаз, поэтому (i 2) / i 1,4. Тогда p |
0,38 105 |
Па. |
||||||||
|
|
|
|
|
|
|
|
4 |
|
|
Работа, совершаемая газом при адиабатном расширении, равна убыли внутренней энергии газа:
A14 U14 Mm 2i R(T1 T4 ) .
Из уравнения Клапейрона – Менделеева, записанного для начального и конечного состояний, получим:
Mm RT1 p1V1 , Mm RT4 p4V2 .
Подставляя эти выражения в формулу для работы, находим
A14 2i ( p1V1 p4V2 ) 600 Дж.
Ответ: A |
1000 Дж; |
p 0,5 105 |
Па; A |
690 Дж; |
12 |
|
3 |
13 |
|
|
p 0,38 105 |
Па; A |
600 Дж. |
|
|
|
4 |
14 |
|
Пример 5. В цилиндре под поршнем |
находится |
водород массой |
||
m 0,02 кг при температуре |
T1 300 K. |
Водород начал расширяться |
||
адиабатно, увеличив свой объем в пять раз, а затем был сжат изотермически, причем объем газа уменьшился в пять раз. Найдите температуру T2 в конце адиабатного расширения и работуA, совершенную
газом. Изобразить процесс графически.
93
Дано: |
|
|
|
|
|
Решение: |
|
||
m 0,02 кг |
Адиабатный переход газа из одного состояния в |
||||||||
T1 300 K |
другое можно описать уравнением |
|
|||||||
|
|
|
|
|
T |
V |
1 |
|
|
T ?, A ? |
|
|
|
|
|
||||
2 |
|
|
|
|
T2 |
V1 |
|
, |
(1) |
|
|
|
|
|
1 |
2 |
|
|
|
где показатель |
адиабаты (для водорода как двухатомного газа 1,4 ). |
||||||||
Из формулы (1) выразим температуру T2 газа после адиабатного рас- |
|||||||||
ширения |
|
|
|
|
|
|
|
|
|
|
|
|
V |
|
1 |
|
|
|
|
|
T |
T |
1 |
|
. |
|
|
|
|
|
2 |
1 |
V |
|
|
|
|
|
|
|
|
|
2 |
|
|
|
|
|
|
T2 300 15 1,4 1 K 300 15 0,4 K 157 K.
Работу A1 газа при адиабатном расширении можно определить по формуле
|
A |
m |
c |
T |
T |
|
m |
|
i |
R T |
T |
. |
|
|
|
M 2 |
|||||||||||
|
1 |
|
M v |
1 |
2 |
|
1 |
2 |
|
||||
A1 |
0,02 |
|
5 8,31 300 |
157 Дж 29,8 103 Дж. |
|||||||||
|
|
||||||||||||
|
2 10 3 2 |
|
|
|
|
|
|
|
|
|
|||
Работа A2 газа при изотермическом сжатии может быть выражена в виде
A2 RT2 (m / M )ln(V2 / V1).
A2 8,31 157(0,02 / 2 10 3 )ln 15 21 104 Дж.
Знак минус показывает, что при сжатии газа работа совершена внешними силами.
Общая работа, совершенная газом при описанных процессах, равна
A A1 A2 29,8кДж ( 21кДж) 8,8кДж.
График процесса имеет вид:
Ответ: T2 157 K, A 8,8кДж.
94
Задачи для самостоятельного решения
Средний уровень
1. Удельная теплоемкость гелия ( M 0,004 кг/моль) при постоянном
объеме равна….Дж/(кгK). |
|
|
|
|
1) 1,5; |
2) 1,7; |
3) 12,5; |
4) 20,8; |
5) 3117. |
2. Молярная теплоемкость гелия ( M 0,004 кг/моль) при постоянном
объеме равна….Дж/(мольK). |
|
|
|
|
1) 1,5; |
2) 1,7; |
3) 12,5; |
4) 20,8; |
5) 3117. |
3. Разность молярных теплоемкостей Cp CV газа с молярной массой M , имеющего i степеней свободы, равна…
1) |
R |
; |
2) |
i 2 |
; |
3) M R ; 4) |
M |
; |
5) R . |
|
M |
i |
R |
||||||||
|
|
|
|
|
|
|
4. Разность удельных теплоемкостей cp cV газа с молярной массой M , имеющего i степеней свободы равна…
1) R ; |
2) |
i 2 |
; |
3) M R ; 4) |
M |
; |
5) |
R |
. |
i |
R |
|
|||||||
|
|
|
|
|
|
M |
|||
5. Молярная теплоемкость идеального газа при постоянном давлении равна Cp 92 R, где R 8,31 Дж/(мольK) – универсальная газовая постоян-
ная. Число вращательных степеней свободы молекулы равно…
1) 4; 2) 6; 3) 2; 4) 3.
6. Если для многоатомных молекул газа при температурах 102 K вклад энергии колебания ядер в теплоемкость газа пренебрежимо мал, то из предложенных ниже идеальных газов (водород, азот, гелий, водяной пар) изохорную теплоемкость CV 3R ( R 8,31 Дж/(мольK) – универсальная
газовая постоянная) имеет один моль…
1)водяного пара;
2)водорода;
3)гелия;
4)азота.
95

7. При комнатной температуре отношение Cp молярных теплоем-
CV
костей при постоянном давлении и постоянном объеме равно 53 для …
1)водяного пара;
2)воздуха;
3)гелия;
4)кислорода.
8. При комнатной температуре отношение Cp молярных теплоемкостей
CV
при постоянном давлении и постоянном объеме равно 75 для …
1)водяного пара
2)неона
3)гелия
4)водорода
9. Молярные теплоемкости гелия в процессах 1-2 |
P |
|
|
|
|
||||||
и 1-3 равны C1 |
и |
C2 |
соответственно. |
Тогда |
|
2 |
|
|
|
||
|
|
|
|
||||||||
отношение |
C1 составляет… |
|
|
|
|
|
|
|
|||
|
C2 |
|
|
|
|
|
|
|
|
|
|
5 |
3 |
3) |
5 |
7 |
|
|
1 |
|
|
|
|
|
|
|
|
|
|||||||
1) 7 ; |
2) 5 ; |
3 ; |
4) 5 . |
|
|
|
3 |
|
|||
|
|
|
|
|
|
|
|
|
|
||
10. Молярные теплоемкости водорода ( H2 ) в |
|
|
|
|
V |
||||||
|
|
|
|
|
|||||||
процессах 1-2 и 1-3 равны C1 и C2 соответственно. |
|
|
|
|
|
||||||
Тогда отношение |
C1 |
составляет… |
|
|
|
|
|
|
|||
|
|
C2 |
|
|
|
5) 2 . |
|
|
|
|
|
1) 5 ; |
2) |
3 ; |
3) 5 ; |
4) 7 ; |
|
|
|
|
|
||
7 |
|
5 |
|
3 |
5 |
5 |
|
|
|
|
|
96
11. Выберите правильное утверждение:
Удельная теплоемкость идеального газа при постоянном давлении cp больше, чемудельнаятеплоемкостьприпостоянномобъеме cV , из-затого, что…
1)давление газа остается постоянным, когда его температура остается постоянной;
2)объем газа остается постоянным, когда его температура остается постоянной;
3)необходимое количество теплоты для нагревания на 1 K больше при постоянном объеме, чем при постоянном давлении;
4)при p const нагреваемый газ pасшиpяется, и часть подводимой
теплоты расходуется на совершение работы над внешними телами;
5) увеличение внутренней энергии газа при нагревании на T при постоянном давлении больше, чем при постоянном объеме.
12. Молярная теплоемкость при постоянном объеме CV для некоторого газа равна 1,5R ( R универсальная газовая постоянная). Сколько атомов содержит молекула этого газа? (Считать, что атомы в молекуле колебаний
не совершают.) |
|
|
|
|
1) |
больше трех; |
2) три; |
3) |
один; |
4) |
для ответа недостаточно данных; |
5) |
два. |
|
13. В двух сосудах при комнатной температуре хранится по 1 моль газа. В первом сосуде газ состоит из одноатомных молекул, а во втором – из двухатомных. Каково отношение молярных теплоемкостей этих газов
при постоянном |
объеме? |
|
|
|
|
1) 1/2; |
2) |
5/3; |
3) 1,0; |
4) 2,0; |
5) 3/5. |
14. В двух сосудах при комнатной температуре хранится по 1 моль газа. В первом сосуде газ состоит из одноатомных молекул, а во втором – из трехатомных. Каково отношение молярных теплоемкостей этих газов
при постоянном |
объеме? |
|
|
|
|
1) 5/3; |
2) |
1/2; |
3) 3/5; |
4) 3; |
5) 1. |
15. В двух сосудах при комнатной температуре хранится по 1 моль газа. В первом сосуде газ состоит из одноатомных молекул, а во втором – из двухатомных. Каково отношение внутренних энергий этих газов?
1) 1/2; 2) 1; 3) 5/3; 4) 2; 5) 3/5.
97
16. В двух сосудах при комнатной температуре хранится по 1 моль газа. В первом сосуде газ состоит из одноатомных молекул, а во втором – из трехатомных. Каково отношение внутренних энергий этих газов?
1) 3/5; 2) 1; 3) 5/3; 4) 1/2; 5) 3.
17. Теплоемкость идеального газа при адиабатическом процессе равна…
1) 5 R ; |
2) |
0; |
|
3) |
R ; |
4) |
3 R . |
|
|
|
|||||
2 |
|
|
|
|
|
|
|
2 |
|
|
|
|
|
||
18. |
Коэффициентом Пуассона называют величину, равную… |
||||||||||||||
|
i |
|
i 2 |
|
|
Cp R |
|
C |
|
|
|
Cp |
|
||
1) |
|
|
; 2) |
|
; |
3) |
|
; 4) |
V |
; |
5) |
|
. |
||
i 2 |
2 |
C |
C |
||||||||||||
|
|
|
|
|
C |
p |
|
|
|
||||||
|
|
|
|
|
|
|
V |
|
|
|
|
V |
|
||
19. |
Коэффициент Пуассона для аргона равен… |
|
|
|
|||||||||||
1) 0,71; |
2) |
1,29; |
|
3) 1,33; |
4) 1,4; |
|
5) 1,67. |
||||||||
20. Расположите идеальные газы O2 , NH3 , He в порядке возрастания коэффициента Пуассона…
1) |
He , O2 , NH3 ; |
2) |
O2 |
, He , NH3 ; |
3) NH3 , O2 , He ; |
4) |
NH3 , He , O2 ; |
5) O2 |
, NH3 , He . |
|
|
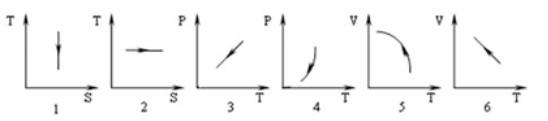
21. Адиабатному расширению газа ( p давление, V объем, T температура, S энтропия) соответствует диаграмма …
Укажите не менее двух вариантов ответа |
|
|
|||
1) 4; |
2) 3; |
3) 6; |
4) 5; |
5) 2; |
6) 1. |
98
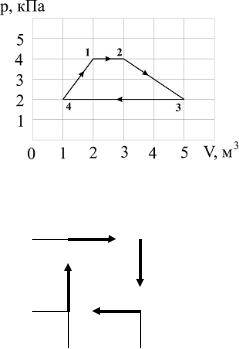
22.При увеличении давления в 3 раза и уменьшении объема в 2 раза внутренняя энергия идеального газа….
1) уменьшится в 6 раз;
2) уменьшится в 1,5 раза;
3) увеличится в 1,5 раза;
4) увеличится в 6 раз.
23.Состояние идеального газа определяется значениями параметров
Т0 , p0 и V0 , где T – термодинамическая температура, p – давление, V –
p0 ,V0 в
2 p0 ,V0 . При этом его внутренняя энергия газа…
1)увеличилась;
2)не изменилась;
3)уменьшилась.
24. Состояние идеального газа определяется значениями параметров
Т0 , p0 и V0 , где T – термодинамическая температура, p – давление, V – |
|
объем |
3 p0 ,V0 |
в состояние p0 ,2V0 . При этом его внутренняя энергия газа… |
|
1) |
не изменилась; |
2) |
уменьшилась; |
3) |
увеличилась. |
25. Диаграмма циклического процесса идеального одноатомного газа представлена на рисунке. Работа газа за цикл (в кДж) равна …
1) 10; |
2) 5; |
3) 20; |
4) 15. |
|
|
p |
|
2 |
3 |
|
|||
|
|
|
|
||||||
26. Найти работу тепловой машины за |
p2 |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||
один цикл, изображенный на рисунке. |
|
|
|
|
|
|
|
|
|
1) A p2 p1 V2 V1 |
; |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||
2) A p2 V2 V1 ; |
|
p1 |
|
|
|
|
|
|
|
|
|
1 |
|
|
|
4 |
|||
3) A p2 p1 V2 ; |
|
|
|
|
|
|
|||
|
|
|
|
|
|
|
|
|
|
|
|
0 V1 |
|
V2 |
V |
||||
4) A p2V2 . |
|
|
|
||||||
99
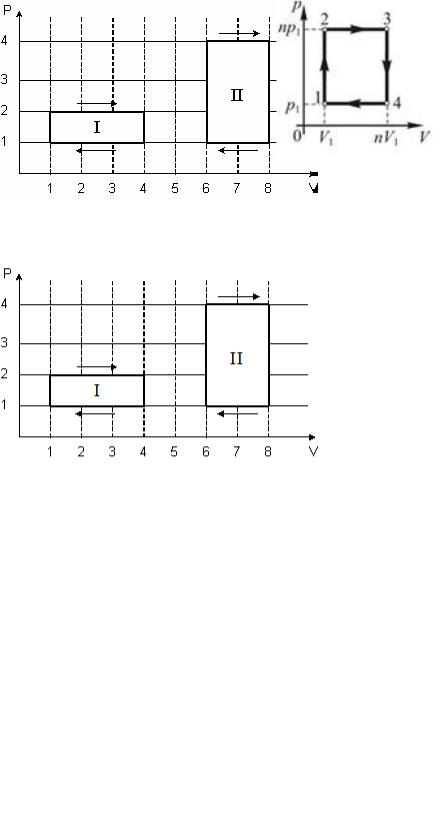
27. Идеальный газ совершает замкнутый цикл 1-2-3-4-1, состоящий из двух изохор и двух изобар. Как давление, так и объем в пределах цикла изменяются в n раз. Если давление и объем в состоянии 1 равны соответственно p1 и V1, то рабо-
та газа за цикл равна ... |
2) A p1V1 n 1 ; |
|||
1) A p1V1n ; |
|
|||
3) A p V n 1 2 |
; |
4) A p V n2 . |
||
1 |
1 |
|
1 |
1 |
28. На ( p,V )-диаграмме изображены два циклических процесса.
Отношение работ |
|
|
AII |
, совершенных в этих циклах, равно … |
||||
|
|
|
||||||
|
|
|
|
|
A |
|
|
|
|
|
1 |
|
|
I |
|
1 . |
|
1) 2; |
2) |
; |
|
3) 2 ; |
4) |
|||
|
|
2 |
|
|
|
|
|
2 |
29. На ( p,V )-диаграмме изображены два циклических процесса.
|
|
|
|
|
|
|
|
|
|
Отношение работ |
|
AI |
, совершенных в этих циклах, равно … |
||||||
|
A |
||||||||
|
|
|
|
|
|
|
|
|
|
|
|
1 |
|
II |
|
|
1 . |
|
|
1) 2; |
2) |
; |
3) 2 ; |
4) |
|
||||
|
|
2 |
|
|
|
|
2 |
|
|
100
