
212
.pdf
МИНИСТЕРСТВО ОБРАЗОВАНИЯ И НАУКИ РОССИЙСКОЙ ФЕДЕРАЦИИ
Федеральное государственное бюджетное образовательное учреждение высшего профессионального образования
«Пензенский государственный университет архитектуры и строительства»
(ПГУАС)
ОЧИСТКА СТОЧНЫХ ВОД
Методические указания по выполнению лабораторных работ Часть 2
Под общей редакцией доктора технических наук, профессора Ю.П. Скачкова
Пенза 2013
УДК 628.3:378.147.091.313(075.8) ББК 38.761.2:74.58я73
ОF94
Рекомендовано Редсоветом университета
Рецензенты: заместитель технического директора по инновациям ООО «Горводоканал» г. ПенF зы П.В. Пивоваров;
главный специалистFэксперт государF ственного автономного учреждения (РеF гиональный центр государственной эксF пертизы и ценообразования в строительF стве Пензенской области) С.А. Ляпин
ОF94 Очистка сточных вод: методические указания по выF полнению лабораторных работ. Ч. 2 / А.М. Исаева, И.И. ШпиF лева, С.И. Коровянский; под общ. ред. дFра техн. наук, проф. Ю.П. Скачкова. – Пенза: ПГУАС, 2013. – 28 с.
Изложены методика и порядок проведения анализа сточных вод, активного ила и осадков.
Направлены на овладение навыками постановки и проведения экспериментов по заданным методикам; выработку умений составлять отчеты по выполненным работам.
Методические указания подготовлены на кафедре «Водоснабжение, водоотвеF дение и гидротехника» и базовой кафедре ПГУАС при ООО «Гипромаш» и предназначены для использования студентами, обучающимися по направлению 270800 «Строительство» (бакалавриат), при выполнении лабораторных работ по курсу «Очистка сточных вод».
Пензенский государственный университет архитектуры и строительства, 2013
Исаева А.М., Шпилева И.И., Коровянский С.И., 2013
2
ВВЕДЕНИЕ
Сточные воды, отводимые с территории промышленных предприяF тий, по своему составу делятся на три вида: производственные, бытовые и атмосферные. Производственные стоки могут быть загрязF ненными и незагрязненными (условно чистыми). Загрязненные проF изводственные сточные воды отличаются большим разнообразием как по наименованиям, так и по количественному содержанию примесей и веществ: минеральные, органические, легкоF и трудноокисляемые, нефть и нефтепродукты, кислоты и щелочи, токсичные и опасные в эпидемиологическом отношении вещества, анионы различных солей
(сульфаты SO42 , фосфаты РO43 , нитриты NO2 , нитраты NO3 , хлориды Сl– и т.д.), катионы тяжелых металлов (никель Ni+2, медь Cu+2,
хром Cr+6, Cr+3, цинк Zn+2, железо Fе+3, Fе+2, свинец Рb+2, марганец Мg+2 и т.д.), СПАВ, радиоактивные отходы, фенолы, взрывоопасные веF щества и т.д.
Загрязненные сточные воды промышленных предприятий в завиF симости от видов загрязнений и требований к дальнейшему их испольF зованию можно после очистки на канализационных сооружениях сбрасывать в горколлектор, в водоемы, использовать в оборотFной системе водоснабжения промышленных предприятий, при этом максимально извлекая ценные примеси из промстоков, утилизировать образующиеся осадки.
Условия выпуска производственных сточных вод в водоемы регF ламентируются «Правилами охраны поверхностных вод от загрязF нения сточными водами», «Правилами санитарной охраны прибрежF ных районов морей» и МДК 3–01.2001.
Содержание вредных веществ в воде водоема и в производственных стоках нормируется значениями предельно допустимых концентраций (ПДК) – основного гигиенического критерия качества воды водоемов, используемого органами Государственного контроля. ПДК – это максимальные концентрации, при которых вещества не оказывают пряF мого или опосредованного влияния на состояние здоровья населения и не ухудшают гигиенических условий водопользования. ПДК – это основа расчета нормативно допустимого сброса предприятий (НДС) очищенных производственных сточных вод в водоемы. ПДК установF лены по санитарноFтоксикологическому, общесанитарному и органоF лептическому показателям вредности для водоемов хозяйственноF питьевого и культурноFбытового, а также рыбохозяйственного водоF пользования.
При расчете условий спуска производственных сточных вод при соF вместном присутствии в них нескольких вредных веществ сумма конF центраций этих веществ (нормируемых по одному признаку вредности),
3
выраженных в долях от соответствующих ПДК для каждого вещества в отдельности, не должна превышать единицы, то есть:
C1/C1пд + С2/С2пд + С3/С3пд + … + Сi/Сiпд 1,
где С1, С2, C3, ..., Сi – |
концентрации загрязняющих веществ по |
|
одному лимитирующему показателю вредности |
|
в воде водоема, мг/л; |
C1пд, С2пд, …, Сiпд – |
ПДК, установленные для соответствующих |
|
загрязняющих веществ в воде водоема, мг/л. |
Расчет необходимой степени очистки производственных сточных вод по концентрации загрязняющим веществом Сст, мг/л, производится по формуле
Ccт [( Qr)/q](Cпд – Сp) + Спд, где – коэффициент смешения;
Qr – расход воды в водоеме, м3/с;
q – средний расход сточных вод, м3/с;
Спд – предельно допустимое содержание загрязняющего вещества в воде водоема, мг/л;
Ср – концентрация загрязняющего вещества в воде водоема выше места выпуска рассматриваемого стока, мг/л.
4
Лабораторная работа 1 ОЧИСТКА СТОЧНЫХ ВОД МЕТОДОМ КОАГУЛЯЦИИ.
ОПРЕДЕЛЕНИЕ ОПТИМАЛЬНЫХ ДОЗ КОАГУЛЯНТА
Цель работы – изучить очистку сточных вод методом коагуляции, определить оптимальные дозы коагулянта без подщелачивания и с подщелачиванием.
Реактивы и оборудование:
1)сульфат алюминия Al2(SO4)3;
2)хлорид железа FeCl3;
3)известковое молоко Ca(OH)2;
4)мерные цилиндры емкостью 500 мл (12 шт.) и 5–10 мл;
5)индикатор – лакмусовая бумага;
6)беззольный фильтр;
7)сушильный шкаф;
8)аналитические весы;
9)пипетки.
Порядок и методика проведения анализа
Оптимальной дозой коагулянта считается наименьшее его колиF чество, при котором достигается наилучший эффект очистки конкретF ной сточной воды. В качестве коагулянта чаще всего применяют различные соли алюминия и железа: сульфат алюминия Al2(SO4)3, алюF минат натрия Na3AlO3, сульфат двухвалентного и трехвалентного жеF леза: FeSO4 и Fe2(SO4)3, хлорид железа FeCl3.
В результате гидролиза коагулянтов снижается величина pH сточF ной воды, что отрицательно сказывается на ходе процесса коагуляции.
Гидролиз коагулянтов можно выразить следующими уравнениями:
Al2(SO4)3+2H2O 2AlOHSO4+H2SO4
FeCl3+H2O FeOHCl2+HCl
Fe(SO4)3+2H2O 2FeOHSO4+H2SO4
Нейтрализация кислот, образующихся при гидролизе коагулянтов, может протекать за счет щелочного резерва сточной воды или щелочей, которые специально вводят в обрабатываемую воду вместе с коагулянF тами.
Предварительно следует определить pH и концентрацию взвешенF ных веществ в исследуемой воде. Затем в 12 мерных цилиндров емF
5

костью 500 мл каждый налить по 250 мл исследуемой воды. В первые шесть цилиндров пипеткой добавить 1 %Fй раствор коагулянта в коF личестве, указанном в табл. 1.
Т а б л и ц а 1
Доза коагулянта
Номер цилиндра |
1 |
2 |
3 |
4 |
5 |
6 |
|
Количество раствора |
0,5 |
1,0 |
2,5 |
5,0 |
7,5 |
10,0 |
|
коагулянта, мл |
|||||||
|
|
|
|
|
|
||
Доза коагулянта FeCl3, |
20,0 |
40,0 |
100,0 |
200,0 |
300,0 |
400,0 |
|
Al2(SO4)3, мг/л |
|||||||
|
|
|
|
|
|
В цилиндры 7–12 вместе с раствором коагулянта ввести 0,1 %Fй
раствор известкового молока в количестве, указанном в табл. 2. |
|
||||||
|
|
|
|
|
|
Т а б л и ц а 2 |
|
|
Доза извести |
|
|
|
|
||
|
|
|
|
|
|
|
|
Номер цилиндра |
|
7 |
8 |
9 |
10 |
11 |
12 |
Количество раствора известF |
2,0 |
6,0 |
12,0 |
20,0 |
30,0 |
50,0 |
|
кового молока, мл |
|
||||||
|
|
|
|
|
|
|
|
Доза извести Сa(OH)2, мг/л |
|
8,0 |
24,0 |
48,0 |
80,0 |
120,0 |
200,0 |
После введения реагентов включить секундомер и содержимое цилиндров быстро перемешать стеклянной палочкой в течение 30 с, затем медленно перемешивать в течение 10 мин, после чего в течение 30 мин (60 мин). Дать отстояться жидкости и отобрать пипеткой или сифоном из верхнего слоя каждого цилиндра (не взмучивая осадка) пробы воды, в которых определить pH и концентрацию взвешенных веществ.
При отстаивании воды в цилиндрах следует отмечать время начала образования хлопьев, их вид (рыхлые, крупные, мелкие). Наблюдения проводить через каждые 10 минут. Результаты вычислений занести в табл. 3.
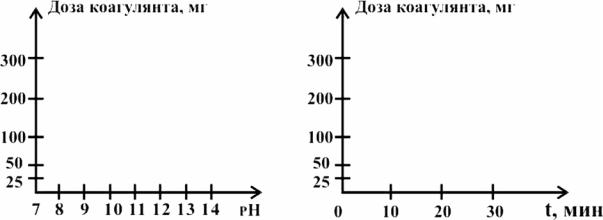
Для каждой серии проведенных опытов построить графики в коорF динатах:
pH – доза коагулянта;
время полного оседания хлопьев – доза коагулянта.
6
Т а б л и ц а 3 Основные параметры, определяемые при очистке стоков
методом коагуляции
|
Доза коагулянта, мг/л |
Доза извести, мг/л |
Время начала |
Время конца оседания хлопьев, мин |
Показатели |
|
|
|||
Номер цилиндра |
|
|
после очистки |
|
|
|||||
образования хлопьев, мин |
оседания хлопьев, мин |
Эффект |
Примечание |
|||||||
|
|
|||||||||
количество водородных ионов pH |
взвешенные вещества, мг/л |
|||||||||
|
|
|
|
|
|
|
|
|
|
|
Графики представить в координатах, приведенных на рис. 1.
Рис. 1. Графики в координатах:
доза коагулянта – pH, доза коагулянта – время оседания хлопьев
На основании анализа графических данных определить оптимальF ную дозу коагулянта, а также влияние подщелачивания на процесс осветления воды.
7
Лабораторная работа 2 ОПРЕДЕЛЕНИЕ СОДЕРЖАНИЯ ОБЩЕГО ЖЕЛЕЗА
КОЛОРИМЕТРИЧЕСКИМ МЕТОДОМ
Цель работы – определить содержание общего железа Fe+3, Fe+2 c применением роданистого аммония колориметрическим методом.
Реактивы и оборудование:
1)стандартный раствор железа Fe+3;
2)роданистый аммоний (20 %Fй раствор);
3)перманганат калия (0,1 н. раствор);
4)азотная кислота HNO3 (6 н. раствор);
5)КФКF2, зеленый светофильтр, = 490 нм, кювета 50,0 мм;
6)электроплитка с асбестовой сеткой;
7)колбы емкостью 200 мл, 100 мл; измерительные цилиндры.
Принцип метода и мешающие влияния
Метод основан на образовании окрашенного в красный цвет родаF нида железа Fe(CNS)3 и его комплексных соединений Fe(CNS)6, Fe(CNS)3 при добавлении раствора роданистого аммония к раствору, содержащему ионы трехвалентного железа. Находящееся в пробе заF кисное железо Fe+2 переводят в окисное железо Fe+3 кипячением с азотной кислотой.
Порядок и методика проведения анализа
В широкогорлую колбу для кипячения вместимостью 200 мл помещают 50 мл хорошо перемешанной пробы, содержащей не более 4 мг железа в 1 л или меньший объем пробы, разбавленной дистилF лированной водой до 50 мл, добавляют 5 мл 6 н. азотной кислоты, кипятят не менее 5 мин. К горячей жидкости прибавляют раствор перманганата калия до слабоFрозового окрашивания после 5Fминутного стояния. Раствор охлаждают, фильтруют через бумажный фильтр и переносят в мерную колбу на 100 мл, добавляют 5 мл роданистого аммония. Объем раствора доводят дистиллированной водой до метки и после перемешивания тут же измеряют оптическую плотность на КФКF2 через зеленый светофильтр с длиной волны = 490 нм (кювета – 50 мм). Вводят поправку на оптическую плотность холостой пробы, приготовленной таким же способом с дистиллированной водой, как и со сточной. По калибровочной кривой находят концентрацию железа
8
Сгр, мг/л, и определяют концентрацию общего железа Сх, мг/л, в пробе по формуле
Cх |
Cгр |
1000 |
|
|
|
, |
|
|
|
||
|
|
V |
|
где V – объем пробы, взятой для анализа, мл.
Результаты в диапазоне до 1 мг/л округляют до сотых долей, от 1 до 10 мг/л – до десятых долей.
ПДК железа, общего в воде водоемов хозяйственноFпитьевого и культурноFбытового водопользования, должна быть не более 0,3 мг/л, в воде рыбохозяйственного водопользования – не более 0,1 мг/л. Концентрация общего железа на очистных сооружениях биологичесF кой очистки с аэротенками снижается на 65 %.
Построение калибровочной кривой
Калибровочная кривая строится на основании анализа серии, соF держащей от 0,5 до 10 мл стандартного раствора железа.
9
Лабораторная работа 3 ОПРЕДЕЛЕНИЕ КОНЦЕНТРАЦИИ СВИНЦА
НЕФЕЛОМЕТРИЧЕСКИМ МЕТОДОМ
Цель работы – определить концентрацию свинца Pb+2 в исслеF дуемой пробе.
Реактивы и оборудование:
1)сегнетовая соль 50 %Fя;
2)едкий натр 27 %Fй;
3)натрий серноватистоFкислый (тиосульфат натрия) 10 %Fй;
4)глицерин химически чистый;
5)сульфид натрия кристаллический Na2S 9H2O;
6)азотная кислота 1:5;
7)индикаторная бумага;
8)водноFглицериновый раствор сульфида натрия;
9)фотоэлектроколориметр ФЭКF56, светофильтр №4, кювета 50,0 мм;
10)колбы, V = 100 мл, измерительные цилиндры.
Принцип метода и мешающие влияния
Сущность метода заключается в том, что при введении в раствор, содержащий свинец, сульфидиона, образуется бурая коллоидная взвесь сульфида свинца, количество свинца во взятом объеме исследуемой воды не должно быть менее 0,1 мг и более 5 мг. Мешающее влияние железа устраняется сегнетовой солью; алюминия и цинка – введением едкого натра меди и тиосульфата натрия.
Порядок и методика проведения анализа
В мерную колбу на 100 мл отбирают 10–80 мл фильтрованной пробы. Приливают в колбу последовательно:
5 мл 50 %Fй сегнетовой соли;
3 мл 27 %Fго едкого натра;
5 мл 10 %Fго тиосульфата натрия.
После введения каждого реактива содержимое колбы хорошо переF мешивается.
Затем приливают 0,2 мл водноFглицеринового раствора сульфида натрия, перемешивают, доводят до метки дистиллированной водой и через 2 минуты колориметрируют с синим светофильтром. КолоF риметрирование ведется быстро, чтобы предотвратить возможное осаждение свинца. В качестве раствора сравнения используют ту же
10
