
- •Особенности факельного сжигания
- •Образование оксидов азота в факеле вихревой горелки
- •Влияние качества топлива
- •Способы, основанные на снижении температуры
- •Способы, основанные на снижении избытка воздуха
- •Специальные конструкции горелок
- •3.2.6. Восстановление оксидов азота в топочной камере
- •3.2.7. Топки с кипятим слоем как метод снижения
- •Влияние качества топлива
- •Методы, основанные на снижении температуры
- •Специальные конструкции горелок
- •5.2.1. Расчет суммарных выбросов
- •Расчет удельных выбросов оксидов азота
- •Расчет удельных выбросов для газомазутных котлов
Библиотека
ТЕПЛОЭНЕРГЕТИКА
Основана в 1959 году
В.Р. Котлер
во А
Оксиды азота в дымовых газах котлов
ББК 31.352
К 73
УДК 662.613.5
Рецензент А. К. Внуков
Котлер В. Р.
К 73 Оксиды азота в дымовых газах котлов. — М.: ЭнергоатОМ- издат, 1987. — 144 с.: ил. — (Б.-ка теплоэнергетика).
ISBN 5-283-OOO13-3.
Рассмотрена актуальная проблема снижения выбросов оксидов азота, образующихся при сжигании органического топлива в котлах тепловых электростанций. Показано влияние состава топлива, параметров топочного процесса и конструктивных особенностей котла на образование оксидов азота. Изложены практические способы уменьшения количества оксидов изота за счет усовершенствования технологии процесса горения, а также способы очистки дымовых газов от оксидов азота.
Для инженерно-технических работников тепловых электростанций, конструкторских, научно-исследовательских и наладочных организаций.
210-88
ББК
31.352

051 (01)-87
ISBN 5-283-OOO13-3
© Энергоатомиздат, 1987
;x
ПРЕДИСЛОВИЕ
Быстрый рост потребления энергии сопровождается, как известно, увеличением вредных выбросов, загрязняющих окружающую среду. В Советском Союзе проблема охраны окружающей среды остается в центре внимания Партии и Правительства. Об этом свидетельствует, в частности, введенный с 1 января 1981 г. Закон СССР ”06 охране атмосферного воздуха”, который регламентирует сложный комплекс вопросов, связанных с выбросами вредных веществ в атмосферу, и устанавливает строгую ответственность за недопустимое загрязнение атмосферного воздуха.
Тепловые электростанции и котельные, потребляя огромное количество газообразного, жидкого и твердого топлива, выбрасывают в атмосферу продукты сгорания, содержащие золу, оксиды серы и азота, а также (в меньших количествах) оксиды углерода и группу органических соединений, называемых полициклическими ароматическими углеводородами (ПАУ).
В последние годы при сооружении новых и расширении действующих ТЭС одной из основных проблем для проектировщиков становится обеспечение установленных санитарными органами предельно допустимых концентраций газообразных примесей (в первую очередь — оксидов азота) в атмосферном воздухе. После введения ГОСТ 17.2.3.02-78 (Правила установления допустимых выбросов вредных веществ промышленными предприятиями) проблема ограничения выбросов оксидов азота приобретает большую остроту и для эксплуатационного персонала тепловых электростанций, обязанного соблюдать нормы предельно допустимых или временно согласованных выбросов по оксидам азота.
Учитывая важность этой проблемы, в большинстве научно-исследовательских институтов энергетического профиля в последние годы резко увеличен объем исследований, связанных с разработкой способов снижения образования оксидов азота в котлах или с очисткой от них дымовых газов. Значительные исследования в этой области проводятся также в США, Японии, ФРГ и в некоторых других странах.
В предлагаемой читателю книге предпринята попытка обобщить накопленный в последние годы материал, относящийся к исследованию процесса образования оксидов азота и к разработке методов снижения их выбросов в атмосферу котельными установками тепловых электростанций. В книге приведены основные достижения в этой области совет-
ских энергетиков, в том числе Всесоюзного теплотехнического института им. Ф. Э. Дзержинского, сотрудником которого является автор книги. Кроме того, в книге широко представлены результаты наиболее значительных исследований зарубежных ученых, которые с успехом могут быть использованы в отечественной энергетике.
Отдавая себе отчет в сложности и многообразии проблем, затронутых в книге, автор не претендует на полноту их изложения, особенно в части теории образования оксидов азота. Например, не рассмотрены весьма важные вопросы, связанные с методикой измерения концентрации оксидов азота в дымовых газах, а также экономический аспект проблемы защиты атмосферы от оксидов азота. Главной своей задачей автор считал ознакомление широких кругов теплотехников с существом проблемы и с путями ее решения, а также оказание практической помощи многочисленным проектировщикам, конструкторам и эксплуатационным работникам, занятым проблемой сокращения выбросов оксидов азота в атмосферу.
Автор выражает благодарность рецензенту доктору техн, наук, проф. А. К. Внукову за ценные замечания, сделанные при просмотре рукописи, и редактору Э. X. Вербовецкому за большой труд по редактированию книги. Автор с благодарностью примет замечания и предложения читателей по устранению возможных недостатков, которые следует присылать по адресу: 113114, Москва, Шлюзовая наб., 10, Энерго- атомиздат.
Автор
Глава первая
ЭНЕРГЕТИКА И ОКСИДЫ АЗОТА
ОКСИДЫ АЗОТА В АТМОСФЕРЕ
В отличие от молекулярного азота N2, который составляет почти 79% атмосферного воздуха, оксиды азота содержатся в атмосфере в значительно меньших количествах, но несмотря на это роль их в жизни человека весьма существенна.
Оксиды азота обычно классифицируют в зависимости от степени окисления азота. При соединении азота с кислородом по мере увеличения его валентности образуются гемиоксид N20, оксид NO, азотистый ангидрид N2 Оз , диоксид NO2, тетраоксид диазота N2 О4 и азотный ангидрид N2O5. В проблеме охраны атмосферного воздуха практическое значение имеют оксид и диоксид азота, сумму которых часто обозначают как NOX. Другие оксиды азота не считаются важными с биологической точки зрения или их присутствие в земной атмосфере ничтожно мало вследствие неустойчивости этих соединений.
Оксид азота NO — малоактивный в химическом отношении бесцветный газ, лишенный запаха и плохо растворимый в воде. При комнатной температуре и атмосферном давлении растворимость NO составляет всего лишь 0,047 см3/г, с повышением температуры растворимость падает. Диоксид азота NO2 более активен, он красно-бурого цвета и отличается резким запахом.
В глобальном масштабе количество оксидов азота, образующихся естественным путем в результате жизнедеятельности почвенных бактерий, а также при вулканической деятельности и разрядах молний, по различным источникам, составляет от 800 до 1100 млн. т/год [1, 3]. Это намного превосходит выброс оксидов азота, образующихся в результате человеческой деятельности (по оценке 1970 г. - приблизительно S3 млн. т/год). Однако необходимо учитывать, что в результате бурного развития Промышленности и транспорта антропогенный выброс оксидов азота увеличивается год от года, практически удваиваясь каждые 20—25 лет. Об этом свидетельствует табл. 1.1, в которой по данным Агентства по охране окружающей среды США приведена динамика выбросов в атмосферу США основных загрязнителей воздуха — твердых частиц, сернистого ангидрида и оксидов азота [2].
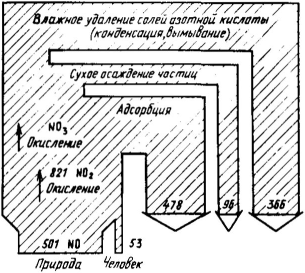
Если сопоставить глобальную концентрацию оксидов азота в атмосферном воздухе и количество поступающих в атмосферу оксидов азота, то окажется, что среднее время пребывания этих оксидов в атмосфере составляет примерно 4 дня. На рис. 1.1 показан материальный баланс циркуляции оксидов азота в атмосфере, составленный по [3].
Годы |
no2 |
so2 |
Твердые частицы |
||||
млн. т/год |
% |
млн. т/год |
% |
млн. т/год |
% |
||
1940 |
7,2 |
100 |
19,2 |
100 |
24,1 |
100 |
|
1950 |
10,3 |
143 |
21,6 |
113 |
25,6 |
106 |
|
1960 |
14,0 |
194 |
21,2 |
110 |
22,3 |
93 |
|
1970 |
20,4 |
283 |
30,8 |
160 |
19,4 |
81 |
|
1980 |
22,8 |
317 |
26,1 |
136 |
8,6 |
36 |
|
Таблица
1.1.
Антропогенные выбросы в атмосферу США
за период с 1940 по 1980 г. (2]
Рис.
1.1.
Циркуляция оксидов азота в атмосфере,
млн. т/год [3]
 Небольшая
доля антропогенных выбросов в общей
массе поступающих в атмосферу оксидов
азота не должна успокаивать: дело в том,
что оксиды азота, генерируемые естественным
путем, распределяются равномерно по
земному шару, и поэтому естественные
фоновые концентрации наиболее
токсичного диоксида азота над континентами
лежат в пределах от 0,4 до 9,4 мкг/м3,
а для оксида азота они составляют 0-7,4
мкг/м3.
Антропогенные выбросы оксидов азота
сосредоточены в местах хозяйственной
деятельности человека, и поэтому
концентрации NOX
в городских районах на 1—2 порядка выше
естественной фоновой концентрации.
Об этом свидетельствуют данные табл.
1.2, в которой приведены концентрации
диоксида азота, мкг/м3,
зарегистрированные в отдельных
городах США и Японии.
Небольшая
доля антропогенных выбросов в общей
массе поступающих в атмосферу оксидов
азота не должна успокаивать: дело в том,
что оксиды азота, генерируемые естественным
путем, распределяются равномерно по
земному шару, и поэтому естественные
фоновые концентрации наиболее
токсичного диоксида азота над континентами
лежат в пределах от 0,4 до 9,4 мкг/м3,
а для оксида азота они составляют 0-7,4
мкг/м3.
Антропогенные выбросы оксидов азота
сосредоточены в местах хозяйственной
деятельности человека, и поэтому
концентрации NOX
в городских районах на 1—2 порядка выше
естественной фоновой концентрации.
Об этом свидетельствуют данные табл.
1.2, в которой приведены концентрации
диоксида азота, мкг/м3,
зарегистрированные в отдельных
городах США и Японии.
Таблица 1.2. Концентрации диоксида азота, мкг/м3, в крупнейших городах США и Японии [ 1 ]
Город |
Среднегодо вая |
Максимальная среднемесячная |
Максимальная среднесуточная |
Максимальная часовая |
Вашингтон |
68 |
— |
130 |
— |
Нью-Йорк |
80 |
— |
243 |
— |
Чикаго |
47 |
— |
114 |
— |
Филадельфия |
73 |
— |
166 |
— |
Токио |
86 |
105 |
426 |
840 |
Кавасаки |
90 |
113 |
200 |
440 |
Осака |
86 |
115 |
228 |
640 |
ОКСИДЫ АЗОТА В ШЛЕЙФЕ ДЫМОВЫХ ГАЗОВ
При сгорании органического топлива в котлах тепловых электростанций и в других топливоиспользующих агрегатах образуется главным образом оксид азота NO. Этот факт был установлен как при лабораторных исследованиях [4], так и в промышленных опытах, при анализе дымовых газов за котлами ТЭС.
В качестве примера можно сослаться на измерения Ештова и др. [5], выполненные на четырех котлах паропроизводительностью от 150 до 1060 т/ч. Дымовые газы отбирались из газохода перед воздухоподогревателем или на входе в дымовую трубу. Концентрация кислорода в отобранных пробах газа менялась от 4 до 9% (аух = 1,23-5-1,75). Авторам не удалось установить четкой зависимости у = 100NO2/(NO + NO2) от каких-либо параметров. Минимальное значение <р оказалось равным 1,34%, а максимальное — 2,77%. В первом случае общая концентрация оксидов азота равнялась 0,6 г/м3, во втором — 2,3 г/м3 (котел паропроизводительностью 1060 т/ч, топка с жидким шлакоудалением).
Другие исследования, в которых осуществлялось раздельное измерение оксида и диоксида азота, также свидетельствуют о том, что в продуктах сгорания котельных установок доля диоксида азота NO2 составляет обычно 2-5% суммарного-содержания оксидов азота NOX. Однако в шлейфе дымовых газов происходит доокисление NO до NO2. Процесс этот имеет немаловажное значение, так как токсичность диоксида азота в несколько раз выше токсичности N0: напомним, что принятая в СССР максимально разовая предельно допустимая концентрация диоксида азота (ПДКМо2) в приземном слое воздуха равна 0,085 мг/м3, в то время как ПДКыо = 0,60 мг/м3 [7].
В настоящее время в СССР директивные документы (СН 369-74) предполагают полный переход NO в NO2, что, конечно, приводит к за- • вышению расчетной загазованности воздуха по сравнению с фактической. Такое решение было принято несколько десятилетий назад в связи с невозможностью рассчитать долю перехода NO в NO2. Исследования, проведенные в 70-е годы советскими (А. К. Внуков, И. Я. Сигал и др.) и зарубежными (Бейлке, Элшоут) учеными, позволили оценить с достаточной точностью степень перехода NO в NO2 в зависимости от некоторых атмосферных параметров.
Окисление NO в NO2 может протекать по трем реакциям:
(1.1)
(1-2)
(1.3)
NO + О3 NO2 + О2;
NO + RO2 -> NO2 + RO.
Реакция (1.1) играет значительную роль только при достаточно высоких концентрациях NO. Такие условия наблюдаются в шлейфе дымовых газов при отсутствии интенсивного перемешивания этих газов с окру-
жающим воздухом (т. е. при низких значениях коэффициента турбулентной диффузии). Скорость этой реакции уменьшается при снижении концентрации N0 и быстро становится несущественной.
Еще меньшую роль играет реакция (1.3): превращение оксида азота в диоксид с помощью пероксидного радикала имеет значение лишь тогда, когда высоки концентрации углеводородных радикалов и интенсивность ультрафиолетового облучения.
Для обычных условий распространения шлейфа дымовых газов в нижних слоях атмосферы, когда происходит интенсивное турбулентное перемешивание, наибольшее значение имеет реакция (1.2) — окисление N0 озоном. Однако необходимо учитывать, что диоксид азота обладает высокой поглощающей способностью в ультрафиолетовой области в диапазоне от 300 до 400 мкм и в течение дня, при наличии ультрафиолетового излучения, протекают также реакции, приводящие к образованию озона: УФ-лучи
N02 >NO + O; (1.4)
0+02+М-*03+М. (1.5)
Две последние реакции в сочетании с реакцией (1.2) определяют динамику системы N0 — N02 — О3, причем в условиях хорошего перемешивания за достаточно длительный период должно устанавливаться равновесное состояние:
[Оз] [NO] = ^4
[NO2[ к/
где К4 и К2 — константы соответствующих реакций, которые изменяются в зависимости от времени суток, широты и некоторых параметров атмосферы. Как правило, в сельских районах со сравнительно чистой атмосферой дневная концентрация оксида азота составляет только малую часть концентрации диоксида азота.
В районах с повышенным загрязнением атмосферы оксидами азота, в том числе в городах с интенсивным движением автотранспорта, реакция (1.2) протекает до завершения, с использованием всего озона, только в ночное время. В дневное время, как убедительно показали опыты Сигала и Домбровской [8], в воздухе преобладает оксид азота, концентрация которого в 5—10 раз превышает концентрацию N02.
Большой объем исследований, направленных на выявление особенностей трансформации оксидов азота в дымовом шлейфе ТЭС, был проведен сотрудниками Белорусского отделения ВНИПИэнергопром под руководством А. К. Внукова и Минского медицинского института [9].
Натурные измерения проводились с помощью вертолета, который позволил отбирать пробы газов из дымового шлейфа крупной ГРЭС, сжигающей экибастузский уголь. Усредненные по сечению дымового факела пробы отбирались на различном расстоянии и анализировались
отдельно на содержание NO и NO2. Для оценки фоновой загазованности атмосферы пробы воздуха отбирались с наветренной стороны дымовой трубы. В дневное время при ясной погоде и скорости ветра 5 м/с фоновые концентрации составляли: N0=0,017 мг/м3; NO2 =0,036 мг/м3. После выхода дымовых газов из трубы концентрация оксида азота быстро снижалась как в результате разбавления факела воздухом, так и вследствие перехода NO в NO2. По тем же причинам концентрация диоксида азота на начальном участке, наоборот, возрастала. На расстоянии 10 км от ГРЭС концентрации NO и NO2 были близки к фоновым значениям. Степень доокисления = 100 NO2/(NO + NO2) по мере рассеивания дымовых газов постепенно увеличивалась, и на удалении 10 км среднее значение у составляло 64%.
Измерения, проведенные при других метеорологических условиях, показали, что с ростом скорости ветра значение несколько увеличивается. Анализ проб воздуха, отобранных на уровне дыхания человека в зоне максимальных приземных концентраций, показал, что значение ни при каких условиях не превышало уровня фоновых значений.
Таким образом, проведенное исследование показало, что принятый в настоящее время метод определения экологической нагрузки в районе ТЭС, состоящий в пересчете всего количества выбрасываемых с дымовыми газами оксидов азота в NO2, дает завышенные результаты. Полного окисления N0 в NO2 не происходит даже в той зоне дымового шлейфа, где содержание токсичных веществ приближается к уровню фоновых концентраций. В связи с этим ведутся работы, направленные на уточнение расчета загазованности атмосферы.
ДЕЙСТВИЕ ОКСИДОВ АЗОТА НА ЧЕЛОВЕКА,
РАСТИТЕЛЬНЫЙ И ЖИВОТНЫЙ МИР
Главной проблемой, возникающей в результате присутствия в воздухе оксидов азота, является их токсическое воздействие на здоровье людей. В течение последних двух десятилетий получены обширные данные о характере и особенностях этого воздействия, причем большая часть исследований представляет собой изучение влияния различных концентраций диоксида азота на подопытных животных. Воздействие : • оксидов азота на человека изучалось в контролируемых условиях (в узком диапазоне концентраций и в течение ограниченного отрезка времени). Кроме того, имеются данные по случайному и профессиональному воздействию на человека повышенных концентраций оксидов азота (такое воздействие имеет место при производстве некоторых кислот, толуола и нитроцеллюлозы, при горнорудных работах и при работе в туннелях с интенсивным движением транспорта).
На основании этих исследований установлено, что даже кратковременное (до 1 ч) воздействие диоксида азота в концентрации 47— 140 мг/м3 может вызвать воспаление легких и бронхит, а при концен-
трации 560-940 мг/м3 велика вероятность летального исхода в результате отека легких и асфикции [ 1 ].
Для оценки влияния оксидов азота на здоровье населения большое значение имеют опыты, проводимые в контролируемых условиях при концентрациях, которые близки к реально существующим в местах с высокой загазованностью. В результате этих исследований было показано, что порог ощущения запаха для диоксида азота и уровень, при котором отмечены изменения адаптации к темноте, регистрируются при концентрации 200 мкг/м3. Функциональные изменения в легких у здоровых людей (такие, как возрастание сопротивления дыхательных путей и др.) начинаются после десятиминутного ингаляционного воздействия диоксида азота в концентрации 1300 мкг/м3.
Повышенные концентрации оксидов азота в воздухе воздействуют не только на людей, но и на растительный мир: по данным американских исследователей, при концентрациях от 280 до 560 мкг/м3 наблюдалось повреждение томатов и бобовых [10].
Следует отметить еще одну проблему, связанную с присутствием в атмосфере оксидов азота. Соединяясь с атмосферной влагой, оксиды азота образуют слабые растворы азотистой и азотной кислот. Это приводит к выпаданию так называемых кислотных дождей, причиной которых являются антропогенные выбросы в атмосферу не только оксидов азота, но и оксидов серы.
Пагубное воздействие кислотных дождей на окружающую человека среду принимает в последние годы все более угрожающие масштабы [6]. Под воздействием кислотных дождей происходит закисление почв и обеднение их питательными элементами. Следствием этого являются снижение продуктивности ряда сельскохозяйственных культур и сильное увеличение кислотности вод поверхностных водоемов, что наносит ущерб рыбному хозяйству: в Швеции, например, 2,5 тыс. озер уже полностью лишены рыбы и еще 16 тыс. озер находятся на грани биологической гибели [11].
От кислотных дождей происходит деградация и полная гибель лесных массивов: в ФРГ леса повреждены на площади свыше 2 млн. га, в Польше — на 500 тыс. га с полным уничтожением древостоя на площади в 180тыс. га. Кислотные дожди усиливают коррозию и разрушение строительных материалов, памятников архитектуры и других культурных ценностей. По некоторым оценкам, ущерб от деградации окружающей среды во многих странах соизмерим с уровнем национального дохода в расчете на душу населения.
Проблема кислотных дождей осложняется тем, что в силу природных условий происходит трансграничный перенос SO2 и NOX. В связи с этим решить проблему на национальном уровне практически невозможно. Так, например, Норвегия имеет самые низкие в Европе выбросы в атмосферу сернистого ангидрида и оксидов азота. Однако реализация норвежского проекта SNSF по изучению кислотных дождей (1972—1980 гг.) 10
показала, что примерно 92% вредных веществ в атмосферу Норвегии ’’импортировано” из других стран. В Швеции эта цифра составляет 82%, в Финляндии — 74% [12].
Очень остро проявляется проблема кислотных дождей в канадо-американских отношениях в связи с тем, что 50—60% кислотных осадков, выпадающих в Канаде, поступает от источников, расположенных в северо-восточных штатах США. При этом Канада подвержена большему по сравнению с США ущербу от кислотных дождей: по сернистому ангидриду — в 4 раза, по оксидам азота — в 11 раз.
В последние годы предпринимаются попытки решения проблемы на международном уровне: на конференции по кислотным дождям, состоявшейся в марте 1984 г. в Оттаве, 9 стран Европы и Канада приняли программу экстренной борьбы с кислотными дождями. В частности, было подписано соглашение о сокращении на 30% выбросов SO2 и NOX за период с 1983 по 1993 г.
Еще одна вредная особенность оксидов азота, имеющая в отличие от кислотных дождей локальный характер, т. е. проявляющаяся в местах интенсивного выброса NOX, состоит в снижении прозрачности атмосферы и в образовании фотохимического тумана — смога. Это явление наблюдается главным образом в городах с интенсивным автомобильным движением и вследствие этого — с повышенной концентрацией углеводородов в воздухе. Под действием солнечной радиации диоксид азота, обладающий высокой поглощающей способностью в ультрафиолетовой области, разлагается на оксид азота и атомарный кислород, образующий озон [13]. Эта диссоциация приводит к большому количеству вторичных реакций, в результате которых появляется ядовитый смог.
ИСТОЧНИКИ ВЫБРОСОВ ОКСИДОВ АЗОТА
Основным антропогенным источником выброса оксидов азота в атмосферу является сжигание ископаемого топлива стационарными установками при производстве теплоты и электроэнергии. Большую роль, особенно в городах, играют также выбросы автотранспорта и некоторых промышленных предприятий (заводов по производству азотной кислоты, взрывчатых веществ и т. д.).
В США, например, по данным [3], суммарные выбросы оксидов азота в пересчете на NO2 составляют 25 млн. т/год. Примерно 49,7% всех выбросов оксидов азота (или 12,27 млн. т/год) приходится на стационарные топливосжигающие установки. Приблизительно 35,4% (8,72 млн. т/год) приходится на транспорт и 11,7% (2,88 млн. т/год) — на технологические выбросы промышленных предприятий.
В том же докладе сообщалось, что из 12,27 млн. т диоксида азота, ежегодно выбрасываемых стационарными топливоиспользующими установками, 5,94 млн. т (48,4%) приходится на производство электроэнергии, 5,39 млн. т (43,9%) — на выбросы котельных, нагревательных пе-
чей и других промышленных топливоиспользующих установок, а остальные 0,94 млн. т (7.7%) — на выбросы торговых предприятий, отопительных установок жилых домов и т. д. Из общего выброса оксидов азота тепловыми электростанциями в США почти 80% приходилось на пылеугольные котлы, а в перспективе эта цифра будет еще выше.
Примерно такое же соотношение между различными источниками ' выбросов оксидов азота наблюдается в большинстве промышленно раз- » витых стран. В ФРГ, например, из общего выброса оксидов азота в атмосферу, равного 3,0 млн. т/год, примерно 940 тыс. т/год приходится на ТЭС общего пользования, еще 580 тыс. т/год — на промышленность (включая ТЭЦ) и 140 тыс. т/год — на коммунальное хозяйство. В сумме это составляет 55,3% всех выбросов NOX в атмосферу. Остальные 44,7% (1340 тыс. т/год) приходится на транспортные средства [14].
1 В Советском Союзе, по данным [15], баланс выброса оксидов азота t предприятиями отдельных отраслей промышленности характеризуется •; следующими показателями: тепловые электростанции — 72,5%, автотранспорт — 17,3%; черная металлургия —. 6,1%; промышленность I строительных материалов — 1,8%; химическая промышленность — 1,7%; нефтеперерабатывающая промышленность — 0,6%.
>. Следовательно, важнейшим участком борьбы с загрязнением атмо- I сферы оксидами азота является крупная энергетика. И в ближайшие ) десятилетия, вероятно, роль этого источника выбросов будет возрастать в связи с увеличением доли электроэнергии в балансе энергетических ресурсов.
Для оценки перспектив загрязнения атмосферы токсичными продуктами сгорания органического топлива важно правильно оценить ожидаемый прирост потребления первичной энергии, а также рост потребления тех энергоносителей, использование которых приводит к выбросам в атмосферу оксидов азота. Таковыми являются нефть и нефтепродукты, используемые для сжигания, природный газ, а также твердые топлива (уголь, горючие сланцы, торф). Не загрязняется атмосфера оксидами азота при производстве энергии на гидравлических, атомных, геотермальных, солнечных и ветровых электростанциях.
Зарубежными футурологами опубликовано за последние годы большое число прогнозов в этой области, причем большинство исследований 70-х годов предсказывало особенно быстрое развитие атомной энергетики и использование возобновляемых видов энергии (солнечной, ветровой, различных видов океанической энергии и т. д.). Однако более поздние прогнозы сводятся к тому, что рост атомной энергетики будет не столь стремительным, возобновляемые источники энергии в обозримом будущем будут играть второстепенную роль, а потребление традиционных энергоносителей (главным образом угля) будет основным еще в течение многих десятилетий.
Сошлемся в качестве доказательства на исследование [16], которое является обобщением прогнозов, представленных различными органи- 12
Годы
Если
говорить о тепловых электростанциях,
то они будут сооружаться главным образом
на твердом топливе. Вероятно также
увеличение числа комбинированных ТЭС
с внутрицикловой газификацией угля
как средства повышения КПД цикла и
одновременно —
снижения
количества вредных выбросов в атмосферу.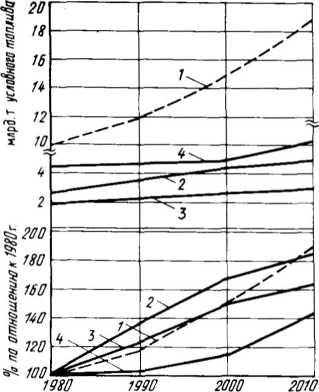


Рис. 1.2. Баланс потребления первичной энергии в 1980-2010 гг. [16]:
1 — вся первичная энергия; 2 - уголь; 3 - природный газ; 4 - нефть
зациями, институтами и фирмами на H-й Международный Энергетический Симпозиум, проходивший в 1983 г. в г. Вене (Австрия), В соответствии с этим обобщением потребление первичной энергии во всем мире вырастет с 9,91 млрд, т условного топлива в 1980 г. до 18,65 млрд, т условного топлива в 2010 г. (т. е. на 88%). Примерно такими же темпами (рис. 1.2) будет расти потребление угля (на 84%), менее интенсивно будет увеличиваться потребление газа (на 63% за 30 лет) и нефти (на 43%). И тем не менее даже в 2010 г. на долю угля, нефти и природного газа будет приходиться почти 3/4 (точнее 74,7%) суммарного потребления первичных ресурсов. Конечно, в 1980 г. доля этих энергоносителей была выше (88%), однако с точки зрения защиты атмосферы имеет значение абсолютное количество сжигаемого топлива. Поэтому учитывать нужно такие цифры: в 1980 г. в мире было сожжено 8,73 млрд, т условного топлива, а в 2010 г. ожидается потребление угля, нефти и природного газа в количестве 13,93 млрд, т условного топлива, т. е. в 1,6 раза больше.
НОРМИРОВАНИЕ УДЕЛЬНЫХ ВЫБРОСОВ И КОНЦЕНТРАЦИИ ОКСИДОВ АЗОТА В АТМОСФЕРЕ
Интенсивное развитие промышленности, рост количества автомобилей и концентрация энергетических мощностей заставляют все развитые в промышленном отношении страны принимать меры к ограничению выбросов в атмосферу вредных примесей и, в частности, оксидов азота. В конце 60-х и в начале 70-х годов Конгресс США, парламенты Японии, ФРГ и некоторых других стран приняли законы, призванные оградить атмосферный воздух от чрезмерного загрязнения.
(1.6:
Основным критерием санитарно-гигиенической оценки качества воздуха является концентрация в нем того или иного загрязнителя. На основании исследований, о которых шла речь в § 1.3, были установлены ПДКмо2 — предельно допустимые концентрации диоксида азота в атмосферном воздухе. Различают среднегодовую, среднемесячную, среднесуточную, часовую и максимально разовую (отобранную в течение 20 мин) концентрации диоксида азота.
В США, в соответствии с принятым в 1971 г. Законом о Чистом Воздухе, была установлена среднегодовая ПДКш)2 = 100 мкг/м3 как для первичных (призванных защитить здоровье населения), так и для вторичных (призванных защитить благосостояние населения путем умень-' шения вредного воздействия загрязнителей на растительный и животный мир, на строительные сооружения и т. д.) стандартов. В Канаде и Италии лимитируется среднесуточная ПДКмо2 (460 и 200 мкг/м3, соответственно). В некоторых странах установлено несколько ПДК с разным периодом осреднения пробы. Так, например, в Чехословакии среднесуточная ПДКко2 составляет 100 мкг/м3, а максимально разовая — 300 мкг/м3. В ФРГ, начиная с 1981 г., действуют ПДКмо2 80 и 300 мкг/м3 при длительном и кратковременном воздействиях. Весьма жесткие ПДКм О 2 были установлены в 1981 г. в Японии: среднегодовая 41-62 и среднесуточная 83—123 мкг/м3.
В СССР среднесуточная и максимально разовая ПДКмо2 равны, соответственно, 40 и 85 мкг/м3 [7]. Кроме того, в СССР установлено правило суммации вредного воздействия оксидов азота и сернистого ангидрида, в связи с чем сумма относительных концентраций NO2 и SO2 не должна быть больше 1, т. е.
cno2 + CSO2
ПДКМО2 пЛк8О2
Это правило приводит к тому, что принятое у нас санитарное законодательство в отношении загрязнения атмосферы продуктами сгорания является более жестким, чем в других промышленно развитых странах.
В последние годы все большее число специалистов приходит к выво ду, что соблюдение ПДК, установленных на основе санитарно-гигиениче ских соображений, еще не исключает вредного воздействия оксидов азо та на природу. Так, например, проблема кислотных дождей, о которо! шла речь в § 1.3, существует независимо от соблюдения норм ПДК по сернистому ангидриду и оксидам азота и связана с массой выбрасываемых в атмосферу SO2 и NOX, которые переносятся на большие расстояния. Кроме того, в некоторых промышленных центрах сложилась такая ситуация, когда концентрация оксидов азота (или других загрязнителей) была близка к норме ПДК и вследствие этого запрещалось сооружение любых новых ТЭС или других предприятий, выбрасывающих в атмосферу даже незначительное количество NO2. Между тем ранее построенные ТЭС могли не заботиться об ограничении своих выбросов.
Все это потребовало наряду с существующей системой ПДК разработки и введения в законодательном порядке системы ограничения абсолютных выбросов, или удельных выбросов оксидов азота (на единицу тепловой или электрической энергии). В 70-80-х годах в США, Японии, ФРГ и в некоторых других промышленно развитых странах в дополнение к санитарно-гигиеническим нормам (ПДК) были введены нормы ПДВ - предельно допустимых выбросов, которые позволили не только более эффективно бороться с увеличением абсолютных выбросов, но и более четко оценивать ответственность каждого предприятия за загрязнение атмосферы.
В течение последнего десятилетия нормы ПДВ неоднократно пересматривались (в сторону ужесточения) и все более дифференцировались по видам топлива, а иногда — и по мощности котельных установок. В табл. 1.3—1,5 приведены нормы ПДВ по оксидам азота, действующие
Таблица 1.3. Нормы ПДВ^п для новых котлов США тепловой мощностью более 73 МВт [14] 2
Топливо |
ПДВко2*. г/м3, при 2 73, 15 К и 101,3 кПа |
Содержание кислорода в пробе газа, % |
Твердое топливо: |
|
|
битуминозный уголь |
0,73 |
6 |
полубитуминозный уголь |
0,61 |
6 |
лигнит |
0,37 |
6 |
Мазут |
0,45 |
3 |
Природный газ |
0,29 |
3 |
* Усредненное значение за 30 дней.
Таблица 1.4. Нормы ПДВ^д^ для новых котлов в Японии [14]
Топлива |
Расход дымовых газов, тыс. м3/ч |
ПДВно2, г/м3• ПРИ 273,15 К и 101,3 кПа |
Содержание кислорода в пробе газа, % |
Твердое |
>700 |
0,41* |
6 |
|
40-700 |
0,51* |
|
|
<40 |
0,72 |
|
Жидкое |
>500 |
0,28 |
3 |
|
10-500 |
0,325 |
|
|
<10 |
0,39 |
|
Газообразное |
>500 |
0,14 |
3 |
|
40-500 |
0,23 ' |
|
|
10-40 |
0,30 - , . - |
|
|
<10 |
0,345 1 ' |
& 1- |
_ ДДо 31.03.87 |
г. допускалось 0,615 г/м3. |
|
|
|
НОВЫХ |
действующих |
НОВЫХ |
действующих |
Уголь: в топках с твер- |
0,80 |
1,30 |
0,2/0,4 |
0,2/0,65 |
дым шлакоуда- лением в топках с жид- |
1,80 |
2,0 |
0,2/0,4 |
0,2/1,30 |
ким шлакоуда- лением Мазут |
0,45 |
0,70 |
0,15/0,30 |
0,15/0,45 |
Газ |
0,35 |
0,50 . |
0,10/0,20 |
0,10/0,35 |
Таблица
1.5.
Нормы ПДВ^о2
для новых и действующих котлов ФРГ [
14]
Топливо
Федеральные
нормы Минимально возможные (по тех-
ПДВ,
г/м3,
для котлов ническим условиям) * нормы
ПДВ,
г/м3,
для котлов
*
Минимально возможные нормы ПДВ были
приняты 5 апреля 1984 г. на конференции
министров земель ФРГ по охране окружающей
среды. В числителе - ПДВ для котлов
тепловой мощностью 300 МВт и выше, в
знаменателе - для котлов мощностью
менее 300 МВт. Эти цифры относятся к
действующим котлам с остаточным ресурсом
более 30 тыс. ч, а при меньшем ресурсе
нормы ПДВ для крупных котлов такие же,
как и для малых.
в США, Японии и ФРГ. В настоящее время в этих странах ведутся интенсивные дискуссии, в результате которых, вероятно, нормы ПДВ будут снова пересмотрены в сторону ужесточения.
В СССР отсутствуют общесоюзные нормы ПДВ, но для каждой ТЭС в соответствии с ГОСТ 17.2.3.02-78 устанавливаются свои ПДВ как по оксидам азота, так и по другим загрязнителям. Это связано с тем, что мероприятия по сокращению выбросов оксидов азота требуют усложнения конструкции горелок или топочных устройств, а в некоторых случаях - установки дополнительного оборудования. Большинство этих мероприятий повышает эксплуатационные расходы или снижает КПД котлов (если они внедряются на уже действующих котлах).
Вместе с тем допустимые выбросы оксидов азота могут быть очень жесткими в крупных городах, где имеется интенсивное автомобильное движение, аналогичные выбросы химических предприятий или часто наблюдаются неблагоприятные метеорологические условия, и менее жесткими для ТЭС, расположенных на равнинной местности вдали от городов.
Глава вторая
ОБРАЗОВАНИЕ ОКСИДОВ АЗОТА ПРИ ГОРЕНИИ ОРГАНИЧЕСКИХ ТОПЛИВ
ОБЩИЕ СВЕДЕНИЯ
Присутствие оксидов азота в продуктах сгорания органического топлива было обнаружено еще в прошлом веке, но только в конце 50-х годов нашего столетия в связи с опасностью образования смога в городах с высокой концентрацией промышленности и автомобильного транспорта были начаты систематические исследования физико- химических процессов генерации NOX в топочных устройствах котлов, в двигателях внутреннего сгорания и в печах различных нагревательных устройств..
Источником оксидов азота может быть молекулярный азот воздуха, используемого в качестве окислителя при горении, или азотсодержащие компоненты топлива. В связи с этим принято делить оксиды азота на воздушные и топливные. Воздушные, в свою очередь, можно разделить на термические, образующиеся при высоких температурах за счет окисления молекулярного азота атомарным кислородом (механизм Зельдовича) , и так называемые ’’быстрые” оксиды азота, образующиеся в зоне сравнительно низких температур в результате реакции углеводородных , радикалов с молекулой азота и последующего взаимодействия атомарного азота с гидроксилом ОН.
Относительная роль трех источников образования NOX зависит от температурного уровня в зоне горения, от содержания связанного азота в топливе, а также от некоторых параметров топочного процесса, влияние которых будет рассмотрено ниже. Понятно, что при сжигании, например, природного газа, не содержащего связанного азота, не приходится говорить о топливных оксидах азота. С другой стороны, при факельном сжигании высоковлажных бурых углей в топках с твердым шлакоудалением, когда температура процесса не превышает 1500— 1600 К, интенсивность образования термических оксидов азота настолько мала, что ими можно пренебречь.
Попадая в атмосферный воздух, все оксиды азота, независимо от их происхождения, представляют одинаковую опасность. Однако для разработки стратегии борьбы с их образованием необходимо подробно рассмотреть физико-химические основы процессов образования каждой из перечисленных выше категорий NO*.
; ---с
ТЕРМИЧЕСКИЕ ОКСИДЫ АЗОТА
17
2 - 6252
новками.
Однако несколько десятилетий назад
стимулом для проведения исследований
в этой области явилась потребность
народного хозяйства в связанном
азоте. В те годы советскими учеными Я.
Б. Зельдовичем, П. Н. Садовниковым и
Д. А. Франк-Каменецким была выполнена
ставшая классической работа [17], в
которой авторы показали термическую
природу реакции окисления молекулярного
азота и по предложению Н. Н. Семенова
исследовали цепной механизм реакции
образования оксида азота, в котором
решающая роль отводится атомарному
кислороду:
О2
+ 20 + М - инициирование;
N2
+O^=NO + N
n
+ o2^no
+ o
Рис.
2.1.
Максимальное время пребывания продуктов
сгорания в топке в функции теплонапряжения
qy:
1
-
каменный уголь, топки с ЖШУ; 2 - то же,
топки с ТШУ; 3
-
бурый уголь, топки с ЖШУ; 4
- то же, топки с ТШУ; 5 - мазут; 6
-
природный газ
.
— цепь;
О
+ О + М-^О2
+ М - обрыв цепи.-
(2.1)
(2.2)
(2.3)
(2.4)
оксида
азота можно рас-
Время
достижения равновесной концентрации
считать по формуле Ю. П. Райзера:
53
750
Т
’
Авторы
изучали реакции окисления азота с
помощью взрывных бомб, в которых
сжигались смеси водорода, оксида
углерода, метана или других горючих с
кислородом и азотом. В ряде опытов в
смеси _ _
добавлялся
оксид азота. Опыты показали, что
количество образующе- Расчет по этому
уравнению показывает, что гося оксида
азота не зависит от кинетики горения,
реакции образования NO происходят
после завершения процесса горения,
когда повышение температуры приводит
к диссоциации молекулярного кислорода:
О2-*^-
О + О.
В
этой же работе было получено
формально-кинетическое уравнение!
скорости обратимой реакции образования
и разложения оксида азота*: I
2,06-10-12
гравн
. ехр
VnT
(2.7)
_ ,
в диапазоне температур
1800-1900
К время достижения равновесных
концентраций NO составляет примерно
23-4 с. В топках котельных установок время
пребывания продуктов сгорания
значительно меньше. На рис. 2.1 приведены
графики, характеризующие зависимость
времени пребывания т от теплового
напряжения топочного объема qv
для котлов, работающих на природном
газе, мазуте, каменных и бурых углях. В
расчетах было принято, что коэффициент
проточности топочных камер равен 1,0,
т. е.
360
000
RT
64
гч м
.
— О2
N2
ехр
180
000
RT
= ——— ехр
dr Vo2
- [NO] 4,
где О2, N2 и NO - мгновенные концентрации избыточного кислорода, азота и оксида азота, моль/л; т — время, с; Т — температура в зоне реаю ции, К; R - газовая постоянная, Дж/(К-моль); энергия активации вы) ражена в джоулях на моль.
Первый член в фигурных скобках представляет собой квадрат равно) весной концентрации оксида азота: '
180 000
2RT
О? ■ No
(NO)paBH = 8 ехр
(2.5)
(2.6)
*
В последующей работе Я.
Б.
Зельдовича [18] энерщя актиаиОШВ
ЭТОМ уравнении
была уточнена.
273
Ит
Т
= L
ВсД'г^
где
Ет
- объем топки, м3;
Вс
- расход топлива, кг/с; Vr
- удельный Побьем продуктов сгорания,
м3/кг;
Г- средняя температура газов в топ- |ке,
К. Если учесть, что qy
= 5се</Кт
и что £ =
Q- /Уг
при а =1,2 для ка- ■менных углей в среднем
равно 2960, для бурых — 2590, для мазута —
■2970 и для природного газа - 2850 кДж/м3,
то формулу (2.8) можно Переписать в виде
I
т= 273£/(7^). (29)
Из
графиков рис. 2.1 видно, что время
пребывания газов в топке достаточно
мало. Если учесть, что термический NO
образуется в основном в узком диапазоне
температур [Гмакс=
(Тмакс
- 60 К)] [19] и время пребывания в этой зоне
еще меньше, то можно сделать вывод, что
при образовании оксида азота в топках
котельных установок не достигаются
Равновесные концентрации и, следовательно,
концентрация NO в дымовых газах
зависит от кинетики химических реакций.
(2.8)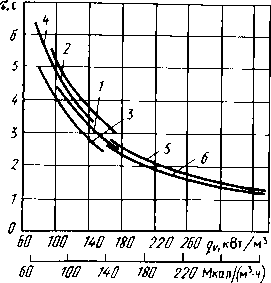
2.3.
БЫСТРЫЕ ОКСИДЫ АЗОТА
Приведенный
выше механизм образования оксида азота
описывает гомогенный процесс, происходящий
в зоне за фронтом пламени, после
завершения процесса горения предварительно
перемешанной горючей смеси с коэффициентом
избытка воздуха а
>
1,0. Ряд исследовании, проведенных в 60-х
годах, подтвердил формальную кинетику
и механизм реакции, предложенный Я.
Б. Зельдовичем. Однако в 1970 г. Фенимор
[20] обнаружил несоответствие термической
теории Зельдовича с тщательно
поставленными экспериментами, в которых
сжигались предварительно перемешанные
смеси этилена, метана и пропана с
кислородом и азотом. В этих опытах
измеренные Фенимором концентрации
NO увеличивались, начиная с определенного
момента времени, в строгом соответствии
с механизмом Зельдовича, однако линейная
экстраполяция зависимости концентрации
NO от времени к началу координат показала,
что во фронте пламени углеводородов
за весьма короткий промежуток времени
образуется оксид азота по механизму,
отличному от предложенного Зельдовичем.
Фенимором
было высказано предположение о наличии
в зоне с большим содержанием горючих
компонентов следующих реакций.
N2
+CH^HCN + N; N + OH^H + NO.
Эти
реакции протекают достаточно энергично
даже при температуре 1600 К, когда
образование термических оксидов азота
практически не происходит. „
Обнаруженный
оксид азота был назван ’’быстрым” в
связи с тем, что скорость его образования
в узкой зоне фронта пламени весьма
велика. Экспериментально наличие
быстрого NO в турбулентном диффузионном
факеле было показано Боумэном [21].
Позднее количественная зависимость
образования быстрых оксидов азота от
некоторых параметров была исследована
И. Я. Сигалом и его сотрудниками [22]. В
институте газа АН УССР ими была
разработана оригинальная установка,
позволившая доказать наличие быстрого
NO без примененного Фенимором метода
экстраполяции (правомерность которого
вызывает сомнения в связи с малостью
концентрации NO и нелинейностью ее роста
в зоне сгоревшего газа). Метод, примененный
в Институте газа АН УССР, основан на
быстром охлаждении продуктов сгорания
и замораживании реакции образования
NO в зоне сгоревшего газа. Горючая смесь
подавалась в изготовленный из кварца
водоохлаждаемый канал конической
формы. Изменяя расход горючей смеси,
авторы добивалиа смещения фронта
воспламенения и находили такое его
положение, когд концентрация N0 в
продуктах сгорания за фронтом пламени
оставалас неизменной. Это позволяло
по результатам одного измерения, бе
экстраполяции к фронту пламени, оценивать
концентрацию быстры см. в приложении.
Рис.
2.2.
Выход оксидов азота во фронте пламени
метана (7), оксида углерода (2) и водорода
(3)
[22]
оксидов
азота. На рис. 2.2 приведены результаты
опытов, проведенных при сжигании
метана, оксида углерода и водорода в
широком диапазоне избытков воздуха.
Приведенные графики показывают, что
при сжигании природного газа в топках
энергетических котлов не
обходимо
считаться с образованием оксидов азота
во фронте пламени. Расчеты, выполненные
сотрудниками ИГ АН УССР, показали, что
для диффузионного пламени природного
газа минимальная концентрация быстрых
оксидов азота составляет примерно 75
мг/м3. '
2.4.
ТОПЛИВНЫЕ ОКСИДЫ АЗОТА
В
конце 60-х годов появился термин
’’топливные” оксиды азота для
обозначения NOX,
образующихся из азотсодержащих
компонентов органической массы
жидких и твердых топлив. В качестве
одной из первых работ, доказавших
наличие еще одного источника оксидов
азота, можно назвать исследование
Томаса и Шоу [23], которые при сжигании
в лабораторной установке оксида углерода
с азотсодержащими добавками
(метилцианид, сек-бутиламин, пиридин)
получали высокую концентрацию NO в
продуктах сгорания (до 1200 см3/м3)*
вне зависимости от того, использовался
ли в качестве окислителя воздух или не
содержащая азота смесь кислорода с
аргоном. Температура горения СО в
опытах Томаса и Шоу была весьма
низкой: 860-1145 К.
Позже
значительная роль топливных оксидов
азота была доказана опытами Ионке в
Аргоннской Национальной Лаборатории
[24], который сжигал природный газ или
твердое топливо в кипящем слое инертного
материала. В первом случае концентрация
оксида азота в продуктах сгорания
не превышала 65 см3
/м3,
а в случае сжигания угля она возрастала
до 650 см3/м3.
Если при сжигании угля вместо воздуха
в качестве окислителя использовали
смесь аргона с кислородом, то концентрация
NO снижалась незначительно (до 580 см3/м3).
В
связи с важностью проблемы топливных
оксидов азота в 70-х годах в СССР и за
рубежом были проведены исследования,
целью кото-
Соотношение
между см3/м3,
г/м3
и другими единицами концентрации NO
20
21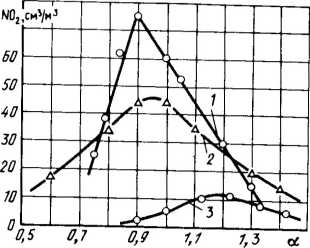
рых было установление основных закономерностей образования оксида азота из азотсодержащих компонентов топлива.
Топливный оксид азота, естественно, будет отсутствовать при сжигании природного газа, однако при сжигании жидкого и твердого топлива нельзя не учитывать наличие азота в топливе. В горючих технических газах концентрация примесей, содержащих связанный азот, может достигать 0,1%. Сжигание таких газов, несомненно, приведет к образованию топливных NO.
Содержание азота в мазуте зависит как от марки нефти, из которой получен мазут, так и от особенностей технологического процесса получения мазута. В большинстве мазутов, поставляемых на электростанции СССР, доля азота составляет 0,25—0,35% массы топлива. Химический состав соединений, в которые входит содержащийся в мазуте азот, изучен еще недостаточно. Считается, что азотистые соединения нефти представляют собой гетероциклические соединения с атомом азота или NH в одном из колец [25]. Азот входит также в состав высокомолекулярных полициклических соединений, содержащих металлы и кислород.
В состав органической массы твердого топлива входят углерод, водород, кислород, азот и сера. В значительно меньших количествах могут присутствовать ванадий, фосфор, германий, галлий, бор и вольфрам. Структура азотсодержащих соединений твердого топлива может быть названа только предположительно, так как все сведения получаются путем анализа продуктов разложения материнских азотсодержащих соединений. Авторы [26] считают, что азотсодержащие соединения в углях состоят на 35% из производных мочевины, аминокислот и пептидов, на 23% — из аминов в виде длинных цепочек, на 10% — из карбо- зольных структур, разлагающихся с выделением азота. При термическом разложении угля вместе с другими летучими выходят смолистые основания (пиридины, хинолины и другие гетероциклические компоненты), аммиак и свободный азот, что составляет примерно половину топливного азота. Соотношение между этими компонентами зависит от состава топлива, скорости его нагрева и температуры. Оставшийся азот входит, вероятно, в более прочные соединения типа нитридов.
С точки зрения образования оксидов азота большое значение имеют закономерности разложения азотсодержащих веществ при быстром нагревании различных топлив. Исследования, проведенные в ВТИ [25] и в Таллинском политехническом институте [27] при сжигании жидкого топлива, убедительно показали, что концентрация топливных оксидов азота в продуктах сгорания зависит не только от содержания азота в топливе, но и от вида азотсодержащих присадок. В первой работе сжигался изопропиловый спирт, во второй — не содержащее азота дизельное топливо. В обоих исследованиях было показано, что при равной присадке азотсодержащих веществ максимальная концентрация NO в продуктах сгорания получается в случае присадки метафенилендиамина (NH2)2C6H4 и значительно меньшая — при использовании в качестве 22
J
 рис.
2.3.
Зависимость выхода летучих и степени
газификации азота от температуры
пиролиза для каменного угля и кокса
1281:
рис.
2.3.
Зависимость выхода летучих и степени
газификации азота от температуры
пиролиза для каменного угля и кокса
1281:
 •
-'битуминозный
уголь месторождения Кентукки; О
-
лигнит;
□
-
битуминозный
уголь месторождения Питсбург; Д
- полукокс
этого угля
•
-'битуминозный
уголь месторождения Кентукки; О
-
лигнит;
□
-
битуминозный
уголь месторождения Питсбург; Д
- полукокс
этого угля
присадки нитробензола, пиридина, азотнокислого никеля и т. д. Было показано также, что при разном количестве азотсодержащих компонентов меняется еще и ход кривых, характеризующих зависимость концентрации оксидов азота от коэффициента избытка воздуха.
Большое значение имеет механизм разложения азотсодержащих компонентов твердого топлива. Известно, что, попадая в топочную камеру, угольная частица нагревается со скоростью 104 —105 К/с. При этом происходит выделение летучих веществ, количество которых определяется степенью метаморфизма угля, а для определенного топлива — температурой термического разложения и скоростью нагрева. Одновременно выделяются азотсодержащие радикалы (амины и цианиды). Опыты, проведенные Першингом и Вендтом [28], показали, что зависимости выхода летучих и газификации азота топлива от температуры пиролиза имеют существенно разный характер. На рис. 2.3 показаны эти зависимости для битуминозного угля с выходом летучих 37% и для полукокса этого угля. Из приведенных графиков видно, что у полукокса выход азотсодержащих компонентов в виде летучих начинается при значительно большей температуре, чем у битуминозного угля, однако при температуре выше 1800 К происходит практически полная газификация азота, содержащегося как в угле, так и в полукоксе. Ход кривых, характеризующих потерю массы проб угля и кокса, по сравнению с кривыми, характеризующими газификацию азота, свидетельствует о том, что при более высоких температурах концентрация азотсодержащих компонентов в летучих будет выше, чем при низких.
Большой интерес представляют опыты, проведенные Блейром [29], при исследовании 20 марок углей и двух марок полукоксов. Эти опыты позволили получить’эмпирическую зависимость массовой доли потерянного азота топлива в зависимости от температуры и выхода летучих на рабочую массу V, %:
0,4861
0,01 Vr
+
3545 exp
1
+ 3545 exp
85
700
RT
85
700
(2.10)

![]()
![]()



Здесь газовая постоянная R = 8,3 Дж/ (моль-К).
В диапазоне температур 800 < Т < 1800 К степень достоверности приведенной формулы а2 = 0,919. Расчеты по этой формуле были выполнены для трех наиболее перспективных углей СССР (кузнецкого Г, ирша- бородинского Б и экибастузского СС). На рис. 2.4 приведены результаты расчетов, из которых следует, что при температуре 1273 К (1000°С) доля азота топлива, перешедшего в газообразное состояние, составляет для экибастузского угля СС - 55, а для кузнецкого Г и ирша-бородин- ского Б — примерно 60%.
Степень газификации азота топлива, безусловно, является одним из важных факторов, влияющих на образование топливных оксидов азота, но не единственным и даже не главным. Дело в том, что в результате газификации азотсодержащих компонентов топлива в факеле появляются не только оксид азота NO, но и радикалы типа аминов (главным образом - NH3) и цианидов (HCN и др.). Это было экспериментально показано в лабораторных опытах американских исследователей (301. которые применили оригинальный метод отбора проб газа из факела: приемное устройство водоохлаждаемого газозаборного зонда было снабжено устройством для впрыска воды. Это не только обеспечивало ’’замораживание” отобранной пробы газа, но и переводило в жидкую фазу цианид водорода и аммиак NH3. Последующий анализ проб влаги позволял рассчитать концентрацию последних в дымовых газах.
Опыты, проведенные при сжигании высокореакционного битуминозного угля {Vdal = 44,5%, Qrs = 19 МДж/кг, = 1,3%), показали, что по мере снижения стехиометрического соотношения в горелке концентрация NO в продуктах сгорания почти линейно снижается, но одновременно возрастает концентрация HCN и NH3 (рис. 2.5). В этих же опытах отбирались пробы уноса из факела. Анализ этих проб показал, что по мере снижения количества воздуха, поданного вместе с топливом, снижается также и доля азота, оставшегося в коксе (с 40% при аг = 1,0 до ; примерно 20% при аг = 0,6). При дальнейшем снижении аг доля азота, Ij оставшегося в твердой фазе, возрастает. Баланс азота топлива показал, >1 что максимальный переход топливного азота в молекулярный азот N2 ( наблюдался при аг =0,6.
Примерно такие же результаты бьши получены в опытах Чена и др. 31], которые в лабораторной установке сжигали угли с разной сте- енью метаморфизма: от антрацита с выходом летучих 4,4% до битуминозного угля и лигнитов, содержащих 30—40% летучих. В отличие от ранее описанных опытов, авторы [31] использовали в качестве окислителя смесь кислорода (21%), аргона (61%) и углекислого газа (18%). ■
Рис.
2.4.
Степень газификации азота топлива в
зависимости от температуры. Расчет по
[28] для кузнецкого газового (7),
ирша-бородинского (2) и экибастузского
(3) углей. Экспериментальные результаты
(точки на рисунке) —
см.
в п. 2.5.2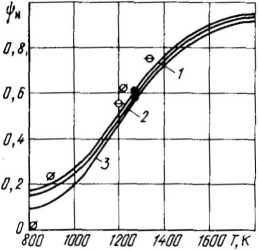
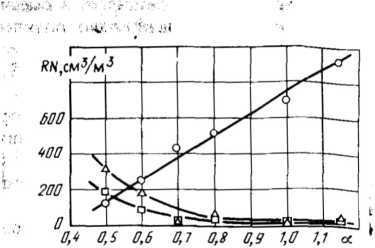
Рис. 2.5. Концентрация азотсодержащих компонентов в продуктах сгорания при различных соотношениях воздух-топливо [30]:
О - NO; A- HCN; □- NH3
Кроме того, установка позволяла часть окислительной смеси подавать не с топливом, а вводить в факел на расстоянии 1,17 м от горелки предварительного смешения. Пробы продуктов сгорания отбирались не только за установкой, но и за первой зоной горения, до ввода вторичного воздуха.
Каждое топливо сжигалось в нескольких опытах, отличавшихся соотношением расходов первичного и вторичного окислителей: общий расход топлива и окислителя во всех опытах оставался постоянным.
Анализ проб газа показал, что за первой зоной горения, как и в [30], уменьшение аг для всех углей, кроме антрацита, снижает концентрацию NO, но увеличивает содержание HCN и NH3. Во второй зоне горения, где концентрация О2 резко возрастает, происходят реакции типа
HCN'+H2O->NH3 + СО; - (2.11)
NH3 + О2 ->NO + H2O+ 1/2Н2, ' (2.12)
что приводит к увеличению содержания оксида азота в продуктах сгорания. Минимальная концентрация NO для различных марок углей была получена в диапазоне аг от 0,5 до 0,7. У антрацита наблюдалось монотонное снижение концентрации NO за установкой в проверенном диапазоне «г (от 1,0 до 0,43).
Заслуживает внимания еще одно исследование, раскрывающее картину перехода топливного азота в оксиды [32]. Опыты проводились на установке, в которой сжигалась пыль битуминозного угля в ламинарном потоке. Содержание азота в топливе (на сухую массу) составляло
25
1,63%. Угольная пыль сжигалась в смеси, содержащей 23,4% кислорода и 76,6% аргона, что исключало появление воздушных N0x. Во всех опытах скорость смеси в выходном сечении горелки оставалась постоянной, а концентрация пыли составляла 285 или 470 г/м3 смеси. В первом случае коэффициент избытка воздуха аг был равен 0,5 (1,25 по отношению к горючим летучим топлива), во втором — аг =0,3 и ап =0,75.
Измерения показали, что при сжигании топлива с аг =0,5 в продуктах сгорания содержится, %на сухую пробу: СО — 3,1; СО2 — 13,8; Н2 - 0,7 и Н2О — 11,1. При сжигании более обогащенной смеси состав продуктов сгорания был иным: СО — 9,5; СО2 — 10,7; Н2 — 2,1% в сухой пробе газа и Н2О — 17,4%. Анализ проб пыли из факела позвол.ш оценить снижение содержания азота в твердой фазе (расчет проводился по балансу золы с учетом того, что изменение количества золы по мере выгорания топлива, связанное с ее испарением, было незначительным). Баланс азота во всех точках по ходу факела был сведен с точностью ± 10%.
Сравнение двух режимов показало, что при сжигании более обогащенной топливом смеси (аг = 0,3) примерно 50% азота топлива переходит в молекулярный азот, 10% — в HCN, 10% — в NO и около 30% остается в твердой фазе. При сжигании смеси с большим количеством окислителя (режим с аг =0,5) в продуктах сгорания за максимумом температур содержалось 20% азота в виде NO, почти 40% - в виде N2 и 40% азота оставалось в твердой фазе. Далее по ходу факела доля азота в твердой фазе снижалась до 5—10%, а содержание N2 возрастало до 60- 65%. В обоих случаях выделение азота из топлива прекращалось при падении температуры факела ниже 1500 К.
В описанных опытах, в отличие от других подобных исследований, были обнаружены только следы NH3. Авторы объясняют это высоким качеством угля и главное — более высоким уровнем температур.
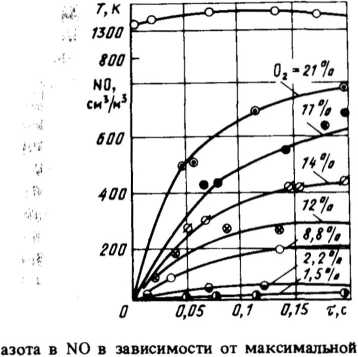
Результаты описанных выше исследований дают представление о механизме образования топливных оксидов азота, но не позволяют сделать количественных оценок образования NOX в зависимости от важнейших параметров топочного процесса и от характеристик сжигаемого угля. Эта задача была в значительной степени решена в работе В. И. Бабия и его сотрудников, выполненной в 1978-1980 гг. в ВТИ им. Ф. Э. Дзержинского [4]. В опытах на лабораторной установке сжигалась пыль различных углей с выходом летучих от 11,7 до 52% и зольностью от 5 до 52%. Содержание азота в топливе Nda^ колебалось от 0,77 до 2,7%. Концентрация кислорода на входе в реакционную камеру менялась в различных опытах от 0 до 21%; максимальная температура в камере Гмакс в различных опытах составляла 950—1800 К. Время пребывания пылегазового потока в реакционной камере составляло 0,2-0,4 с.
В результате проведения сравнительных опытов на воздушном дутье и на смеси, содержащей 79% аргона и 21% кислорода, было установлено, что при горении пыли угля с N^a^= 2,0% и при максимальной темпера- 26
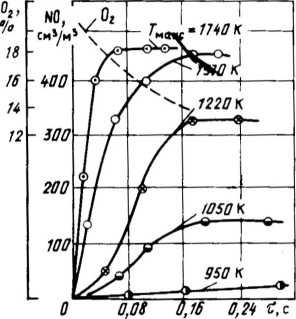 Рис.
2.6.
Зависимость скорости образования
оксидов азота от температуры при горении
экибастузского угля [4]
Рис.
2.6.
Зависимость скорости образования
оксидов азота от температуры при горении
экибастузского угля [4]
гуре факела до Тмакс = 1800 К оксиды азота в основном (на 95%) образуются из азота топлива и только около 5% NOX появляется в результате окисления атмосферного азота. Раздельное измерение концентраций оксида и диоксида азота в продуктах сгорания показало, что NOX на 97— 98% состоят из оксида азота.
Влияние температуры процесса горения на образование NOX исследовалось для ряда углей. На рис. 2.6 показано характерное изменение концентрации NO по ходу факела, выраженное во временных координатах, при различных значениях максимальной температуры. Точки на графике получены в опытах с пылью экибастузского угля на воздушном дутье при коэффициенте избытка воздуха аг ъ 1,0. На рис. 2.6 приведено также изменение концентрации кислорода по ходу факела в опыте с Тмакс = 1740 К.
Изменение концентрации NOX вдоль оси реакционной камеры показало, что образование N0 происходит на начальном участке факела и, достигнув определенной, характерной для условий опыта концентрации (NOK), в дальнейшем по ходу факела не изменяется, несмотря на продолжающееся активное горение угольной пыли и довольно высокие концентрации кислорода в потоке. Часто образование NO прекращается даже раньше, чем температура факела станет максимальной. Все это свидетельствует о том, что образование NO происходит на стадии выгорания летучих, которое в основном завершается на начальном участке факела. При температуре пылегазового потока в камере ниже 7макс = = 950 К, когда летучие не воспламенялись, образование NO происходило в незначительном количестве.
С повышением степени метаморфизма каменных углей и снижением выхода летучих с 37 до 11% при прочих равных условиях в опытах наблюдалось замедление скорости образования NO в факеле, хотя это не оказывало влияния па конечный выход оксидов азота NOK.
Изображенный на рис. 2.6 ход кривых на первый взгляд противоречит существующему у некоторых специалистов мнению о том, что за интенсивным образованием топливных оксидов азота в начале факела имеется участок, на котором содержание NO уменьшается, и только после этого кривая стабилизируется на уровне концентрации NOK. При этом ссыла
ются, как правило, на экспериментальные результаты, полученные при сжигании мазута [34] или дизельного топлива с присадкой нитробензола или пиридина [27]. Этому противоречию можно дать следующее объяснение. В опытах Бабия и Титова [4] концентрация кислорода была достаточно высокой, и в реакционной камере не образовывались продукты неполного сгорания. А в опытах сотрудников САФ ВНИИПромгаз [34] на начальном участке камеры сгорания образовывались газы — восстановители СО и Н2, причем участку факела, на котором наблюдалось снижение концентрации NO, соответствует уменьшение содержания этих газов. Вероятно, в этой зоне происходили реакции восстановления NO до молекулярного азота, что возможно при образовании не только топливных, но и термических оксидов азота. В опытах на чистом дизельном топливе, не содержащем связанного азота [27], также наблюдался участок факела со снижением концентрации NO, хотя и не такой значительный, как в случае использования азотсодержащих присадок, повышающих общий уровень концентрации оксидов азота.
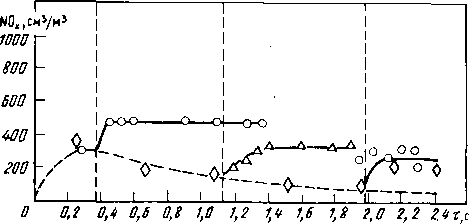
Из результатов зарубежных исследований можно сослаться на опыты Брауна и др. [35], которые сжигали подготовленную топливовоздушную смесь в туннельной лабораторной топке. Результаты их опытов, приведенные на рис. 2.7, показывают, что после участка, соответствующего моменту времени 0,3 с, наблюдалось снижение концентрации оксидов азота, если не добавлялся вторичный воздух. Однако в этих опытах вместе с топливом подавалось только 40% теоретически необходимого количества воздуха, что, по всей видимости, приводило к образованию продуктов неполного сгорания.
Влияние температуры факела на конечный выход оксидов азота при горении пыли различных углей в потоке воздуха (аг = 0,984-1,2) иллюстрирует график на рис. 2.8. На этом графике можно выделить две области: при низких температурах факела (Т’макс =9004-1350 К) наблюдается быстрое увеличение доли перехода топливного азота в оксиды,
Рис.
2.7.
Изменение концентрации оксидов азота
по длине камеры при ступенчатом сжигании
в зависимости от места ввода добавочного
воздуха [35 ]:
О
- только первичный воздух (а = 0,4); о, Д-
ввод вторичного воздуха в разных
сечениях

однако в области Гмакс > 1400 К влияние температуры на NOK/NOMaKC сказывается гораздо слабее. Здесь NOMaKC — предельная концентрация топливных оксидов в потоке при условии, что весь азот топлива перешел в NO.
Результаты японских ученых [36], которые сжигали различные каменные угли в лабораторной установке, состоящей из двух последовательно расположенных камер, позволили оценить влияние температуры на процесс образования топливных оксидов азота отдельно для стадии горения летучих и стадии горения коксового остатка. Оказалось, что при подаче вместе с топливом только 41% теоретически необходимого количества воздуха (при сжигании каменного угля с выходом летучих 42,6%) увеличение температуры в первой реакционной камере с 1373 до 1773 К снижает концентрацию оксидов азота с 0,28 до 0,14 г/м3. Если же сохранять постоянной температуру первой камеры (1620 К) и повышать температуру во второй камере, куда подается еще 75% теоретически необходимого количества воздуха, то концентрация NO, наоборот, увеличивается с 0,16 до 0,27 г/м3 (в том же температурном интервале: 1373—1773 К). Вероятно, аномальную на первый взгляд зависимость содержания NO от температуры в первичной зоне можно объяснить тем, что рост Т в условиях недостатка окислителя (коэффициент подачи воздуха по отношению к летучим ал < 1,0) увеличивает образование продуктов неполного сгорания, которые частично восстанавливают образовавшиеся оксиды азота.
Оценивая влияние температуры на образование оксидов азота, необходимо учитывать, что при горении угольных частиц их температура значительно превышает температуру окружающих газов. Опыты, проведенные В. И. Бабием и его сотрудниками [37] с частицами углей различных марок, позволили установить зависимость превышения температуры горящих угольных частиц над температурой окружающего газа с учетом размера частиц, температуры среды и концентрации в ней кислорода:
Д 7’= 0,068(1900 - 7’г)°’745-°’16[О2], (2.13)
где Тт — 'температура газовой среды, К; S — размер угольной частицы, м; [О2 ] — объемная концентрация кислорода, %.
Из этой формулы следует, например, что при температуре газовой среды 1600 К горящая частица пыли размером 500 мкм при концентрации кислорода 10% будет иметь температуру, превышающую окружающую среду примерно на 150 К, а при [О2] = 21% уже на 330 К. И если для температуры 1600 К, исходя из формально-кинетического уравнения Зельдовича, можно уверенно говорить о практическом отсутствии термических оксидов азота, то при температуре 1750 К (и тем более 1930 К) необходимо учитывать образование оксидов азота из изота воздуха. При уменьшении размера частиц, так же как и при снижении температуры окружающей среды, значение ДТ еще больше увеличивается.
Рис.
2.8.
Доля перехода топливного

температуры пылегаэового потока:
1 (-О-) - экибастузский уголь; 2(-®~) - ишидейский уголь; 3(-ф~) — ирша-бородинский уголь
Рис. 2.9. Образование NO в зависимости от начальной концентрации кислорода в потоке пылевзвеси при сжигании кузнецкого угля марки 2СС [4]:
О - температура, остальные обозначения - NO при разных концентрациях кислорода
В исследовании, выполненном в ВТИ им. Дзержинского [4], была проведена серия опытов с изменением концентрации кислорода в газовом потоке на входе в камеру при неизменных прочих условиях. Результаты этих опытов с пылью кузнецкого угля марки 2СС представлены на рис. 2.9. Из графика видно, что уменьшение концентрации кислорода в аэросмеси с 21 до 1,5% приводит к резкому снижению скорости образования и уменьшению конечного выхода NOK. Обработка полученных данных показала, что при заданной температуре пылегазового потока (1780—1800 К) конечная концентрация NOK зависит от среднеинтегральной концентрации кислорода на участке образования оксидов азота в факеле примерно в степени 2. Следует отметить, что в этих опытах концентрация кислорода на входе в камеру снижалась за счет присадки СО2, но коэффициент подачи воздуха а оставался примерно одинаковым («г = 0,984-1,02).
Японские специалисты [36], используя возможности своей установки, показали, что зависимость образования оксидов азота от количества воздуха, подаваемого вместе с топливом, имеет сложный характер. На рис. 2.10 по данным [361 построен график изменения концентрации NOX при изменении коэффициента подачи воздуха в первую камеру. В тех опытах, когда значение аг было меньше 1,0, во вторую камеру подавал- 30
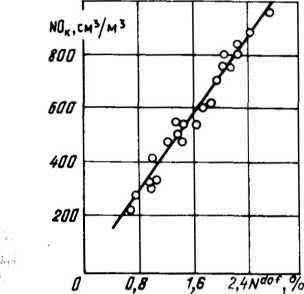
Рис.
2.11.
Зависимость концентрации оксидов азота
в продуктах сгорания от содержания
азота в горючей массе угля
Рис.
2.10.
Зависимость NOX
от коэффициента подачи первичного
воздуха при сжигании японского
каменного угля [36]:
О
- фракция
угольной пыли от 57 до 74 мкм; • - фракция
меньше 37 мкм![]()
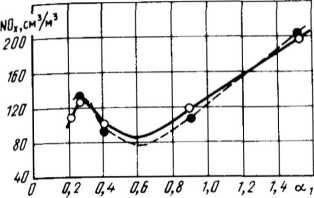
ся воздух, необходимый для полного сгорания топлива. Сжигался японский каменный уголь, содержащий 1,09% азота и 10,1% золы на сухую массу. Выход летучих составлял 42,6%, а температура в первой камере поддерживалась на уровне 1620 К.
Из приведенного графика видно, что вне зависимости от фракционного состава пыли имеется минимум концентрации NOX, соответствующий а, =0,6. Затем, при снижении с 0,41 до 0,26 концентрация NOX за установкой увеличивается примерно на 30% (в данном случае — со 100 до 130 см3/м3 в пересчете на пробу газа, содержащую 3% кислорода). Этот рост концентрации NOX объясняется, безусловно, доокисле- нием большого количества промежуточных азотистых радикалов (цианидов и аминов) после ввода дополнительного воздуха во вторую камеру. При дальнейшем снижении at до 0,2 концентрация NO* снова уменьшается. Вероятно, увеличение времени пребывания продуктов сгорания в первой камере приводит к тому, что часть азотистых радикалов успевает прореагировать до молекулярного азота, который уже не разрушается во второй ступени.
Такое предположение основано на результатах другой серии опытов, 0 которых на той же установке в широких пределах менялось время пребывания продуктов горения в первой камере (при этом коэффициент подачи воздуха ах и температура оставались постоянными, равными соответственно 0,41 и 1620 К). По мере увеличения т от 0,15 до 0,2 и 0,5 с концентрация оксидов азота за установкой снижалась со 100 до 88 и 75 см3/м3. Увеличение времени пребывания продуктов сгорания в первой камере до 9 с привело к снижению концентрации NOX до
38 см3/м3. Эти цифры удовлетворительно согласуются с результатами опытов Брауна и Мейсона, приведенными на рис. 2.7.
Для выяснения взаимосвязи между содержанием азота в угле и концентрацией оксидов азота в продуктах сгорания в ВТИ им. Ф. Э. Дзержинского были проведены опыты с пылью каменных и бурых углей различных марок и месторождений, содержание азота в которых составляло от 0,77 до 2,7% [33]. Максимальная температура газов в камере при этом поддерживалась на уровне Тмакс = 1650^-1720 К, что практически исключало образование термических NOX.
Результаты исследований представлены на рис. 2.11. Г рафик свидетельствует о линейной зависимости между содержанием азота в топливе и выходом оксидов азота в проведенных опытах.
В исследованиях зарубежных ученых также отмечается прямая зависимость количества образующихся при горении оксидов азота от содержания азота в исходном топливе, однако эта зависимость обычно получается не столь однозначной. Так, например, в упоминавшейся уже работе американских исследователей [31] при сжигании 21 марки углей' (от антрацита до высоковлажного лигнита) также наблюдалось увеличение концентрации оксидов азота в продуктах сгорания за туннельной топкой по мере роста содержания азота в топливе от 0,8 до 1,9%. Однако экспериментальные результаты имеют значительный разброс, если их аппроксимировать линейной зависимостью. Вероятно, в этих опытах сказывались разные условия воспламенения при сжигании углей различного качества.
Японские исследователи, проводившие опыты [36] с шестью марками высококачественных битуминозных углей, пришли к выводу, что концентрация оксидов азота в продуктах сгорания определяется не только содержанием азота в исходном топливе, но и так называемым ’’топливным коэффициентом”, который является отношением связанного в топливе углерода СсвI к выходу летучих на рабочую массу Vr. Однако результаты большого числа опытов из [31], нанесенные на график зависимости NOX от ’’топливного коэффициента”, не подтвер дили мнение японских специалистов, основанное на опытах с использо ванием только битуминозных углей с узким диапазоном изменения Ссв Vr.
На лабораторной установке ВТИ в сопоставимых условиях (одинако вые температуры, концентрации кислорода и т. д.) были проведень опыты с различными углями, зольность которых Ad изменялась от f до 52%. Эти опыты показали, что минеральные примеси, содержащиеся в топливе, не оказывают заметного влияния на относительный выхо;
оксидов азота NOK/NOMaKC. Следует, однако, отметить, что в пылеугольном факеле котла влияние изменения зольности топлива может проявиться косвенно, вследствие изменения условий воспламенения и других параметров топочного процесса, которые могут в конечном ЙТОге существенно повлиять на выход оксидов азота.
В [4] было исследовано влияние фракционного состава пыли на образование топливных оксидов азота. Остаток на сите с размером ячеек 90 мкм менялся от 2 до 80%. Опыты показали, что при прочих равных условиях фракционный состав пыли не влияет на образование оксидов азота.
Практически к такому же выводу пришли японские исследователи в опытах сжигания каменных углей в лабораторной установке с двумя камерами сгорания [36]. На рис. 2.10 показано, что во всем диапазоне проверенных избытков воздуха образование оксидов азота было почти одинаковым как для сравнительно крупной пыли (от 56 до 74 мкм), так и для мелкой пыли (с размером пылинок менее 37 мкм).
2.5. ОБРАЗОВАНИЕ ОКСИДОВ АЗОТА
ПРИ ФАКЕЛЬНОМ СЖИГАНИИ ТОПЛИВА
Особенности факельного сжигания
В работах, результаты которых описаны в предыдущих разделах, использовалась, как правило, поточная методика исследования, когда топливовоздушная смесь поступала через торец трубчатого реактора или туннельной топочной камеры. При этом основные параметры процесса изменялись только по направлению движения топливовоздушной смеси. В реальных топочных устройствах котлов или других топливоиспользующих установок, как известно, процесс сжигания топлива организован иначе. В крупной энергетике, например, основным является факельное сжигание, когда в топочную камеру через горелки подаются прямоточные или закрученные потоки воздуха и топлива или топливовоздушной смеси (а иногда — еще и газы рециркуляции). Реже применяется циклонный (вихревой) метод сжигания, когда часть топлива сгорает на пленке шлака, покрывающей поверхность циклона. В последние годы много внимания уделяется методу сжигания твердого топлива в кипящем (псевдоожиженном) слое инертного материала. В коммунально-бытовом секторе и в мелких промышленных котельных еще используются слоевые топки для сжигания твердого топлива, производственных отходов и мусора.
При факельном сжигании газообразного топлива возможны чисто кинетический режим (когда топливо до поступления в топочную камеру тщательно перемешивают со всем воздухом, необходимым для полного сгорания топлива) или чисто диффузионный режим (когд? топливо и воздух вводят в топку в виде отдельных струй). Образ 3 - 62 52
 Рис.
2.12.
Концентрация NO в зависимости от избытка
воздуха для заглубленного (У) и выдвинутого
на срез горелки (2) положений газового
сопла [38]
Рис.
2.12.
Концентрация NO в зависимости от избытка
воздуха для заглубленного (У) и выдвинутого
на срез горелки (2) положений газового
сопла [38]
вание оксидов азота происходит по-разному в диффузионном и кинетическом режимах. На огневом стенде при сжигании природного газа была использована горелка с подвижным газовым соплом [38]. В опытах с предварительным смешением топлива с воздухом концентрация NO увеличивалась от 75 до 150 см3 /м3 по мере увеличения коэффициента избытка воздуха от 1,10 до 1,24 (рис. 2.12). После того как газовое сопло было выдвинуто на срез горелки и процесс смешения топлива с воздухом был перенесен в камеру горения, концентрация NO в продуктах сгорания существенно снизилась. И только при очень больших избытках воздуха (аг > 1,4) диффузионный режим горения давал большую концентрацию оксидов азота, чем кинетический.
В энергетических котлах газовые горелки обычно устроены так, что только часть воздуха смешивается с топливом до поступления в топоч- кую камеру. В этом случае скорость процесса горения на разных этапах развития факела определяется или кинетикой процесса, или скоростью диффузии окислителя (кислорода воздуха) к фронту пламени. Соответственно и ход кривых NO(ar) получается различным при разном конструктивном выполнении горелки. Чем лучше перемешивается топливо с воздухом, тем выше пик температур, выше концентрация оксидов азота, и при меньших аг наступает экстремальное значение NOX. При вялом смешении образуется растянутый факел с более удаленным от горелки и меньшим экстремальным значением NOX. Об этом, в частности, свидетельствуют опыты сотрудников САФ ВНИИПромгаз, проведенные при сжигании газа на котлах с разной конструкцией горелок [34].
При сжигании жидкого топлива смешение воздуха с топливом происходит в объеме факела. Жидкое топливо (в крупной энергетике это, как правило, мазут) распиливается с помощью водяного пара, сжатого воздуха или под действием потенциальной энергии топливной струй (механическое распиливание).
Как правило, для сжигания жидкого и газообразного топлива используют вихревые горелки, в которых весь воздух или его часть закручивается с помощью лопаточного аппарата или за счет улиточного подвода воздуха к горелке. Однако во многих странах успешно рабо-
тают газомазутные котлы с тангенциальным расположением прямоточных горелок. В ВТИ им. Дзержинского были разработаны встречноударные прямоточные горелки, которые обеспечили эффективное сжигание мазута в крупных энергетических котлах [39].
При факельном сжигании твердого топлива конструкции горелок чрезвычайно разнообразны, так как диапазон изменения характеристик углей очень велик. Например, выход летучих, в значительной степени определяющий реакционные качества топлива, меняется от 2% у метаантрацита до 92% у эстонского сланца. Тем не менее практически всеII пылеугольные горелки имеют поток первичного воздуха, который смешивается с топливом до поступления в топку, и поток вторичного воздуха, который смешивается с аэросмесью после выхода из горелки. Выделение первичного воздуха необходимо для улучшения теплового баланса зоны воспламенения, однако такое решение имеет и отрицательные последствия: повышение степени выгорания топлива достигается только за счет специальных мер для организации вторичного смесеобразования в факеле и увеличения коэффициента избытка воздуха в горелке с^.
Прогрев поступающей в топку смеси угольной пыли с первичным воздухом (аэросмеси) происходит за счет конвекции и лучистого теплообмена. Большинство специалистов считает, что роль конвекции, осуществляемой за счет подмешивания к аэросмеси горячих газов из зоны развитого горения, является определяющей, по крайней мере для вихревых горелок. Прогрев аэросмеси приводит к выходу летучих и их воспламенению. При сгорании летучих расходуется главным образом кислород, содержащийся в первичном воздухе. Горение летучих ускоряет прогрев коксовых частиц и их воспламенение. Горение коксовых частиц происходит в основном за счет кислорода вторичного воздуха.
Изложенная схема развития пылеугольного факела является, безусловно, весьма упрощенной, так как в реальных котлах сжигается полидисперсная пыль. Вследствие этого выход летучих и горение коксового остатка протекают последовательно только для каждой отдельной частицы. А для всего факела эти процессы протекают параллельно, так как мелкие частицы (с размером в несколько микрометров) прогреваются, воспламеняются и сгорают значительно быстрее, чем крупные частицы, имеющие максимальный размер в сотни (каменные угли) и даже тысячи микрометров (бурые угли, сланцы и торф). Подробные сведения об интенсивности протекания различных этапов процесса горения угольных частиц разных размеров приведены в [37].
Учитывая особую важность борьбы с оксидами азота при сжигании твердого топлива, рассмотрим особенности их образования в прямоточном и вихревом факелах пылеугольных котлов.
- 2.5.2. Образование оксидов азота в факеле прямоточных горелок
В прямоточном факеле подмешивание высокотемпературных топочных газов к топливовоздушной струе происходит за счет эжектирую- щих свойств вдуваемой в топку горелочной струи. Для тангенциальных топочных камер можно говорить еще и о ’’принудительном” подводе горячих топочных газов к корню факела в результате вихревой аэродинамической структуры.
По мере выгорания летучих концентрация кислорода в струе аэросмеси быстро уменьшается, так как количество первичного воздуха, как правило, не превышает 20—40% стехиометрического (в расчете на все топливо, поданное через горелки). Вторичный воздух при использовании прямоточных горелок подмешивается к воспламенившейся аэросмеси недостаточно интенсивно (особенно при небольшой поверхности контакта аэросмеси и вторичного воздуха). В результате этого в определенных зонах прямоточного факела создается восстановительная среда с более или менее высокой концентрацией продуктов неполного сгорания: СО, Н2, а иногда и СН4. В дальнейшем по мере смешения с вторичным воздухом происходит почти мгновенное догорание этих компонентов, и при работе топки с нормальным избытком воздуха в уходящих газах наличие оксида углерода можно обнаружить только при помощи очень чувствительных приборов. Но в зоне горения летучих в прямоточном факеле практически все экспериментаторы отмечали присутствие значительного количества газов-восстановителей. В качестве примера сошлемся на результаты газового анализа при зондировании поперечного сечения факела в опытах на реконструированном котле ПК-10Ш Красноярской ТЭЦ-1 [40].
Барабанный котел ПК-10Ш (230 т/ч, 9,8 МПа, 510°С) в заводском исполнении имел шахтно-мельничную топку с четырьмя амбразурами, размещенными по фронту. После реконструкции топочная камера котла с твердым шлакоудалением была оборудована 8 прямоточными горелками, расположенными тангенциально в два яруса по высоте. Продольный разрез котла и выходное сечение прямоточной горелки приведены на рис. 2.13.
Опыты проводились при сжигании ирша-бородинского и березов- ского бурых углей Канско-Ачинского бассейна. Аэросмесь к горелкам поступала от молотковых частиц с температурой $ас =65°C. Вторичный воздух имел температуру £г в = 386° С. Расчетные значения скоростей в горелках составляли 17—20 м/с по аэросмеси и 38—42 м/с по вторичному воздуху (большие цифры относятся к режиму работы на трех мельницах с 90%гной нагрузкой).
Пробы газа отбирались из различных участков факела с помощью водоохлаждаемого газозаборного зонда. Зонд вводился поочередно через лючки А, В и С (рис. 2.14) и перемещался вдоль собственной оси. Благодаря тому, что эти лючки установлены под углом к плоскости
Рис.
2.13.
Реконструированный котел ПК-10111 и
выходное сечение прямоточной горелки
IH
ф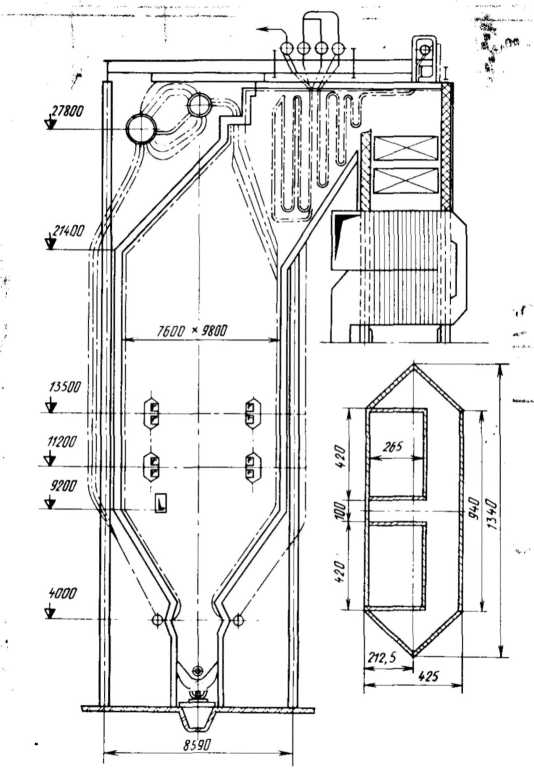


Фронтового экрана, удалось определить поля концентраций NOX в трех сечениях, перпендикулярных геометрической оси горелки и отстоящих от выходного сечения на расстоянии 450, 1500 и 2780 мм (1; 3,5 и 6,5 калибров). Во всех сечениях факела, кроме отбора проб газа, измерялась температура, а также отбирались пробы недогоревшей пыли из факела для анализа ее химического состава.
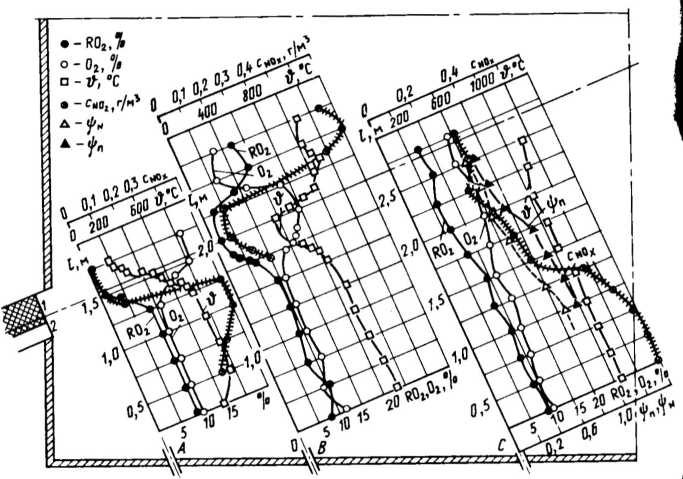
Рис. 2.14. Поля газового состава, степени выгорания топлива и температуры i? в поперечных сечениях факела при сжигании ирша-бородинского угля
Основываясь на балансе азота топлива и полагая, что количество золы на пути факела от горелки до исследуемого сечения остается неизменным, можем получить следующее выражение для подсчета степени газификации азота топлива:
Дт/ Kidaf г .г
, _ _ . __пр_ 1 Ун Л
N nhcx 100-Гун юо- Ar~Wr ' '
где и содержания азота на горючую массу в отобранной из факела пробе и в исходном топливе; Гун — содержание горючих в пробе из факела.
Из 1 кг азота топлива при полной его газификации должно получиться 46/14 = 3,28 кг NO2. Если бы весь азот, перешедший в газообразное состояние, превращался в оксиды азота, то на каждый килограмм сожженного топлива мы получали бы массу оксидов азота (в пересчете на NOj)
Nr
GNO2=3,28^N—(2.15)
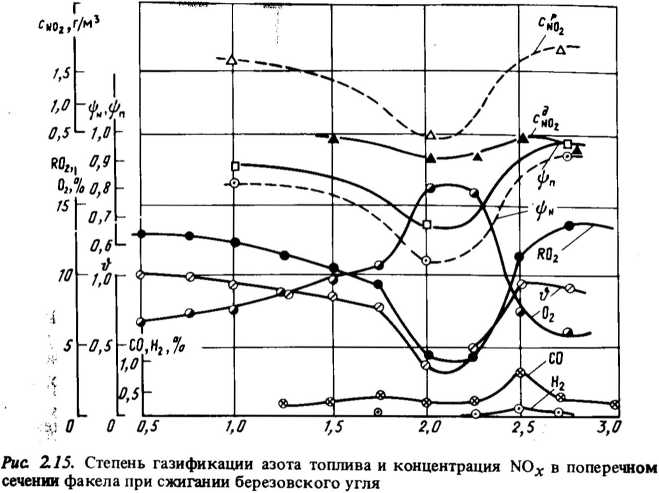
а на каждый кубический метр дымовых газов, приведенных к условиям Г = 273,15 К и р= 101,3 кПа
i//NNr
cNOj = 32,8—р—, (2.16)
где cN0 — концентрация оксидов азота в пересчете на диоксид NO2, г/м3, а Уг — объем дымовых газов при избытке воздуха в том месте, где отобрана проба пыли, имеющая степень газификации азота топлива i//N. Локальный коэффициент избытка воздуха определялся по ’’азотной” формуле
я N2 - 3,76 (О2 - 0,5СО- 0,5 Н2) v '
На рис. 2.14 и 2.15 приведены результаты зондирования факела при сжигании ирша-бородинского и березовского угля. Из рис. 2.15 видно, что при сжигании березовского бурого угля на расстоянии 1,5 м от выходного сечения горелки на наружной стороне горелочной струи (на расстоянии примерно 2,5 м от бокового экрана) концентрация оксида углерода составляла 0,8, а водорода - 0,2%. Температура в этой зоне достигала 1100°С, поэтому весьма вероятны восстановительные
![]() реакции:
реакции:
2N0 + 2СО->2СО2 + N2;
2NO + 2H2 ->2H2O + N2.
О наличии таких реакций говорит также тот факт, что именно в этой зоне разница между расчетной концентрацией оксидов азота c^q2 (подсчитанной при условии, что весь газифицированный азот переходит в NO2) и измеренной (действительной) концентрацией с^О2 максимальна.
На рис. 2.14 приведены результаты опыта при сжигании ирша-боро- динского угля. Коэффициент избытка воздуха в горелке аг = 1,06, а коэффициент подачи первичного воздуха aj =0,32.
Степень газификации топлива в пробах, отобранных на оси горелки, нанесена на график рис. 2.4. Учитывая невысокую точность измерения температуры в опытах на промышленном котле, можно считать удовлетворительным совпадение расчетных и экспериментальных значений. На периферии факела значение оказалось выше расчетного, что объясняется, вероятно, попаданием в отобранные пробы частиц, подсосанных к струе факела из объемов топки с более высокой температурой.
Подробные измерения в поперечных сечениях факела позволили сделать еще ряд выводов:
Уровень температур в прямоточном факеле даже на расстоянии 6,5 калибра от выходного сечения горелки еще настолько низок, что расчет по известному уравнению Зельдовича дает пренебрежимо малые значения концентрации NOX. Следовательно, измеренные оксиды азота можно полностью отнести к топливным NOX, образование которых связано с газификацией азота топлива.
Степень газификации азота топлива, как показали измерения, практически не зависит от концентрации кислорода в топливовоздуш ной смеси (в исследованном диапазоне рециркуляции дымовых газов г = 0-М5%).
Концентрация оксидов азота, рассчитанная по степени газификации азота топлива, т. е. в соответствии с (2.16), во всех сечениях факела оказалась значительно выше измеренной концентрации NOX.
Таким образом, в промышленных условиях было подтверждено, что часть азота топлива, газифицируясь, переходит не в оксиды азота, а в молекулярный азот N2.
