
3 курс / Патологическая физиология / ПАТОФИЗИОЛОГИЯ СИСТЕМЫ КРОВИ 2
.pdfОбъем и скорость кровопотери в значительной степени зависят от величины и вида повреж-денного сосуда, механизма повреждения (per rexin, per diapedesin, per diabrosin).
2.Соотношение активности факторов свертывающей, противосвертывающей и фибринолитической систем организма.
Снижение активности или содержания факторов свертывающей и/или повышение противосвертывающей и фибринолитической систем, ведущее к понижению свертываемости крови, может обусловить увеличение скорости и объёма кровопотери, что усугубляет её течение и последствия.
3.Скорость включения и выраженность компенсаторных реакций организма.
4.Реактивность организма, которая зависит от пола (женщины менее чувствительны к кровопотере), возраста (взрослые переносят кровопотерю легче, чем дети), предшествующих и сопутствующих кровопотере состояний (перегревание, переохлаждение, заболевания сердца, глубокий наркоз, травматический шок и др.). При перегревании или охлаждении последствия кровопотери тяжелее, чем при нормальной температуре тела. Установлено, что для собак в таких условиях потеря 15-20% ОЦК является смертельной; при глубоком наркозе смерть наступает при потере 15-20% крови; физиологический сон стимулирует компенсаторные возможности организма.
Патогенез острой кровопотери
В патогенезе острой кровопотери условно выделяют 3 стадии:
І. Начальная стадия. Характеризуется уменьшением объема ОЦК – простой (нормоцитемической) гиповолемией, понижением АД, гипоксией (преимущественно циркуляторного типа).
ІІ. Компенсаторная стадия. Обусловлена включением комплекса защитно-компенсаторных реакций, направленных на ликвидацию последствий потери крови.
ІІІ. Терминальная стадия. Характеризуется нарастанием патологических изменений в организме вплоть до летального исхода. Развивается при недостаточности компенсаторных реакций, а также при обильной и быстрой кровопотере, на фоне действия неблагоприятных факторов (охлаждение, большая травма, заболевания сердечно-сосудистой системы) и при отсутствии лечебных мероприятий.
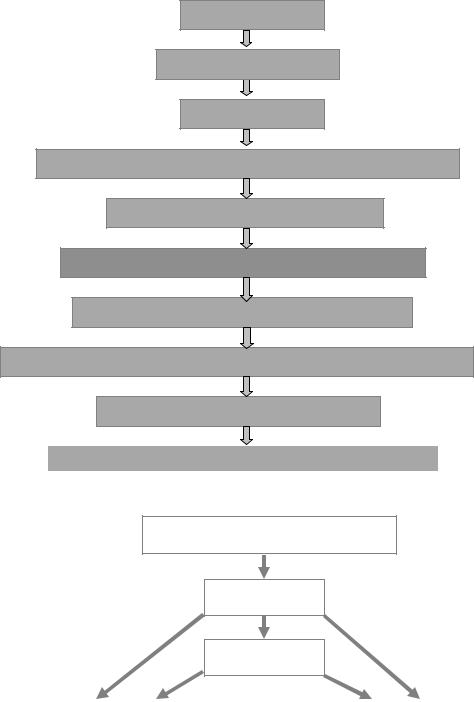
На начальном этапе кровопотери в большей или меньшей степени снижается ОЦК при сохранении нормального гематокрита (нормоцитемическая гиповолемия). В связи с этим уменьшается приток венозной крови к сердцу, его ударный и минутный выброс. Это приводит к падению АД и перфузионного давления в сосудах органов и тканей. В результате уменьшается транспорт О2 и субстратов метаболизма из крови к клеткам, а от последних – СО2 и продуктов обмена веществ. Развиваются капилляротрофическая недостаточность, интоксикация организма продуктами нарушенного метаболизма, гипоксия. Это вызывает расстройства функции органов и тканей, что нередко сопровождается выраженной в большей или меньшей мере их недостаточностью. Существенно расстраивается жизнедеятельность организма в целом. Механизм развития патологических изменений в организме при острой кровопотере представлен на рисунке 8.
Главным звеном патогенеза острой кровопотери являются нарушения, связанные с изменением общей гемодинамики – уменьшение ОЦК (гиповолемия) и обусловленное этим падение АД (гипотензия), вплоть до крайнего его уровня – коллапса. На этом фоне развивается гипоксемия. Гипоксемия обуславливает развитие собственно патологических изменений в организме (анемии, гипоксии органов и тканей, ацидоза, интоксикации), а с другой, – включает сложный комплекс рефлекторных и гуморальных защитно-компенсаторных реакций, направленных на восстановление и сохранение гомеостаза (рис. 9).
11
Кровопотеря
Уменьшение ОЦК
Снижение АД
Уменьшение перфузионного давления в сосудах
Нарушения микроциркуляции
Капилляротрофическая недостаточность
Гипоксия, токсемия, ацидоз, дистония
Нарушение энергетич. и пластич. обеспечения клеток
Полиорганная недостаточность
Расстройства жизнедеятельности организма
Рис. 8. Механизм развития патологических изменений в организме при острой кровопотере
Кровопотеря
↓ОЦК
↓АД
Компенсаторные реакции |
|
Патологические изменения |
|
|
|
|
|
|
Рис. 9. Главное звено патогенеза острой кровопотери
Патологические изменения, возникающие при кровопотере:
1.Нарушения системной гемодинамики (уменьшение ОЦК, падение АД) и местного кровообращения (микроциркуляции) вплоть до развития шока.
2.Острая постгеморрагическая анемия.
3.Гипоксия. Вначале является циркуляторной, а затем гемической (анемической).
4.Негазовый (метаболический) ацидоз. Обусловлен гипоксией и поступлением в кровь молочной кислоты.
12
5.Нарушение экскреторной функции почек. При падении АД уменьшается скорость клубочковой фильтрации и развиваются явления ОПН: олиго- и анурия, интоксикация (азотемия).
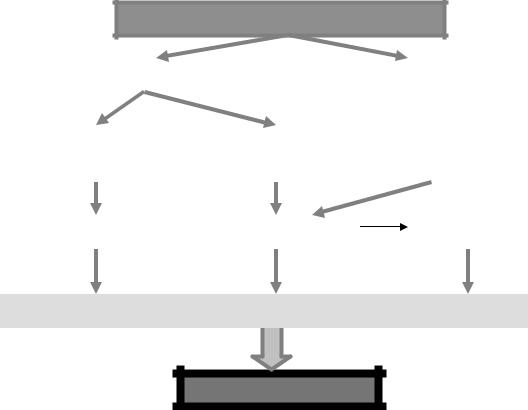
Крайняя степень расстройств жизнедеятельности организма обозначается как постгеморрагический шок. Ведущим механизмом его развития является снижение ОЦК, что вызывает падение АД, нарушения микроциркуляции, расстройства кровоснабжения жизненно важных органов (головного мозга, сердца, почек). Следствием этого является развитие гипоксии, ацидоза и интоксикации, что усугубляет течение шока, создает «порочные круги» в его патогенезе и в конечном итоге ведет к смерти (рис. 10).
Кровопотеря
|
|
Гиповолемия |
|
|
|
Анемия |
|
|
||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||
Острая почечная |
|
|
Нарушения |
|
|
|
|
|
|
|||
недостаточность |
|
гемодинамики |
|
|
|
|
|
|
||||
|
|
|
|
|
|
|
|
|
|
|
||
|
|
|
|
|
|
|
|
|
|
|
|
|
Интоксикация |
|
|
|
Гипоксия |
|
|
|
Ацидоз |
|
|||
|
|
|
|
|
|
|
|
|
|
|
|
|
ЦНС и другие жизненно важные органы
СМЕРТЬ
Рис. 10. Патогенез геморрагического шока
Защитно-компенсаторные реакции при кровопотере
Взависимости от сроков возникновения защитные реакции организма подразделяют на срочные и несрочные.
Взависимости от направленности выделяют следующие группы механизмов компенсации
(рис. 11):
1)направленные на уменьшение объема сосудистого русла;
2)направленные на увеличение ОЦК;
3)направленные на защиту от гипоксии;
4)направленные на восстановление состава крови.
1.Компенсаторные реакции, направленные на уменьшение объёма сосудистого русла (централизации кровообращения)
Цель рассматриваемой группы реакций – привести в соответствие объём сосудистого русла с уменьшенным ОЦК (централизация кровообращения). Это позволяет на какое-то время поддержать необходимое давление крови и обеспечить кровоснабжение жизненно важных органов. Механизмы централизации кровообращения при острой кровопотере представлены на рисунке 12.
1)Снижение АД → возбуждение барорецепторов → возбуждение симпатоадреналовой системы → действие катехоламинов на α-адренорецепторы гладких мышц артерий, артериол, прекапиллярных сфинктеров и вен.
13
 Защитные реакции организма
Защитные реакции организма 

Срочные |
Несрочные |
Направленные на уменьшение объема сосудистого русла
Направленные на увеличение ОЦК
Направленные на защиту от гипоксии
Направленные на восстановление состава крови
Рис. 11. Группы механизмов компенсации кровопотери
|
Катехоламины |
|
|
|
Вазопрессин |
|
|
|
Ангиотензин II |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
Спазм артериол
Открытие артериовенозных шунтов
Веноконстрикция
Рис. 12. Механизмы централизации кровообращения при острой кровопотере
2)Уменьшение ОЦК и АД → возбуждение волюмо- и барорецепторов → активация нейросекреторных клеток гипоталамуса, продуцирующих вазопрессин → действие этого гормона на V1-рецепторы гладких мышц сосудов с последующей вазоконстрикцией.
3)Уменьшение ОЦК и активация симпатоадреналовой системы → выделение клетками ЮГА почек ренина → активация РАС с образованием ангиотензина II → спазм гладких мышц кровеносных сосудов.
Врезультате включения указанных механизмов происходит:
a)спазм артериол кожи, мышц, органов пищеварительной системы;
b)открытие артериовенозных анастомозов указанных органов и тканей в результате спазма прекапиллярных сфинктеров;
c)веноконстрикция (сокращение гладких мышц), увеличивающая поступление крови к сердцу и уменьшающая емкость венозного отдела кровообращения.
2.Компенсаторные реакции, направленные на увеличение ОЦК
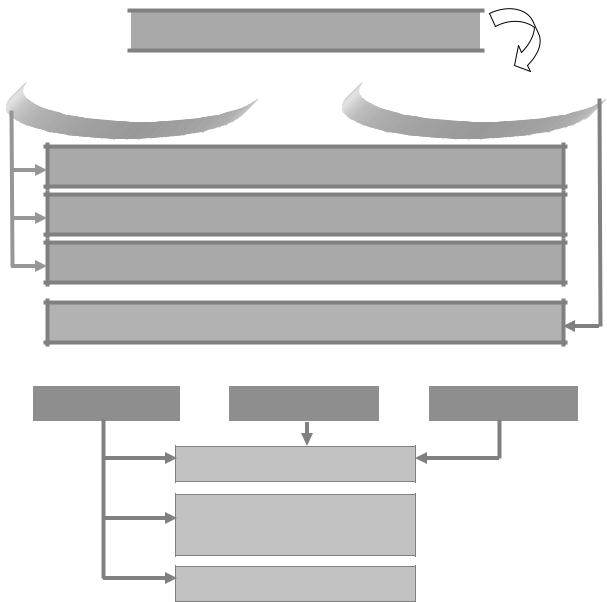
Реакции этой группы реализуются в период времени от нескольких часов до нескольких суток после кровотечения. Увеличение ОЦК достигается с помощью следующих механизмов (рис. 13):
14
↓ Гидростатиче- |
|
|
|
|
Переход тканевой |
|
ского давления |
|
|
|
|
жидкости |
|
|
|
|
|
|
в кровеносные сосуды |
|
|
|
|
||||
|
|
↑ Реабсорбции |
|
|
|
|
Вазопрессин |
|
воды |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
↑ Реабсорбции |
|
|
Усиление реабсорбции |
|
Альдостерон |
|
натрия |
|
|
воды и ионов натрия |
|
|
|
|
|
|
в почках |
|
|
|
|
||||
|
|
↑ Реабсорбции |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
воды и натрия |
|
|
|
|
Катехоламины |
|
|
|
|
||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
Спазм |
|
|
Выход крови из депо |
|
|
|
|
|
|
|
||
|
||||||
|
|
периферических |
|
|
в кровеносное русло |
|
|
|
сосудов |
|
|
|
|
Рис. 13. Механизмы увеличения ОЦК при острой кровопотере
●Переход тканевой жидкости в кровеносные сосуды. Основу этого процесса составляет механизм, описанный Старлингом. В результате уменьшения ОЦК уменьшается гидростатическое давление в капиллярах, что приводит к уменьшению фильтрации воды в артериальной части капилляров и увеличению реабсорбции жидкости в венозной. Уменьшению гидростатического давления способствует развивающийся спазм артериол.
●Усиление реабсорбции воды и ионов натрия в почках. Эта реакция, предотвращая потерю жидкости с мочой, обусловлена следующими механизмами:
a)действие вазопрессина (антидиуретического гормона) на V2-рецепторы эпителия дистальных извитых канальцев и собирательных трубочек почек, в результате увеличивается факультативная реабсорбция воды;
b)активация РААС с последующим выделением альдостерона, который повышает реабсорбцию натрия в дистальных извитых канальцах нефронов;
c)активация симпатоадреналовой системы, приводящая к перераспределению кровотока между сосудами кортикальных и юкстамедуллярных нефронов, в результате чего возрастает площадь и интенсивность канальцевой реабсорбции воды и натрия.
●Выход крови из депо в кровеносное русло. Основу этой реакции составляет активация симпатоадреналовой системы и действие катехоламинов на сосуды печени, селезенки, подкожной жировой клетчатки.
3.Компенсаторные реакции, направленные на компенсацию гипоксии
Гипервентиляция. Ускорение и углубление дыхания происходит вследствие рефлекторного возбуждения дыхательного центра импульсами с хеморецепторов сосудистого русла, преимущественно синокаротидной и аортальной зон, которые реагируют на изменения
химического состава крови (в первую очередь на накопление СО2 и ионов водорода). Гипервентиляция сопровождается мобилизацией резервных альвеол и улучшением диффузии
газов через альвеолярно-капиллярные мембраны, что способствует уменьшению дефицита О2 в организме.
15

Усиление кровообращения направлено на улучшение доставки кислорода тканям. Реализуется за счет ускорения и усиления сокращений сердца.
Увеличение количества эритроцитов и гемоглобина вследствие выхода крови из депо, что увеличивает кислородную емкость крови и обеспечивает быстрое приспособление к гипоксии.
Изменения кривой диссоциации оксигемоглобина заключаются в том, что при ацидозе усиливается способность молекулы Нb отдавать О2 тканям.
Реакция регуляторных систем (нервной и эндокринной) на гипоксию проявляется возбуждением дыхательного и сосудодвигательного нервных центров, освобождением катехоламинов, что обеспечивает гипервентиляцию, а также аварийную гиперфункцию сердца и системы кровообращения в целом.
Активация системы утилизации О2 и энергообразования. Процесс энергообразования перестраивается на более интенсивный, которым является окисление янтарной кислоты – сукцината, кинетические преимущества которого – увеличение скорости фосфорилирования АДФ (этот путь транспортирования более стойкий к гипоксии, чем НАД-зависимый, и через него интермедиаты цикла Кребса – сукцинат и α-кетоглутарат – получают выход в терминальное окисление). Катехоламины и оксид азота (II) активируют этот процесс, ацетилхолин, серотонин – тормозят. В митохондриях головного мозга усиливается сочетание фосфорилирования с окислением, эффективнее используются запасы макроэргов. В таких структурах, как мембраны, также существуют быстрые приспособительные изменения. Во время гипоксии диффузия газов через мембрану может усиливаться благодаря конформационной перестройке мембранных белковых молекул и изменениями особенностей липидного слоя.
4.Компенсаторные реакции, обеспечивающие восстановление состава периферической крови (рис. 14)
Мобилизация тканевых ресурсов белка
Усиление синтеза белка в печени
Восстановление белкового состава крови
Гипоксия
Стимуляция продукции эритропоэтина в почках
Красный костный мозг
Активация эритропоэза
Восстановление состава периферической крови
Рис. 14. Механизмы восстановления состава периферической крови при острой кровопотере
Восстановление состава периферической крови обеспечивается долговременными реакциями, которые реализуются в период времени от нескольких суток до 1-2 недель после кровотечения. В их основе лежит циркуляторная (уменьшение ОЦК) и гемическая (анемическая) гипоксия. Основное значение придают кислородному голоданию почек, следствием которого является образование и поступление в кровь большого количества почечных эритропоэтинов. Последние действуют на кроветворные клетки красного костного мозга (эритропоэтинчувствительные клетки III класса) и стимулируют эритропоэз – увеличивается поступление молодых регенераторных форм эритроцитов в периферическую кровь. Эритропоэтин
16
воздействует на генетический аппарат эритропоэтинчувствительной клетки, которая дифференцируется в эритробласт и далее до зрелых эритроцитов, обеспечивая ускорение деления эритроидных клеток и синтез гена гемоглобина, активацию биосинтетических и энергетических процессов. Показателем усиленного эритропоэза служит увеличение числа ретикулоцитов в крови (на 5-е сутки).
Клиническая оценка тяжести кровопотери
Клиническая оценка тяжести кровопотери является самым ранним способом определения постгеморрагических нарушений гомеостаза, и в настоящее время – самым распространенным способом. Описание основополагающих клинических признаков острой массивной кровопотери мы находим уже в дневниках Н.И. Пирогова, относящихся к периоду Крымской кампании 1854 г.: «Лежит такой окоченелый на перевязочном пункте неподвижно; он не кричит, не вопит, не жалуется, не принимает ни в чем участия и ничего не требует; тело его холодно, лицо бледно, как у трупа; взгляд неподвижен и обращен вдаль; пульс как нитка, едва заметен под пальцем и с частыми перемежками. На вопросы окоченелый или вовсе не отвечает, или только про себя, чуть слышным шепотом; дыхание тоже едва приметно...».
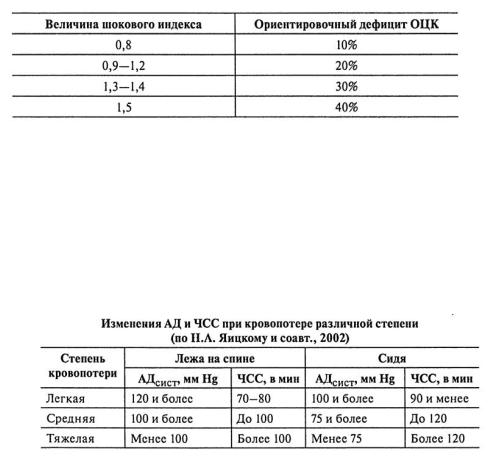
Для скрининговой оценки тяжести кровопотери применяют предложенный в 1967 г. Альговером и Бури шоковый индекс, представляющий собой отношение ЧСС к систолическому АД. В норме индекс равен 0,5. Чем больше индекс, тем массивнее кровопотеря и хуже прогноз. Нарастание индекса Альговера свидетельствует о прогрессировании тяжести кровопотери.
В связи с этим, все большему числу клиницистов представляются более физиологически обоснованными и клинически значимыми классификации кровопотери, основанные на клинически определяемой резистентности к ней организма. Уровень компенсации перенесенной кровопотери представляет несомненный практический интерес, ведь все последующие лечебные мероприятия направлены на стабилизацию функций организма. Несомненно, что в экстренной ситуации целесообразна и практически применима такая система оценки кровопотери, которая по минимальному числу параметров позволяет адекватно и быстро определять тяжесть кровопотери не только в стационаре, но и на догоспитальных этапах медицинской помощи. Так, Н.А. Яицкий и соавт. (2002) разделяют острую кровопотерю на 3 степени только на основании величин АДсист и ЧСС.
Отражающее состояние макроциркуляции и весьма ориентировочно состояние микроциркуляции АД может служить быстрым методом оценки гемодинамики и ее простого мониторинга.
Классификации острой кровопотери, основанные только на лабораторных данных, несостоятельны ввиду невозможности применения в ранние сроки кровотечения. При массивном кровотечении в первые часы показатели гемоглобина, эритроцитов, гематокрита остаются в пределах исходных значений, так как аутогемодилюция не успевает развиться. В некоторых работах прямо указывается, что величина гематокрита отражает лишь проводимую инфузионную терапию, но не выраженность кровотечения. Лишь спустя 6-24 ч вследствие аутогемодилюции и заместительной инфузионной терапии показатели красной крови снижаются и позволяют рассчитать предварительный объем кровопотери. Уровень эритроцитов, гемоглобина и гематокрита в периферической крови в ранние сроки
17
кровотечения (1-2-е сутки) не отражает истинной тяжести возникшей кровопотери, что затрудняет изолированное использование этих гематологических показателей на ранних этапах диагностики.
Наибольшее распространение получили методы оценки тяжести кровопотери по комплексу клинических и рутинных лабораторных критериев.
В1982 г. Американская коллегия хирургов на основании интегрального анализа десятков тысяч случаев острых кровотечений различной этиологии предложила различать кровопотерю на 4 класса в зависимости от клинической симптоматики (по P.L. Marino, 1998):
Класс I – клинические симптомы отсутствуют или имеется тахикардия в покое, прежде всего в положении стоя; тахикардия считается ортостатической тогда, когда ЧСС увеличивается не менее чем на 20 в минуту при переходе из горизонтального положения в вертикальное (соответствует потере 15% объема циркулирующей крови или менее).
Класс II – ортостатическая гипотензия или снижение АД не менее чем на 15 мм рт.ст. при переходе из горизонтального положения в вертикальное; в положении лежа АД нормальное или несколько снижено, диурез сохранен (соответствует потере от 20 до 25% ОЦК).
Класс III – гипотензия в положении лежа на спине, олигурия менее 400 мл/сут (соответствует потере от 30 до 40% ОЦК).
Класс IV – коллапс и нарушение сознания до комы (потеря более 40% ОЦК).
Всовременной трансфузиологии тяжесть кровопотери определяют по состоянию сознания, достаточному диурезу [более 0,5 мл/(кг × ч)], отсутствию гипервентиляции, показателям гемокоагуляции, динамике центрального венозного, пульсового и среднего динамического АД, изменению ар- терио-венозной разницы по кислороду (Зильбер А.П., 1999; Ярочкин B.C., 1997; 2004).
Одну из последних классификаций острой кровопотери предложил А.И. Воробьев (2002). Автор подчеркивает, что именно клинические, а не лабораторные показатели нужно считать определяющими при оценке тяжести кровопотери.
|
Показатель |
|
|
|
|
|
|
Степень тяжести кровопотери |
|
|
|
||||
|
|
|
|
I |
|
|
II |
|
|
III |
|
|
IV |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||
ЧСС, в мин |
<100 |
|
>100 |
|
>120 |
|
>140 |
|
|||||||
АД |
|
|
N |
|
N |
|
|
|
|
||||||
Пульсовое дав- |
|
|
N или |
|
|
|
|
|
|
||||||
ление |
|
|
|
|
|
||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|||
Почасовой ди- |
> 30 |
|
20-30 |
|
5-15 |
|
|
Анурия |
|||||||
урез, мл |
|
|
|
|
|||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|||
Уровень созна- |
|
|
Легкое возбуж- |
|
Возбуждение |
|
Заторможенность |
|
Прекома |
||||||
ния |
|
|
дение |
|
|
|
|||||||||
|
|
|
|
|
|
|
|
|
|
|
|||||
Частота дыхания, |
|
|
N |
20-30 |
|
|
30–40 |
>45 |
|
||||||
в мин |
|
|
|
|
|
||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|||
Тест заполнения |
|
|
Норма |
|
Замедленный |
|
Очень |
|
Заполнение |
||||||
капилляров |
|
|
|
|
замедленный |
|
отсутствует |
||||||||
|
|
|
|
|
|
|
|
|
|||||||
Объем кровопо- |
|
|
|
|
|
|
|
|
|
|
|
|
|
||
тери у взрослого |
< 750 |
|
750-1500 |
|
1500-2000 |
|
>2000 |
|
|||||||
пациента массой |
|
|
|
|
|
|
|
|
|
|
|
|
|
||
70 кг, мл (% |
(<15) |
|
(15-30) |
|
(30-40) |
|
(>40) |
|
|||||||
ОЦК) |
|
|
|
|
|
|
|
|
|
|
|
|
|
||
Классификация тяжести кровопотери, основанная как на клинических критериях (уровень сознания, признаки периферической дисциркуляции, АД, ЧСС, ЧДД, ортостатическая гипотензия, диурез), так и на основополагающих показателях картины красной крови – величин гемоглобина и гематокрита (Гостищев В.К., Евсеев М.А., 2005). Классификация различает 4 степени тяжести острой кровопотери:
I степень (легкая кровопотеря) – характерные клинические симптомы отсутствуют, возможна ортостатическая тахикардия, уровень гемоглобина выше 100 г/л, гематокрит не менее
40%. Дефицит ОЦК до 15%.
18
II степень (кровопотеря средней тяжести) – ортостатическая гипотензия со снижением АД более чем на 15 мм рт.ст. и ортостатическая тахикардия с увеличением ЧСС более чем на 20 в минуту, уровень гемоглобина в пределах 80-100 г/л, гематокрит в пределах 30-40%. Дефицит
ОЦК 15-25%.
III степень (тяжелая кровопотеря) – признаки периферической дисциркуляции (дистальные отделы конечностей холодные на ощупь, выраженная бледность кожи и слизистых оболочек), гипотензия (АДсист 80-100 мм рт. ст.), тахикардия (ЧСС более 100 в минуту), тахипноэ (ЧДД более 25 в минуту), явления ортостатического коллапса, диурез снижен (менее 20 мл/ч), уровень гемоглобина в пределах 60-80 г/л, гематокрит в пределах 20-30%. Дефицит ОЦК 25-
35%.
IV степень (кровопотеря крайней тяжести) – нарушение сознания, глубокая гипотензия (АДсист менее 80 мм рт. ст.), выраженные тахикардия (ЧСС более 120 в минуту) и тахипноэ (ЧДД более 30 в минуту), признаки периферической дисциркуляции, анурия; уровень гемоглобина ниже 60 г/л, гематокрита – 20%. Дефицит ОЦК больше 35%.
Предложенная классификация тяжести кровопотери представляется приемлемой и удобной для клиники ургентной хирургии как минимум по двум причинам. Во-первых, оценка кровопотери не требует проведения сложных специальных исследований. Во-вторых, определение кровопотери сразу же в приемном отделении позволяет по показаниям начать инфузионную терапию и госпитализировать пациента в отделение интенсивной терапии.
Принципы терапии кровопотери
Этиотропная терапия
Устранение причины кровопотери (восстановление целостности сосуда, устранения дефицита факторов свертывания, мероприятия по уменьшению проницаемости сосудистой стенки и др.).
Патогенетическая терапия
Для восстановления ОЦК устраняют или уменьшают степень расстройств центрального и органотканевого кровообращения (переливание крови, плазмы, плазмозаменителей).
Для нормализации транскапиллярного обмена следует устранить или уменьшить степень рас-
стройств микроциркуляции (вливание плазмозаменителей).
Для устранения сдвигов или уменьшения степени водного, белкового и ионного дисбаланса
надо (помимо восстановления ОЦК и нормализации транскапиллярного обмена) вводить растворы, содержащие белки и ионы в количестве и соотношении, устраняющих их дисбаланс в организме.
Для коррекции КОС требуется нормализовать его показатели. Для этого восстанавливают ОЦК, устраняют или уменьшают степень расстройств микроциркуляции, вводят буферные растворы и нормализуют (активируют) функции органов, компенсирующих сдвиги КОС.
Симптоматическая терапия
Направлена на нормализацию функций органов и систем, нарушенных в результате кровопотери и гипоксии (ССС, дыхательная, почки, печень).
Постгемотрансфузионные реакции и осложнения
Гемотрансфузии при тщательном соблюдении правил являются безопасным методом лечения различных патологических состояний человека. Нарушение правил и техники гемотрансфузий может привести к развитию посттрансфузионных реакций и осложнений. Возникновение любого осложнения или подозрение на возможность его развития требует немедленного проведения лечения больного в условиях отделения интенсивной терапии.
Классификация неблагоприятных последствий гемотрансфузий
Большинство гемотрансфузионных реакций и осложнений достаточно подробно описаны в работах А.Н. Филатова (1973).
I. Осложнения механического характера, связанные с погрешностями в технике переливания крови:
19
1.Острое расширение сердца.
2.Воздушная эмболия.
3.Тромбозы и эмболии.
4.Нарушения кровообращения в конечностях после внутриартериальных трансфузий.
II. Осложнения реактивного характера:
1.Посттрансфузионный шок при переливании несовместимой крови (гемолитический шок): а) при переливании крови, несовместимой в групповом отношении; б) при переливании резус-несовместимой крови; в) при переливании крови, несовместимой по другим факторам.
2.Посттрансфузионный шок при переливании крови, совместимой по изосерологическим свойствам:
а) при переливании инфицированной крови; б) при переливании измененной крови (гемолизированной, перегретой и т.д.).
3.Анафилактический шок.
4.Цитратный шок.
5.Посттрансфузионная пирогенная реакция.
6.Синдром массивных гемотрансфузий.
III.Перенесение инфекционных заболеваний при переливании крови:
1.Заражение острыми инфекционными заболеваниями.
2.Заражение сифилисом.
3.Заражение малярией.
4.Заражение гепатитом.
Вклинической практике широкое распространение получила приводимая ниже классификация В.А. Аграненко и Н.Н. Скачиловой (1979).
Гемотрансфузионные реакции
1.По степени тяжести: а) легкие;
б) средней степени тяжести; в) тяжелые.
2.По этиологии и клинике: а) пирогенные,
б) антигенные (негемолитические), в) аллергические (анафилактические).
Гемотрансфузионные осложнения
1.Несовместимость крови донора и реципиента по эритроцитам (по групповым факторам АВ0, Rh-фактору и др.).
2.Недоброкачественность перелитой крови (бактериальное загрязнение, перегревание, гемолиз, денатурация белков вследствие длительного хранения, нарушения температурного режима хранения и др.).
3.Погрешности в методике проведения трансфузии (воздушная эмболия, тромбоэмболия, циркуляторная перегрузка, сердечно-сосудистая недостаточность и др.).
4.Массивные дозы гемотрансфузий.
5.Недоучет противопоказаний к переливанию крови и недооценка состояния реципиента перед проведением гемотрансфузии (аллергическая настроенность, сенсибилизация, повышенная реактивность и др.).
20
