
Рис. 12-2. Солитарный метастаз опухоли прямой кишки в IV сегменте печени. Компьютерная томограмма
блюдение, поскольку результаты разных (по времени) исследований легко пересмотреть и сопоставить по снимкам. Точность диагностики повышается при использовании болюсного внутривенного контрастирования. КТ-волюметрия помогает определить объем непораженной паренхимы печени при планировании обширных резекций органа (чтобы оценить риск развития печеночной недостаточности после операции).
МРТ обладает сопоставимой с КТ чувствительностью и специфичностью. Однако стоимость проведения МРТ-исследования очень высока, особенно при использовании контрастного усиления (рис. 12-3).
Данная книга в списке рекомендаций к покупке и прочтению форума сайта https://meduniver.com/
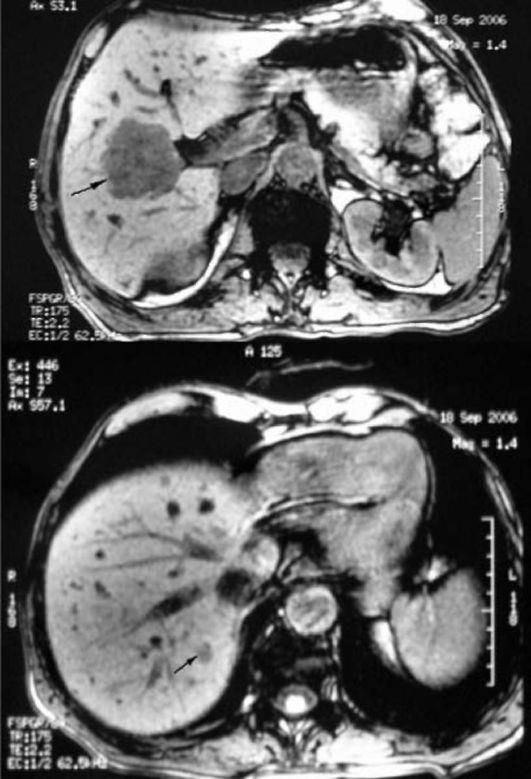
Рис. 12-3. Единичные метастазы колоректального рака в правой доле печени. Магнитнорезонансная томограмма
Преимущества МРТ:
•возможность получить изображение органа в любой плоскости без перемещения пациента или сканирующего устройства;
•большой диапазон контрастности при исследовании;
• высокое пространственное разрешение.
Для уточнения характера очагового поражения печени с помощью МРТ используют три вида контрастов: неспецифический контрастный агент; контраст, специфичный для ретикулоэндотелиальной системы печеночной ткани; гепатоцитспецифический контраст.
Позитронно-эмиссионную томографию проводят при планировании оперативного лечения для визуализации субклинических опухолевых очагов в печени и за ее пределами (рис. 12-4).
Данная книга в списке рекомендаций к покупке и прочтению форума сайта https://meduniver.com/
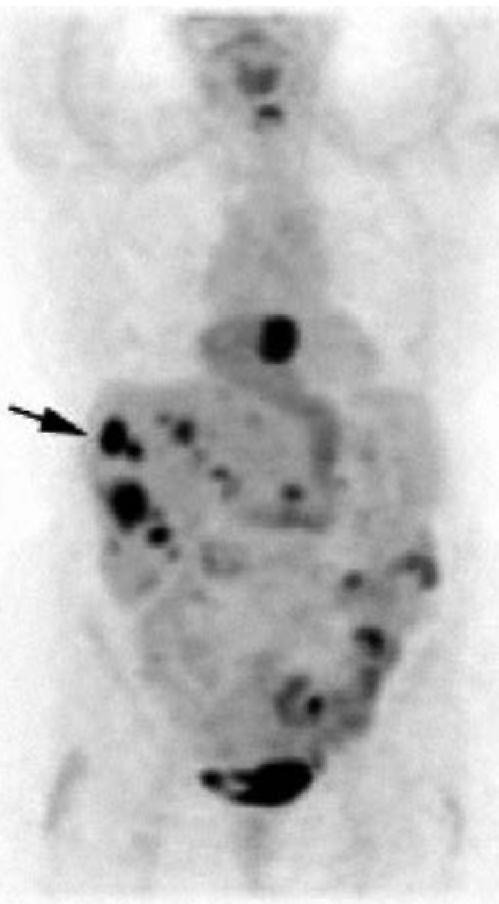
Рис. 12-4. Множественные метастазы в печени. Позитронно-эмиссионная томограмма
Важнейшей задачей уточняющей диагностики (при метаста-зировании опухолей в печень) считают морфологическую верификацию процесса. Для этой цели в настоящее время выполняют пункционную биопсию под контролем УЗИ (реже - под контролем КТ) с последующим гистологическим или цитологическим исследованием полученного материала. В случае затруднения морфологической верификации при первично-множественных опухолях, а также при метастазах без определенного первичного очага проводят гистологическое исследование биопсийного материала (при необходимости дополненное иммуногистохими-ческим анализом), сопоставляя его результаты с клиническими данными. Лечение
Распространенность метастатического поражения печени с учетом характера первичной опухоли определяет лечебную тактику.
При раке толстой кишки, нейроэндокринных опухолях, уве-альной меланоме метастазы в печени, как правило, отграничены. В этих случаях целесообразно проводить активное хирургическое лечение, в том числе при множественных метастазах и поражении обеих долей. Основной метод оперативного вмешательства - резекция печени (рис. 12-5, см. цв. вклейку). Резекции печени могут
быть анатомическими, при этом удаляют фрагмент печени в соответствии с ее сегментарным строением (наиболее часто выполняют правостороннюю или левостороннюю гемигепатэктомию, бисегментэктомию, сегментэктомию); неанатомическими (клиновидные, атипичные); резекциями печени ex vivo (вне организма).
Для повышения резектабельности проводят предоперационную эмболизацию печеночной артерии и неоадъювантную химиотерапию. При рецидиве метастазов в оставшейся части печени необходимо выполнить повторную резекцию.
При нерезектабельных метастазах, противопоказаниях к оперативному лечению используют различные методы локальной деструкции очагов (рис. 12-6, см. цв. вклейку), проводимые чрескожным, оперативным или лапароскопическим способом под контролем УЗИ или КТ. В группу методов локальной деструкции очагов входят алкогольная аблация, криодеструкция, лазер-индуцированная термоаблация, радиочастотная термоаблация (проводят наиболее часто), микроволновая деструкция.
При невозможности оперативного лечения и локальной деструкции выполняют артериальную химиоэмболизацию и регионарную внутриартериальную химиотерапию. Наибольший эффект при внутриартериальном введении оказывает флоксуридин.
При опухолях желудка, пищевода, почки поражение печени редко носит изолированный характер (прогноз, как правило, неблагоприятный). Хирургическое лечение проводят при солитар-ных или единичных метастазах (при отсутствии внепеченочных очагов заболевания). Альтернативой обширному хирургическому вмешательству служит радиочастотная термоаблация как вариант циторедуктивного лечения.
При метастазах опухолей, чувствительных к консервативной терапии (например, рак молочной железы или яичников), резекции печени выполняют при наличии изолированной остаточной опухоли в печени после проведенного лекарственного (гормонального) лечения, при этом допускают выполнение экономных резекций или радиочастотной термоаблации.
Лучевую терапию (как самостоятельный метод) для лечения метастазов в печени не используют. Однако сочетание ее с дистанционным облучением и регионарной химиотерапией позволяет повысить вероятность резорбции опухоли и уменьшить болевой синдром.
Прогноз
Данная книга в списке рекомендаций к покупке и прочтению форума сайта https://meduniver.com/
При метастазировании опухолей в печень средняя продолжительность жизни больных, как правило, невелика (1 год). Вероятность пятилетней выживаемости после резекции печени при метастазах колоректального рака составляет 20-50%, при метастазах карциноидов - 60-80%, при метастазах других опухолей - 10-40%.
Факторы, благоприятно влияющие на прогноз:
•изолированный характер поражения печени;
•солитарные метастазы;
•метахронно обнаруженные метастазы. Продолжительность жизни больных после химиотерапии
не превышает нескольких месяцев.
Глава 13. Опухоли головы и шеи
13.1. РАК ГОРТАНИ
Код по МКБ-10
C32. Злокачественное новообразование гортани.
Эпидемиология
В структуре общей заболеваемости злокачественными опухолями рак гортани занимает 9-е место (2-4%), а в структуре заболеваемости мужского населения - 4-е место. За последние 10 лет заболеваемость раком гортани в России увеличилась на 20%. В 2009 г. в России выявлено 6718 новых случаев заболевания раком гортани, что составляет 1,5% общего числа впервые выявленных злокачественных новообразований.
Классификация
В настоящее время применяют Международную клиническую классификацию рака гортани по критерию TNM.
Первичная опухоль
•Тх - недостаточно данных для оценки первичной опухоли.
•Т0 - первичная опухоль не определяется.
•Tis - преинвазивная карцинома (carcinoma in situ).
Надскладочный отдел
•Т1 - опухоль ограничена одной анатомической частью над-складочного отдела, подвижность голосовых складок сохранена.
•Т2 - опухоль поражает слизистую оболочку нескольких анатомических частей надскладочного или складочного отдела, голосовых складок, подвижность голосовых складок сохранена.
•Т3 - опухоль ограничена гортанью с фиксацией голосовых складок и/или распространением на соседние области.
•Т4 - опухоль распространяется на щитовидный хрящ и/или другие прилежащие к гортани ткани: ротоглотку, мягкие ткани шеи, щитовидную железу и/или пищевод.
Складочный отдел
• T1 - опухоль ограничена голосовой складкой (складками) без нарушения подвижности (могут быть вовлечены передняя или задняя комиссуры).
T1a - опухоль ограничена одной голосовой складкой.
T1b - опухоль распространяется на обе голосовые складки.
•T2 - распространение опухоли на надскладочную и/или под-складочную области и/или нарушение подвижности голосовых складок.
•T3 - опухоль ограничена гортанью с фиксацией одной или обеих голосовых складок.
•T4 - опухоль распространяется на щитовидный хрящ и/или на другие прилежащие к гортани ткани: мягкие ткани шеи, трахею, щитовидную железу, глотку.
Подскладочный отдел
• T1 - опухоль ограничена подскладочным отделом.
Данная книга в списке рекомендаций к покупке и прочтению форума сайта https://meduniver.com/
•T2 - опухоль распространяется на одну или обе голосовые складки со свободной или ограниченной подвижностью.
•T3 - опухоль ограничена гортанью с фиксацией одной или обеих голосовых складок.
•T4 - опухоль распространяется на перстневидный или щитовидный хрящ и/или на прилежащие к гортани ткани: ротоглотку, мягкие ткани шеи, щитовидную железу, пищевод.
Регионарные лимфатические узлы
Регионарные лимфатические узлы для всех отделов головы и шеи (за исключением носоглотки и щитовидной железы): подбородочные, подчелюстные, у основания черепа около магистральных сосудов (глубокие шейные), в зоне бифуркации общей сонной артерии (глубокие шейные), по ходу общей сонной артерии (глубокие шейные), задние шейные (поверхностные шейные), узлы вдоль добавочного нерва, надключичные, предгортанные, паратрахеаль-ные, заглоточные, околоушные, щечные, заушные и затылочные.
•N/pNx - недостаточно данных для оценки состояния регионарных лимфатических узлов.
•N/pN0 - нет признаков метастатического поражения регионарных лимфатических узлов.
•PN0 - гистологическое исследование материала выборочного участка тканей шеи, включающее шесть и более лимфатических узлов. Гистологическое исследование материала с помощью радикальной или модифицированной радикальной шейной лимфаденэктомии включает десять и более лимфатических узлов.
•N/pN1 - метастазы в одном лимфатическом узле на стороне поражения, 3 см и менее в наибольшем измерении.
•N/pN2 - метастазы в одном или нескольких лимфатических узлах на стороне поражения до 6 см в наибольшем измерении или метастазы в лимфатических узлах шеи с обеих сторон (или с противоположной стороны) до 6 см в наибольшем измерении.
N/pN2a - метастазы в одном лимфатическом узле на стороне поражения до 6 см в наибольшем измерении.
N/pN2b - метастазы в нескольких лимфатических узлах на стороне поражения до 6 см в наибольшем измерении.
N/pN2c - метастазы в лимфатических узлах с обеих сторон или с противоположной стороны до 6 см в наибольшем измерении.
• N/pN3 - метастаз в лимфатическом узле более 6 см в наибольшем измерении.
Отдаленные метастазы
•M0 - нет признаков отдаленных метастазов.
•M1 - отдаленные метастазы.
•MX - недостаточно данных для определения отдаленных метастазов.
Клиническая картина
Рак гортани поражает преимущественно мужчин (80-95%). Больные раком гортани находятся в возрастном периоде 40-60 лет. Типичная морфологическая форма злокачественной опухоли гортани - плоскоклеточный рак (ороговевающий в 7580% случаев, с тенденцией к ороговению - в 17,5-18,5%, неоро-говевающий - в 6-8% случаев). Саркомы составляют 0,9-3,2%.
Жалобы на ранних стадиях встречаются редко. Для рака гортани не существует патогномоничных симптомов, более характерна динамика заболевания и постоянное нарастание жалоб, зависящих от локализации опухоли.
Надскладочный отдел: дискомфорт или присутствие инородного тела при глотании.
Складочный отдел: охриплость вплоть до афонии, нарастающее затруднение дыхания, развитие стеноза гортани по мере роста опухоли.
Подскладочный отдел: охриплость, нарастающее затруднение дыхания, по мере роста опухоли возможно развитие стеноза гортани.
Диагностика
Лабораторно-инструментальные исследования
•Непрямая ларингоскопия.
•Рентгенография органов грудной клетки.
•Рентгенотомография гортани.
•Компьютерная томография.
•Фиброларингоскопия (с биопсией и проведением цитологического и гистологического исследования биоптата).
•УЗИ лимфатических узлов шеи.
Дифференциальная диагностика
Рак гортани обычно дифференцируют со следующими заболеваниями: хронические воспалительные заболевания гортани, предопухолевые заболевания гортани, папиллома, папилломатоз гортани, пахидермия, дискератозы (лейкоплакия, лейкокератоз), фиброма.
Лечение
Хирургическое лечение
Лечение рака гортани построено на четких показаниях к той или иной операции, основанных на клинико-анатомических особенностях течения опухоли и онкологических принципах. С этих позиций обоснованно выделение трех групп операций:
•различные виды резекций гортани (хордэктомия, передне-боковая резекция гортани, надскладочная горизонтальная резекция гортани);
•полное удаление гортани (ларингэктомия);
•расширенные и комбинированные операции удаления гортани.
Ларингэктомия показана при первичном или рецидивном раке гортани, соответствующем Т3 при условии, что опухоль не распространяется за пределы гортани.
Расширенные и комбинированные ларингэктомии показаны при распространении опухоли за пределы гортани с вовлечением соседних органов и тканей. При наличии метастазов в регионарных лимфатических узлах одномоментно выполняется лимфо-диссекция.
Лучевая терапия
При раке гортани, соответствующем Т1, применяют лучевое лечение с использованием различных источников и очаговой дозой от 50 до 70 Гр. После проведенной лучевой терапии клинического излечения без рецидивов и метастазов продолжительностью 5 лет достигают у 83-95% больных.
При раке гортани Т2 применение лучевой терапии как самостоятельного метода обеспечивает клиническое излечение у 70-76% больных. При местнораспространенных формах рака гортани (Т3-4) лучевая терапия рассматривается как один из этапов комбинированного лечения.
Химиотерапия
Данная книга в списке рекомендаций к покупке и прочтению форума сайта https://meduniver.com/
Применение системной и регионарной химиотерапии при раке гортани как самостоятельного метода лечения нецелесообразно из-за низкой чувствительности опухоли и непродолжительности эффекта. Проводятся исследования по сочетанию лекарственной терапии с ионизирующим воздействием в различных вариантах.
Комбинированное лечение
Выбор варианта комбинированного лечения больных раком гортани зависит от выявленных клинико-морфологических особенностей заболевания.
Сочетание хирургического метода и лучевой терапии.
•1-й этап - лучевая терапия.
•2-й этап - хирургическое вмешательство.
Химиолучевая терапия более эффективна, чем последовательное применение данных методов, однако при этом возможны более выраженные побочные реакции.
В настоящее время, особенно при местнораспространенных формах рака гортани, должно отдаваться предпочтение комбинированному лечению.
Дальнейшее ведение
После проведения лучевого, химиолучевого и хирургического лечения необходимо наблюдать больного не реже 1 раза в 3 мес в течение первого года, 1 раз в 6 мес в течение второго года, в последующем - 1 раз в год с проведением клинического обследования (осмотр, непрямая ларингоскопия, фиброларингоскопия).
13.2. ЗЛОКАЧЕСТВЕННЫЕ ОПУХОЛИ НОСА И ОКОЛОНОСОВЫХ ПАЗУХ
Код по МКБ-10
С30.0. Злокачественное новообразование полости носа. C31.0. Злокачественное новообразование верхнечелюстной пазухи.
C31.1. Злокачественное новообразование решетчатой пазухи.
C31.2. Злокачественное новообразование лобной пазухи.
C31.3. Злокачественное новообразование клиновидной пазухи.
C31.8. Поражение придаточных пазух, выходящее за пределы одной и более вышеуказанных локализаций.
C31.9. Злокачественное новообразование придаточной пазухи неуточненное.
Эпидемиология
Злокачественные опухоли слизистой оболочки полости носа и околоносовых пазух составляют 1-4% всех злокачественных новообразований.
Эти опухоли примерно с равной частотой возникают у мужчин и женщин, чаще встречаются у людей старше 40 лет, наиболее часто - в возрасте 50-75 лет (до 65-70%).
Классификация
Используют Международную клиническую классификацию злокачественных опухолей слизистой оболочки полости носа и околоносовых пазух по критериям ТNМ и стадиям (см. справочник ТNМ).
Этиология
