
2 курс / Нормальная физиология / ФЗЛ ЧЕЛОВЕКА
.pdf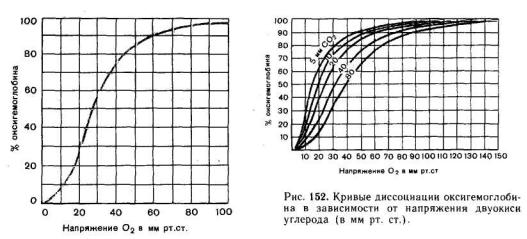
Рис. 151. Кривая диссоциации оксигемо-
глобина при напряжении двуокиси углеро да 40 мм рт. ст. на умеренное снижение его парциально
го давления во вдыхаемом воздухе. И в этих условиях ткани достаточно снаб жаются кислородом.
Крутая часть кривой диссоциации соответствует напряжениям кислорода, обычным для тканей организма (35 мм рт. ст. и ниже). В тканях, поглощающих много кислорода (работающие мышцы, печень, почки), оксигемоглобин диссоциирует в большей степени, иногда почти полностью. В тканях, в которых интенсивность окислительных процессов мала, большая часть оксигемоглобина не диссоциирует. Переход тканей из состояния покоя в деятельное состояние (сокращение мышц, секреция желез) автоматически создает условия для увеличения диссоциации оксигемоглобина и увеличения снабжения тканей кислородом.
Сродство гемоглобина к кислороду (отражается кривой диссоциации оксигемоглобина) непостоянно. Особенно значительно на него влияют следующие факторы. 1. В эритроцитах содержится особое вещество 2, 3-дифосфоглицерат. Его количество увеличивается, в частности, при снижении напряжения кислорода в крови. Молекула 2, 3-дифос- фоглицерата способна внедряться в центральную часть молекулы гемоглобина, что приводит к снижению сродства гемоглобина к кислороду. Кривая диссоциации смещается вправо. Кислород легче переходит в ткани. 2. Сродство гемоглобина к кислороду снижается при увеличении концентрации Н+ и двуокиси углерода (рис. 152). Кривая диссоциации оксигемоглобина в этих условиях также смещается вправо. 3. Подобным же образом действует на диссоциацию оксигемоглобина повышение температуры. Нетрудно понять, что эти изменения сродства гемоглобина к кислороду имеют важное значение для обеспечения снабжения им тканей. В тканях, в которых процессы обмена веществ протекают интенсивно, концентрация двуокиси углерода и кислых продуктов увеличивается, а температура повышается. Это ведет к усилению диссоциации оксигемоглобина.
Гемоглобин крови плода (HbF) обладает значительно большим сродством к кислороду, чем гемоглобин взрослых (НbА). Кривая диссоциации HbF по отношению к кривой диссоциации НbА сдвинута влево.
В волокнах скелетных мышц содержится близкий к гемоглобину миоглобин. Он обладает очень высоким сродством к кислороду.
Количество кислорода в крови. Максимальное количество кислорода, которое может связать кровь при полном насыщении гемоглобина кислородом, называется кислородной емкостью крови. Для ее определения кровь насыщают кислородом воздуха.
Кислородная емкость крови зависит от содержания в ней гемоглобина.

Один моль кислорода занимает объем 22,4 л. Грамм-молекула гемоглобина способна присоединить 22 400X4 = 89 600 мл кислорода (4 — число гемов в молекуле гемоглобина). Молекулярная масса гемоглобина — 66 800. Значит, 1 г гемоглобина способен присоединить 89 600:66 800=1,34 мл кислорода. При содержании в крови 140 г/л гемоглобина кислородная емкость крови будет 1,34 -• 140= 187,6 мл, или около 19 об. % (без учета небольшого количества физически растворенного в плазме кислорода).
В артериальной крови содержание кислорода лишь немного (на 3—4%) ниже кислородной емкости крови. В норме в 1 л артериальной крови содержится 180—200 мл кислорода. При дыхании чистым кислородом его количество в артериальной крови практически соответствует кислородной емкости. По сравнению с дыханием атмосферным воздухом количество переносимого кислорода увеличивается мало (на 3—4%), но при этом возрастают напряжение растворенного кислорода и способность его диффундировать в ткани.
Венозная кровь в состоянии покоя содержит около 120 мл/л кислорода. Таким образом, протекая по тканевым капиллярам, кровь отдает не весь кислород. Часть кислорода, поглощаемая тканями из артериальной крови, называется коэффициентом утилизации кислорода. Для его вычисления делят разность
содержания кислорода в артериальной и венозной крови на содержание кислорода в артериальной крови и умножают на 100. Например: (200— 120) :200-100 = 40%. В покое коэффициент утилизации кислорода колеблется от 30 до 40%. При тяжелой мышечной работе он повышается до 50— 60%.
Транспорт двуокиси углерода
Двуокись углерода переносится кровью в трех формах. Из венозной крови можно извлечь около 58 об. % (580 мл/л) двуокиси углерода, из них лишь около 2,5 об. % находятся в состоянии физического растворения. Остальное количество двуокиси углерода химически связано и содержится в виде кислых солей угольной кислоты (51 об. %) и
карбгемоглобина (4,5 об. %).
Двуокись углерода непрерывно образуется в клетках и диффундирует в кровь тканевых капилляров. В эритроцитах она соединяется с водой и образует угольную кислоту. Этот процесс катализируется (ускоряется в 20 000 раз) ферментом карбоангидразой. Карбоангидраза содержится в эритроцитах, в плазме крови ее нет. Поэтому гидратация двуокиси углерода происходит практически только в эритроцитах. В зависимости от напряжения двуокиси углерода карбоангидраза катализирует как образование угольной кислоты, так и расщепление ее на двуокись углерода и воду (в капиллярах легких).
Часть молекул двуокиси углерода соединяется в эритроцитах с гемоглобином, образуя карбгемоглобин.
Благодаря указанным процессам связывания напряжение двуокиси углерода в эри-
302

троцитах оказывается невысоким. Поэтому все новые количества двуокиси углерода диффундируют внутрь эритроцитов. Концентрация ионов НСОз-, образующихся при диссоциации солей угольной кислоты, в эритроцитах возрастает. Мембрана эритроцитов обладает высокой проницаемостью для анионов. Поэтому часть ионов НСОз- поступает в плазму крови. Взамен ионов HCO3- в эритроциты из плазмы входят ионы С1-, отрицательные заряды которых уравновешиваются ионами К+ В плазме крови увеличивается количество бикарбоната натрия (NaHCO3).
Накопление ионов внутри эритроцитов сопровождается повышением в них осмотического давления. Поэтому объем эритроцитов в капиллярах большого круга кровообращения несколько увеличивается.
Для связывания большей части двуокиси углерода исключительно большое значение имеют свойства гемоглобина как кислоты. Оксигемоглобин имеет константу диссоциации в 70 раз большую, чем дезоксигемоглобчн. Оксигемоглобин — более сильная кислота, чем угольная, а дезоксигемоглобин — более слабая. Поэтому в артериальной крови оксигемоглобин, вытеснивший ионы К+ из бикарбонатов, переносится в виде соли КНbО2. В тканевых капиллярах часть КНbО2 отдает кислород и превращается в КНb. Из него угольная кислота как более сильная вытесняет ионы К+:
Таким образом, превращение оксигемоглобина в гемоглобин сопровождается увеличением способности крови связывать двуокись углерода. Это явление носит название эффекта Хрлдейна. Гемоглобин служит источником катионов (К+), необходимых для связывания угольной кислоты в форме бикарбонатов.
Итак, в эритроцитах тканевых капилляров образуется дополнительное количество бикарбоната калия, а также карбгемоглобин, а в плазме крови увеличивается количество бикарбоната натрия. В таком виде двуокись углерода переносится к легким.
В капиллярах малого круга кровообращения напряжение двуокиси углерода снижается. От карбгемоглобина отщепляется СО2 Одновременно происходит образование оксигемоглобина, увеличивается его диссоциация. Оксигемоглобин вытесняет калий из бикарбонатов. Угольная кислота в эритроцитах (в присутствии карбоангидразы) быстро разлагается на Н2О и СО2. Ионы НСОз входят в эритроциты, а ионы Сl- выходят в плазму крови, где уменьшается количество бикарбоната натрия. Двуокись углерода диффундирует в альвеолярный воздух. Схематически все эти процессы представлены на рис. 153.
ОБМЕН ГАЗОВ В ТКАНЯХ
Наименьшее напряжение кислорода наблюдается в местах его потребления — митохондриях клеток, в которых кислород используется для процессов биологического окисления. Молекулы кислорода, освобождающиеся по ходу кровеносных капилляров в результате диссоциации оксигемоглобина, диффундируют в направлении более низких величин напряжения кислорода. Напряжение кислорода в тканях зависит от многих факторов: скорости тока крови, геометрии капилляров и расстояния между ними, расположения клеток по отношению к капиллярам, интенсивности окислительных процессов и т. д. В тканевой жидкости около капилляров напряжение кислорода значительно ниже (20—40 мм рт. ст.), чем в крови. Особенно низко оно в участках тканей, равноудаленных от соседних капилляров. При большой интенсивности окислительных процессов напряжение кислорода в клетках может приближаться к нулю. Увеличение скорости кровотока резко повышает напряжение кислорода в тканях. Например, увеличение скорости тока крови вдвое может повысить напряжение кислорода в нервной клетке на 10 мм рт. ст. В мышцах увеличению снабжения кислородом способствует раскрытие так называемых резервных капилляров.
Наибольшее напряжение двуокиси углерода (до 60 мм рт. ст.) отмечается в клетках в результате образования этого газа в митохондриях. В тканевой жидкости напряжение
303
двуокиси углерода изменчиво (в среднем 46 мм рт. ст.), а в артериальной крови составляет 40 мм рт. ст. Двуокись углерода диффундирует по градиенту напряжений в кровеносные капилляры и транспортируется кровью к легким.
РЕГУЛЯЦИЯ ДЫХАНИЯ
Вентиляция легких осуществляется возвратно-поступательным движением воздуха в результате периодических сокращений дыхательных мышц. Частота, сила и форма этих сокращений соответствуют потребностям организма.
Иннервация дыхательных мышц. Подобно другим скелетным мышцам, дыхательные мышцы иннервируются соматическими нервными волокнами. Если перерезать нервы, подходящие к дыхательным мышцам, последние оказываются парализованными. Например, перерезка диафрагмального нерва ведет к прекращению сокращений соответствующей половины диафрагмы. Значит, периодические сокращения дыхательных мышц вызываются импульсами, поступающими из мозга.
Мотонейроны, аксоны которых иннервируют диафрагму, находятся в спинном мозге в передних рогах серого вещества /// и IV шейных сегментов. Мотонейроны межреберных мышц и мышц живота расположены в грудных сегментах спинного мозга. Вместе с интернейронами, участвующими в координации сокращений, мотонейроны образуют спинномозговые центры дыхания (ядра дыхательных мышц).
После отделения головного мозга от спинного на уровне верхних шейных сегментов дыхательные движения прекращаются. Лишь изредка удается наблюдать слабые сокращения дыхательных мышц, но они имеют неправильные ритм и форму. Если перерезать мозг на уровне нижних шейных сегментов, дыхательная активность диафрагмы сохраняется, а межреберных мышц — прекращается. Следовательно, в регуляции дыхания принимают участие и центры головного мозга.
ДЫХАТЕЛЬНЫЙ ЦЕНТР
После перерезки мозгового ствола между средним мозгом и мостом (децеребрация) дыхание у животных в состоянии покоя существенно не нарушается. Значит, центральные механизмы, управляющие дыхательными движениями, находятся в продолговатом мозге и мосту. Совокупность сгруппированных здесь нейронов носит название бульбопонтинного дыхательного центра. После отделения моста от продолговатого мозга дыхательный ритм может сохраниться, но будет отличаться от нормального. Следовательно, важнейшие структуры дыхательного центра находятся в продолговатом мозге. Это бульбарный дыхательный центр. Его разрушение локальным повреждением полностью прекращает периодические сокращения дыхательных мышц.
Дыхательный цикл. Явления, происходящие в аппарате внешнего дыхания между началом следующих друг за другом вдохов, называются дыхательным циклом. Его длительность у человека составляет от 3 до 5 с. Все уровни дыхательного центра обеспечивают характерный рисунок (паттерн) возбуждения дыхательных мышц.
В определенный момент возникает возбуждение диафрагмальных мотонейронов (начало фазы инспирации). Это возбуждение постепенно усиливается (рис. 154) за счет увеличения частоты разрядов отдельных мотонейронов, а также вследствие вовлечения в возбуждение новых («поздних») мотонейронов (в диафрагмалвном нерве содержится около 1000 аксонов мотонейронов). При спокойном дыхании у человека возбуждение усиливается в течение 1—2,5 с. В результате сила сокращения диафрагмы постепенно возрастает. Затем возбуждение диафрагмальных мотонейронов резко ослабевает: инспирация сменяется фазой экспирации. Через 2—3,5 с наступает следующая инспирация. Как правило, длительность инспирации меньше, чем экспирации.
Возбуждение инспираторных межреберных мышц имеет рисунок возбуждения, близкий к возбуждению диафрагмы, но обычно возникает несколько позже, чем возбуждений диафрагмы.
304
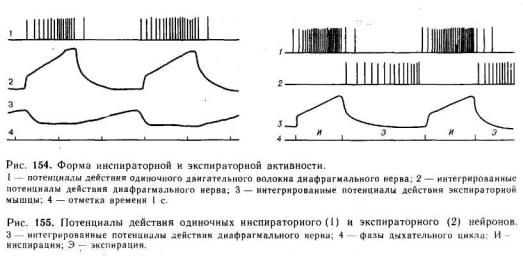
При активном выдохе возбуждение мышц живота и внутренних межреберных мышц усиливается по ходу экспирации и резко ослабевает перед началом следующей инспирации (см. рис. 154).
Дыхательные нейроны. Для установления локализации дыхательного центра использовали методы разрушения и раздражения ограниченных участков мозга. Однако основные сведения о расположении структур дыхательного центра были получены при помощи микроэлектродов путем регистрации потенциалов действия отдельных нейронов, возбуждающихся в соответствии с фазами дыхательного цикла.
Обнаружены две основные группы дыхательных нейронов — инспираторные и экспираторные. Потенциалы действия типичных инспираторных нейронов возникают за 0,1 — 0,2 с до начала вдоха. При вдохе частота разрядов постепенно увеличивается и к концу инспирации достигает 70—100 в 1 с (при сильных вдохах до 300). При смене вдоха выдохом разряды прекращаются или их частота резко уменьшается.
Частота потенциалов действия экспираторных нейронов увеличивается в течение выдоха. Прекращение разрядов или уменьшение их частоты происходит перед самым началом следующей инспирации (рис. 155).
Реже встречаются инспираторные и экспираторные нейроны, максимальная частота разрядов которых соответствует началу данной фазы дыхательного цикла («ранние» нейроны) или моменту смены дыхательных фаз (инспираторно-экспираторные и экспираторно-инспираторные нейроны).
Локализация дыхательных нейронов. В правой и левой половинах продолговатого мозга содержатся по два скопления дыхательных нейронов — дорсальные и вентральные дыхательные ядра. Ориентиром их расположения служит задвижка (обекс), находящаяся у нижнего угла ромбовидной ямки.
Дорсальное дыхательное ядро входит в состав серого вещества, окружающего одиночный пучок (ядро одиночного пучка) (рис. 156). Оно содержит преимущественно инспираторные нейроны, аксоны которых направляются в основном к диафрагмальным ядрам шейного отдела спинного мозга. Коллатерали аксонов следуют также в вентральное дыхательное ядро, образуя возбуждающие синапсы на инспираторных нейронах. Таким образом, возбуждение нейронов дорсального дыхательного ядра тормозит возбуждение экспираторных нейронов вентрального дыхательного ядра. Экспираторные нейроны в дорсальном дыхательном ядре встречаются редко (их здесь около 5%).
Вентральное дыхательное ядро имеет большую протяженность — от каудального края ядра лицевого нерва до I шейного сегмента спинного мозга. Оно включает в себя обоюдное ядро, в котором находятся мотонейроны мышц гортани и глотки. Часть вентрального ядра, расположенная латеральнее и каудальнее обоюдного ядра, называется
305

ретроамбигуальным ядром. Вентральное дыхательное ядро расположено в вентролатеральной области продолговатого мозга. В вентральном дыхательном ядре содержатся как инспираторные, так и экспираторные нейроны.
Большая часть нейронов вентрального дыхательного ядра посылает аксоны к спинномозговым ядрам дыхательных мышц, в основном межреберных мышц и мышц живота. Примерно 25% волокон разветвляется в области диафрагмальных ядер, 90% аксонов инспираторных нейронов и все аксоны экспираторных нейронов перекрещиваются в продолговатом мозге и следуют к спинномозговым ядрам в вентральном канатике и передней части бокового канатика белого вещества противоположной стороны спинного мозга. Кроме того, в вентральном дыхательном ядре имеются нейроны, аксоны которых оканчиваются в продолговатом мозге (проприобульбарные нейроны).
Небольшое количество дыхательных нейронов встречается и вне дыхательных ядер — в ретикулярной формации продолговатого мозга и моста.
Третье компактное скопление дыхательных нейронов было обнаружено у животных после перерезки блуждающих нервов в передней части моста, сразу за четверохолмием. Это скопление находится в медиальном парабрахиальном ядре (латеральнее его). При сохраненных блуждающих нервах нейроны этих ядер имеют непрерывную тоническую импульсную активность. Дыхательное ядро переднего моста носит название пневмотак-
сического центра (рис. 157). Таким образом, дыхательный центр имеет сложную нейронную структуру.
Зависимость деятельности дыхательного центра от газового состава крови
Деятельность дыхательного центра, определяющая частоту и глубину дыхания, зависит прежде всего от напряжения газов, растворенных в крови, и концентрации в ней водородных ионов. Ведущее значение в определении величины вентиляции легких имеет напряжение двуокиси углерода в артериальной крови: оно как бы создает запрос на нужную величину вентиляции альвеол.
Образование в тканях двуокиси углерода пропорционально интенсивности окислительных процессов. Количество этого газа в крови в значительной степени обусловливает ее кислотно-щелочное состояние. Отсюда следует целесообразность поддержания на постоянном уровне напряжения двуокиси углерода в артериальной крови.
Организм здорового человека в обычных условиях снабжается кислородом в достаточном (а не минимальном) количестве. Исключение составляют лишь условия напряженной физической работы. Так, парциальное давление кислорода в альвеолярном воздухе может быть снижено до 80 мм рт. ст. без заметных нарушений в организме. С другой стороны, увеличение содержания кислорода во вдыхаемом воздухе до 40% (парциальное давление 304 мм рт. ст.) также является безвредным.
Таким образом, организм наземных животных и человека в процессе эволюции приспособился к дыханию атмосферным воздухом при обычном (на уровне моря) или несколько сниженном (на небольших высотах) атмосферном давлении. При этом напряжение двуокиси углерода поддерживается на относительно постоянном уровне, при котором организм обеспечивается вполне достаточным количеством кислорода.
Для обозначения повышенного, нормального и сниженного напряжения двуокиси углерода в крови используют термины «гиперкапния», шормокапния» и "гипокапния" соответственно. Нормальное содержание кислорода называется нормоксией, а недостаток кислорода в организме и тканях — гипоксией, в крови — гипоксемией. Увеличение напряжения кислорода есть гипероксия. Состояние при котором гиперкапния и гипоксия существуют одновременно, называется асфиксией.
Нормальное дыхание в состоянии покоя называется эйпноэ. Гиперкапния, а также снижение величины рН крови (ацидоз) сопровождаются увеличением вентиляции легких — гиперпноэ, направленным на выведение из организма избытка двуокиси углерода. Вентиляция легких возрастает преимущественно за счет глубины дыхания (увеличения дыхательного объема), но при этом возрастает и частота дыхания.
Гипокапния и повышение уровня рН крови ведут к уменьшению вентиляции, а затем и к остановке дыхания — апноэ.
Развитие гипоксии вначале вызывает умеренное гиперпноэ (в основном в результате возрастания частоты дыхания), которое при увеличении степени гипоксии сменяется ослаблением дыхания и его остановкой. Апноэ вследствие гипоксии смертельно опасно. Его причиной является ослабление окислительных процессов в мозге, в том числе в нейронах дыхательного центра. Гипоксическому апноэ предшествует потеря сознания.
Гиперкапнию можно вызвать вдыханием газовых смесей с повышенным до 6% содержанием двуокиси углерода. Деятельность дыхательного центра человека находится под произвольным контролем. Произвольная задержка дыхания на 30—60 с вызывает асфиктические изменения газового состава крови, после прекращения задержки наблюдается гиперпноэ. Гипокапнию легко вызвать произвольным усилением дыхания, а также избыточной искусственной вентиляцией легких (гипервентиляция). У бодрствующего человека даже после значительной гипервентиляции остановки дыхания обычно не возникает вследствие контроля дыхания передними отделами мозга. Гипокапния компенсируется постепенно, в течение нескольких минут.
Гипоксия наблюдается при подъеме на высоту вследствие снижения атмосферного давления, при крайне тяжелой физической работе, а также при нарушениях дыхания, кровообращения и состава крови.
307
Во время сильной асфиксии дыхание становится максимально глубоким, в нем принимают участие вспомогательные дыхательные мышцы, возникает неприятное ощущение удушья. Такое дыхание называется диспноэ.
В целом поддержание нормального газового состава крови основано на принципе отрицательной обратной связи. Так, гиперкапния вызывает усиление активности дыхательного центра и увеличение вентиляции легких, а гипокапния — ослабление деятельности дыхательного центра и уменьшение вентиляции.
Роль хеморецепторов в регуляции дыхания
Давно установлено, что деятельность дыхательного центра зависит от состава крови, поступающей в мозг по общим сонным артериям.
Это было показано Фредериком (1890) в опытах с перекрестным кровообращением. У двух собак, находившихся под наркозом, перерезали и соединяли перекрестно сонные артерии и отдельно яремные вены (рис. 158). После такого соединения и перевязки позвоночных артерий голова первой собаки снабжалась кровью второй собаки, голова второй собаки — кровью первой. Если у одной из собак, например у первой, перекрывали трахею и вызывали таким путем асфиксию, то гиперпноэ развивалось у второй собаки. У первой же собаки, несмотря на увеличение в артериальной крови напряжения двуокиси углерода и снижение напряжения кислорода, через некоторое время наступало апноэ. Это объясняется тем, что в сонную артерию первой собаки поступала кровь второй собаки, у которой в результате гипервентиляции в артериальной крови снижалось напряжение двуокиси углерода.
Двуокись углерода, водородные ионы и умеренная гипоксия вызывают усиление дыхания, действуя не непосредственно на нейроны дыхательного центра. Возбудимость дыхательных нейронов, как и других нервных клеток, под влиянием этих факторов снижается. Следовательно, эти факторы усиливают деятельность дыхательного центра, оказывая влияние на специальные хеморецепторы. Имеется две группы хеморецепторов,
регулирующих дыхание: периферические (артериальные) и центральные (медуллярные).
Артериальные хеморецепторы. Хеморецепторы, стимулируемые увеличением напряжения двуокиси углерода и снижением напряжения кислорода, находятся в каротидных синусах и дуге аорты. Они расположены в специальных маленьких тельцах, обильно снабжаемых артериальной кровью. Важными для регуляции дыхания являются каротидные хеморецепторы. Аортальные хеморецепторы на дыхание влияют слабо и имеют большее значение для регуляции кровообращения.
Каротидные тельца расположены в развилке общей сонной артерии на внутреннюю и наружную. Масса каждого каротидного тельца всего около 2 мг. В нем содержатся относительно крупные эпителиоидные клетки I типа, окруженные мелкими интерстициальными клетками II типа. С клетками I типа контактируют окончания афферентных волокон синусного нерва (нерва Геринга), который является ветвью языкоглоточного нерва. Какие структуры тельца — клетки I или II типа либо нервные волокна — являются собственно рецепторами, точно не установлено.
Хеморецепторы каротидных и аортальных телец являются уникальными рецепторными образованиями, на которые гипоксия оказывает стимулирующее влияние. Афферентные сигналы в волокнах, отходящих от каротидных телец, можно зарегистрировать и при нормальном (100 мм рт. ст.) напряжении кислорода в артериальной крови. При снижении напряжения кислорода от 80 до 20 мм рт. ст. частота импульсов увеличивается особенно значительно.
Кроме того, афферентные влияния каротидных телец усиливаются при повышении в артериальной крови напряжения двуокиси углерода и концентрации водородных ионов. Стимулирующее действие гипоксии и гиперкапнии на данные хеморецепторы взаимно усиливается. Наоборот, в условиях гипероксии чувствительность хеморецепторов к двуокиси углерода резко снижается.
Хеморецепторы телец особенно чувствительны к колебаниям газового состава крови. Степень их активации возрастает при колебаниях напряжения кислорода и двуокиси
308

углерода в артериальной крови даже в зависимости от фаз вдоха и выдоха при глубоком и редком дыхании.
Чувствительность хеморецепторов находится под нервным контролем. Раздражение эфферентных парасимпатических волокон снижает чувствительность, а раздражение симпатических волокон повышает ее
Хеморецепторы (особенно каротидных телец) информируют дыхательный центр о напряжении кислорода и двуокиси углерода в крови, направляющейся к мозгу.
Центральные хеморецепторы. После денервации каротидных и аортальных телец исключается усиление дыхания в ответ на гипоксию. В этих условиях гипоксия вызывает только снижение вентиляции легких, но зависимость деятельности дыхательного центра от напряжения двуокиси углерода сохраняется. Она обусловлена функцией центральных хеморецепторов.
Центральные хеморецепторы были обнаружены в продолговатом мозге латеральнее пирамид (рис. 159). Перфузия этой области мозга раствором со сниженным рН резко усиливает дыхание. Если рН раствора увеличить, то дыхание ослабевает (у животных с денервированными каротидными тельцами останавливается на выдохе, наступает апноэ). То же присходит при охлаждении или обработке местными анестетиками этой поверхности продолговатого мозга.
Хеморецепторы расположены в тонком слое мозгового вещества на глубине не более 0,2 мм. Обнаружены два рецептивных поля, обозначаемые буквам М и L. Между ними находится небольшое поле S. Оно нечувствительно к концентрации ионов Н+, но при его разрушении исчезают эффекты возбуждения полей М и L. Вероятно, здесь проходят афферентные пути от сосудистых хеморецепторов к дыхательному центру.
В обычных условиях рецепторы продолговатого мозга постоянно стимулируются ионами Н+, находящимися в спинномозговой жидкости. Концентрация Н+ в ней зависит от напряжения двуокиси углерода в артериальной крови, она увеличивается при гиперкапнии.
Центральные хеморецепторы оказывают более сильное влияние на деятельность дыхательного центра, чем периферические. Они существенно изменяют вентиляцию легких. Так, снижение рН спинномозговой жидкости на 0,01 сопровождается увеличением вентиляции легких на 4 л/мин.
309
Вместе с тем центральные хеморецепторы реагируют на изменение напряжения двуокиси углерода в артериальной крови позже (через 20—30 с), чем периферические хеморецепторы (через 3—5 с). Указанная особенность обусловлена тем, что для диффузии стимулирующих факторов из крови в спинномозговую жидкость и далее в ткань мозга необходимо время.
Сигналы, поступающие от центральных и периферических хеморецепторов, являются необходимым условием периодической активности дыхательного центра и соответствия вентиляции легких газовому составу крови. Импульсы от центральных хеморецепторов усиливают возбуждение как инспираторных, так и экспираторных нейронов дыхательного центра продолговатого мозга.
Роль механорецепторов в регуляции дыхания
Рефлексы Геринга и Брейера. Смене дыхательных фаз, т. е. периодической деятельности дыхательного центра, способствуют сигналы, поступающие от механорецепторов легких по афферентным волокнам блуждающих нервов. После перерезки блуждающих нервов, выключающей эти импульсы, дыхание у животных становится более редким и глубоким. При вдохе инспираторная активность продолжает нарастать с прежней скоростью до нового, более высокого уровня (рис. 160). Значит афферентные сигналы, поступающие от легких, обеспечивают смену вдоха на выдох раньше, чем это делает дыхательный центр, лишенный обратной связи с легкими. После перерезки блуждающих нервов удлиняется и фаза выдоха. Отсюда следует, что импульсы от рецепторов легких способствуют и смене выдоха вдохом, укорачивая фазу экспирации.
Геринг и Брейер (1868) сильные и постоянные дыхательные рефлексы обнаружили при изменениях объема легких. Увеличение объема легких вызывает три рефлекторных эффекта. Во-первых, раздувание легких при вдохе может его преждевременно прекратить (инспираторно-тормозящий рефлекс). Во-вторых, раздувание легких при выдохе задерживает наступление следующего вдоха, удлиняя фазу экспирации (экспираторно-облег- чающий рефлекс). В-третьих, достаточно сильное раздувание легких вызывает короткое (0,1—0,5 с) сильное возбуждение инспираторных мышц, возникает судорожный вдох —
«вздох» (парадоксальный эффект Хэда).
Уменьшение объема легких обусловливает усиление инспираторной активности и укорочение выдоха, т. е. способствует наступлению следующего вдоха (рефлекс на спадение легких).
Таким образом, деятельность дыхательного центра зависит от изменений объема легких. Рефлексы Геринга и Брейера обеспечивают так называемую объемную обратную связь дыхательного центра с исполнительным аппаратом дыхательной системы.
Значение рефлексов Геринга и Брейера состоит в регулировании сортношения глубины и частоты дыхания в зависимости от состояния легких. При сохраненных блуждающих нервах гиперпноэ, вызываемое гиперкапнией или гипоксией, проявляется увеличением как глубины, так и частоты дыхания. После выключения блуждающих нервов учащения дыхания не происходит, вентиляция легких постепенно растет только вследствие увеличения глубины дыхания. В результате максимальная величина вентиляции легких оказывается сниженной приблизительно вдвое. Таким образом, сигналы от рецепторов легких обеспечивают повышение частоты дыхания при гиперпноэ, наступающем при гиперкапнии и гипоксии.
Увзрослого человека в отличие от животных значение рефлексов Геринга и Брейера
врегуляции спокойного дыхания невелико. Временная блокада блуждающих нервов местными анестетиками не сопровождается существенным изменением частоты и глубины дыхания. Однако увеличение частоты дыхания при гиперпноэ у человека, как и животных, обеспечивается рефлексами Геринга и Брейера: это увеличение выключается блокадой блуждающих нервов.
Рефлексы Геринга и Брейера хорошо выражены у новорожденных. Эти рефлексы играют важную роль в укорочении дыхательных фаз, в особенности выдохов. Величина
310
