
2 курс / Нормальная физиология / Общий_курс_физиологии_человека_и_животных_Том_1_Ноздрачев_А_Д_,
.pdf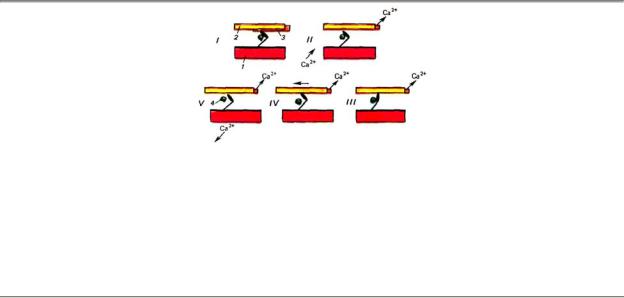
показано, что амплитуда этих движений составляет 20 нм, а частота — 5—50 колебаний/с. Каждый мостик то прикрепляется и тянет нить, то открепляется и «ждет» условий для нового прикрепления. Но огромное множество мостиков работает «вразнобой» и поэтому их общая тяга оказывается равномерной во времени. Разнообразные исследования привели к следующему представлению о механизме циклической работы миозинового мостика.
В покое мостик заряжен энергией (миозин фосфорилирован), но он не может соединиться с нитью актина, ибо между ними вклинена система из нити тропомиозина и глобулы тропонина (рис. 1.42).
Рис. 1.42. Работа головки миозина (актомиозинового мостика): I — в покое головка миозина (1)
фосфорилирована, но ее взаимодействие с актином (2) запрещено гропонин-тропомиозиновым комплексом (3); II — при возбуждении волокна и росте концентрации кальция в миоплазме последний связывается с тропонином. Тропонин «отводит» тропомиозин в сторону, разрешая взаимодействие фосфорилмиозина с актином; III—IV — при взаимодействии фосфорилмиозина с актином головка миозина «нагибается», перемещая нить актина; при этом тратится энергия и фосфорилмиозин распадается на миозин, АДФ и фосфат (не показано); V — при наличии свободного АТФ в среде головка миозина отрывается от актина; далее происходит фосфорилирование миозина и его блокировка системой тропонин-тропомиозина из-за ухода Са2+ в саркоплазматический ретикулум
При активации мышечного волокна и появлении в миоплазме ионов Са2+ (в присутствии АТФ) тропонин изменяет свою конформацию и отодвигает нить тропомиозина, открывая для миозиновой головки возможность соединения с актином. Соединение головки фосфорилированного миозина с актином приводит к резкому изменению конформации мостика (его «сгибанию») и перемещению нити актина на один шаг (20 нм) с последующим разрывом мостика. Энергию на этот акт дает распад макроэргической фосфатной связи, включенной в фосфорилактомиозин.
После этого в силу падения локальной концентрации Са2+ и отсоединения его от тропонина тропомиозин снова блокирует актин, а миозин снова фосфорилируется за счет АТФ. Последний не только заряжает системы для дальнейшей работы, но и способствует временному разобщению нитей, т. е. пластифицирует мышцу, делает ее способной растягиваться под влиянием внешних сил. Полагают, что на одно рабочее движение одного мостика тратится одна молекула АТФ, причем роль АТФазы играет актомиозин
(в присутствии ионов Mg2+ и Са2+). Всего при одиночном сокращении тратится 0,3 мкМ АТФ на 1 г мышцы.
Необходимо еще раз подчеркнуть, что АТФ играет в мышечной работе двоякую роль: фосфорилируя миозин, он обеспечивает энергией сокращение, но, находясь в свободном состоянии, он обеспечивает и расслабление мышцы (ее пластификацию). При исчезновении АТФ из миоплазмы развивается непрерывное сокращение — контрактура.
Все эти феномены могут быть продемонстрированы и на изолированных актомиозиновых комплексах-нитях. Такие нити без АТФ твердеют (ригор), при добавлении АТФ — расслабляются, а при добавлении еще и Са2+ производят обратимое сокращение, аналогичное нормальному.
1.2.5. Механика мышцы
Различают два режима сократительной деятельности мышц: изотонический (когда мышца укорачивается при неизменном внутреннем напряжении, что, например, бывает при небольшой величине поднимаемого груза) и изометрический (при этом режиме мышца не укорачивается, а лишь развивает внутреннее напряжение, что бывает при ее закреплении с обоих концов и при нагрузке неподъемным грузом). Кроме того, различают два основных вида мышечных сокращений: одиночные и тетанические.
Одиночные сокращения (или напряжения) возникают при действии на мышцу одиночного нервного импульса или краткого толчка тока.
При этом в миоплазме мышцы происходит кратковременный подъем концентрации Са2+ВН, сопровождаемый кратковременной работой — тягой мостиков, сменяющейся снова покоем. В изометрическом режиме одиночное напряжение начинается через 2 мс после пика ПДм, причем напряжению предшествует краткое и незначительное так называемое латентное расслабление, создаваемое выходом Са2+ из саркоплазматического ретикулума, что приводит к потере ретикулумом тургора. В портняжной мышце лягушки одиночное напряжение достигает максимума за 0,15—0,20 с. и далее спадает экспоненциально за 0,7—0,8 с. В изотоническом режиме одиночное сокращение портняжной мышцы лягушки имеет фазу подъема 0,05 с и фазу спада 0,05 с. Мышца укорачивается на 5—10% длины покоя.
Тетанус возникает при ритмической стимуляции мышцы с частотой более 10 имп./с. При этом происходит слияние и наложение (суперпозиция) одиночных сокращений (напряжений).
Общая величина укорочения (и напряжения) при этом растет и тем больше, чем чаще нервная активация. Это продолжается до известных пределов, так как при чрезмерной частоте нервных импульсов развивается частичный блок в синапсе, так называемый пессимум (по Н. Е. Введенскому). Укорочение мышцы в состоянии оптимального тетануса составляет 20%. Напряжение оптимального изометрического тетануса 50 Н/см2, что превосходит напряжение одиночного рывка.
Суперпозиция одиночных сокращений и рост напряжения при тетанусе отчасти объясняются накоплением Са2+ в миоплазме. Однако в мышце лягушки при частоте стимуляции 10 имп./с накопления Са2+ в миоплазме еще нет (рис. 1.43), а явная суперпозиция одиночных напряжений наблюдается. Можно полагать, что в этом случае суперпозиция одиночных напряжений связана с использованием механической инерции в системе, для преодоления которой одного краткого рывка недостаточно. Видимо, напряжение, развиваемое в сухожилии, запаздывает по отношению к усилию, создаваемому сократительным механизмом.
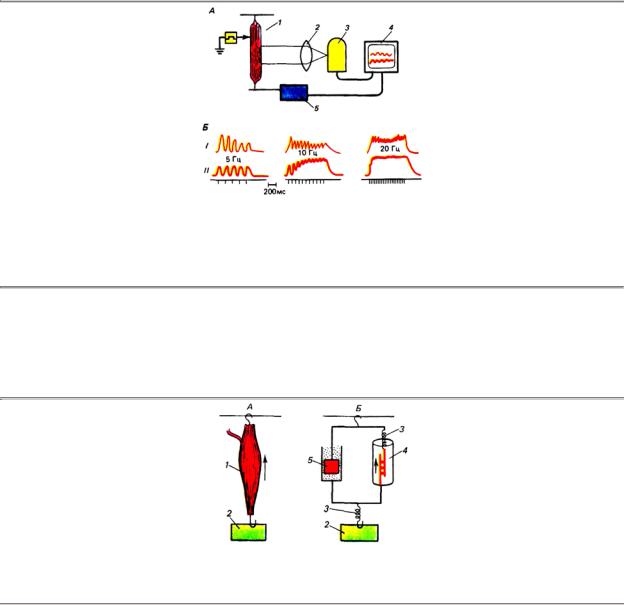
Рис. 1.43. Соотношение изометрических сокращений мышцы и изменений концентрации Са2+ в
миоплазме. А — схема одновременной регистрации концентрации Са2+ в миоплазме по свечению введенного в нее экворина и сокращений мышечного волокна; Б — записи изменения концентрации Са2+ (I) и мышечных сокращений (II) при разных частотах стимуляции: 1 — мышечное волокно, в которое введен экворин, 2 — линза, 3 — фотоумножитель, 4 — осциллограф, 5 — регистратор силы
Работа сократительного механизма (актомиозиновых мостиков) в разных условиях. Сократительный аппарат миофибрилл подключен последовательно к эластическому элементу (сухожилию) и, кроме того, имеет параллельно включенный пластический вязкостный элемент (рис. 1.44). У покоящейся мышцы вязкость мала, а у возбужденной велика (зацепление мостиков).
Рис. 1.44. Соотношение сократительного, эластического и вязкого компонентов мышцы. А — мышца
(1) с грузом (2); Б — эквивалентная схема мышцы: 3 — эластический элемент (сухожи-лие и т. п.), 4 — сократительный элемент (система мостиков, тянущих нити), 5 — вязкий элемент
В изометрическом режиме активности работа мостиков приводит лишь к растяжению и напряжению эластического элемента. Эта работа может быть изображена как ритмическое микроперемещение тонких нитей мостиками к центру саркомера, каждый раз сопровождаемое возвратом в исходное состояние за счет эластической силы. Общая сила мышцы FM при этом пропорциональна силе элементарного рывка (мостика) FЭ и числу работающих мостиков N при постоянной средней частоте их срабатывания: FM = FЭN. Зависимость FM от числа работающих мостиков демонстрируется в опыте с оценкой FM изометрических напряжений при разной исходной длине мышцы (саркомеров) l. Оказывается, что если мышца перерастянута так, что тонкие и толстые нити ее саркомеров не перекрываются, то FM = 0. По мере приближения к натуральной длине покоя l0, при которой все головки миозиновых нитей могут контактировать с актиновыми нитями, FM растет до максимума. Но при дальнейшем уменьшении l ввиду «заползания» тонких нитей в соседние саркомеры и уменьшения возможной амплитуды их перемещения, а значит, и снижения растяжения эластического элемента внешняя FM падает снова (рис. 1.45).
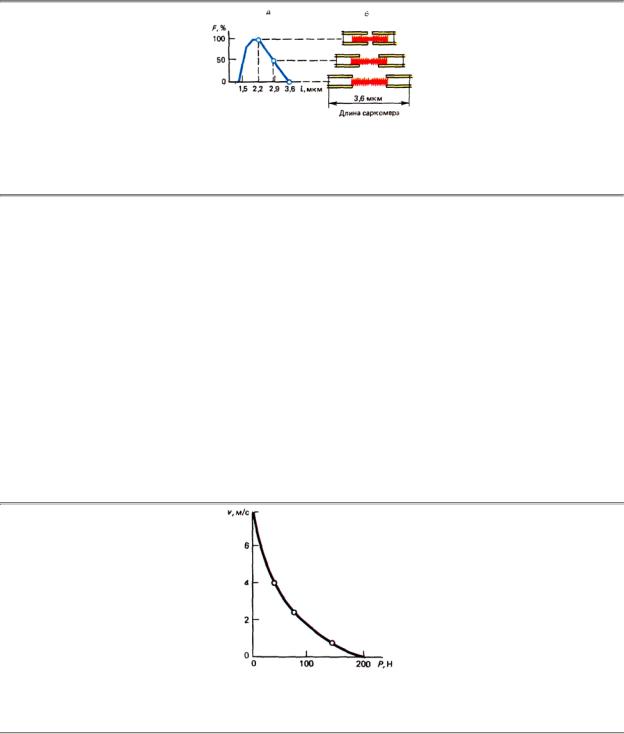
Рис. 1.45. Зависимость силы F максимального изометрического тетануса волокна от заданной длины l саркомера (А) и объяснение этой зависимости разным количеством актомиозиновых мостиков, формирующихся при различной степени растяжения волокна и соответственно перекрытия толстых и тонких нитей (Б)
Внешняя механическая работа мышцы (А) возможна только в изотоническом режиме с грузом при условии, что вес груза Р< FM. В этом случае сократительный аппарат сначала растягивает и напрягает эластический элемент — сухожилие, а затем поднимает подвешенный к нему груз Р.
При подъеме разных грузов на одну и ту же высоту от подпорки до упора, например в условиях тетанической активации мышцы, чем больше груз, тем он медленнее поднимается (рис. 1.46), т. е. тем большее время тратится на эту работу. При постоянных средней частоте работы мостиков, FЭ и N это означает, естественно, и большую трату энергии, что соответствует и большей внешней механической работе. Внешняя механическая работа мышцы по подъему груза Р на высоту h, как уже отмечалось, исчисляется по формуле:
А = Ph = Р 1,
где 1 — укорочение мышцы. Заметим, что при Р = 0 А = 0 и что при Р ≥ P0, Т. е. при неподвижности груза, А тоже равна нулю. Внешняя механическая работа мышцы максимальна при средних нагрузках. Это называют законом средних нагрузок.
Рис. 1.46. Соотношение между нагрузкой Р и скоростью v укорочения мышцы (для руки человека) При данной мощности мышцы, чем тяжелее поднимаемый груз, тем ниже скорость его подъема, т. е. укорочения мышцы (объяснение см. в тексте)
Если мышца предварительно растянута, то ее пассивное напряжение добавляется к активному, возникающему при возбуждении, но последнее (по рассмотренным выше причинам) при чрезмерном растяжении падает до нуля (рис. 1.47).
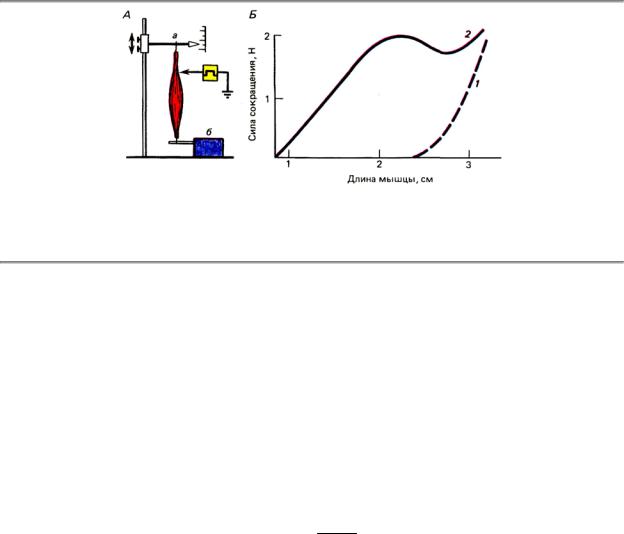
Рис. 1.47. Соотношение между силой изометрического сокращения и задаваемой длиной мышцы. А — схема опыта; Б — графическое отражение измеряемых соотношений: 1 — пассивное напряжение растягиваемой мышцы в покое, 2 — общая сила, развиваемая мышцей при максимальном тетанусе; а — предварительное растяжение, б — регистратор силы
1.2.6. Энергетика мышцы
Энергетические источники для сокращения и коэффициент полезного действия мышцы. Энергетическим источником для мышечного сокращения по существу является АТФ. Источником энергии и материала для ресинтеза АТФ являются распад креатинфосфата, анаэробный гликолиз и окислительное фосфорилирование субстратов
(в митохондриях).
Необходимо заметить, что и хемомеханическая реакция в системе актомиозиновых мостиков, и все последующие процессы идут с потерей энергии в форме теплоты. Коэффициент полезного действия (КПД) мышцы как механической машины (здесь надо оговориться, что мышца не только механическая машина, но и основной обогреватель организма, поэтому ее тепловой выход не бесполезен) может быть вычислен по формуле:
КПД = A A +Q
Тепловой выход мышцы (Q) сложен. Во-первых, существует выход теплоты при изометрическом напряжении мышцы, при задержке ее сокращения стопором. Этот выход (Q1) называют теплотой активации. Если на фоне этого состояния мышца с грузом освобождается от стопора и, сокращаясь, поднимает груз, то она выделяет дополнительную теплоту (Q2) — теплоту укорочения, пропорциональную механической работе (эффект Фенна). По-видимому, перемещение нитей с подключением в работу все новых (заряженных энергией) мостиков способствует высвобождению дополнительной энергии (и механической, и тепловой).
В условиях свободного подъема груза теплота активации (соответствующая фазе напряжения сухожилия) и теплота укорочения сливаются, образуя так называемое начальное теплообразование. После сокращения (одиночного или краткого тетануса) в мышце возникает задержанное теплообразование, которое связано с процессами, обеспечивающими ресинтез АТФ, оно длится секунды и даже минуты. Если рассчитывать КПД мышцы по начальному теплообразованию, то он составит примерно 50—60% (для оптимальных условий стимуляции и нагрузки). Если же вести расчет КПД исходя из всех видов теплопродукции, связанных с данной механической работой, то КПД составит примерно 20—30% (КПД мышц млекопитающих падает при адаптации к холоду, что способствует усилению теплопродукции в организме).
Кислородная задолженность и утомление. Известно, что 1 моль АТФ дает 48 кДж энергии и что для ресинтеза 1М АТФ нужно 3 моля кислорода. В условиях срочной мышечной работы человека (бег на короткую дистанцию, прыжок, подъем штанги)
запасов O2 в организме не хватает для немедленного ресинтеза АТФ. Такая работа обеспечивается за счет мобилизации энергии анаэробного распада креатинфосфата и гликогена. В итоге в организме накапливается много недоокисленных продуктов (молочной кислоты и др.). Создается кислородная задолженность. Такой долг погашается после работы за счет автоматической мобилизации дыхания и кровообращения (одышка и усиленное сердцебиение после работы). Если же работа, несмотря на наличие кислородного долга, продолжается, то наступает тяжелое состояние (утомление), которое иногда прекращается при достаточной мобилизации дыхания и кровообращения (второе дыхание спортсменов).
В естественных условиях утомление развивается, прежде всего, как отказ от работы аппаратов ЦНС. При этом электрическое раздражение мышц выявляет их дееспособность. Но и изолированные мышцы, а также децентрализованные мышцы в организме при их прямой стимуляции или стимуляции соответствующего нерва работают не бесконечно. Они тоже утомляются. С разной скоростью утомляются так называемые быстрые и медленные мышцы, имеющие разный тип энергетического обеспечения. Волокна быстрых фазных мышц, например портняжной мышцы лягушки или длинного разгибателя пальцев крысы, богаты гликогеном, но имеют мало митохондрий и практически не содержат миоглобина (аналог гемоглобина крови, депонирующий кислород). Они работают на энергетической основе анаэробного цикла реакций, а значит, быстро, но недолго. Эти мышцы быстро утомляются. Волокна медленных мышц с одиночной иннервацией, генерирующих ПД, например камбаловидной мышцы крысы, наоборот, бедны гликогеном, но богаты митохондриями и миоглобином, придающим им красный цвет. Эти мышцы при работе используют главным образом энергию аэробных реакций. Они особенно хорошо кровоснабжаются и могут работать долго без утомления.
Специальные тонические мышечные волокна, имеющие множественную иннервацию и работающие на основе низкочастотного локального возбуждения (ПСП), вообще слабы и соответственно тратят мало энергии. Поэтому при небольшом энергетическом обеспечении (в них относительно мало гликогена и митохондрий) они могут долго работать.
Утомление изолированных скелетных мышц, выражающееся в снижении их силы и далее в отказе от функции, имеет в качестве своей основной причины накопление в мышцах (внутри волокон и в межклеточных щелях) ряда продуктов метаболизма, прежде всего молочной кислоты (L-лактата), а также Н3РО4. Эти вещества нарушают функции мышечных и нервных элементов и в особенности нервно-мышечную передачу. В свою очередь, накопление L-лактата (недоокисленного продукта) зависит от нехватки О2. Что касается энергетических ресурсов мышцы (гликогена, креатинфосфата), то они при обычных условиях утомления не исчерпываются.
1.2.7. Особенности мышцы сердца позвоночных
Сердце у позвоночных построено из вытянутых одноядерных мышечных клеток — кардиомиоцитов, обладающих поперечной исчерченностью. Таким образом, мышца сердца является поперечно-полосатой.
Важной особенностью строения мышцы сердца является то, что кардиомиоциты связаны между собой низкоомными электрическими контактами — нексусами. Таким образом, масса кардиомиоцитов в конечном счете образует функциональную единицу, что важно для выполнения сердцем функции насоса.
Электрическое раздражение любой точки сердца в силу этих связей вызывает электрическую и сократительную реакцию всех его мышечных клеток. Поэтому сердце (в отличие от скелетной мышцы, включающей много независимых ДЕ) отвечает на электрическое раздражение как единица по правилу «все или ничего».
В естественных условиях стимул к сокращению сердца возникает в самом сердце,

точнее в специфических мышечных клетках синусного узла (у млекопитающих он находится в правом предсердии). В этих клетках строго периодически наблюдается спонтанная деполяризация (из-за роста РNа), приводящая к развитию ПД. Отсюда ПД распространяется по мышечным элементам предсердий и далее через мышечные клетки атриовентрикулярного узла и пучка Гиса к мышце желудочка (подробнее см. разд. 8.1.3).
Потенциал действия кардиомиоцитов предсердий имеет большую длительность, чем в скелетно-мышечных волокнах. Но особенно длительны ПД в кардиомиоцитах желудочков сердца. У этих ПД проявляется обычный крутой подъем с овершутом, но затем обнаруживается плато (на уровне, близком к пику ПД). Длительность этого плато, например, в мышце сердца собаки, составляет около 250 мс. Затем ПД быстро компенсируется (табл. 1.5).
Ионный механизм ПД волокон сердца позвоночных состоит в быстрой активации деполяризующим стимулом натриевых каналов и натрий-кальциевых каналов при параллельной инактивации части калиевых каналов (это особое свойство К+-каналов данного объекта). Последующая инактивация каналов входящих токов (Na-Ca-каналов) происходит медленно. И поэтому активация части К-каналов здесь задержана на многие десятки (сотни) миллисекунд удерживающейся деполяризацией. Лишь при достижении определенного МП начинается открытие массы К-каналов и спад (завершение) ПД. Такая организация ПД клеток желудочка сердца обеспечивает их относительно длительное сокращение (250—300 мс), что необходимо для выполнения функции нагнетательного насоса. Длительность ПД кардиомиоцитов определяет длительную абсолютную рефрактерную фазу сердца.
Таблица 1.5 Величины МПП и ПД в некоторых поперечно-полосатых мышечных волокнах позвоночных
Объект |
МПП, мВ |
АПД, мВ |
tПД. мс |
|
Скелетно- |
|
|
|
|
мышечное |
—90 |
120 |
2,5 |
|
волокно лягушки |
|
|
|
|
Мышечное |
|
|
|
|
волокно |
—80 |
100 |
250,0 |
|
желудочка |
||||
|
|
|
||
сердца собаки |
|
|
|
|
|
|
|
|
Суммарная электрическая активность сердца позвоночных и человека представляет собой ритмическое повторение комплекса колебаний, включающего зубцы Р, Q, R, S, Т (см. разд. 8.3).
Электромеханическая связь в сердечно-мышечных элементах в общем подобна описанной в скелетных мышцах позвоночных. Особенность состоит лишь в том, что источником ионов Са2+ здесь лишь отчасти является саркоплазматический ретикулум (развитый относительно слабо), остальной Са2+ поступает в возбужденные кардиомиоциты извне. Сократительный механизм сердечно-мышечных волокон позвоночных подобен скелетно-мышечному. Зависимость силы напряжения мышцы сердца от исходной длины ее волокон имеет тот же характер, что и в скелетной мышце
(см. рис. 1.47).
Для желудочков сердца как нагнетательных насосов, открывающих выходные клапаны давлением на заключенную в полости желудочков кровь, важно, что их предварительное пассивное растяжение поступающей кровью усиливает общее напряжение при активном сокращении. На этой основе осуществляется саморегуляция сердечной функции — усиление выброса крови при усилении ее притока (закон Старлинга).
Сердечная мышца позвоночных работает автоматически, т. е. без приказов из ЦНС. Однако сердце имеет симпатическую (норадренэргическую) и парасимпатическую (холинэргическую) иннервацию, обеспечивающую центральный контроль ритма и силы сердечной деятельности. Подробности нервной регуляции сердца рассматриваются далее.

1.2.8. Общая физиология гладких мышц позвоночных
Гладкие мышцы позвоночных, формирующие мышечные слои стенок желудка, кишечника, мочеточников, бронхов, кровеносных сосудов и других внутренних органов, построены из веретенообразных одноядерных мышечных клеток. Толщина этих клеток колеблется от 2 до 10 мкм, длина — от 50 до 400 мкм. Отдельные клетки в гладких мышцах связаны между собой низкоомными электрическими контактами — нексусами. В гладкомышечных клетках имеются такие же миофибриллы с саркомерами, как и в поперечнополосатых. Однако эти структуры расположены в гладкомышечной клетке нерегулярно, почему сама эта клетка (волокно) и не имеет поперечной исчерченности. Гладкие мышцы иннервируются парасимпатическими и симпатическими нервами, а также метасимпатической нервной сетью (см. разд. 5.4.3). Однако не все гладкомышечные клетки иннервированы; многие из них контролируются нервной системой не прямо, а косвенно через другие гладкомышечные клетки.
Среди гладкомышечных клеток есть пейсмекерные14, генерирующие спонтанные ПД кальциевой природы с овершутами. Непосредственной причиной этих ПД является спонтанная медленная деполяризация мембраны (препотенциал). Периодически возникающие ПД пейсмекерных клеток, распространяясь по прочей массе мышечных клеток (со скоростью 5—10 см/с), создают миогенный гпонус гладких мышц (см. разд. 8.5).
Каждый ПД сам по себе вызывает одиночное сокращение гладкомышечной клетки, длящееся несколько секунд. Тетанус в этой системе возникает при очень низких частотах ПД. Периодическое изменение частоты ПД пейсмекерных клеток (под влиянием нервной системы или других факторов) создает колебания миогенного тонуса и более сложные формы двигательной активности гладких мышц. Важно отметить, что гладкомышечные клетки, будучи растяжимыми и пластичными, могут при определенной степени растяжения деполяризоваться и отвечать на это растяжение сокращением. Данный феномен лежит в основе периферической саморегуляции тонуса гладких мышц, сосудов,
мочевого пузыря и других органов.
Описанная форма миогенной активности и периферической саморегуляции не в равной мере свойственна всем гладким мышцам. В гладких мышцах цилиарного тела, радужной оболочки глаза, артерий и семенных протоков, имеющих более мощную (плотную) иннервацию и слабое развитие межклеточных (электрических) контактов, тонус и его колебания имеют в основном нейрогенную природу.
Электромеханическое сопряжение в гладких мышцах осуществляется с помощью ионов Са2+, поступающих и снаружи, и из внутриклеточных депо. Но Са-насос саркоплазматического ретикулума здесь слаб, что отчасти объясняет медленное расслабление гладкой мышцы. Сокращение гладкой мышцы начинается при [Са2+]вн>10-8 моль/л.
Однако инициация сокращения ионами Са2+ здесь имеет несколько иной механизм, чем в поперечно-полосатых волокнах.
Ионы Са2+ воздействуют на белок кальмодулин, который активирует киназы легких цепей миозина. Это приводит к переносу фосфатной группы с АТФ на миозин и вызывает сокращение (срабатывание мостиков). О существовании здесь тропонин-тропомиозиновой системы сведений не имеется. При удалении Са2+ из миоплазмы (концентрация Са2+ ниже 10-8 моль/л) фосфатаза дефосфорилирует миозин и он теряет способность связываться с актином.
Сила сокращения гладких мышц позвоночных сравнима с силой сокращения (напряжения) поперечно-полосатых мышц и равна 30—40 Н/см2, но скорость сокращения, как уже отмечалось, на 1—2 порядка ниже. Трата энергии гладкими мышцами (при той же силе напряжения) в 100—500 раз меньше, чем у поперечнополосатых мышц. Последнее, видимо, связано с особой организацией сократительного акта.
14 От англ. pacemaker — задающий темп, водитель ритма
1.2.9.Характеристика некоторых мышц беспозвоночных
Убеспозвоночных, как и у позвоночных, существуют поперечно-полосатые мышцы, управляющие скелетом (крыльями, конечностями), а также сердечная и гладкие мышцы, обеспечивающие работу соответствующих внутренних органов. У кольчатых червей и моллюсков имеется сходная с поперечно-полосатой «косоисчерченная» мускулатура.
Поперечно-полосатые мышцы скелета у беспозвоночных, например у членистоногих, как правило, имеют помимо моторной (возбуждающей) еще и тормозящую иннервацию. Моторная иннервация мышечного волокна здесь осуществляется с помощью множества синапсов одного мотонейрона. Более того, все волокна мышцы могут получать эту иннервацию от одного мотонейрона, т. е. быть одной нейромоторной единицей («экономия» нервных элементов).
Иногда имеется два возбуждающих аксона (нейрона) — быстрый и медленный, различающиеся по силе действия и соответственно по скорости вызываемой мышечной реакции. Тормозная иннервация здесь также осуществляется множеством синапсов одного нейрона. Медиатором моторных нервов у раков и насекомых является L-глутамат, медиатором торможения — ГАМК.
В мышцах конечностей у ракообразных и насекомых электромеханическая связь и сократительный акт организованы в основном так же, как у позвоночных. Здесь, как и у позвоночных, при активности число одиночных сокращений равно числу моторных нервных импульсов (и числу ПД мышечного волокна). Отсюда название всех таких мышц
—мышцы синхронного действия.
Наиболее быстрые летательные мышцы у некоторых насекомых (мухи, шмели, жуки)
имеют особую организацию (их иногда называют фибриллярными, так как миофибриллы здесь чрезвычайно толсты).
Эти мышцы являются мышцами асинхронного действия. Они производят серию одиночных сокращений с очень высокой частотой (до 300 в 1 с), значительно (на порядок) превосходящей частоту порождающих их моторных нервных импульсов и мышечных ПД.
Сокращения относительно слабы (3 Н/см2) и имеют очень небольшую амплитуду (1 — 2% от длины покоя мышц). Они вызывают небольшие ритмические деформации туловищного экзоскелета, что в силу механических связей туловища и крыльев приводит к махам крыльев с той же частотой. В силу такой непрямой (опосредованной) связи с крыльями мышцы асинхронного действия называют также мышцами непрямого действия.
По электрофизиологическим свойствам асинхронные мышцы принципиально не отличаются от синхронных. Их ПД, по-видимому, имеют натриевый механизм. Электромеханическая связь здесь осуществляется с помощью ионов Са2+. Но саркоплазматического ретикулума в асинхронных мышцах почти нет; Са2+ поступает в возбужденное волокно извне, причем необходимая концентрация его удерживается в течение всего периода ритмической активности. Структура саркомеров асинхронных мышц сходна с описанной у обычных мышц. Особенность ее состоит лишь в том, что толстые миозиновые нити имеют соединение через эластический элемент (связку) с Z- мембраной. Это ограничивает колебания длины саркомеров и делает коротким их I-диск.
Тонкие (актиновые) нити здесь представлены в большем количестве (три тонких на одну толстую). Показано, что мостики между толстыми и тонкими нитями в покое асинхронной мышцы направлены перпендикулярно нитям, а при активации угол между мостиком и толстой нитью становится острым, направленным вершиной к центру саркомера. Предполагают, что это сгибание, или «толчок», множества мостиков порождает смещение тонких нитей относительно толстых (к центру саркомера). Сокращение мышцы, точнее, ее одиночное напряжение (изометрический режим), и приводит к деформации экзоскелета и движению, например опусканию, крыльев. При этом осуществляется переход упругих элементов экзоскелета из одного состояния в другое «щелчком». Мышца оказывается освобожденной от сопротивления и

укорачивается примерно на 20 нм (1% длины саркомера). Но в этой ситуации ее работа почему-то прекращается. Данный феномен (прекращение тяги при снятии упругого сопротивления) воспроизводится и на изолированной мышце. Причина его не выяснена. На рис. 1.48 это явление изображено совершенно условно как «соскакивание» миозиновой головки с того участка двойной спирали актина, к которому возможно (или наиболее вероятно) прикрепление.
Рис. 1.48. Попеременная работа активируемых асинхронных мышц-антагонистов (1, II) Упругие щелчки экзоскелета (III) попеременно создают условия растяжения, необходимые для тяги мостиков одной или другой мышц (объяснение см. в тексте)
Дальнейшие события в естественной обстановке определяются тем, что при новом положении экзоскелета и крыльев до нужной длины растягивается асинхронная мышцаантагонист. Она тянет в свою сторону и переводит экзоскелет щелчком в исходное положение (поднимает крылья). При этом мышца-опускатель крыльев включается в работу (рис. 1.48), а ее антагонист инактивируется. Так, поочередно растягивая друг друга, эти мышцы, видимо, и создают высокочастотные ритмические сокращения и соответственно махи крыльев.
Асинхронные мышцы при активности потребляют значительное количество АТФ, О2 и существенно нагреваются (температура тела летящего насекомого может подняться до 40—42°С). При такой работе асинхронных мышц нервные импульсы и порождаемые ими мышечные ПД нужны лишь для того, чтобы создавать и поддерживать необходимую для сократительной активности концентрацию Са2+ВН. По прекращении нервной стимуляции и соответственно мышечных ПД концентрация Са2+вн снижается и сократительная активность прекращается.
Есть сведения о том, что асинхронные мышцы (с частотой сокращений 100 в 1с) имеются и у ракообразных. У позвоночных такие мышцы не описаны.
Из числа гладких мышц беспозвоночных животных особый интерес представляет
запирательный мускул двустворчатых моллюсков. Эта мышца относится к так называемым парамиозиновым, так как в ней много белка парамиозина (он связан с миозином и формирует остов толстых нитей в мышечных клетках). Взаимное расположение толстых и тонких нитей здесь беспорядочно. Мышца активируется холинэргическим нервом и тормозится серотонинэргическим. При действии возбуждающего нервного импульса мышца сокращается и далее остается в достигнутом «укороченном» состоянии неопределенно долгое время. Такой эффект обозначают как запирательное действие. Установлено, что сокращение мышцы инициируется ее потенциалом действия и входом Са2+ в волокно. Но запирательное действие не сопровождается ПД; потребление О2 при нем в 11 раз ниже, чем при сокращении.
Природа запирательного действия не выяснена. Предполагают, что оно может быть связано либо с формированием «неразрывной» связи миозиновых головок с актиновыми нитями, либо с кристаллизацией парамиозина, либо, наконец, с комбинацией этих двух явлений. При запирательном действии Са2+ и АТФ, по-видимому, оказываются связанными. Действие тормозного нерва (медиатор-серотонин) снимает запирание и расслабляет мышцу.
