
6 курс / Кардиология / Vatutin__Kardiologia
.pdfрая (под влиянием лечения) обратимость. Достаточно часто, особенно при повторных атаках ревматизма, бывает не артрит, а полиартралгия.
Хорея – это проявление ревматического поражения центральной нервной системы, которое характеризуется мышечной слабостью, бесцельными и беспорядочными движениями, эмоциональной нестабильностью. В тяжелых случаях могут возникнуть расстройство ходьбы, параличи, потеря способности к передвижению. Интересно, что хаотические и непроизвольные подергивания мышц конечностей и мимической мускулатуры исчезают во время сна больного.
Кольцевидная (анулярная) эритема – представляет собой розово-красные пятна до 5-7 см в диаметре кольцевидной (реже звездчатой) формы, бледнеющие при надавливании, не сопровождающиеся зудом и уплотнением кожи. Типичная локализация – живот, грудь, спина, конечности. Характерно спонтанное исчезновение и редкое рецидивирование.
Подкожные ревматические узелки представляют собой плотные, округлые, размером от нескольких миллиметров до 1-2 см, безболезненные образования в периартикулярных тканях. Наблюдаются редко, в основном у больных с возвратным ревмокардитом. Образовавшись, исчезают через несколько дней (недель).
Другие проявления. Крайне редко развиваются ревматический полисерозит (плеврит, перитонит, перикардит), васкулит с поражением легких и почек, а также пневмониты.
Дополнительные методы исследования.
Лабораторные данные. Специфических тестов, характерных для ревматизма нет, однако с помощью лабораторных данных можно определить наличие воспалительного процесса и степень его выраженности. В частности, у больных с активным ревматизмом в крови нередко выявляют:
−лейкоцитоз (нейтрофильный);
−ускорение СОЭ;
−С-реактивный белок;
−повышение титров противострептококковых антител
ианти-О стрептолизинов, из зева таких больных часто высевают
β-гемолитический стрептококк группы А. Электрокардиография. Выявляются различные наруше-
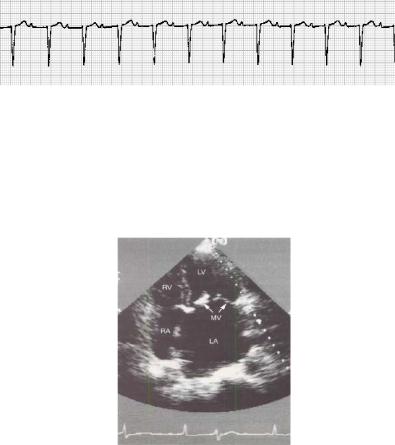
ния ритма (синусовая тахикардия, брадикардия, экстрасистолия, фибрилляция предсердий) и проводимости сердца (рис. 10), в частности удлинение интервала PQ свыше 0.2 с относят к малым диагностическим критериям ревматизма (критериям Джонса).
Рис. 10 – ЭКГ больного ревматизмом (АВБ 1 степени)
Эхокардиография. Метод является информативным в выявлении кардита и клапанных изменений, особенно при использовании в динамике (рис. 11). Эхокардиографическими признаками ревматического эндокардита могут быть краевое утолщение створок клапанов, их пролабирование, клапанная регургитация.

Рис. 11 – ЭхоКГ больного ревматизмом (пролабирование и утолщение створок митрального клапана)
Рентгенография. Обычно используется в уточнении характера пороков сердца, выявлении серозитов, пневмонитов, гемодинамических нарушений, а также дифференциальной диагностике. Вместе с тем рентгенологических признаков, характерных только для ревматизма, нет.
Другие методы. Ранее в диагностике эндокардита широко использовалась фонокардиография (ФКГ), однако с появлением современной ультразвуковой диагностической техники ФКГ утратила свое значение.
Диагноз. Начиная с 1988 г., эксперты ВОЗ рекомендуют основывать диагноз ревматизма на критериях (табл. 1) американского ревматолога Джонса (T.D. Jones), предложенных еще в 1944 г. В 1992 г. эти критерии были в очередной раз пересмотрены, модифицированы и выглядят следующим образом.
Табл. 1 – Критерии диагностики ревматизма
Большие критерии: |
Малые критерии: |
|
− |
кардит, |
− артралгии, |
− |
полиартрит, |
− лихорадка, |
− |
хорея, |
− увеличение СОЭ или появ- |
− |
кольцевидная эритема, |
ление С-реактивного белка, |
− |
подкожные узелки. |
− увеличение интервала PQ. |
 Диагноз ревматизма считается вероятным у больных, недавно
Диагноз ревматизма считается вероятным у больных, недавно 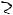 перенесших стрептококковую инфекцию, при наличии у них двух больших либо одного большого и двух малых критериев.
перенесших стрептококковую инфекцию, при наличии у них двух больших либо одного большого и двух малых критериев.
Дифференциальный диагноз. Ревматизм дифференциру-
ют с инфекционным эндокардитом, диффузными болезнями соединительной ткани и, в первую очередь, с системной красной волчанкой, ювенильным ревматоидным артритом, реактивными артритами, сывороточной и лекарственной болезнями, краснухой, саркоидозом, васкулитом Шенлейна-Геноха и некоторыми другими заболеваниями.
Лечение. Как правило, лечение ревматизма должно быть трехэтапным (стационар, местный санаторий, поликлиника).
Лечение активного ревматизма проводят в стационаре, желательно специализированном. Показаны постельный режим (особенно при ревмокардите) и назначение антибиотика (пенициллин, эритромицин) на 10-14 дней для санации организма больного от стрептококковой инфекции.
Основа терапии ревматизма – стероидные и нестероидные противовоспалительные средства (НПВС).
Кортикостероиды показаны при первичном ревмокардите, высокой активности возвратного. Начальная доза преднизолона обычно составляет 1-3 мг/кг/сут. с постепенным уменьшением. При снижении дозы до 10-15 мг/сут. к терапии добавляют НПВС (аспирин, индометацин, вольтарен, бруфен или другие) на срок до 3-5 мес. В других случаях НПВС назначают с самого начала лечения, иногда в сочетании с небольшими дозами глюкокортикоидов или аминохинолинами.
При появлении сердечной недостаточности, нарушений ритма сердца и проводимости проводят соответствующее лечение.
Критерии эффективности и ожидаемые результаты лечения.
1.Отсутствие кардиальных и артралгических синдромов.
2.Нормализация показателей активности воспалительного процесса.
3.Нормализация титров стрептококковых антител.
4.Стабильность морфофункциональных показателей по данным эхокардиографии со стороны клапанов и камер сердца.
Течение и прогноз. При первой атаке заболевания порок сердца формируется примерно у 20-25% больных. Если острая ревматическая лихорадка не закончилась пороком сердца, то в дальнейшем поражение клапанов, как правило, не происходит. С другой стороны, если начало заболевания сопровождалось тяжелым кардитом, то в последующем наблюдается прогрессирующее поражение клапанного аппарата сердца.
Экспертиза трудоспособности. Больные с активным ревматизмом нуждаются в лечении в условиях стационара.
В дальнейшем трудоспособность зависит от характера клапанных изменений и степени гемодинамических нарушений.
Профилактика. Первичная – предусматривает комплекс мер по предупреждению заболеваемости ревматизмом здоровых лиц:
−улучшение социальных условий жизни населения;
−пропаганда здорового образа жизни (физкультура, спорт, закаливание);
−выявление носителей стрептококковой инфекции и своевременная их санация;
−обязательное лечение острых стрептококковых инфекций антибиотиками. Для этого используются пенициллин (1-2 млн. МЕ/сут. – 10 дней), амоксициллин или эритромицин.
Вторичная - заключается в длительном (часто пожизненном, хотя общепринятой точки зрения на длительность такой терапии нет) применении бициллина или экстенциллина (бициллин-5 по 1.5 млн МЕ внутримышечно каждые 3-4 недели). В частности, Американский Ревматологический Колледж при наличии ревмокардита рекомендует непрерывную профилактическую бициллинотерапию на протяжении 10 лет (или до 25-летнего возраста больного); без ревмокардита – 5 лет (или до 18летнего возраста).

В связи с тем, что больные ревматическими пороками сердца входят в группу высокого риска развития инфекционного эндокардита, в целях его профилактики им назначаются антибиотики при проведении диагностических и лечебных мероприятий, сопровождающихся бактериемией.
3. ИНФЕКЦИОННЫЙ ЭНДОКАРДИТ
Инфекционный эндокардит (ИЭ) – это инфекционное воспа-
лительное поражение соприкасающихся с кровью внутрисердечных структур (клапанов сердца или пристеночного эндокарда, имплантированных инородных тел) или эндокарда крупных внутригрудных сосудов.
Термин «инфекционный эндокардит» впервые применил
S.Jaccoud в 1885 г.
Эпидемиология. По данным различных авторов, частота ИЭ колеблется от 0.16 до 5.4 случаев на 1 тыс. госпитализированных больных. Наиболее уязвимой считается популяция в возрасте 20-50 лет. Чаще (в 2-4 раза) болеют мужчины.
За последние десятилетия повсеместно отмечается увеличение заболеваемости ИЭ. Среди причин называют широкое распространение:
−оперативных вмешательств на сердце;
−инвазивных методов диагностики и лечения;
−наркомании.
Этиология. Причиной ИЭ может быть любой инфекционный агент, но чаще всего стрептококки (30-80%), стафилококки (20-35%) и энтерококки (5-15%). Значительно реже ИЭ вызывается другими микроорганизмами, грибами.
Патогенез. Считается, что ИЭ развивается под воздействием ряда факторов (например, при ослаблении резистентности организма больного, высокой вирулентности возбудителя), однако решающими из них являются следующие два:
1.Повреждение эндотелия клапанов сердца или пристеночного эндокарда.
2.Бактериемия (транзиторная или длительная).
Высокий риск повреждения эндотелия имеется у лиц с врожденными и приобретенными пороками сердца, клапанными протезами, имплантированными устройствами (электрокардиостимуляторами, кардиовертерами-дефибрилляторами), подвергающихся зондированию полостей сердца.
Бактериемия чаще всего возникает при стоматологических, отоларингологических, урологических или гинекологических вмешательствах, глубоких инфицированных ранах конечностей.
В зоне поврежденного эндотелия обычно формируется тромб – вначале рыхлый, тромбоцитарный, затем плотный, фибринный.
Возбудитель ИЭ, внедрившись в такой тромб (называемый вегетацией), не только в нем быстро размножается, но и укрывается от воздействия защитных сил макроорганизма и лекарственных средств (таких как антибиотики) изнутри створкой клапана, не имеющей сосудов, а снаружи – плотным слоем фибринного тромба.
Инфицированная вегетация представляет собой динамическое образование, она может увеличиваться, дробиться (так как при ИЭ идет непрерывное повреждение створок клапана, пристеночного эндокарда), периодически или постоянно выбрасывать в ток крови огромное количество возбудителя заболевания, отрываться (полностью или частично), что приводит к появлению септических эмболических очагов в различных органах и тканях. В последующем персистирующая бактериемия стимулирует гуморальный и клеточный иммунитет и запускает иммунноопосредованный механизм воспаления.
Патологическая анатомия. Патоморфологической ба-
зой ИЭ является полипозно-язвенный эндокардит, для которого характерно наличие вегетаций на створках клапанов и пристеночном эндокарде (иногда с вовлечением в процесс интимы аорты и крупных артерий). Чаще поражаются аортальный и митральный клапаны с разрушением створок и формированием недостаточности, реже (примерно у 6%) – трехстворчатый (как правило, у инъекционных наркоманов или лиц, принимавших цитостатики). При ИЭ во многих органах (почках, селезенке, легких, мозге) находят септические очаги и инфаркты, обусловленные диссеминацией инфекции и эмболиями (фрагментами разрушенных створок и вегетаций).
Классификация. Согласно рекомендациям Европейского кардиологического общества (2004 г.) выделяют активный, из- леченный и рецидивирующий ИЭ. Если заболевание развивается на фоне врожденных или приобретенных пороков сердца, то такой эндокардит называют вторичным. Первичный ИЭ возникает у больных, не имевших такой фоновой кардиальной патологии. В зависимости от возбудителя ИЭ может быть стрептококковым, стафилококковым, хламидийным, грибковым и т.д.
При поражении протезированных клапанов выделяют ранний (в течение года после операции) и поздний ИЭ.
Клиника. Клиническая картина при ИЭ чрезвычайно вариабельна, в связи с чем у каждого второго пациента правильный диагноз устанавливается слишком поздно – через 1-3 месяца от начала заболевания. К основным признакам ИЭ относят: лихорадку, эмболии, геморрагические высыпания и шум при аускультации сердца, связанный с разрушением клапанов и формированием клапанной недостаточности.
В большинстве случаев симптомы ИЭ появляются спустя нескольких дней после провоцирующего события, сопровож-
даемого транзиторной бактериемией (например, экстракции зуба, инфицированной раны, внебольничного аборта и т.д.).
Лихорадка, как правило, носит упорный, гектический характер, сопровождается ознобами и проливными потами, хотя

во многих случаях она бывает субфебрильной, а примерно у 8- 10% больных (ослабленных, пожилых, страдающих почечной недостаточностью) вообще отсутствует.
Эмболии наблюдаются у 15-60% больных ИЭ и обусловлены отрывом инфицированных вегетаций или фрагментов разрушенных клапанов. Их локализация самая разная – мозг, селезенка, почки, артерии ног, сердца, легких (при поражении трехстворчатого клапана). В зонах эмболий развиваются инфаркты, абсцессы, септические аневризмы. Угроза эмболии существенно возрастает на фоне приема непрямых антикоагулянтов (в подобных случаях, если больной нуждается в продолжении антикоагулянтной терапии непрямые антикоагулянты заменяют гепарином).
Высыпания. Довольно часто при ИЭ находят геморраги- ческие высыпания (рис. 12), связанные с микротромбозом и васкулитом – петехии (конъюнктива, слизистая рта), пятна Джэйнуэя (безболезненные геморрагии диаметром 1-4 мм на ладонях
истопах), узелки Ослера (болезненные образования на пальцах)
ипятна Рота (кровоизлияние в сетчатку глаза с белой точкой в центре).
Рис. 12 – Геморрагические высыпания при ИЭ
Шум при аускультации сердца. Одной из важнейших осо-
бенностей ИЭ, отличающей его от эндокардитов другого происхождения, является быстрое (в течение нескольких дней, недель) разрушение пораженных створок с формированием (или усугублением) недостаточности клапанов левых, реже правых отделов сердца. Появление (или изменение) шума в сердце, определяемое при динамической аускультации, дает возможность ранней диагностики ИЭ.
В связи с циркуляцией инфекционного агента в крови, эмболиями, интоксикацией и присоединением иммунноопосредованных нарушений при ИЭ возможны разнообразные поражения любого органа или системы:
сердца: помимо эндокардита, может развиваться миокардит, перикардит, абсцесс и инфаркт миокарда, сердечная недостаточность (острая или хроническая);
почек: эмболии артерий, инфаркт, абсцесс, пиелонефрит, гломерулонефрит, амилоидоз, почечная недостаточность;
центральной нервной системы: эмболия артерий, септиче-
ская аневризма, абсцесс с тяжелой очаговой симптоматикой, энцефалит, менингит;
селезенки: спленомегалия, инфаркт, абсцесс; печени: гепатит;
опорно-двигательного аппарата: миалгия, артралгия, артри-
ты (в том числе септические), остеомиелит.
Дополнительные методы исследования.
Лабораторные данные. Часто выявляют анемию, тромбоцитопению, ускорение СОЭ, лейкоцитоз со сдвигом влево и патологические изменения в моче.
Наиболее надежный лабораторный тест – посев крови. Забор крови для исследования производят из разных вен не менее трех раз с интервалом не менее 1 часа до начала антибактериальной терапии. Если больной до этого получал антибиотики, то при возможности посев выполняют через трое суток после их отмены. В каждую пробирку набирают 10-15 мл крови, так как вероятность выявления возбудителя прямо пропорциональна объему крови, взятому для анализа. Посев крови производят в две среды – для выявления аэробной и анаэробной флоры. В процессе лечения такие посевы повторяют до получения отрицательного результата.
Электрокардиография. Изменения при ИЭ неспецифичны. При быстром разрушении клапанов возможно появление картины острой перегрузки левых или правых отделов сердца.
Эхокардиография. Достоверным ЭхоКГ признаком ИЭ являются вегетации (рис. 13), которые обычно образуются спустя 2-3 недели от начала заболевания и сохраняются в течение нескольких месяцев после выздоровления. К сожалению, при
