
- •Оглавление
- •Список сокращений
- •Аминокислоты, входящие в состав белков
- •Предисловие
- •Введение
- •Глава 1. Биохимия соединительной ткани
- •1.1. Клеточные элементы соединительной ткани
- •1.2. Коллаген
- •1.3. Эластин
- •1.4. Протеогликаны
- •1.5. Адгезивные и антиадгезивные белки
- •1.6. Контрольные вопросы и задания
- •1.7. Задания в тестовой форме
- •1.8. Ситуационные задачи
- •Глава 2. Биохимия костной ткани
- •2.1. Клетки костной ткани
- •2.2. Межклеточный матрикс костной ткани
- •2.3. Неколлагеновые белки костной ткани
- •2.4. Вещества небелковой природы органического матрикса костной ткани
- •2.5. Ремоделирование костной ткани
- •2.6. Факторы, регулирующие ремоделирование костной ткани
- •2.7. Контрольные вопросы и задания
- •2.8. Задания в тестовой форме
- •2.9. Ситуационные задачи
- •Глава 3. Биохимия мышечной ткани
- •3.1. Структура поперечнополосатой скелетной мышечной ткани
- •3.2. Химический состав поперечнополосатой скелетной мышечной ткани
- •3.3. Механизмы сокращения и расслабления скелетной мышцы
- •3.4. Источники энергии для мышечного сокращения
- •3.5. Особенности биохимии гладкой мышечной ткани
- •3.6. Особенности структуры и химического состава мышечной ткани сердца (миокарда)
- •3.7. Контрольные вопросы и задания
- •3.8. Задания в тестовой форме
- •3.9. Ситуационные задачи
- •Глава 4. Биохимические особенности нервной ткани
- •4.1. Химический состав нервной ткани
- •4. 2. Энергетические субстраты головного мозга
- •4.3. Гематоэнцефалический барьер
- •4.4. Особенности метаболизма в нервной ткани
- •4.5. Сигнальные молекулы: нейромедиаторы и их рецепторы
- •4.6. Контрольные вопросы и задания
- •4.7. Задания в тестовой форме
- •4.8. Ситуационные задачи
- •Глава 5. Обмен веществ в печени
- •5.1. Роль печени в белковом обмене
- •5.2. Особенности углеводного обмена в печени
- •5. 3. Метаболизм липидов в печени
- •5. 4. Внешнесекреторная и экскреторная функции печени
- •5. 5. Гомеостатическая функция печени
- •5. 6. Роль печени в обезвреживании токсинов и ксенобиотиков
- •5.7. Контрольные вопросы и задания
- •5.8. Задания в тестовой форме
- •5.9. Ситуационные задачи
- •Глава 6. Метаболизм лекарственных соединений
- •6.1. Всасывание, транспорт по крови и распределение лекарственных соединений в тканях
- •6. 2. Реализация фармакологических эффектов лекарственных веществ
- •6.3. Химические механизмы первой фазы биотрансформации лекарственных соединений
- •6.4. Реакции второй фазы инактивации лекарственных веществ
- •6.5. Удаление лекарственных веществ из организма
- •6.6. Факторы, влияющие на скорость биотрансформации лекарственных соединений
- •6.7. Контрольные вопросы и задания
- •6.8. Задания в тестовой форме
- •6.9. Ситуационные задачи
- •Эталоны ответов на задания в тестовой форме Биохимия соединительной ткани
- •Биохимия костной ткани
- •Биохимия мышечной ткани
- •Биохимические особенности нервной ткани
- •Обмен веществ в печени
- •Метаболизм лекарственных соединений в организме человека
- •Эталоны ответов на ситуационные задачи Биохимия соединительной ткани
- •Биохимия костной ткани
- •Биохимия мышечной ткани
- •Биохимические особенности нервной ткани
- •Обмен веществ в печени
- •Метаболизм лекарственных соединений в организме человека
- •Рекомендуемая литература
- •Библиографический список
5. 6. Роль печени в обезвреживании токсинов и ксенобиотиков
Для сохранения жизни организма огромное значение имеет антитоксическая (или барьерная) функция печени. В печени происходит обезвреживание токсических веществ эндогенного происхождения (продукты гниения аминокислот в кишечнике, билирубин, аммиак), инактивация биологически активных веществ (гормонов, биогенных аминов), а также метаболизируются и инактивируются лекарственные препараты, обезвреживаются токсические соединения экзогенного происхождения (ксенобиотики, этанол).
Ксенобиотики – это чужеродные для организма вещества, которые поступают в него из окружающей среды, но не используются организмом для построения тканей и в качестве источника энергии (продукты хозяйственной деятельности человека, вещества бытовой химии). Ксенобиотики и лекарственные соединения, имеющие гидрофильные свойства, выводятся из организма в неизменном виде с мочой, гидрофобные могут накапливаться в тканях и нарушать их функции. В связи с этим в организме выработались механизмы, обеспечивающие обезвреживание и удаление токсичных веществ.
В печени существует несколько механизмов обезвреживания эндогенных и экзогенных токсичных веществ таких, как микросомальные, внемикросомальные и макрофагальные. В микросомальной детоксикации в гепатоцитах участвуют специфические ферментативные системы (монооксигеназы) микросом, наиболее важным из которых является цитохром Р-450, связанный функционально с оксигеназами со смешанной функцией. Эта система может метаболизировать многие липофильные эндогенные (стероиды, жирные кислоты) и экзогенные (лекарственные препараты, органические растворители, канцерогены) соединения. Результатом действия этой системы не всегда является инактивация метаболизируемых веществ, т.к. возможно образование токсичных продуктов, таких как эпоксиды и свободные радикалы – реакционноспособные молекулы, способные повреждать белки и нуклеиновые кислоты.
Внемикросомальные механизмы локализованы в цитозоле, в митохондриях, в пероксисомах и лизосомах и обеспечивают инактивацию, в основном, водорастворимых соединений.
Макрофагальные механизмы инактивации в печени обеспечиваются клетками Купфера, которые удаляют из кровотока продукты распада и жизнедеятельности тканей. Макрофаги печени фагоцитируют циркулирующие в крови иммунные комплексы, а также бактерии и их эндотоксины, появляющиеся в крови при инфекционных и воспалительных заболеваниях. Гепатоцитиы и макрофаги печени также синтезируют различные белковые молекулы, выполняющие важные функции в реакциях неспецифического иммунитета (белки системы комплемента, С-реактивный белок и др.). Реакции специфического иммунитета обеспечиваются в печени лимфоцитами, циркулирующими по кровеносным и лимфатическим сосудам этого органа.
Печень играет ключевую роль в метаболизме гормонов. В ней разрушаются стероидные гормоны (глюко- и минералокортикоиды, половые гормоны), тироксин, АДГ, инсулин. При однократном прохождении крови через печень инактивируется до 80 % гормонов. Инактивация гормонов в печени зависит от их химической природы. Пептидные гормоны гидролизуются в печени протелитическими ферментами, например, инсулин гидролизуется инсулиназой. Катехоламины сначала дезаминируются окислительным путем при участии моноаминооксидазы, а затем метилируются по гидроксильным группам. Стероидные гормоны в микросомальной фракции гидроксилируются при участии гидроксилаз, а затем конъюгируют с глюкуроновой или серной кислотой. Тироксин в гепатоцитах вовлекается в трансаминирование, превращаясь в кетопроизводное, а затем происходит реакция коньюгации. Водорастворимые продукты катаболизма гормонов выводятся с мочой.
В печени обезвреживаются продукты гниения аминокислот: крезол, фенол, образующиеся при распаде тирозина, а также скатол и индол - при распаде триптофана. Инактивация этих веществ также первоначально включает реакции гидроксилирования, а затем образуются их конъюгаты с глюкуроновой и серной кислотами, элиминируемые с мочой. Примером такой инактивации является детоксикация индола с образованием животного индикана (Рис. 31):
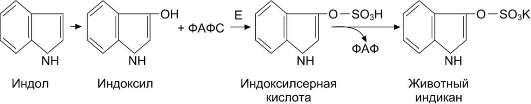
Рис. 31. Схема обезвреживания индола при участии сульфотрансферазы [15].
Катаболизм этанола главным образом также осуществляется в печени (до 98% экзогенного этилового спирта). В печени окисление алкоголя происходит через стадию превращения его в ацетальдегид (токсичный промежуточный метаболит), которое осуществляется несколькими путями.
Основную роль в метаболизме этанола играет НАД-зависимая алкогольдегидрогеназа, локализующаяся в основном в цитозоле и митохондриях печени (до 95%), в которой этанол превращается в ацетальдегид, где акцептором водорода является НАД+. Данная реакция обратима, ее направление зависит от концентрации ацетальдегида и соотношения НАДH/НАД+ в клетке:
С2H5ОН + НАД+ ↔ CH3CHO + НАДH + H+
Другой вариант играет незначительную роль в окислении этанола, но индуцируется им, а также другими спиртами и некоторыми лекарственными соединениям и приобретает существенное значение при злоупотреблении этими веществами. Этот путь происходит при участии цитохром Р450-зависимой микросомальной этанолокисляющей системы, локализованной в мембране гладкого ЭПР гепатоцитов:
С2H5ОН + НАДФН + Н+ + О2 → CH3CHO + НАДФ+ + 2Н2О
Второстепенную роль в превращении этанола в ацетальдегид играет каталаза, локализованная в пероксисомах цитоплазмы и митохондрий клеток печени. Каталаза расщепляет около 2% этанола, но при этом утилизирует пероксид водорода:
СН3СН2ОН + Н2О2 → СН3СНО +2 Н2О
Далее образовавшийся ацетальдегид окисляется до уксусной кислоты с помощью двух ферментов: ФАД-зависимой альдегидоксидазой или НАД-зависимой ацетальдегиддегидрогеназой. Уксусная кислота затем активируется под действием фермента ацетил-КоА-синтетазы при участии коэнзима А и АТФ с образованием ацетил-КоА, который в зависимости от соотношения АТФ/АДФ и количества оксалоацетата в митохондриях гепатоцитов, может далее окисляться в ЦТК, идти на синтез жирных кислот или кетоновых тел. Интенсивный метаболизм этанола в гепатоцитах приводит к накоплению токсичного ацетальдегида, увеличению отношения НАДН/НАД+, что приводит к нарушению биохимических процессов и функций как печени, так и других органов и тканей.
Таким образом, в печени происходит обезвреживание многих эндогенных токсических соединений (продукты гниения аминокислот в кишечнике, билирубин, аммиак), а также инактивация гормонов и других биологически активных веществ. Значительная часть токсических соединений экзогенного происхождения (ксенобиотики, этанол) также обезвреживается в печени, в том числе и лекарственные вещества.
