
- •Контрольная работа №8. Обмен и функции аминокислот.
- •1. Био. Роль белков. Био. Ценность белков. Заменимые и незаменимые аминокислоты.
- •11) Экспрессия ген. Информации.
- •2. Нормы белка в питании. Азотистый баланс, его виды, значение.
- •3. Переваривание белков и всасывание аминокислот в желудочно-кишечном тракте.
- •5. Окислительное дезаминирование аминокислот.
- •6.Трансаминирование аминокислот (а.Браунштейн, и.Крицман). Диагностическое значение определения активности трансаминаз. Связь трансаминирования с дезаминированием (непрямое дезаминирование).
- •7. Декарбоксилирование аминокислот. Образование биогенных аминов: гистамина, серотонина, гамма-аминомасляной кислоты (гамк), биологическая роль и их инактивация.
- •8. Образование аммиака и судьба аммиака в организме. Гипераммониемия. (*Токсическое действие аммиака).
- •1) Синтез аминокислот из соответствующих кетокислот:
- •3) Синтез пуриновых и пиримидиновых нуклеотидов.
- •4) Синтез мочевины – основной путь обезвреживания аммиака.
- •9. Биосинтез мочевины. Клиническое значение определения мочевины.
- •10. Синтез креатина, креатин – фосфата, биологическая роль. Клиническое значение определения креатинина.
- •11* Особенности обмена аминок-т (глицин, метионин, глутаминовая и аспарагиновая кислоты, триптофан, фенилаланин).
- •12* Патология азотистого обмена: белковая недостаточность (Квашиоркор).
- •13. Механизм возникновения наследственных нарушений обмена аминокислот (фенилпировиноградная олигофрения, алкаптонурия, альбинизм).
- •14. Переваривание и всасывание нуклеопротеинов.
- •15. Распад пуриновых нуклеотидов.
- •16. Заболевания, связанные с нарушением обмена нуклеотидов: подагра, синдром Леша – Нихена.
- •Ситуационные задачи по теме: «обмен и функции аминокислот».
7. Декарбоксилирование аминокислот. Образование биогенных аминов: гистамина, серотонина, гамма-аминомасляной кислоты (гамк), биологическая роль и их инактивация.
Декарбоксилирование – процесс отщепления группы СО2 при участии декарбоксилаз, небелковый компонент которых пиридоксальфосфат (ПФ), активная форма витамина В6. Реакции декарбоксилирования необратимы. Их продуктами являются СО2 и биогенные амины, которые выполняют функцию нейромедиаторов (серотонин, дофамин, ГАМК), гормонов (адреналин, норадреналин), регуляторных факторов местного действия (гистамин, карнозин и др.).
Г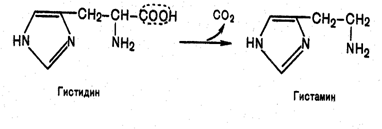 ИСТАМИН
– образуется путем декарбоксилирования
гистидина в тучных клетках соед. ткани.
Секретируется в кровь при повреждении
ткани (удар, ожог), развитии иммунных и
аллерг. реакций. Роль:
ИСТАМИН
– образуется путем декарбоксилирования
гистидина в тучных клетках соед. ткани.
Секретируется в кровь при повреждении
ткани (удар, ожог), развитии иммунных и
аллерг. реакций. Роль:
1) Стимулирует секрецию жел. сока, слюны;
2) Повышает проницаемость капилляров, вызывает отеки, снижает АД (но увел.внутричерепное давление, вызывает головную боль);
3) Сокращает гладкую мускулатуру легких, вызывает удушье;
4) Участвует в формировании воспалительной реакции – вызывает расширение сосудов, покраснение кожи, отечность ткани;
5) Выполняет роль нейромедиатора;
6) Является медиатором боли.
С ЕРОТОНИН
– нейромедиатор проводящих путей.
Образуется в надпочечниках и ЦНС из
аминокислоты 5-окситриптофана. Он может
превращаться в гормон мелатонин,
регулирующий суточные и сезонные
изменения метаболизма организма и
участвующий в регуляции репродуктивной
функции. Роль:
ЕРОТОНИН
– нейромедиатор проводящих путей.
Образуется в надпочечниках и ЦНС из
аминокислоты 5-окситриптофана. Он может
превращаться в гормон мелатонин,
регулирующий суточные и сезонные
изменения метаболизма организма и
участвующий в регуляции репродуктивной
функции. Роль:
1) Стимулирует сокращение гладкой мускулатуры;
2) Оказывает сосудосуживающий эффект;
3) Регулирует АД, температуру тела, дыхание;
4) Обладает антидепрессантным действием;
5) Принимает участие в аллергических реакциях.
ГАМК – γ-аминомаслянная кислота – образуется путем декарбоксилирования глутаминовой кислоты. Основной тормозной медиатор высших отделов мозга. Роль:
1) Увеличивает проницаемость постсинаптических мембран для ионов К+, что вызывает торможение нервного импульса;
2) Повышает дыхательную активность нервной ткани;
3) Улучшает кровоснабжение головного мозга.
ГАМК в виде препаратов гаммалон или аминалон применяют при сосудистых заболеваниях головного мозга (атеросклероз, гипертония), нарушениях мозгового кровообращения, умственной отсталости, эндогенных депрессиях, травмах головного мозга, эпилепсии.
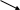 СО2
СО2
C OOH-CH2-CH2-CH(NH2)-COOH
COOH-CH2-CH2-CH2(NH2)
OOH-CH2-CH2-CH(NH2)-COOH
COOH-CH2-CH2-CH2(NH2)
Глутаминовая кислота ФП ГАМК
ОБЕЗВРЕЖИВАНИЕ БИОГЕННЫХ АМИНОВ. Биогенные амины подвергаются дезаминированию. Процесс катализирует моноаминооксидаза (МАО), кофермент ФАД. В результате образуются: альдегиды, NH3, H2O2. МАО наиболее акивна в печени, желудке, почках, кишечнике, нервной ткани.
8. Образование аммиака и судьба аммиака в организме. Гипераммониемия. (*Токсическое действие аммиака).
ОБРАЗОВАНИЕ. Аммиак в организме образуется в результате дезаминирования аминокислот, биогенных аминов и нуклеотидов. Часть аммиака образуется в кишечнике в результате действия бактерий на пищевые белки (гниение). Концентрация аммиака в крови в норме – 0,4-0,7мг/л. Это токсичное соединение, поэтому аммиак не накапливается, а вступает в реакцию с глутаминовой или аспарагиновой кислотами с образованием индифферентной транспортной формы – глутамина или аспарагина.
+NН3
Н ООС-(СН2)2-СН-СООН
Н 2NОС-(СН2)2-СН-СООН
ООС-(СН2)2-СН-СООН
Н 2NОС-(СН2)2-СН-СООН
АТФ
NН2 -Н2О NН2
глутаминовая кислота глутамин
+NН3
 НООС-СН2-СН-СООН
Н2NОС-СН2-СН-СООН
НООС-СН2-СН-СООН
Н2NОС-СН2-СН-СООН
АТФ
NН2 -Н 2О NН2
аспарагиновая кислота аспарагин
Основные источники аммиака:
1) Окислит. дезаминирование глутамата во всех тканей, кроме мышц.
2) Трасндезаминирование аминок-т.
3) Дезаминирование амидов глутамата (глутамина) и аспартата – в печени и почках.
4) Дезаминирование биогенных аминов.
5) Распад пуриновых и пиримидиновых оснований.
Пути использования аммиака в организме:
