
- •Введение
- •Катаболизм (распад) основных пищевых веществ - углеводов, жиров, белков (аминокислот).
- •Связь окислительного декарбоксилирования пирувата с процессом окислительного фосфорилирования
- •Регуляция пируватдегидрогеназного комплекса
- •Цикл лимонной кислоты
- •Реакции цикла трикарбоновых кислот
- •Зависимость цикла трикарбоновых кислот от недостатка кислорода
- •Регуляция общего пути катаболизма
- •Механизмы регуляции цитратного цикла
- •Анаболические функции цикла лимонной кислоты
- •Связь между общим путем катаболизма и цепью переноса электронов и протонов.
- •Макроэргические соединения
- •Дегидрирование субстратов и окисление водорода (образование воды) как источник энергии для синтеза атф
- •Митохондриальная цепь переноса электронов
- •Компоненты дыхательной цепи
- •Переносчики электронов
- •Система цитохромов дыхательной цепи, убихинол-дегидрогеназа (цитохром с редуктаза). Цитохром с оксидаза.
- •Структурная организация дыхательной цепи
- •Трансмембранный электрохимический потенциал как промежуточная форма энергии при окислительном фосфорилировании
- •Структурная организация цепи переноса электронов
- •Регуляция цепи переноса электронов (дыхательный контроль).
Макроэргические соединения
Макроэргические соединения - соединения, содержащие макроэргическую связь, при гидролизе которой освобождается энергия больше чем 30 кДж/моль.
К клеточным макроэргическим соединениям относят фосфоенолпируват, 1,3-дифосфоглицерат, которые образуются в гликолизе (в процессе распада глюкозы до пирувата). К ним относят также сукцинил-КоА (образуется в цикле трикарбо-новых кислот, переносит фосфатную группу на ГДФ), карбамоилфосфат (образуется в первой реакции цикла мочевины) и креатинфосфат. Эти молекулы обладают большим потенциалом переноса фосфатной группы на АДФ с образованием АТФ, потому что энергия, выделяемая при распаде этих макроэргических молекул более высокая, чем требуется для синтеза АТФ из АДФ. По отношению к АДФ, перечисленные макроэргические молекулы доноры энергии. В свою очередь АТФ - источник энергии для важных метаболических путей, в которые входят глюкоза, фруктоза и многие другие молекулы. Получая фосфатную группу от АТФ, эти молекулы увеличивают уровень своей свободной энергии (AG), что обеспечивает течение ряда ферментативных реакций и клеточных процессов.
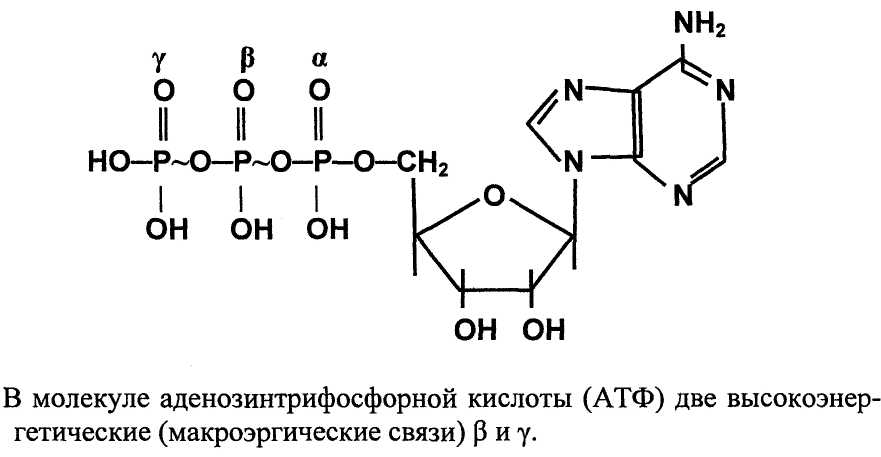
Таким образом, АТФ среди клеточных фосфорилированных соединений (по уровню свободной энергии) занимает некоторое промежуточное положение. Это определяет биологическое значение АТФ как универсального донора энергии в огромном числе реакций. Вместе с тем, АДФ универсальный акцептор энергии (и фосфатной группы) от клеточных макроэргов, которые обладают более высоким уровнем свободной энергии. Цикл АТФ-АДФ основной механизм обмена энергии в клетке. Расчеты показывают, что в организме в сутки образуется 40-45 кг АТФ. Некоторые анаболические реакции осуществляются с участием других нуклео-зидтрифосфатов. К ним относятся гуанозинтрифосфат (ГТФ) - участвует в рибо-сомальном синтезе белка, уридинтрифосфат (УТФ) - участвует в синтезе гликогена, цитидинтрифосфат (ЦТФ) - участвует в синтезе мембранных липидов.
Дегидрирование субстратов и окисление водорода (образование воды) как источник энергии для синтеза атф
АТФ - чрезвычайно важная молекула клетки. Она непрерывно синтезируется и используется. Энергия для синтеза АТФ поступает от субстратов, содержащих высокоэнергетические электроны в ходе их дегидрирования. Электроны высоких энергий извлекаются из субстратов в ходе гликолиза (в цитозоле), при преобразовании пирувата в ацетил-КоА и в цикле трикарбоновых кислот (в митохондриаль-ном матриксе). Молекулы НАДН и ФАДН2 переносят эти электроны в дыхательную цепь, локализованную в во внутренней митохондриальной мембране.
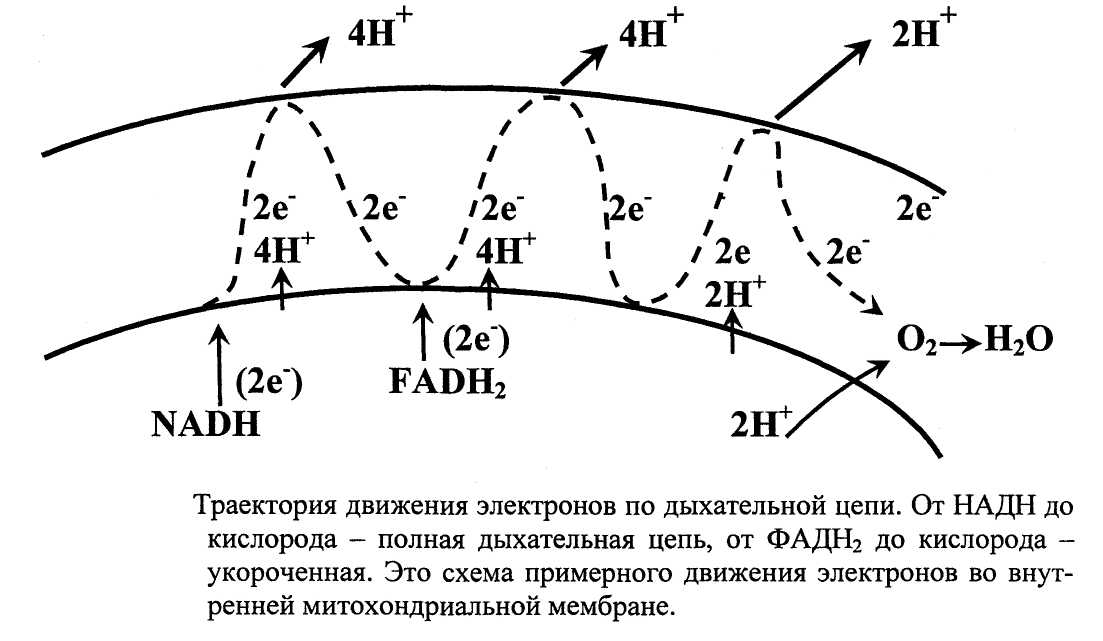
Дыхательная цепь состоит из переносчиков электронов, сгруппированных в 4 ферментативных комплекса, и ферментов. Особенность переносчиков электронов дыхательной цепи в том, что каждый способен принимать электроны от предыдущего и отдавать последующему. Прием и передача электронов молекулами переносчиков происходит упорядоченно в соответствии с их электрохимическими потенциалами. Под электрохимическим потенциалом молекулы понимают её способность вступать во взаимодействие с электроном. Т.е. присоединять электрон и при этом восстанавливаться и отдавать его и при этом окисляться. Электрохимический потенциал молекулы это её способность участвовать в окислительно-восстановительных реакциях. В начало дыхательной цепи электроны вносит НАДН - он обладает самым низким электрохимическим потенциалам. В конце дыхательной цепи находиться кислород - его электрохимический потенциал самый высокий. Электроны, перемещаясь по дыхательной цепи в сторону кислорода, совершают полезную работу по переносу протонов из митохондриалыуого матрикса в межмембранное пространство (рис. 13). На восходящих участках тра-
ектории каждый электрон перемещается вместе с протоном, т.е. в форме атома водорода, затем отделяется от протона на внешней стороне мембраны и продолжает движение внутри мембраны. В межмембранном пространстве накапливаются протоны из митохондриального матрикса. Электрон теряет порции своей энергии на всех участках траектории. На восходящих участках траектории электрон расходует энергию на совершение полезной работы, а на нисходящих участках полезная работа не совершается, хотя электрон также теряет часть своей энергии. 40-45 % энергии электронов используется для создания протонного градиента, который, в свою очередь расходуется на синтез АТФ. 20-25 % энергии электронов используется для транспорта необходимых субстратов. Остальная энергия электронов рассеивается в виде тепла, поэтому митохондрии место теплообразования. Движение электронов по дыхательной цепи создает протонный градиент и значительную трансмембранный электрохимический потенциал между межмембранным пространством и митохондриальным матриксом (его обозначают АцН+ = 0,25 Вольта). ДцН* складывается из ДЧ* = 0,2 Вольта (это электрический потенциал, обусловленный разными зарядами по обе стороны мембраны) и АН+ = 0,05 Вольта (химический потенциал, обусловленный различной концентрацией протонов по обе стороны мембраны).
Энергия этого электрохимического градиента затем используется для синтеза АТФ (её использует АТФ-синтетазный комплекс, комплекс V) и транспорта необходимых субстратов. Эндогенная вода
Эндогенной называется вода, возникающая в клетках в основном при функционировании дыхательных цепей в митохондриях. Некоторое количество эндогенной воды образуется при микросомальном окислении и при разложении пероксида водорода. У взрослого человека в сутки возникает 400^-450 мл эндогенной воды. Каталаза присутствует во всех клетках организма и разлагает пероксид водорода:
Н2О2 + Н2О2 -+ О2 + 2 Н2О
Глутатионпероксидаза также присутствует во всех клетках организма и разлагает пероксид водорода. Содержит селеноцистеин в активном центре.
2 Глутатион-SH + Н2О2 -> Глутатион-SS + 2Н2О Глутатионпероксидаза также восстанавливает гидроперикиси липидов. В конце дыхательной цепи электроны взаимодействуют с кислородом и протонами из матрикса и образуется молекулы воды: 4е' + 4Н+ + О2 —» 2Н2О. Особенность образования воды в этой реакции состоит в том, что в неё входят электроны с достаточно низким уровнем энергии. Они уже израсходовали свою значительную энергию на создание протонного градиента. Поэтому роль многочисленных переносчиков электронов, локализованных во внутренней митохонд-риальной мембране, состоит в замедлении взаимодействия высокоэнергетических электронов с кислородом. Если бы их не было, то выделяющаяся тепловая энергия разрушила бы митохондриальную мембрану.
