
- •1. Предмет и значение аналитической химии. Связь с другими науками.
- •1.1. Определение.
- •1.2. Предмет и значение.
- •1.3. Теоретическая основа. Связь с другими науками.
- •2. Методы аналитической химии. Прикладные виды химического анализа.
- •3. Классификация качественного и количественного анализа.
- •3.1. Классификация качественного анализа.
- •4.2. Взятие навески.
- •4.3. Пробоподготовка.
- •5. Разложение (вскрытие) пробы: растворение, сплавление, спекание, специальные методы.
- •5.1. Растворение в жидкостях.
- •5.2. Сплавление.
- •5.3. Примеры практического применения сплавления.
- •5.4. Спекание.
- •5.5. Специальные методы. Термическое разложение.
- •5.6. Пирогидролиз.
- •11.2. Способы осуществления.
- •21. Общая характеристика титриметрического анализа (та). Понятие, терминология. Требования к реакциям, применяемым в та.
- •21.1. Общая характеристика.
- •21.2. Требования к реакциям, применяемым в та.
- •22. Основные приёмы титрования. Прямое, обратное, косвенное титрование. Примеры.
- •22.1. Прямое титрование.
- •22.2. Обратное титрование (титрование по остатку).
- •31.2. Термодинамическая и концентрационная константы равновесия реакции.
- •60.2. Условное произведение растворимости.
- •61. Растворение малорастворимого соединения: под действием кислот, комплексонообразователей, окислительно-восстановительных реакций.
- •61.1. Растворение малорастворимого соединения.
- •61.2. Растворение осадков под действием кислот.
- •61.3. Растворение осадков вследствие комплексообразования.
- •61.4. Растворение в результате овр.
- •69.2. Преимущества га.
- •69.3. Недостатки га.
60.2. Условное произведение растворимости.
Практическое применение правила ПР осложняется различными побочными реакциями, в которые вступают ионы малорастворимого соединения.
Анионы слабых кислот (CO32-, PO43--ионы) и катионы Fe3+, Al3+ могут вступать в реакции кислотно-основного взаимодействия, а могут образовывать комплексные соединения с присутствующими анионами.
Для расчёта равновесий в таких условиях можно воспользоваться условным ПР. В этом случае, это будет произведение суммарной концентрации всех форм существования в растворе катиона малорастворимого соединения на суммарную концентрацию существования всех форм аниона в растворе этого соединения.
ПР’MX=ПРMX*aM*ax
(ПР’ – условное произведение растворимости, aM и aX – коэффициенты побочных реакций; ≥1).
61. Растворение малорастворимого соединения: под действием кислот, комплексонообразователей, окислительно-восстановительных реакций.
61.1. Растворение малорастворимого соединения.
Если в систему, которая представляет собой осадок, находящийся в равновесии со своим насыщенным раствором, ввести реагент, способный взаимодействовать с катионом, анионом или с тем и с другим, то в результате конкурирующего взаимодействия равновесные концентрации ионов малорастворимого соединения уменьшатся.
Чтобы обеспечить концентрации ионов, удовлетворяющие ПР, в раствор из осадка должно перейти некоторое количество вещества. Процесс растворения пойдёт частично или полностью.
Для растворения малорастворимых соединений используют:
1. Сильные кислоты.
2. Комплексообразователи.
3. Окислители или восстановители.
61.2. Растворение осадков под действием кислот.
Равновесие в насыщенном растворе CaC2O4 при введении сильной кислоты будет смещаться вправо:
CaC2O4(тв.) Ca2++C2O42-
Т.к. ионы кислоты будут взаимодействовать с протонами, это будет приводить к растворению осадка:
C2O42-+H+ HC2O4- (1)
HC2O4-+H+ H2C2O4 (2)
Растворимость соли CaC2O4 будет равна:
S=[Ca2+]
S=[C2O42-]+[HC2O4-]+[H2C2O4]
Выразим равновесные концентрации продуктов побочных реакций 1 и 2:
K2=
[HC2O4-]=[C2O42-]*
Выразим концентрацию H2C2O4:
K1*K2=
[H2C2O4]=[C2O42-]*
Подставим в уравнение растворимости:
S=[C2O42-](1+ + )
Концентрация C2O42—иона может быть найдена:
[C2O42-]=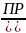 ,
поскольку [Ca2+]=S.
,
поскольку [Ca2+]=S.
Итоговое выражение:
S= )
)
Вывод: выражение под знаком корня является условным ПР, а выражение в круглых скобках является коэффициентом побочных реакций аниона малорастворимого соединения:
ПР’*ПР(CaC2O4)*a(C2O42-(H+))
61.3. Растворение осадков вследствие комплексообразования.
Равновесие в насыщенном растворе AgCl при введении аммиака будет смещать влево, т.к. катионы серебра будут взаимодействовать с аммиаком, с образованием аммиачных комплексов и это приведёт к растворению осадка:
AgCl(тв.) Ag++Cl-
Конкурирующие побочные реакции:
Ag++NH3 Ag(NH3)+ (1)
Ag(NH3)++NH3 Ag(NH3)2 (2)
Растворимость:
S=[Cl-]
S=[Ag+]+[Ag(NH3)+]+[Ag(NH3)2+]

61.4. Растворение в результате овр.
Применение реакций ОВР нередко является единственным способом растворения осадка. Типичным примером является растворение сульфидов (CuS) и оксидов (MnO2). Так, CuS практически не растворяется в концентрированной HCl, зато легко растворяется в разбавленной HNO3:
3CuS+8HNO3 3Cu(NO3)2+2NO+3S+4H2O
MnO2 не растворяется в HNO3, но хорошо растворяется в HCl:
MnO2+4HCl MnCl2+Cl2+H2O
В неорганическом анализе, часто для растворения используют «царскую водку», которая действует как сильная кислота и как сильный окислитель благодаря HNO3.
62. Соосаждение. Уравнение Ленгмюра. Адсорбция ионов. Правило Панета-Фаянса-Гана.
63. Причины соосаждения: адсорбция, окклюзия, изоморфизм. Понятие диффузионного слоя.
64. Аргентометрия. Кривые титрования. Метод Мора.
65. Аргентометрия. Метод Фольгарда. Метод Фаянса.
66. Методы гравиметрического анализа. Гравиметрическая форма. Форма осаждения. Требования к форме осаждения.
67. Относительное пересыщение. Метод возникающих реактивов. Старение осадка.
68. Условия образования аморфных осадков. Промывание осадка.
69. Расчёты в гравиметрическом анализе. Применение и преимущество методов осаждения.
69.1. Расчёты в ГА.
X(S)=m(BaSO4)* (1)
(1)
m1=m2*F
m(BaSO4)=m1-m2 (m1 – масса тигля с осадком, m2 – масса пустого тигля)
Если есть гравиметрическая форма BaSO4 массой m, а требуется определить m(S), воспользуемся формулой (1).
Отношение молярных масс определяемого компонента в гравиметрической форме называется фактором пересчёта (гравиметрический фактор). Обозначается F.
X=mF (2)
При расчёте F нужно учитывать стехиометрические коэффициенты, как в числителе, так и в знаменателе.
Mg в виде Mg2P2O7:
F=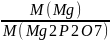 (3)
(3)
Абсолютная погрешность определения массы осадка:
m(BaSO4)= =3*104
=3*104
Относительная погрешность определения массы осадка:
σ= *100%=0,1%
*100%=0,1%
m(S)=m(BaSO4)*F*
