
анал реф 1
.docxМИНИСТЕРСТВО ОБРАЗОВАНИЯ РЕСПУБЛИКИ БЕЛАРУСЬ
УЧРЕЖНЕНИЕ ОБРАЗОВАНИЯ
«ПОЛЕССКИЙ ГОСУДАРСТВЕННЫЙ УНИВЕРСИТЕТ»
Кафедра биохимии и биоинформатики
Реферат
по дисциплине «Аналитическая и коллоидная химия»
На тему:
«Приемы определения неизвестной концентрации компонента в инструментальных методах анализа: методы градуировочного графика, стандартов, добавок и инструментальное титрование»
Подготовил: |
Студентка 2 курса, группы 22БХ-1 Децук Валерия Петровна
|
Проверил: |
ассист. Каф. биохим. и биоинф. Приловская Екатерина Игоревна
|
Пинск 2023
Оглавление
Введение 3
Глава 1. Метод градуированного графика 4
Глава 2. Метод стандартов (метод молярного свойства) 5
2.1 Метод одного стандарта. 5
2.2 Метод двух стандартов (ограничивающих растворов). 5
Глава 3. Метод добавок 6
3.1 Метод однократной добавки 6
3.2 Метод серии добавок 6
Глава 4. Инструментальное титрование 8
Заключение 9
Список используемой литературы 10
Введение
Зависимость интенсивности излучения от концентрации атомов в пламени для резонансных линий имеет линейный характер лишь на небольшом участке концентраций. Для большей точности желательно работать в прямолинейном участке градуировочного графика, который может оказаться разным при работе на различных приборах. Поэтому независимо от выбранного способа определения неизвестной концентрации вещества в растворе нужно провести градуировку прибора. Для этого с помощью эталонных растворов необходимо найти зависимость между показаниями прибора и концентрацией соли металла в растворе.
Для определения неизвестной концентрации вещества по величине АС химики-аналитики используют несколько прямых и косвенных приёмов, общих для всех физических и физико-химических методов анализа.
П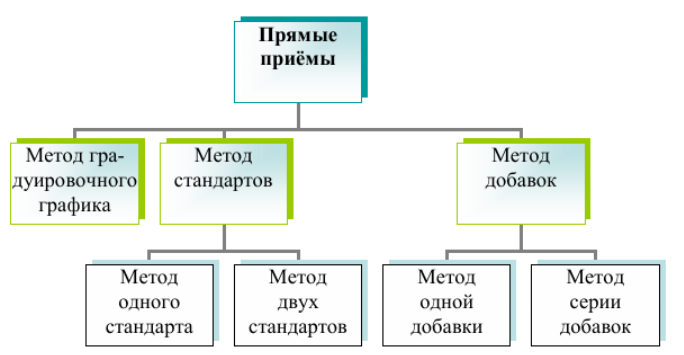 рямые
приёмы основаны на использовании
зависимости I = f(C). Они требуют наличия
эталонов, могут быть графическими и
расчётными.
рямые
приёмы основаны на использовании
зависимости I = f(C). Они требуют наличия
эталонов, могут быть графическими и
расчётными.
Рисунок 1 – Прямые приёмы определения неизвестной концентрации по величине аналитического сигнала
Косвенные приёмы (инструментальное титрование) основаны на измерении АС в ходе титрования. Они не требуют наличия эталонов. Кривую титрования строят в координатах «АС – объём титранта».
Глава 1. Метод градуированного графика
Метод градуировочного графика – это графический приём нахождения неизвестной концентрации (Сх) по величине аналитического сигнала пробы (Iх).
Д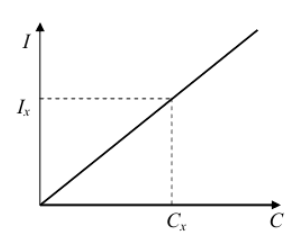 ля
проведения анализа готовят серию
стандартных растворов, измеряют величины
АС этих растворов и строят градуировочный
график I = f(C) (рис.2).
ля
проведения анализа готовят серию
стандартных растворов, измеряют величины
АС этих растворов и строят градуировочный
график I = f(C) (рис.2).
Рисунок 2 – Определение неизвестной концентрации методом градуировочного графика.
Затем в точно таких же условиях измеряют аналитический сиг-
нал пробы Iх и по графику определяют концентрацию анализируемого
вещества в пробе Сх.
Особенности метода:
желательно, чтобы график был линеен, т. к. нелинейность градуировочного графика снижает точность проведения анализа;
желательно, чтобы график выходил из начала координат;
график надо периодически проверять, а при замене каких-либо реагентов, растворов, приборов, условий проведения анализа – построить заново;
в случае большого разброса точек надо применять метод наименьших квадратов, а не строить график «на глаз», особенно при работе с малыми концентрациями.
Глава 2. Метод стандартов (метод молярного свойства)
Метод стандартов – это расчётный приём нахождения неизвестной концентрации. Он имеет две разновидности (рис. 1).
2.1 Метод одного стандарта.
Для проведения анализа готовят один стандартный раствор с концентрацией определяемого вещества Сст, затем измеряют величины АС этого раствора (Iст) и пробы (Iх) в одинаковых условиях.
И![]() сходя
из того, что Iх = kCх и Iст
= kCст, получаем:
сходя
из того, что Iх = kCх и Iст
= kCст, получаем:
О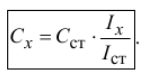 тсюда
выводим формулу, по которой рассчитывают
неизвестную концентрацию:
тсюда
выводим формулу, по которой рассчитывают
неизвестную концентрацию:
2.2 Метод двух стандартов (ограничивающих растворов).
Д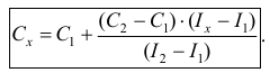 ля
проведения анализа готовят серию
стандартных растворов и измеряют
величины АС этих растворов и пробы в
одинаковых условиях. Затем выбирают
два стандартных раствора – «ограничивающие
растворы» – так, чтобы С1 <Сx
<С2 и I1 <Ix <I2.
Расчёт неизвестной концентрации
проводят по формуле:
ля
проведения анализа готовят серию
стандартных растворов и измеряют
величины АС этих растворов и пробы в
одинаковых условиях. Затем выбирают
два стандартных раствора – «ограничивающие
растворы» – так, чтобы С1 <Сx
<С2 и I1 <Ix <I2.
Расчёт неизвестной концентрации
проводят по формуле:
Особенность метода: оба варианта метода можно применять только в том случае, когда зависимость I = f(C) является линейной.
Глава 3. Метод добавок
Сущность метода добавок заключается в том, что сначала измеряют АС пробы (Iх), а затем – АС той же пробы с добавкой стандартного раствора определяемого вещества (Iх+ст). Метод имеет две разновидности.
3.1 Метод однократной добавки
М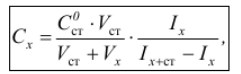 етод
однократной добавки является расчётным.
Неизвестную концентрацию рассчитывают
по формуле:
етод
однократной добавки является расчётным.
Неизвестную концентрацию рассчитывают
по формуле:
где
Сст0 – исходная концентрация стандартного раствора;
Vст – объём стандартного раствора, добавленный к пробе;
Vх – объём пробы.
3.2 Метод серии добавок
М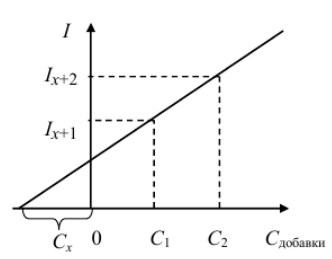 етод
серии добавок является графическим.
Для проведения анализа измеряют величины
АС пробы и нескольких растворов той же
пробы с добавками стандартного раствора.
Строят график в координатах «Аналитический
сигнал – концентрация добавки» и по
нему находят Сх как величину
отрезка, отсекаемого прямой на оси
абсцисс (рис. 3).
етод
серии добавок является графическим.
Для проведения анализа измеряют величины
АС пробы и нескольких растворов той же
пробы с добавками стандартного раствора.
Строят график в координатах «Аналитический
сигнал – концентрация добавки» и по
нему находят Сх как величину
отрезка, отсекаемого прямой на оси
абсцисс (рис. 3).
Рисунок 3 – Определение неизвестной концентрации методом добавок
Особенности метода:
метод добавок можно применять только в том случае, когда зависимость I = f(C) является линейной;
чаще всего метод добавок используют при анализе проб сложного состава, т. к. прирост АС при добавке стандартного раствора связан только с определяемым компонентом, а сигналы от мешающих компонентов пробы остаются постоянными.
Глава 4. Инструментальное титрование
При проведении анализа с использованием инструментального титрования измеряют какое-либо свойство раствора в процессе титрования. Кривые титрования получаются разными в зависимости от измеряемой величины.
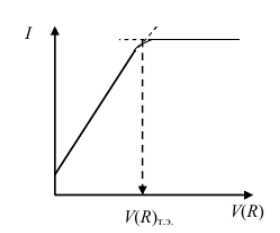 Линейные
кривые титрования получают, если АС
линейно меняется при изменении
концентрации вещества в растворе. К
таким сигналам относятся, например,
светопоглощение, сила тока, электрическая
проводимость и др. Объём в точке
эквивалентности (т. э.) находят по излому
кривой (рис. 4).
Линейные
кривые титрования получают, если АС
линейно меняется при изменении
концентрации вещества в растворе. К
таким сигналам относятся, например,
светопоглощение, сила тока, электрическая
проводимость и др. Объём в точке
эквивалентности (т. э.) находят по излому
кривой (рис. 4).
Рисунок 4 – Линейная кривая титрования
Л
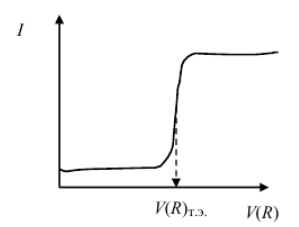 огарифмические
кривые титрования получают, если АС
связан с логарифмом концентрации
вещества в растворе. К таким сигналам
относятся, например, потенциал, рН и
др. Точку эквивалентности находят по
перегибу кривой (рис. 5).
огарифмические
кривые титрования получают, если АС
связан с логарифмом концентрации
вещества в растворе. К таким сигналам
относятся, например, потенциал, рН и
др. Точку эквивалентности находят по
перегибу кривой (рис. 5).
Рисунок 5 – Логарифмическая кривая титрования
В любом случае после построения кривой титрования и определения с её помощью объёма титранта, который потребовался для достижения т. э., расчёт результатов анализа проводят по закону эквивалентов.
Заключение
В заключение, можно отметить, что определение неизвестной концентрации компонента в инструментальных методах анализа является важной задачей в области аналитической химии. Для решения этой задачи используются различные приемы, среди которых основные – методы градуировочного графика, стандартов, добавок и инструментальное титрование.
Метод градуировочного графика основан на установлении зависимости между концентрацией анализируемого компонента и его интенсивностью, измеряемой с помощью инструментальных методов. Градуировочный график строится на основе измерений стандартных растворов с известными концентрациями компонента. Затем на основе полученной зависимости можно определить неизвестную концентрацию компонента в образце.
Метод стандартов основан на использовании стандартных растворов с известными концентрациями компонента для сравнения с образцом и установления его концентрации. Для этого с помощью инструментальных методов производится измерение интенсивности компонента в стандартных растворах и в образце, а затем проводится сравнение полученных результатов.
Метод добавок позволяет определить неизвестную концентрацию компонента путем последовательного добавления определенного количества этого компонента в образец. Затем с помощью инструментальных методов измеряется интенсивность добавленного компонента и на основе полученных данных рассчитывается концентрация компонента в образце.
Инструментальное титрование – метод, основанный на реакции между анализируемым компонентом и реактивом. Путем измерения изменения интенсивности реакции с помощью инструментальных методов можно определить концентрацию компонента в образце.
Все эти методы имеют свои преимущества и ограничения, и выбор метода зависит от требований анализа и доступных средств и оборудования. Однако, несмотря на различия в этих методах, их основная цель заключается в определении неизвестной концентрации компонента с высокой точностью и достоверностью.
Список используемой литературы
Физико-химические методы анализа: Тексты лекций по дисциплине «Аналитическая химия и физико-химические методы анализа» для студентов химико-технологических специальностей заочной формы обучения / А. Е. Соколовский, Е. В. Радион. – Минск.: БГТУ, 2007 – 128 с.
Физико - химические методы анализа: Учеб. пособие / Н.М.Дубова, Т.М.Гиндуллина, Г.Н.Сутягина, Е.И.Короткова. - Томск: Изд.ТПУ, 1999 - 123с.
Аналитическая и коллоидная химия : специальность «1 31 01 02 Биохимия» [Электронный ресурс] : электронный учебно-методический комплекс / Н.А. Глинская [и др.]; УО "Полесский государственный университет". – Пинск : ПолесГУ, 2022. - 445 с.
