Реакции и процессы в анал химии
.docxРеакции и процессы, используемые в аналитической химии
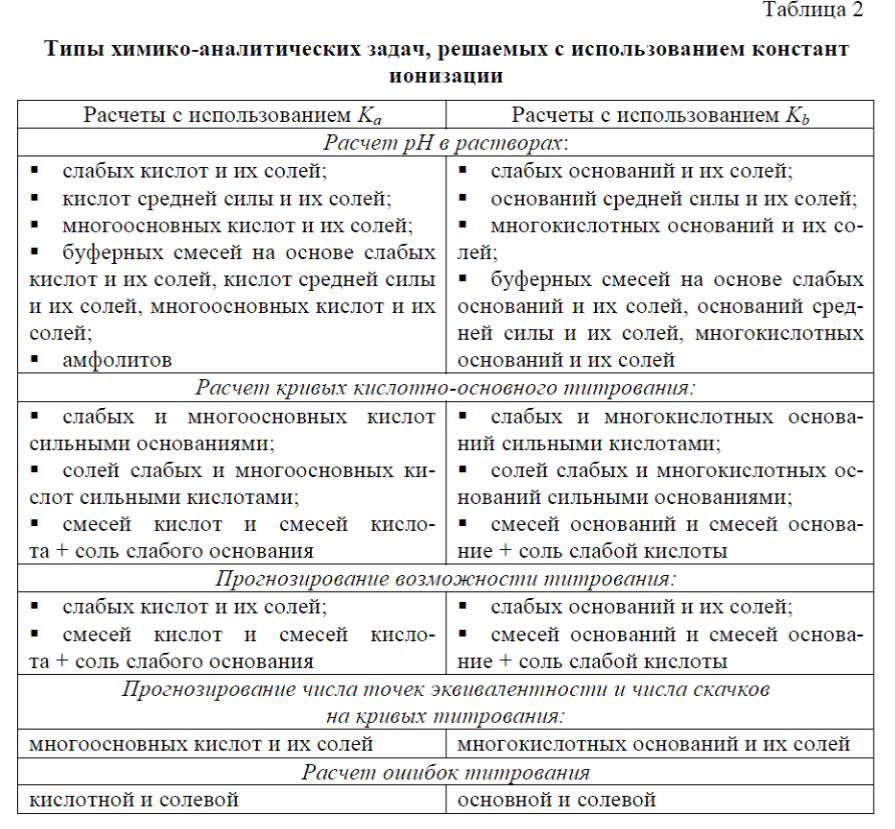
КИСЛОТНО-ОСНÓВНОЕ РАВНОВЕСИЕ
Кислотно-оснóвные реакции – это реакции с переносом протона Н+, поэтому иначе их называют протолитическими реакциями. В аналитической химии чаще всего используют две теории кислот и оснований: - теория электролитической диссоциации (теория Аррениуса);
 -протолитическая
(протонная) теория Бренстеда и
Лоури.
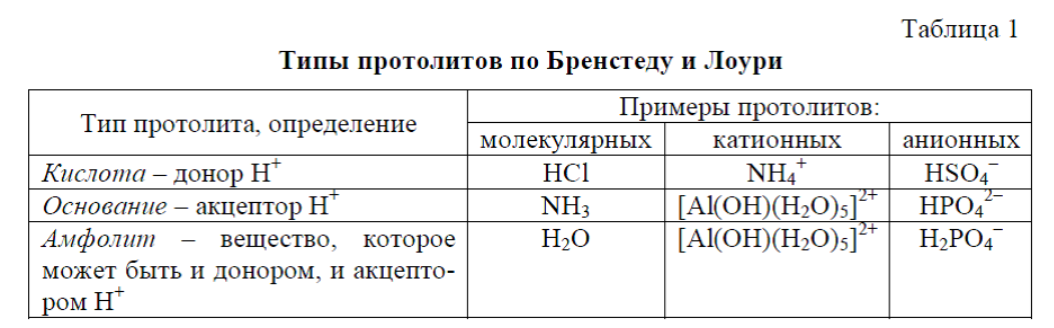
Согласно теории Бренстеда
и Лоури, вещества, которые участвуют в
протолитических реакциях,
называются протолитами. Протолиты
могут быть молекулярными, катионными
и анионными. Типы протолитов приведены
в таблице 1.
-протолитическая
(протонная) теория Бренстеда и
Лоури.
Согласно теории Бренстеда
и Лоури, вещества, которые участвуют в
протолитических реакциях,
называются протолитами. Протолиты
могут быть молекулярными, катионными
и анионными. Типы протолитов приведены
в таблице 1.
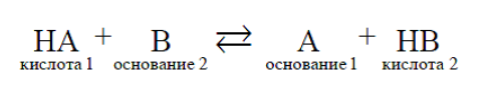 Протолитическое
равновесие – это взаимодействие кислоты
и основания
с образованием новой кислоты и нового
основания. В нем может
принимать участие растворитель-амфолит,
например вода.
Сущность
протолитического равновесия заключается
в обратимом переносе протона Н+ от
кислоты к основанию:
Протолитическое
равновесие – это взаимодействие кислоты
и основания
с образованием новой кислоты и нового
основания. В нем может
принимать участие растворитель-амфолит,
например вода.
Сущность
протолитического равновесия заключается
в обратимом переносе протона Н+ от
кислоты к основанию:
В протолитическом равновесии всегда участвуют две сопряженные кислотно-оснóвные пары. В приведенном примере пара 1 состоит из кислоты НА и сопряженного с ней основания А, пара 2 – из кислоты НВ и основания В.
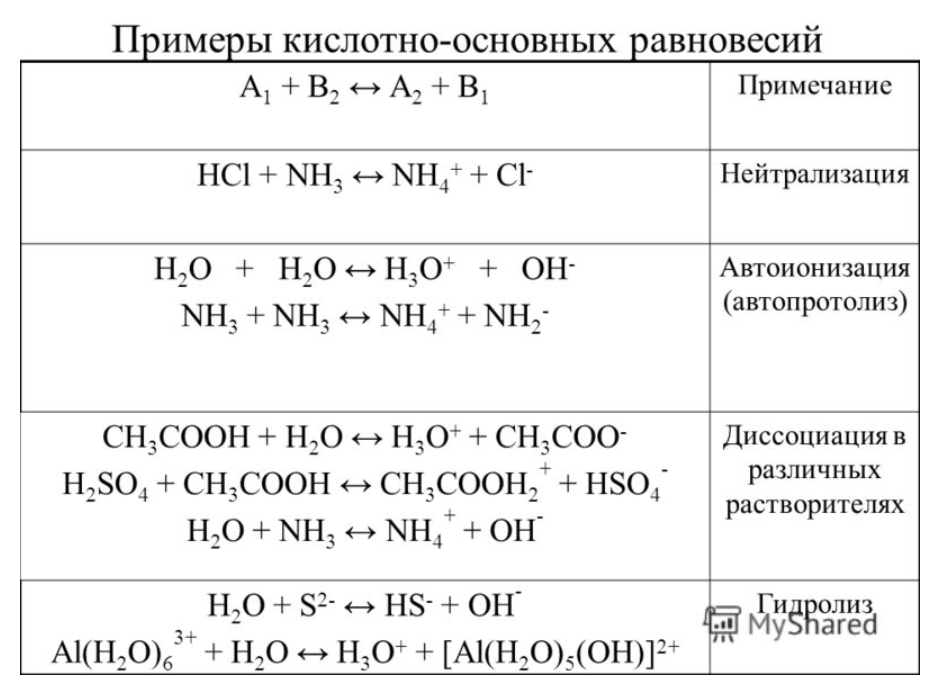 Силу
кислотных и оснóвных свойств отдельных
компонентов сопряженной пары оценивают
с помощью константы кислотности Kа и
константы основности Kb.
Силу
кислотных и оснóвных свойств отдельных
компонентов сопряженной пары оценивают
с помощью константы кислотности Kа и
константы основности Kb.
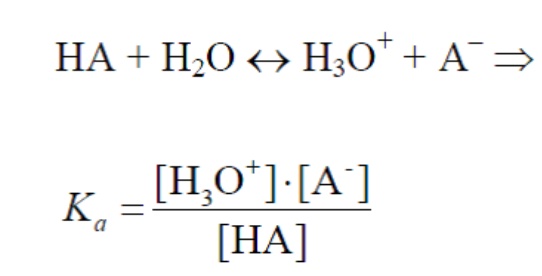 Константа
кислотности – это константа равновесия:
Константа
кислотности – это константа равновесия:
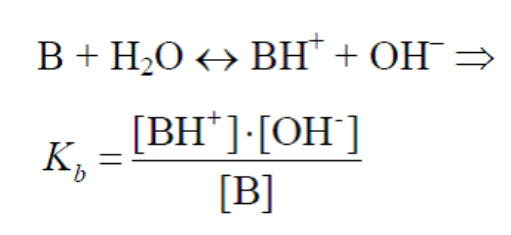 Константа
основности – это константа равновесия:
Константа
основности – это константа равновесия:
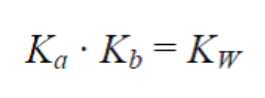 В
водном растворе константы кислотности
и основности сопряженной кислотно-оснóвной
пары связаны между собой через константу
автопротолиза воды KW:
В
водном растворе константы кислотности
и основности сопряженной кислотно-оснóвной
пары связаны между собой через константу
автопротолиза воды KW:
(1.1)
 Константа
автопротолиза воды KW = 10–14, она
характеризует равновесие автопротолиза
воды:
Константа
автопротолиза воды KW = 10–14, она
характеризует равновесие автопротолиза
воды:
Если прологарифмировать формулу (1.1) с обратным знаком, тО получим удобное для использования выражение:
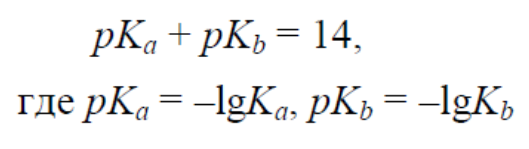
(1.2)
Таким образом, чем сильнее кислота, тем слабее сопряженное с ней основание и наоборот. Например, НCl – сильная кислота, значит, ион Cl– является чрезвычайно слабым основанием.
Для водных растворов численные значения констант кислотности и основности (теория Бренстеда и Лоури) совпадают со значениями констант диссоциации (ионизации) (теория Аррениуса), поэтому можно пользоваться справочной литературой, составленной на основе классической теории. Для молекулярных кислот и оснований константы Kа и Kb, а также их отрицательные логарифмы рKa и рKb приведены в таблицах, для катионных и анионных протолитов эти значения рассчитываются по формулам (1.1) или (1.2).
Равновесия в водных растворах кислот, оснований и амфолитов.
Расчет рН протолитических систем
Водородный показатель рН – это отрицательный логарифм активности или концентрации ионов Н+ (ионов гидроксония Н3О+):
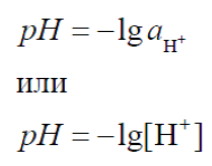
Расчет численного значения рН проводят с точностью до сотых долей единицы рН, например рН = 6,15.
Рассмотрим наиболее распространенные случаи расчета рН.
 Равновесия
и расчет рН в растворах кислот
Равновесия
и расчет рН в растворах кислот
Необходимость учета автопротолиза воды можно продемонстрировать на следующем примере. Рассчитаем значение рН в растворе хлороводородной кислоты при С(HCl) = 10–8 моль/л по формуле (1.3), которая используется в теории Аррениуса независимо от концентрации кислоты:
рН = – lg10–8 = 8
Ответ является абсурдным (щелочная среда в растворе кислоты!). Если провести расчет по теории Бренстеда-Лоури, т. е. учесть автопротолиз растворителя-амфолита H2O, то по формуле (1.4) получим
 ответ
рН = 6,98
ответ
рН = 6,98
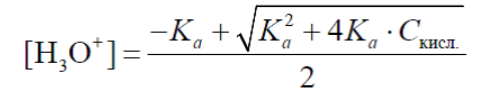

В этой реакции аммиак NH3 является молекулярным основанием, а ион NH4+ – сопряженной катионной кислотой. Следовательно, для расчета рН в растворе NH4Cl выбираем формулу (1.5). В нее входит величина рKa, в нашем случае рKa(NH4+), которой в таблицах нет. Для ее расчета используем табличное значение рKb(NH3) и формулу (1.2):
рKa(NH4+) = 14 – рKb(NH3)
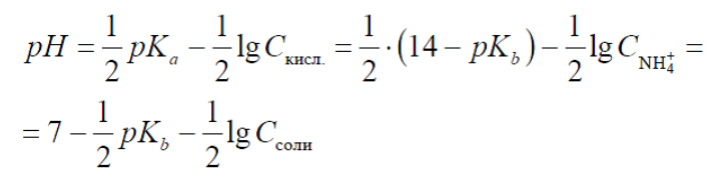 Подставив
это выражение в формулу (1.5), получим
Подставив
это выражение в формулу (1.5), получим

 Равновесия
и расчет рН в растворах оснований
Равновесия
и расчет рН в растворах оснований


 Следовательно,
для расчета рН в растворе CH3COONa выбираем
формулу (1.10). В нее входит величина рKb,
в нашем случае рKb(CH3COO–), которой в
таблицах нет. Для ее расчета используем
табличное значение рKа(CH3COOH) и формулу
(1.2):
Следовательно,
для расчета рН в растворе CH3COONa выбираем
формулу (1.10). В нее входит величина рKb,
в нашем случае рKb(CH3COO–), которой в
таблицах нет. Для ее расчета используем
табличное значение рKа(CH3COOH) и формулу
(1.2):
рKb(CH3COO–) = 14 – рKа(CH3COOH)
Подставив это выражение в формулу (1.10), получим





 В
каждой сопряженной паре есть кислота.
Для использования формулы (1.13) необходимо
знать константы кислотности HCN и NH4+.
Первую из них можно найти в справочнике,
а вторую – рассчитать по формуле (1.2),
используя табличное значение рKb(NH3):
В
каждой сопряженной паре есть кислота.
Для использования формулы (1.13) необходимо
знать константы кислотности HCN и NH4+.
Первую из них можно найти в справочнике,
а вторую – рассчитать по формуле (1.2),
используя табличное значение рKb(NH3):
рKa(NH4+) = 14 – рKb(NH3)
 Подставив
это выражение в формулу (1.13), получим
Подставив
это выражение в формулу (1.13), получим