
- •1.Состав органических веществ, их многообразие. Место органической химии в системе естественных наук. Источники органических соединений.
- •4.Основные признаки классификации органических веществ. Основные классы органических веществ.(с 5)
- •5.Номенклатура органических соединений. Основные принципы построения названий органических соединений. С 27
- •7. Типы связей в молекулах органических соединений. Σ- и π-связи. Гибридизация, понятие о молекулярных орбиталях.
- •8.Представление о механизмах реакций. Представление о промежуточных частицах: радикалы, карбокатионы, карбанионы. Классификация реагентов: радикалы, нуклеофилы, электрофилы.
- •10.Кислоты и основания (Бренстед, Льюис). Сопряженные кислоты и основания. Кислотно-основные равновесия. Константа кислотной ионизации и ее показатель (рКа)
- •11.Взаимное влияние атомов в молекулах, ионах, радикалах. Электронные и пространственные эффекты в органических реакциях (индуктивный эффект, эффект поля, мезомерный эффект, гиперконьюгация).
- •13.Гомологический ряд, номенклатура, электронное строение, sp3-гибридизация и физические свойства алканов.(с 26)
- •14.Химические свойства алканов. Общие представления о механизме цепных радикальных реакций замещения в алканах (на примере реакции галогенирования).
- •15.Номенклатура, структурная и пространственная изомерия, электронное строение, sp2-гибридизация и физические свойства алкенов.
- •17.Химические свойства алкенов: реакции присоединения галогенов, галогеноводородов, воды. Правило Марковникова и его объяснение.
- •18.Представление о стереохимии присоединения галогенов у алкенов. Перегруппировки карбокатионов. Реакции радикального присоединения (по Харашу).
- •20.Окислительное расщепление алкенов (восстановительный и окислительный озонолиз). Гидроборирование алкенов и использование в синтезе спиртов.
- •22.Аллильное хлорирование алкенов, механизм. Аллильный радикал. Окисление алкенов кислородом воздуха (пероксидное окисление).
- •23.Номенклатура, классификация, изомерия диеновых углеводородов.
- •25.Изопреновое звено в природных соединениях. Понятие об изопреноидах. Каучук. Синтетические каучуки.
- •26.Номенклатура, электронное строение, sp-гибридизация и физические свойства алкинов.
- •27.Химические свойства алкинов: каталитическое гидрирование и восстановление натрием в жидком аммиаке, использование в синтезе (z)- и (e)-алкенов.
- •28.Химические свойства алкинов: реакции электрофильного присоединения к тройной связи – галогенирование, гидрогалогенирование, гидратация (реакция Кучерова)
- •29.Кислотность ацетилена и терминальных алкинов. Димеризация, тримеризация ацетилена. Полиацетилен.
- •30.Классификация, номенклатура, структурная изомерия и пространственное строение циклоалканов.
- •32. Классификация и номенклатура аренов. Природа связей в молекуле бензола. Конденсированные ароматические углеводороды: нафталин, антрацен, фенантрен, бензпирен.
- •33. Ароматичность, критерии ароматичности. Правило Хюккеля.
- •35. Влияние заместителей в бензольном кольце на изомерный состав продуктов и скорость реакции. Активирующие и дезактивирующие заместители. Орто-, пара- и мета-ориентанты.
- •36. Реакции радикального замещения и окисления в боковой цепи. Причины устойчивости бензильных радикалов.
- •37. Классификация, номенклатура, изомерия галогенуглеводородов.
- •40. Литий- и магнийорганические соединения и их использование в органическом синтезе.
- •41. Биологическое действие галогенпроизводных, их применение в народном хозяйстве. Хлороформ, иодоформ, перфторуглеводороды, перфторполиэтилен (тефлон). Инсектициды.
- •42. Одноатомные спирты. Номенклатура, изомерия. Электронное строение. Физические свойства спиртов, роль водородной связи.
- •43. Химические свойства спиртов: кислотно-основные свойства. Алкоголяты металлов, их основные и нуклеофильные свойства.
- •44. Реакции нуклеофильного замещения с участием спиртов. Биологически важные реакции нуклеофильного замещения с участием эфиров фосфорных кислот.
- •45. Внутри- и межмолекулярная дегидратация спиртов (образование алкенов и простых эфиров). Окисление первичных и вторичных спиртов.
- •47. Фенолы. Номенклатура и изомерия. Простейшие представители: фенол, крезолы, пирокатехин, резорцин, гидрохинон, флороглюцин, пирогаллол. Электронное строение фенола. Кислотность фенолов.
- •48. Образование простых и сложных эфиров фенолов. Реакции электрофильного замещения в ряду фенолов (галогенирование, сульфирование, нитрование, алкилирование).
- •49. Карбоксилирование фенолятов щелочных металлов (реакция Кольбе). Окисление фенолов.
- •50. Хиноны и их биологическая роль. Фенольные соединения в природе. Витамин е. Флавоноиды.
- •51. Простые эфиры. Номенклатура, классификация. Расщепление кислотами. Образование гидропероксидов, их обнаружение и разложение. Циклические простые эфиры. Тетрагидрофуран. 1,4-Диоксан.
- •52. Оксираны: получение, взаимодействие с водой, аммиаком и аминами, магнийорганическими соединениями. Краун-эфиры: комплексообразование с ионами металлов, применение.
- •53. Кислотность тиолов. Нуклеофильные свойства тиолов, тиолятов и органических сульфидов. Окисление тиолов. Образование дисульфидов и их роль в биохимических процессах.
- •54. Классификация, номенклатура и изомерия аминов. Алифатические и ароматические амины, первичные, вторичные и третичные амины.
- •57. Классификация, номенклатура и изомерия карбонильных соединений.
- •58. Строение карбонильной группы в альдегидах и кетонах и реакции нуклеофильного присоединения (реактивами Гриньяра, циановодородом). Механизм реакций.
- •59. Реакции карбонильных соединений с гетеронуклеофилами:
- •60. Реакции енольных форм карбонильных соединений: a-галогенирование, галоформное расщепление, изотопный обмен водорода. Альдольно-кротоновая конденсация, кислотный и основный катализ.
- •61. Взаимодействие неенолизирующихся альдегидов со щелочами (реакция Канниццаро). Реакции окисления и восстановления карбонильных соединений.
- •62. Монокарбоновые кислоты. Номенклатура. Строение карбоксильной группы и карбоксилат-иона. Кислотность карбоновых кислот.
- •63. Производные карбоновых кислот: сложные эфиры и тиоэфиры (s-эфиры карбоновых кислот), галогенангидриды, ангидриды, амиды, нитрилы, их получение и взаимопревращения.
- •64. Кислотный и щелочной гидролиз сложных эфиров и амидов.
- •65. Реакции ацилирования, этерификации, аминирования и восстановления карбоновых кислот и их производных.
- •66. Жирные кислоты, важнейшие представители (пальмитиновая, стеариновая, олеиновая, линолевая, линоленовая). Жиры, сложные липиды (фосфатидовая кислота и ее производные), мыла.
- •67. Ненасыщенные карбоновые кислоты: акриловая, метакриловая, полимеры на их основе.
- •68. Дикарбоновые кислоты. Основные представители: щавелевая, малоновая, адипиновая, фталевые кислоты. Фумаровая и малеиновая кислоты. Полиэфирные волокна на основе терефталевой и адипиновой кислот.
- •69. Классификация углеводов. Биологическая роль и распространенность углеводов.
- •72. Дисахариды и их типы (восстанавливающие и невосстанавливающие). Сахароза, лактоза, мальтоза, целлобиоза.
- •73. Полисахариды (крахмал, целлюлоза, хитин, гликоген).
- •75. Классификация аминокислот. Основные представители природных a-аминокислот, их стереохимия.
- •76. Свойства аминокислот: амфотерность, изоэлектрическая точка.
- •77. Пептидная связь. Синтез пептидов: активация и защита функциональных групп аминокислот. Белки, их строение и биологическая роль
- •79. Шестичленные гетероциклы с одним гетероатомом: пиридин, хинолин, изохинолин. Ароматичность пиридина и особенности проведения реакций электрофильного замещения. Пиридин как основание.
4.Основные признаки классификации органических веществ. Основные классы органических веществ.(с 5)
Основой органического вещества является углеродный скелет, а составные части — это функциональные группы, гетероатомы, кратные связи. Классификация также необходима для того, чтобы правильно называть соединения. Поэтому классификация лежит в основе Международной номенклатуры органических соединений.
В основе классификации органических веществ можно выделить несколько основных подходов:
1. Строение углеводородной цепи: циклические, линейные, разветвленные.
2. Наличие кратных связей: предельные и непредельные
3. Наличие функциональных групп и замещающих атомов: кислородсодержащие, азотсодержащие, галлоидзамещенные УВ.
4. Наличие гетероатома (N, O, S в структуре цикла): гетероциклические УВ.
5. Природное происхождение: белки, жиры, углеводы, нуклеиновые кислоты, гормоны, витамины.
Функциональная группа — это совокупность атомов, определяющая характерные химические свойства целого класса веществ. По типу функциональных групп органические соединения делят на следующие классы:
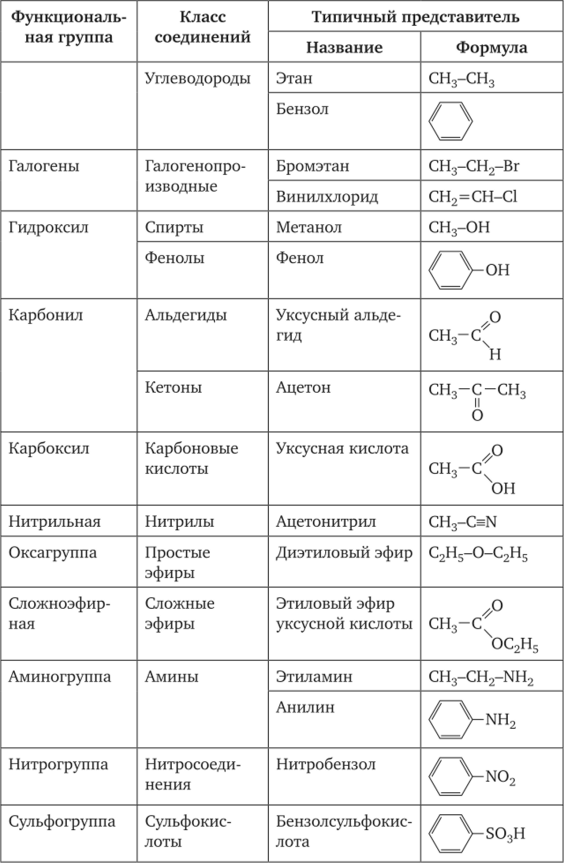
5.Номенклатура органических соединений. Основные принципы построения названий органических соединений. С 27
Тривиальная номенклатура. Первые названия, которые давали органическим соединениям, были случайными. Тривиальные, или эмпирические, названия соединений отражают природные источники соединений (муравьиная кислота, мочевина, индиго, кофеин), способы получения (пировиноградная кислота), характерные свойства (пикриновая и капроновая кислоты), имена первооткрывателей (реактив Гриньяра).
Рациональная номенклатура. Это первая номенклатура, в которой стали учитывать в названии вещества его строение. В основе рациональных названий используется принцип деления органических соединений на гомологические ряды.
Гомологическим называют ряд соединений, в котором каждый последующий представитель отличается от предыдущего на группу СН2.
Однако для названия сложных химических структур рациональная номенклатура оказалась непригодной. В настоящее время применение этой номенклатуры ограничено.
Международная номенклатура (IUPAC). Основы международной номенклатуры заложены в 1892 году на международном конгрессе химиков в Женеве (женевская номенклатура).
Номенклатура IUPAC предусматривает несколько вариантов образования названий органических соединений, из которых наиболее широко применяются заместительный и радикало-функциональный. Иногда с целью максимального упрощения построения названий соединений используют соединительный, заменительный и другие варианты номенклатуры IUPAC.
Заместительная номенклатура. При образовании названий по заместительной номенклатуре органические соединения рассматривают как производные простейших углеводородов, в молекуле которых один или несколько атомов водорода замещены на другие атомы или группы атомов, называемые заместителями.
При составлении названия по заместительному варианту номенклатуры
IUPAC прежде всего определяют, какие функциональные группы входят в состав соединения, и выбирают среди них старшую.
6. Типы изомерии: структурная и пространственная. Способы изображения пространственного строения молекул. 7.Конформации, конформеры. Энантиомеры. Понятие об оптической активности и хиральности. Рацематы. Принципы R-, S-номенклатуры; D- и L-ряды. Диастереомеры. Пространственная изомерия алкенов: цис-, транс- и Z-, E-номенклатуры.
Изомерия — явление, заключающееся в существовании соединений, одинаковых по качественному и количественному составу, но различающихся порядком связывания атомов в молекуле или расположением их в пространстве, а вследствие этого имеющих различные физические и химические свойства.
Различают два основных вида изомерии — структурную и пространственную (стереоизомерия).
Структурные изомеры отличаются друг от друга последовательностью связывания атомов в молекуле, то есть структурой. Структурную изомерию подразделяют на изомерию углеродной цепи, изомерию положения, изомерию функциональных групп.
Изомерия углеродной цепи обусловлена разной последовательностью связывания атомов, образующих углеродный скелет молекулы.
Изомерией
функциональных групп называют вид
структурной изомерии, при котором
изомеры отличаются природой функциональной
группы
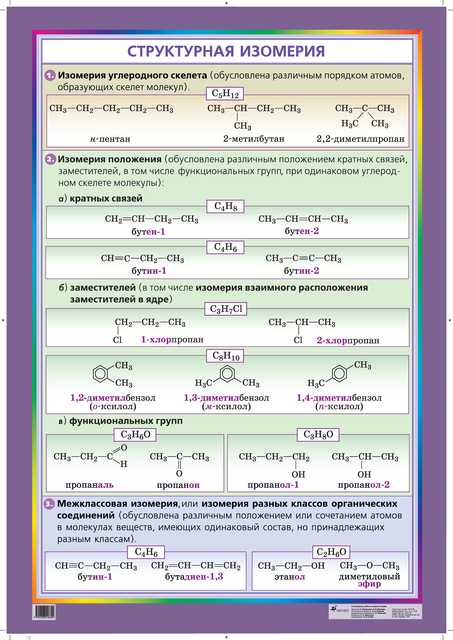
Вещества, имеющие одинаковый состав и порядок связывания атомов в молекуле, но отличающиеся друг от друга их расположением в пространстве, называют пространственными изомерами, или стереоизомерами.
Для изображения пространственного строения органических соединений используют молекулярные модели и стереоформулы.

Молекулярные модели. Более наглядное представление о пространственном строении молекулы дают молекулярные модели. Обычно применяют три основных типа моделей — шаростержневые, скелетные и полусферические.
В шаростержневых моделях молекул атомы представлены разноцветными
шариками, а химические связи — стержнями. Шарики связаны друг с другом стержнями с учетом взаимного расположения атомов в пространстве. Шаростержневые модели удобны для рассмотрения валентных углов и вращения вокруг простых связей, однако они не отражают относительных размеров атомов и межатомных расстояний в молекуле.
Модели Драйдинга, в отличие от шаростержневых, ограничиваются изображением лишь скелета молекулы, то есть химических связей между атомами, причем межатомные расстояния в этих моделях пропорциональны истинным.
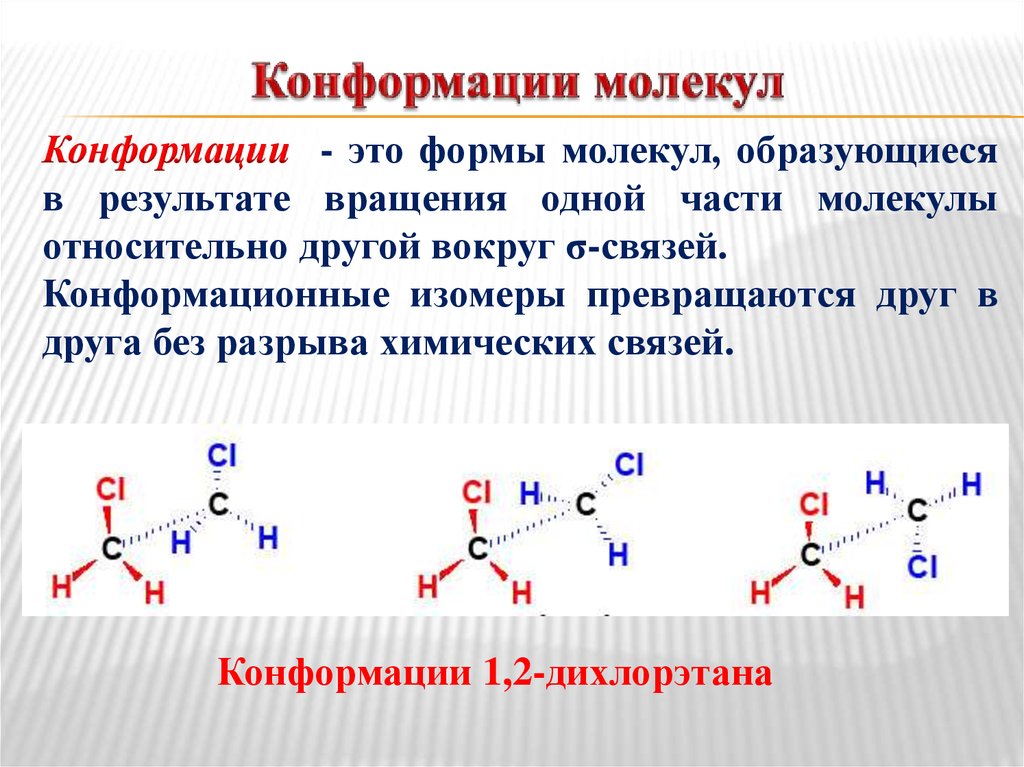
Конформация молекул, геометрические формы, которые могут принимать молекулы органических соединений при вращении атомов или групп атомов (заместителей) вокруг простых связей при сохранении неизменными порядка химической связи атомов, длины связей и валентных углов. Конформеры — молекулы, одинаковые по количеству всех атомов и атомов, связанных друг с другом, но различающиеся по их третичной структуре. Итак, конформации – это различающиеся по внутренней энергии состояния молекулы, которые возникают при свободном вращении вокруг одинарной связи. Конформеры – это стереоизомерные структуры, находящиеся в подвижном равновесии и способные к взаимопревращению путем вращения вокруг простых связей.
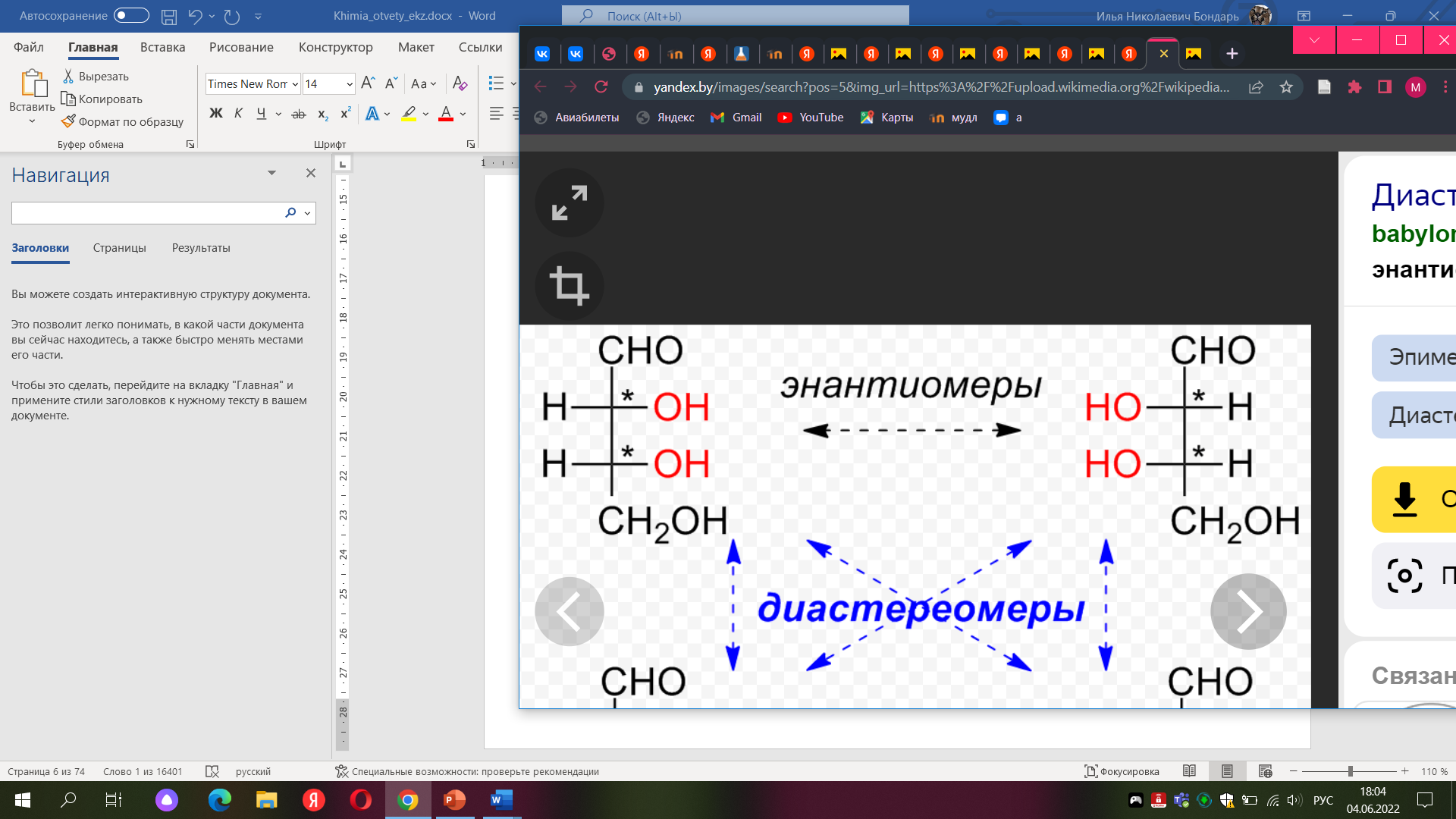
Энантиомеры — пара стереоизомеров, представляющих собой зеркальные отражения друг друга, не совмещаемые в пространстве.
Понятие о хиральных объектах было введено в конце XIX в. Кельвином. Согласно определению, любая геометрическая фигура или группа точек называется хиральной, если отображение в идеальном плоском зеркале не может быть совмещенным с нею самою.
Оптическая активность - это способность среды (кристаллов, растворов, паров вещества) вызывать вращение плоскости поляризации проходящего через нее оптического излучения.
Рацемат — эквимолярная смесь двух энантиомеров. Рацематы не обладают оптической активностью, а также отличаются по свойствам от индивидуальных энантиомеров. Являются продуктами нестереоселективных реакций.
R/S-Номенклатура является наиболее широко используемой в данное время, поскольку позволяет охарактеризовать энантиомер по его абсолютной конфигурации. Это стало возможным благодаря открытию рентгеноструктурного анализа, позволяющего установить точное пространственное расположение атомов в молекуле.
Данный вид номенклатуры основывается на присвоении хиральному атому углерода обозначения R или S на основании взаимного расположения четырёх связанных с ним заместителей.
D/L-Номенклатура была введена Э. Фишером для описания относительной конфигурации моносахаридов. Она основана на конфигурации глицеринового альдегида, существующего в виде двух энантиомеров, из которых путём последовательных реакций наращивания углеродной цепи можно получить производные моносахариды.

Диастереомеры — стереоизомеры, не являющиеся зеркальными отражениями друг друга. Диастереомерия возникает, когда соединение имеет несколько стереоцентров.
