
- •План лекции
- •Энзимология – наука, изучающая ферменты
- •1. Кинетика ферментативных реакций
- •Теории о механизмах действия ферментов
- •2. Теория «индуцированного соответствия»
- •3. Теория «индуцированного соответствия» (современные представления)
- •Теория переходных состояний (промежуточных соединений)
- •Механизмы ферментативных реакции
- •Энергетика ферментативных реакций
- •Неферментативная реакция
- ••ЭНЕРГЕТИЧЕСКИЙ БАРЬЕР РЕАКЦИИ –
- •Каталаза
- •Кинетика
- •Зависимость скорости реакции от концентрации фермента
- •Влияние температуры на скорость ферментативной реакции
- •Влияние рН на скорость ферментативной реакции
- •Зависимость скорости ферментативной реакции от рН
- •Константа Михаэлиса-Ментона
- •Уравнение скорости ферментативной реакции
- •Влияние активаторов и ингибиторов на скорость ферментативных реакций
- •Реакции ингибирования ферментативных процессов
- •Варианты взаимодействия ингибитора с ферментом
- •Конкурентный тип ингибирования
- •Неконкурентный тип ингибирования
- •2. Регуляция скорости ферментативных реакций в организме
- •Важнейшим свойством живых организмов является способность к поддержанию гомеостаза. Гомеостаз в организме поддерживается
- •I. Доступность молекул субстрата и кофермента
- •Инсулин
- •II. Регуляция каталитической активности фермента
- •Механизмы специфической регуляции каталитической активности ферментов:
- •1. Аллостерическая регуляция
- •2.Регуляция каталитической активности ферментов
- •3). Регуляция каталитической активности ферментов путем их ковалентной модификации
- •III. Механизмы регуляции количества ферментов
- ••Репрессоры (точнее корепрессоры) - вещества, которые останавливают синтез ферментов.
- •3. Клеточная сигнализация
- •В многоклеточных организмах поддержание гомеостаза обеспечивают 3 системы:
- •Гормоны - это сигнальные молекулы беспроводного системного действия Истинные гормоны в отличии от
- •Каскадные системы
- •каскадные системы состоят из:
- •Рецепторы
- •Рецептор, связанный с ионным каналом
- •Работа рецептора связанная с G-белком (серпантинный)
- •Рецептор с ферментативной активностью (тирозинкиназный)
- •Аденилатциклазная система
- •Сигнальные молекулы:
- •Гормоны:
- •Трансмембранная передача информации с участием цитоплазматических рецепторов
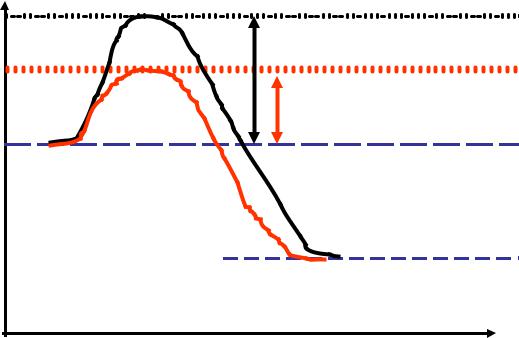
•ЭНЕРГЕТИЧЕСКИЙ БАРЬЕР РЕАКЦИИ –
кол-во энергии, которое необходимо молекуле, чтобы вступить в химическую реакцию.
•ЭНЕРГИЯ АКТИВАЦИИ - кол-во энергии, которое необходимо сообщить молекуле для преодоления энергетического барьера.
|
|
S* |
|
|
системы |
|
|
Энергия активации |
|
|
|
некатализируемой реакции |
||
S |
ES* |
Энергия активации |
||
энергия |
катализируемой реакции |
|||
|
||||
Исходное |
|
|||
состояние |
|
|||
Свободная |
P |
|||
|
|
|||
|
|
Конечное состояние |
||
|
|
|
Ход реакции |
|
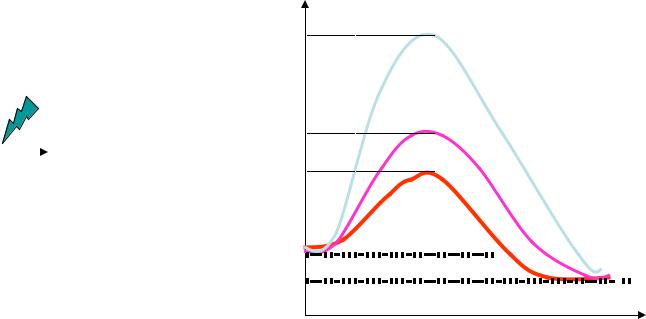
Каталаза
1) 2Н2О2 |
|
2Н2О + О2 |
|
Энергия активации:
Свободная энергия системы
1.
2.
3.
Энергия ктивацииа
Ход реакции
1.В спонтанной реакции – 18 ккал/моль
2.При использовании катализатора Fe2+ – 12 ккал/моль
3.В присутствии фермента каталазы – 5 ккал/моль
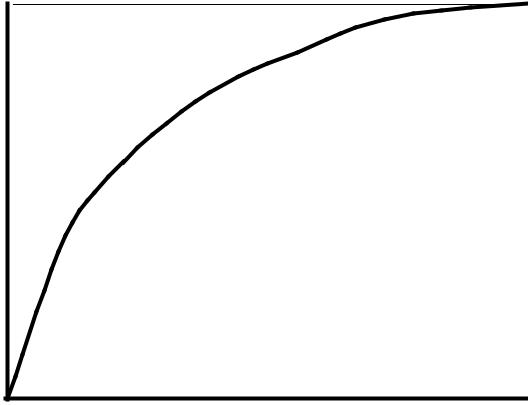
Кинетика |
ферментативных реакций |
Зависимость скорости реакции |
от концентрации субстрата |
Vmax |
Концентрация |
фермента - |
константа |
[S] |

Зависимость скорости реакции от концентрации фермента
V
Концентрация субстрата – константа
концентрация
фермента
Влияние температуры на скорость ферментативной реакции
•Повышение температуры на 10 градусов повышает скорость химической реакции в 2-4 раза.
•При повышение температуры фермент подвергается денатурации и теряет свою активность.

|
|
|
|
Скорость |
|
|
V |
|
|
ферментативной |
|
|
|
|
|
|
реакции |
|
|
|
|
|
|
|
|
|
|
|
Количество |
|
|
|
Скорость |
|
|
активного |
|
|
реакции активного |
||
|
фермента |
|
|
|
фермента |
|
0 |
10 |
20 |
30 |
40 |
50 |
60 T |
Влияние рН на скорость ферментативной реакции
•Изменение концентрации Н+ меняет химический состав фермента, его строение и каталитическую активность.
•Изменение концентрации Н+ меняет химический состав субстрата, его строение и способность вступать в ферментативную реакцию.
•Денатурацией фермента при очень высоких или очень низких рН.

Зависимость скорости ферментативной реакции от рН
V |
|
|
|
|
|
|
|
0 |
4 |
5 |
6 |
7 |
8 |
9 |
pH |
|

Константа Михаэлиса-Ментона
•Km – концентрация субстрата [S], при которой скорость ферментативной реакции V равна половине от максимальной
Vmax |
|
Vmax |
|
2 |
|
Km |
[S] |
