
Полезные материалы за все 6 курсов / Ответы к занятиям, экзаменам / Адсорбция
.pdfЗАДАНИЕ № 2
Определение зависимости поверхностного натяжения раствора от концентрации ПАВ сталагмометрическим методом
Цель работы. Изучить зависимость величины поверхностного натяжения раствора от концентрации ПАВ
Работа выполняется аналогично действиям в работе № 1.
1.Как и в задании 1, вначале подсчитывают число капель воды.
2.Затем подсчитывают число капель водных растворов амилового спирта следующих концентраций: 0,01 М; 0,025 М; 0,05 М; 0,1 М; 0,2М. Подсчёт капель нужно начинать производить, начиная с растворов низшей концентрации.
3.Рассчитывают поверхностное натяжение водных растворов амилового спирта по формуле, приведённой в задании 1.
4.Графически представляют зависимость поверхностного натяжения водных растворов амилового спирта от его концентрации.
5.Делают вывод о зависимости σ от концентрации растворов амилового спирта.
ЗАДАНИЕ № 3
Изучение адсорбции вещества из раствора на твёрдом адсорбенте
Цель работы. Экспериментально определить величину адсорбции уксусной кислоты из раствора на активированном угле.
Сущность работы сводится к приведению растворов известной концентрации в контакт с адсорбентом. Затем через некоторое время после установления адсорбционного равновесия находят концентрацию равновесного раствора. Количество адсорбированного вещества из раствора вычисляют по разности между концентрацией раствора до и после адсорбции. Определяя эту разность для растворов различной концентрации и зная массу адсорбента, получают данные об удельной адсорбции вещества при разных значениях равновесных концентраций. По этим данным строят изотерму адсорбции. Изотерма описывается с помощью уравнения Лэнгмюра.
Ход работы
Начертите таблицу по форме, указанной ниже:
№ |
Концентрация |
Концентрация NaOH |
Объём |
Равновесная |
Адсорбция |
колбы |
СН3СООН в исходном |
в растворе для |
раствора |
концентрация |
СН3СООН, |
|
растворе, моль/л |
титрования, моль/л |
NaOH, мл |
СН3СООН в |
моль/г |
|
|
|
|
фильтрате, моль/л |
|
1 |
0,1 |
|
|
|
|
2 |
0,2 |
|
|
|
|
3 |
0,3 |
|
|
|
|

4 |
0,4 |
|
|
|
|
С помощью мерного цилиндра в четыре сухие пронумерованные колбы наливают по 25 мл раствора уксусной кислоты, концентрации указаны в таблице. Затем в каждую колбу вносят одновременно по 0,5 г предварительно измельчённого активированного угля. Содержимое колб перемешивают круговыми движениями в течение 10 минут. После этого растворы фильтруют через сухие складчатые фильтры в отдельные колбочки. Из каждого фильтрата с помощью пипетки отбирают по 10 мл и переносят в колбочки для титрования, добавляют по 2 капли индикатора фенолфталеина и титруют каждую пробу раствором гидроксида натрия (до устойчивой слабо-розовоой окраски). Результаты титрования записывают в таблицу. Далее рассчитывают равновесную концентрацию уксусной кислоты по формуле
Сравн (CH3COOH) =
c(NaOH ) V (NaOH ) |
|
V (CH |
COOH ) |
3 |
|
где V(СН3СООН) – объём, взятый для титрования.
Адсорбцию уксусной кислоты рассчитывают по формуле
= |
(с |
исх |
− с |
равн |
) V |
исх |
1000 |
|
|
|
|
||||
|
|
|
m |
|
|
||
|
|
|
|
|
|
||
(моль/г)
где Сисх – концентрация раствора уксусной кислоты до адсорбции, моль/л; Сравн
– концентрация раствора уксусной кислоты после адсорбции или равновесная концентрация, моль/л; Vисх – объём раствора кислоты, взятый для адсорбции (в нашем опыте – это 0,025 л); m – масса адсорбента (в нашем случае это 0,5
г).
Чтобы построить изотерму адсорбции, по оси абсцисс откладывают равновесные концентрации Сравн, а по оси ординат – соответствующие им значения адсорбции Г.
Исходя из полученных данных, делают вывод о том, как зависит величина адсорбции уксусной кислоты из раствора на угле от её равновесной концентрации.
ЗАДАНИЕ 4
Адсорбция на активированном угле
К воде прилить несколько капель чернил для авторучки. Полученный раствор пропустить 1 – 2 раза через колонку, заполненную активированным углем. Отметить, что при этом наблюдается.
Повторить опыт с растворами окрашенных веществ, например с растворами лакмуса или фуксина.
ЗАДАНИЕ 5
Адсорбционные свойства силикагеля
К раствору сульфата меди (II) добавить раствор аммиака. При этом образуется комплексное соединение ярко синего цвета (написать реакцию образования комплекса). Затем в раствор всыпать 0,5 – 1 г измельчённого силикагеля и раствор взбалтывают. Бесцветный порошок силикагеля принимает тёмно-синюю окраску, а раствор бледнеет. Раствор слить с силикагеля, промыть водой (2 – 3 раза) и после этого добавить соляную кислоту. Темно-синяя окраска силикагеля исчезает, так как кислота разрушает медно-аммиачный комплекс и вымывает из силикагеля ионы меди.
Образцы решения типовых задач
Задача № 1 К 60 мл раствора уксусной кислоты с концентрацией раствора 0,1
моль/л добавили 2 г адсорбента и взболтали. После достижения равновесия пробу раствора объёмом 10 мл оттитровали раствором гидроксида натрия с концентрацией 0,05 моль/л. На титрование затрачено 15 мл титранта.
Рассчитайте величину адсорбции уксусной кислоты.
Решение
1. Найдём равновесную концентрация раствора уксусной кислоты по результатам титрования:
Сравн(СН3СООН) = 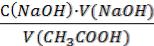
Сравн(СН3СООН) = 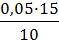 = 0,075 моль/л
= 0,075 моль/л
2. Рассчитываем величину адсорбции уксусной кислоты по формуле:
Г(СН3СООН) =  =
= 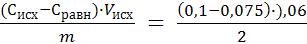
Г(СН3СООН) = 7,5 ∙ 10-4 моль/г = 0,75 ммоль/ г
Задача № 2 Определите величину адсорбции кислоты С8Н17СООН на поверхности
водного раствора при 10 0С, если массовая доля кислоты в растворе 0,005%. Поверхностное натяжение чистой воды и раствора при этой температуре равны соответственно 74,22 ∙ 10-3 и 57,0 ∙ 10-3 Дж/м2.
Решение
1. Для расчёта адсорбции Г на поверхности раствора воспользуемся уравнением Гиббса:
Г= - 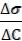 ∙
∙  = -
= - 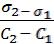 ∙
∙ 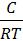
Вуравнении Гиббса величина С2 означает молярную концентрацию кислоты, С1 = 0 (чистая вода).
2. Считая, что плотность разбавленного раствора кислоты около 1 г/мл (т.е. такая же, как и воды), используя ω% кислоты, находим, что в 100 мл раствора
содержится 0,005 г кислоты. Молярная масса кислоты равна |
158 |
г/моль, поэтому молярная концентрация раствора будет: |
|
СМ =  =
=  = 3,16 ∙ 10 -4 моль/л.
= 3,16 ∙ 10 -4 моль/л.
3. В уравнение Гиббса подставляем необходимые данные:
Г = - 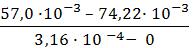 ∙
∙ 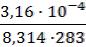 = 7,3 ∙ 10-6 моль/м2
= 7,3 ∙ 10-6 моль/м2
Ответ: 7,3 ∙ 10-6 моль/м2
3адача № 3 Экспериментально установлено, что максимальная величина адсорбции
ПАВ (М = 60 гмоль) некоторым адсорбентом составляет 5,0 ∙ 103 мольг. Величина К равна 0,06 моль/л. Какая масса (в граммах) вещества адсорбировалась двумя граммами данного адсорбента из раствора, если равновесная концентрация ПАВ стала равна 0,1 моль/л?
Решение
1. Рассчитываем величину адсорбции ПАВ по уравнению Лэнгмюра:
Г= Г∞ 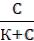
Г= 5,0 ∙ 10 -3 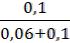 = 3,125 ∙ 10-3 (моль/г)
= 3,125 ∙ 10-3 (моль/г)
2. Количество адсорбированного вещества на адсорбенте массой 2 г будет в 2 раза больше:

nПАВ = 3,125 ∙ 10-3 моль/г ∙ 2г = 6,25 ∙ 10-3 моль
3. Масса адсорбированного вещества будет равна:
mПАВ = т∙М = 6,25 ∙ 10-3 ∙ 60 = 0,375 г
Ответ: m адсорбированного ПАВ равна 0,375 г.
Задачи для самостоятельного решения
Задача 1.
Чему равно поверхностное натяжение водного раствора амилового спирта, если число капель этого раствора, вытекающего из сталагмометра, равно 72, а число капель воды – 60? Поверхностное натяжение воды при 293 К равно72,8 ∙ 10 -3 Дж/м2 (плотность раствора принять равной 1 г/см3). (Перед решением задачи ознакомьтесь с лабораторной работой «определение зависимости поверхностного натяжения растворов от длины углеводородной цепи и концентрации ПАВ».
Ответ: 60,6 ∙ 10-3 Дж/м2
Задача 2.
При 200С поверхностное натяжение 0,2 М водного раствора ПАВ равно 55 ∙ 10-3 Дж/м2. Вычислите величину адсорбции ПАВ (поверхностное натяжение воды при 200С равно 75,75 ∙ 10 -3 Дж/м2).
Задача 3.
Экспериментально установлено, что величина максимальной адсорбции пропионовой кислоты на угле 3,0∙10-3 моль/г; коэффициент К равен 6,0 10-3 моль/л. Какая масса пропионовой кислоты адсорбировалась из раствора, если равновесная концентрация кислоты равна 0,1 моль/л? Масса адсорбента равна 1 г.
Ответ: 0,139 г.
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
Тесты для самоконтроля |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||||||||||||||||||||||
ПОВЕРХНОСТНЫЕ ЯВЛЕНИЯ, АДСОРБЦИЯ |
|
|
|
|
|
ТЕСТ № 1 |
||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
1. Выберите верное утверждение: |
|
|
|
|
|
1) атомы или молекулы на границе |
||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
|
|
|
|
|
|
|
раздела фаз обладают большой энергией по сравнению с атомами или |
|||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
|
|
|
|
|
|
|
молекулами в глубине фазы; |
|
|
|
|
2) атомы или молекулы на границе |
||||||||||||||||||||||||||||||||||||||||||||||||||||||||
|
|
|
|
|
|
|
раздела фаз обладают меньшей энергией по сравнению с атомами или |
|||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
|
|
|
|
|
|
|
молекулами в глубине фазы; |
|
|
|
|
|
3) атомы или молекулы на границе |
|||||||||||||||||||||||||||||||||||||||||||||||||||||||

раздела фаз и в глубине фазы обладают одинаковой энергией;
4) верное утверждение отсутствует.
2.Укажите, какие вещества, формулы которых указаны ниже, обладают
отрицательной адсорбцией на поверхности водного раствора?
1) NH4OH; 2) C3H7NH2 ; 3) C3H13SO3; 4) Na2SO3
3.При увеличении температуры значение поверхностного натяжения: 1) уменьшается; 2) увеличивается; 3) не изменяется.
4. |
Поглощение вещества всей массой адсорбента называется: |
1) |
|||
|
адсорбцией; |
2) абсорбцией; 3) сорбцией; |
4) десорбцией. |
|
|
5. |
Укажите, в каком ряду возрастает адсорбция веществ из водных |
||||
|
растворов |
на |
активированном |
угле? |
|
|
1) СН3СООН, СН3СООNa; С2Н5ОН; |
С3Н7ОН; |
2) С3Н7ОН, С2Н5ОН, |
||
|
СН3СООН, СН3СООNa; 3) СН3СООNa, СН3СООН, С2Н5ОН, С3Н7ОН; |
||||
4) СН3СООNa, С3Н7ОН, СН3СООН, С2Н5ОН.
6.Чем лучше адсорбат растворяется в данном растворителе, тем он
|
адсорбируется из этого растворителя: |
1) хуже; |
2) лучше; |
3) |
|||
|
растворимость адсорбата не влияет на адсорбцию. |
|
|||||
7. |
Адсорбция газов на твёрдом адсорбенте зависит от: 1) от давления; |
2) |
|||||
|
температуры; |
3) природы адсорбента и адсорбата; 4) от |
|||||
|
удельной поверхности адсорбента. |
|
|
|
|
||
8. |
Если число капель водного раствора, вытекающего из сталагмометра, |
||||||
|
больше числа капель воды, то растворённое вещество: |
1) |
|||||
|
ПНВ; |
2) ПИВ; |
3) ПАВ. |
|
|
|
|
9. |
Молекулярная адсорбция зависит |
от: |
а) |
природы адсорбента; |
|||
|
б) природы растворителя; в) природы адсорбата; г) концентрации |
||||||
|
раствора; |
д) температуры? |
|
|
|
1) |
|
|
а,б,в; |
2) а,в, г, д; |
3) а, б, в, г, д; |
|
4) а,б,г,д. |
|
|
10.Укажите единицы измерения поверхностного натяжения в системе СИ:
|
|
|
|
|
|
|
|
|
|
1) Н∙м2∙моль -1; |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
2) Дж∙м∙моль-1; |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
3) Дж ∙ м2; |
||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
|
|
|
|
|
|
|
|
|
|
4) Н∙ м. |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||||||||||||||||||||||||||||
ПОВЕРХНОСТНЫЕ |
|
|
ЯВЛЕНИЯ, АДСОРБЦИЯ |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
ТЕСТ № 2 |
||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
1. |
Адсорбция нелетучего растворённого вещества на поверхности его |
||||
|
раствора зависит: 1) |
от природы растворённого вещества; |
|||
|
2) температуры; |
3) |
давления; |
4) концентрации растворённого |
|
|
вещества. |
|
|
|
|
2. |
Величина поверхностной энергии уменьшается при: |
а) увеличении |
|||
|
поверхности; |
б) |
уменьшения |
поверхности; |
в) увеличения |
|
поверхностного натяжения; г) уменьшения поверхностного натяжения. |
||||
|
1) б, г; 2) б, в; |
3) а,в; |
4) а,г. |
|
|
3.Краситель фуксин будет лучше адсорбироваться углём из: 1) водных растворов; 2) спиртовых растворов; 3) природа растворителя значения не имеет; 4) в одинаковой степени.
4. Согласно теории БЭТ адсорбция завершается образованием: 1) мономолекулярного слоя; 2) цепей молекул, первая из которых связана с поверхностью адсорбента.
5.Укажите, какие утверждения верны: 1) химическая адсорбция может быть необратимой; 2) физическая адсорбция происходит за счёт сил Ван-дер-Ваальса; 3) адсорбция не зависит от температуры.
6.Из неполярных растворителей с ростом длины гидрофобного радикала
величина адсорбции: 1) увеличивается; |
2) уменьшается; |
|
3) |
||||
не меняется; |
4) одинакова. |
|
|
|
|
|
|
7. Среди перечисленных веществ выберите ПИВ: |
а) NaNO3; |
б) NaOH; |
|||||
в) пальмитат калия; |
г) H2SO4; |
д) бутановая кислота: |
|
1) |
|||
все; 2) а, б, г; |
3) а, б, г, д; |
4) в,д. |
|
|
|
|
|
8. Какие факторы влияют на поверхностное натяжение жидкости? |
1) |
||||||
природа жидкости; 2) природа граничащей фазы; |
3) объём жидкости |
||||||
(р, Т – константы); |
4) температура. |
|
|
|
|
||
9. Выберите правильные утверждения: |
|
|
|
а) |
|||
иониты – адсорбенты, способные к ионному обмену; |
|
б) |
|||||
иониты используются для смягчения и очистки воды, консервации |
|||||||
крови; |
|
|
|
|
|
|
в) |
иониты нельзя |
использовать для |
детоксикации |
организма; |
||||
г) иониты нельзя использовать для беззондовой диагностики |
|||||||
желудочного сока. |
|
|
|
|
|
1) |
|
|
|
|
|
|
|
|
|
|
|
|
|
а,б; 2) а,в; |
3) б,в; 4) а,г. |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
10. Труднее адсорбируемые вещества в хроматографической колонке |
|||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
двигаются: |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
1) быстрее; |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
2) медленнее |
|||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
ПОВЕРХНОСТНЫЕ ЯВЛЕНИЯ, АДСОРБЦИЯ |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
ТЕСТ № 3 |
|||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
1.Гемо- и лимфосорбция основаны на: 1) адсорбции ионов из растворов на твёрдом адсорбенте; 2) молекулярной адсорбции на твёрдом адсорбенте; 3) адсорбции белков и форменных элементов крови; 4) адсорбции газов на твёрдом адсорбенте.
2. |
Ионы лучше адсорбируются на: |
|
1) полярных адсорбентах; |
|
2) природа адсорбента значения не имеет; 3) неполярных адсорбентах. |
||
3. |
Укажите, какие утверждения верны: |
1) состояние молекул в |
|
|
поверхностном слое жидкости не отличается от состояния молекул в |
||
|
объёме жидкости; 2) поверхностное натяжение – это поверхностная |
||
|
энергия единицы площади поверхности; |
3) адсорбция – это способ |
|
|
изменения свободной поверхностной энергии. |
||
4. |
К ПИВ относятся вещества, обладающие: |
1) положительной |
|
|
поверхностной активностью, при |
этом |
адсорбция отрицательная; |
|
2) отрицательной поверхностной активностью, при этом адсорбция |
||
|
положительная; 3) положительной поверхностной активностью, при |
||
|
этом адсорбция положительная; |
4) отрицательной поверхностной |
|
активностью, при этом адсорбция отрицательная.

5. |
Величина адсорбции жирных кислот из бензольного раствора |
|||||
|
силикагелем по |
мере увеличения молярной |
массы |
кислоты: |
||
|
1) не изменяется; |
2) увеличивается; |
3) уменьшается. |
|
||
6. |
Нитробензол из раствора в бензоле |
будет лучше |
адсорбироваться: |
|||
|
1) на угле; 2) на силикагеле; |
3) в одинаковой степени; |
4) природа |
|||
|
адсорбента не имеет значения. |
|
|
|
|
|
7. |
Укажите единицы измерения поверхностного натяжения в системе СИ: |
|||||
|
1) Н∙м2∙моль -1; |
2) Дж∙м∙моль-1; |
3) Дж ∙ м2; |
4) Н∙ м. |
||
8. |
Укажите, какой катион из водного раствора лучше всего адсорбируется |
|||||
|
на отрицательно |
заряженных |
участках поверхности адсорбента: |
|||
1) К+; 2) Na+; 3) Li+; 4) Cs+
9.При увеличении температуры значение поверхностного натяжения:
1) уменьшается; 2) увеличивается; 3) не изменяется.
10.Согласно теории БЭТ адсорбция завершается образованием: |
|
1) мономолекулярного слоя; |
2) цепей молекул, первая из которых |
связана с поверхностью адсорбента. |
|
ПОВЕРХНОСТНЫЕ ЯВЛЕНИЯ, АДСОРБЦИЯ |
ТЕСТ № 4 |
1.Уменьшение поверхностной энергии Гиббса происходит за счёт самопризвольного: 1) изменение межфазной поверхности не влияет на
поверхностную энергию; 2) увеличения межфазной поверхности; 3) уменьшения межфазной поверхности; 4) нет верного ответа.
2. Из перечисленных веществ: вода, муравьиная кислота – максимальным
поверхностным натяжением обладает: |
1) вода; |
2) муравьиная |
кислота. |
|
|
3.Укажите, какие ионы из водного раствора преимущественно могут адсорбироваться на поверхности кристаллического йодида серебра: 1)
|
K+; 2) Ag+; |
3) I1-; 4) NO31- |
|
|
|
4. |
Притяжение атомов, молекул, ионов внутри отдельной фазы |
||||
|
называется: |
1) смачиванием; |
2) адсорбцией; |
3) когезией; 4) |
|
|
адгезией. |
|
|
|
|
5. |
Адсорбция – экзотермический процесс, поэтому при увеличении |
||||
|
температуры величина адсорбции: |
1) не меняется; |
2) |
||
|
увеличивается; |
3) уменьшается; |
4) одинакова. |
|
|
6. |
Многослойная адсорбция характеризуется: |
|
|
||
|
1) теорией Ленгмюра; |
2) теорией БЭТ; |
|
3) теорией |
|
|
Фрейндлиха; |
4) теорией Генри. |
|
|
|
7. |
Силикагель лучше адсорбирует вещества из растворов с: |
1) полярным |
|||
|
растворителем; |
2) неполярным растворителем; |
3) в одинаковой |
||
|
степени; 4) полярность растворителя роли не влияет на адсорбцию. |
||||
8. |
Согласно правилу Дюкло-Траубе, поверхностная активность с |
||||
|
увеличением длины углеродного радикала на |
одну |
СН2-группу: |
||

|
|
|
|
1) не изменяется; 2) увеличивается в 3 – 3,5 раза; |
|
|
|
|
|
|
|
|
|
|
|
3) |
|||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
|
|
|
|
уменьшается в 3 – 3,5 раза; |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
4) изменяется незакономерно. |
|||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
9. |
|
|
Среди перечисленных веществ выберите ПАВ: а) NaCl; |
б) желчные |
|||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
|
|
|
|
кислоты; |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
в) стеарат натрия; |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
г) Na2SO4; |
д) фосфолипиды |
||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
|
|
|
|
1) все; |
|
|
|
2) б,в, д; |
|
|
|
|
|
|
|
|
|
|
|
|
3) а,г; |
|
|
|
|
|
|
|
|
|
|
4) б,в |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||||||||||||||||||||||||||||||||||||||||||||||||||||||
10.Уравнение Гиббса применимо: |
|
|
1) только для подвижных границ |
||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
|
|
|
|
раздела; 2) только для неподвижных границ раздела; |
|
3) как для |
|||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
|
|
|
|
подвижных, так и для неподвижных границ раздела фаз. |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
|
ПОВЕРХНОСТНЫЕ ЯВЛЕНИЯ, АДСОРБЦИЯ |
ТЕСТ № 5 |
|||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
1. |
|
|
Адсорбция растворённого вещества из раствора на поверхности |
||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
|
|
|
|
твёрдого адсорбента зависит: |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
1) от природы адсорбента и |
|||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
|
|
|
|
растворённого вещества; 2) температуры; |
|
|
|
3) природы растворителя; |
|||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
|
|
|
|
4) концентрации растворённого вещества |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
2. |
|
|
К ПИВ относятся: |
|
|
|
а) КОН; |
б) Na3PO4; |
|
в) H2SO4; |
|
|
|
|
|
|
г) СН3СООН; |
||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
|
|
|
|
д) С17Н35СООNa. |
|
|
|
1) г, д; |
2) а, б, в; |
|
|
|
|
|
|
|
|
|
3) а,б, в, г; |
|
4) а,б. |
||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
3. |
|
|
На молекулярную |
|
адсорбцию |
|
влияют |
|
факторы: |
|
|
|
|
|
|
|
|
|
|
|
1) природа |
||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
|
|
|
|
растворителя; |
|
|
|
|
2) природа адсорбента; |
|
|
|
3) равновесная концентрация |
||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
|
|
|
|
растворённого |
|
|
|
вещества; |
4) |
|
|
природа |
|
|
растворённого вещества; |
||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
|
|
|
|
5) температура и время адсорбции |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
4. |
|
|
Укажите формулы ПАВ: |
1) С3Н7СООNa; 2) NaHCO3; |
3) |
||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
|
|
|
|
С2Н5ОН; |
|
|
|
|
|
|
|
|
|
|
|
|
|
4) С2Н5NH2; |
5) Н2N – CH2 – COOH |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
5.При адсорбции ПИВ на границе раздела фаз величина поверхностной активности (g) и величина адсорбции (Г) имеют следующие значения:
|
1) g < 0, Г < 0; |
2) g > 0, Г > 0; |
3) g < 0, Г > 0; |
4) g > 0, Г < 0; |
6. |
Из ионов одинакового заряда максимальную адсорбционную |
|||
|
способность проявляют ионы: |
|
1) |
|
|
наименьшего радиуса; |
2) величина радиуса иона значения не |
||
|
имеет; |
3) наименьшего радиуса |
|
|
7. |
Чаще всего удельную адсорбцию выражают: 1) в г/моль; 2) в моль/г; |
|||
3) г/кг;
8.Энергия взаимодействия при хемосорбции составляет: 1) 20 – 30
кДж/моль; 2) 10 – 40 кДж/моль; 3) 40 – 400 кДж/моль.
9. Величина адсорбции углём карбоновых кислот из их водных растворов
по мере увеличения длины гидрофобного радикала: |
1) не меняется; |
|
2) уменьшается; |
3) возрастает |
|
10.Избирательная адсорбция сильных электролитов подчиняется правилу:
1) |
Ребиндера; |
|
|
|
|
|
|
|
|
|
|
2) Шилова; |
|
|
|
3) Фаянса; |
|
|
|
|
|
|
|
|
|
4) Гиббса |
|
|
|
|
|
|
|
|
|
|
|
|||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
|
ПОВЕРХНОСТНЫЕ ЯВЛЕНИЯ, АДСОРБЦИЯ |
|
|
|
|
|
|
|
|
ТЕСТ |
|
|
|
№ 6 |
||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
1. Адсорбенты, |
|
|
|
|
|
|
способные |
|
к обмену |
|
|
|
|
|
|
ионами |
называются: |
|||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
1) |
силикагелями; 2) алюмосиликатами; 3) ионитами; 4) кварцитами |
|||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||

2. Из полярных растворителей с ростом длины гидрофобного радикала величина адсорбции: 1) уменьшается; 2) не меняется;
3) одинакова; 4) увеличивается
3.Если число капель водного раствора, вытекающего из сталагмометра,
больше числа капель воды, то растворённое вещество является:
1) ПИВ; 2) ПАВ; 3) ПНВ
4.Нитробензол из водных растворов будет лучше адсорбироваться: 1) на
|
угле; 2) на силикагеле; |
3) в одинаковой степени; |
4) природа |
||||
|
адсорбента не имеет значения |
|
|
|
|
||
5. |
Притяжение атомов, молекул, ионов внутри отдельной фазы |
||||||
|
называется: |
1) когезией; |
2) смачиванием; |
3) |
|||
|
адгезией; |
4) адсорбцией |
|
|
|
|
|
6. |
При физической адсорбции частицы удерживаются на поверхности |
||||||
|
адсорбента за счёт: |
а) химического взаимодействия; |
|||||
|
б) межмолекулярных сил Ван-дер-Ваальса; |
в) проникновения в поры |
|||||
|
адсорбента; |
г) водородной связи. |
1) а; |
2) а,г; |
3) б,в; |
4) б,г |
|
7. |
Поглощение |
вещества всей |
массой |
адсорбента |
называется: |
||
|
1) адсорбцией; 2) смачиванием; |
3) абсорбцией; |
|
4) |
|||
|
десорбцией |
|
|
|
|
|
|
8. |
Твёрдое тело на поверхности которого происходит адсорбция принято |
||||||
|
называть: |
1) адсорбтивом; |
2) адсорбатом; |
3) адсорбентом; |
|||
4) микропором.
9.Зависимость адсорбции от равновесного давления при постоянной
|
|
|
|
|
|
температуре |
|
|
|
|
и |
|
выражаемой |
|
|
|
|
кривыми |
|
|
|
Г |
= |
|
|
|
|
f(р) |
|
|
|
|
называемыми: |
|||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
|
|
|
|
|
|
1) изобарами; |
2) изохорами; |
|
|
|
3) изотермами; |
|
|
4) гиперболами |
||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
10.Поверхностное |
натяжение повышают |
|
|
вещества: |
1) |
|
|
|
сахароза; |
|||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
|
|
|
|
|
|
2) щелочи; |
3) этанол; 4) амины |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
ПОВЕРХНОСТНЫЕ ЯВЛЕНИЯ, АДСОРБЦИЯ |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
ТЕСТ |
|
|
|
№ 7 |
|||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
1. |
|
|
Основными факторами, обусловливающими специфичность адсорбции |
|||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
|
|
|
|
|
|
сильных электролитов являются: |
1) знак |
|
заряда поверхности |
|||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
|
|
|
|
|
|
адсорбента; 2) величина и знак заряда иона электролита; |
3) радиус |
|||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
|
|
|
|
|
|
иона; 4) сольватация иона |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||||||||||||||||||||||||||||||||||||||||||||||||||||||||
2. |
|
|
Активированный уголь – гидрофобный сорбент и лучше адсорбирует 1) |
|||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
|
|
|
|
|
|
полярные вещества из неполярных растворителей; |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
2) |
|||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
|
|
|
|
|
|
неполярные вещества из полярных растворителей; |
3) |
|
полярные |
|||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
|
|
|
|
|
|
вещества из полярных растворителей; |
|
4) неполярные вещества из |
||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
|
|
|
|
|
|
неполярных растворителей |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||||||||||||||||||||||||||||||||||||||||||||||||||||||||
3.Чем легче конденсируются газы, тем: 1) труднее они сорбируются на твёрдых адсорбентах; 2) легче они сорбируются на твёрдых адсорбентах; 3) процесс адсорбции не зависит от температуры конденсации газов; 4) нет верного утверждения
