
Полезные материалы за все 6 курсов / Ответы к занятиям, экзаменам / Адсорбция
.pdfАДСОРБЦИЯ НА ТВЁРДЫХ ПОВЕРНОСТЯХ
УДЕЛЬНАЯ АДСОРБЦИЯ
При адсорбции веществ на поверхности твёрдых адсорбентов изменяется химический состав поверхности адсорбента. Количественной характеристикой этого процесса является величина удельной адсорбции Г.
Удельная адсорбция – это равновесное количество поглощаемого вещества, приходящееся на единицу поверхности или массы адсорбента.
В качестве адсорбентов обычно применяют мелкоизмельченные вещества или пористые тела, что обеспечивает большую площадь поверхности раздела фаз, которую определить практически невозможно. Поэтому удельная адсорбция для твердых адсорбентов преимущественно выражается в молях поглощенного вещества на единицу массы адсорбента:
Г =  (моль/г),
(моль/г),
где n –количество адсорбата, моль; m – масса адсорбента, г.
Адсорбция газов и паров адсорбата на твердых адсорбентах – процесс, протекающий за счет сил Ван-дер-Ваальса и водородных связей. Количество поглощенного газа или пара на твёрдых поверхностях зависит от следующих факторов.
1.От свободной поверхностной энергии адсорбента. Она весьма велика у адсорбентов с аморфной структурой (активированный уголь) и у кристаллических веществ (оксиды алюминия, кремния). Адсорбент тем эффективнее, чем меньше измельчен.
2.От сродства адсорбтива к поверхности адсорбента. Полярные вещества лучше адсорбируются на полярных адсорбентах, а неполярные на неполярных. Чем больше адсорбент склонен к межмолекулярным взаимодействиям, тем интенсивнее идет адсорбция.
3.При физической адсорбции из смеси газов или паров лучше адсорбируется тот компонент, который легче сжимается, поскольку его молекулы более склонны к межмолекулярным взаимодействиям.
4.От концентрации адсорбата. Зависимость имеет сложный характер, так как с адсорбцией идет одновременно процесс десорбции. При равенстве скоростей этих процессов наступает равновесие.
ТЕОРИЯ МОНОМОЛЕКУЛЯРНОЙ АДСОРБЦИИ ЛЕНГМЮРА. УРАВНЕНИЕ ЛЕНГМЮРА
Изучая адсорбцию на твердых поверхностях Ленгмюр предложил теорию мономолекулярной адсорбции и уравнение адсорбции. Основные положения теории Ленгмюра следующие:
адсорбция молекул происходит не на всей поверхности адсорбента, а только на адсорбционных центрах, где имеются участки с наиболее нескомпенсированными силовыми полями;
каждый адсорбционный центр может удерживать только одну молекулу адсорбата, при этом адсорбированные молекулы не взаимодействуют со свободными молекулами, что приводит к образованию мономолекулярного слоя поглощаемого вещества;
процесс адсорбции обратим и носит динамический характер, т.к. адсорбированные молекулы удерживаются адсорбционными центрами только в течение определенного промежутка времени, после чего происходит десорбция этих молекул и адсорбция такого же числа новых молекул.
Исходя из этих положений, Ленгмюр предложил уравнение адсорбции:
Г = Kc
1 + Kc
Где Г∞ - значение предельной адсорбции; с – равновесная концентрация адсорбента в системе; К – константа адсорбционного равновесия.
Зависимость адсорбции от концентрации ПАВ (изотерма адсорбции) имеет вид:
α
α∞ |
|
|
|
|
|
III |
|
|
|
II |
|
|
I |
|
с |
|
|
|
|
|
|
с∞ |
|
Рис. 4. Зависимость адсорбции от концентрации ПАВ |
|||
На кривой четко видны три участка:
I - ый участок – это прямая линия, выходящая из начала координат. Действительно, при малых концентрациях, когда с → 0 и (1 + Кс) ≈1, уравнение принимает вид Г = Г∞·Кс, т.е. величина адсорбции прямо пропорциональна концентрации или давлению адсорбата.
III – участок – соответствует прямой, параллельной оси абсцисс, что означает, что адсорбция достигла своего предельного значения. При этом Кс ›› 1 и (1 + Кс) ≈ Кс, тогда Г = Г∞ (произошло насыщение поверхности адсорбента молекулами адсорбата, так как сформировался мономолекулярный слой).
II – ой участок соответствует криволинейной части графика и описывается полным уравнением Ленгмюра.
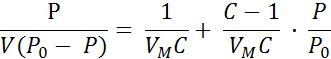
ОСНОВЫ ТЕОРИИ ПОЛИМОЛЕКУЛЯРНОЙ АДСОРБЦИИ Уравнение Ленгмюра даёт хорошие результаты при условии, что
адсорбция вещества сопровождается образованием мономолекулярного слоя. Это происходит при хемосорбции и при физической адсорбции газов при небольших давлениях и температуре выше критической (отсутствует конденсация на поверхности адсорбента).
Опыт показал, что, если адсорбция протекает с образованием полимолекулярного адсорбционного слоя, то изотерма отличается от ленгмюровской и имеет более сложный вид. Такие изотермы называют S-изотермы, так как адсорбция не останавливается на образовании монослоя.
Возможность образования полимолекулярных адсорбционных слоёв рассматривается в теории Поляни. Эта теория допускает существование на поверхности твёрдых адсорбентах адсорбционных сил, действующих на расстоянии, значительно превышающих диаметр молекул адсорбата.
Основные положения теории Поляни следующие:
1.Адсорбция создаётся чисто физическими силами.
2.На поверхности адсорбента нет активных центров, а адсорбционные силы действуют вблизи от поверхности адсорбента, образуя непрерывное силовое поле.
3.Силовое поле, обусловливающее адсорбцию, действует на расстояния, которые больше, чем размеры отдельных молекул адсорбата. Иначе говоря, у поверхности адсорбента существует так называемый адсорбционный объём, который заполняется при адсорбции молекулами адсорбата.
4.Притяжение молекул адсорбата поверхностью адсорбента не зависит от наличия в адсорбционном объёме других молекул. Поэтому идёт полимолекулярная адсорбция.
5.Адсорбционные силы не зависят от температуры, поэтому с изменением температуры адсорбционный объём не изменяется.
Теория Поляни не дала математического выражения изотермы адсорбции. Однако представления Поляни легли в основу современной теории адсорбции, которую создали С.Брунауэр, П. Эммет и Е. Теллер. Поэтому сокращённо эту теорию называют теорией БЭТ.
Теория постулирует, что при температуре ниже критической каждая молекула, адсорбированная в первом слое является центром для молекул, образующих второй слой, и т.д.
Авторы этой теории вывели уравнение
где Р0 – упругость насыщенного пара, V- объём адсорбированного газа при данном давлении газа Р; VM – объём адсорбированного газа в монослое и с = 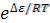 (∆ε – разность между теплотой адсорбции газа в первом слое и теплотой сжижения газа).
(∆ε – разность между теплотой адсорбции газа в первом слое и теплотой сжижения газа).
Уравнение БЭТ получило широкое применение. Из величины VM может быть вычислена полная адсорбирующая поверхность адсорбента S, что имеет важное практическое значение, а из величины С вычисляется теплота адсорбции газа в монослое. В качестве примера значений площади S укажем, что адсорбирующая поверхность 1 г испытанного образца силикагеля составила 500 м2, а 1 г коллагена – 350 м2. Хорошие адсорбенты обладают весьма значительной удельной поверхностью, например, активированный уголь – до 1000 м2/г.
Уравнение БЭТ применялось также для определения удельной поверхности различных аморфных и кристаллических полимеров.
АДСОРБЦИЯ НА ГРАНИЦЕ ТВЕРДОЕ ТЕЛО – ЖИДКОСТЬ
Существенным отличием адсорбции веществ из растворов является конкуренция между растворенным веществом и растворителем за возможность взаимодействовать с адсорбционными центрами на поверхности твердого адсорбента. Рассматривая этот вид адсорбции, остановимся на следующем:
1.При адсорбции из раствора важным фактором является величина удельной поверхности адсорбента и его сродство к поглощаемому веществу. Гидрофильные адсорбенты (силикагель, глины, пористые стекла) хорошо поглощают полярные вещества, а гидрофобные (сажа, активированный уголь) -–неполярные вещества.
2.Природа растворителя:
Чем хуже данный растворитель смачивает поверхность адсорбента и чем хуже растворяет вещество, тем лучше будет происходить адсорбция растворенного вещества.
3.Природа поглощаемого вещества:
а) выполняется правило «подобное взаимодействует с подобным», т.е. должно быть сродство между адсорбентом и адсорбтивом; б) Выполняется правило Шилова:
Чем больше растворимость вещества в данном растворителе, тем хуже оно адсорбируется на поверхности твердого адсорбента.
в) правило Ребиндера (правило уравнивания полярностей Ребиндера):
На поверхности раздела фаз прежде всего адсорбируются те вещества, при адсорбции которых происходит выравнивание полярностей соприкасающихся фаз, причём с увеличением разности полярности фаз способность к адсорбции этих веществ возрастает

Эффективней всего адсорбируются молекулы веществ, имеющих дифильное строение. В этом случае идёт эффективная адсорбция на твердом адсорбенте с самопроизвольной четкой ориентацией их молекул на границе раздела, выравнивающей полярности фаз. Полярный фрагмент молекулы обращен всегда к полярной фазе – к воде, силикагелю, а неполярный фрагмент – к неполярной (гидрофобной) фазе – активированному углю, маслу.
4.Влияние концентрации растворенного вещества на процесс адсорбции при постоянной Т описывается уравнением Ленгмюра.
5.Повышение температуры снижает эффективность адсорбции. Это
объясняется ослаблением взаимодействия между адсорбентом и адсорбатом.
Молекулярная адсорбция из растворов на твердом адсорбенте широко используется в медицинской практике. Активированный уголь хорошо адсорбирует газы, алкалоиды, барбитураты, токсины из пищеварительной системы. Одна таблетка активированного угля массой 0,25 г имеет адсорбционную поверхность около 100 м2.
АДСОРБЦИЯ РАСТВОРЁННОГО В ЖИДКОСТИ ВЕЩЕСТВА НА ТВЁРДОМ АДСОРБЕНТЕ
Различают молекулярную и ионную адсорбцию.
Молекулярная адсорбция – это адсорбция из растворов неэлектролитов (или очень слабых электролитов). При молекулярной адсорбции вещество адсорбируется на поверхности твёрдого тела в виде молекул.
Особенности молекулярной адсорбции: наряду с растворённым веществом адсорбируются молекулы растворителя. Поэтому для адсорбции растворённого вещества его молекулы должны вытеснять с поверхности молекулы растворителя.
Экспериментально величину адсорбции «а» изучают измеряя молярную концентрацию раствора до контакта с адсорбентом (с0) и после наступления
адсорбционного равновесия (сs):
a = (c − cs ) V m
а – количество адсорбированного вещества, приходящееся на 1 г адсорбента; m – масса адсорбента, г: V – объём раствора, из которого идёт адсорбция, л.
На молекулярную адсорбцию влияют:
равновесная концентрация растворённого вещества;
природа растворителя;
природа адсорбента;
природа растворённого вещества;
температура, время адсорбции.

Ионная адсорбция – это адсорбция из растворов сильных электролитов; в этом случае адсорбируется растворённое вещество на поверхности твёрдого адсорбента в виде ионов.
Ионная адсорбция – процесс более сложный, так как в растворе присутствуют уже частицы как минимум 3 видов: катионы, анионы растворённого вещества и молекулы растворителя.
Особенности ионной адсорбции:
1.Адсорбируются заряженные частицы (ионы), а не молекулы.
2.Адсорбция происходит только на полярных адсорбентах, поэтому её часто называют полярной адсорбцией.
3.Адсорбция сопровождается образованием двойного электрического слоя (ДЭС).
4.Адсорбция является избирательной, т.е. на каждом данном адсорбенте катионы и анионы адсорбируются неодинаково.
5.В основе ионной адсорбции лежат химические силы, и она чаще всего
кинетически необратима.
6.Для ионной адсорбции характерно явление обменной адсорбции.
ФАКТОРЫ, ВЛИЯЮЩИЕ НА ИОННУЮ АДСОРБЦИЮ
1.Химическая природа адсорбента
Чем более полярным является адсорбент, тем лучше он адсорбирует ионы из водных растворов. На активных центрах, несущих положительный заряд, адсорбируются анионы, на отрицательных - катионы.
2.Химическая природа ионов
а) На адсорбцию ионов большое влияние оказывает величина радиуса иона. Чем больше кристаллический радиус иона при одинаковом заряде, тем лучше он адсорбируется, так как с увеличением кристаллического радиуса иона возрастает его поляризуемость, а следовательно, способность притягиваться к полярной поверхности – адсорбироваться на ней. Одновременно увеличение кристаллического радиуса приводит к
уменьшению гидратации иона, а это облегчает адсорбцию. В соответствии с этим ионы можно расположить в ряды по возрастающей способности к адсорбции. Эти ряды называют лиотропными рядами или рядами Гофмейстера:
Li+ ‹ Na + ‹ K + ‹ Rb + ‹ Cs +
Mg 2+ ‹ Са 2+ ‹ Sr 2+ ‹ Ва 2+
Cl ‾ ‹ Br ‾ ‹ NO3 ‾ ‹ I ‾ ‹ NCS ‾
Адсорбционная способность возрастает
б) Чем больше заряд иона, тем сильнее ион притягивается противоположно заряженной поверхностью твердого тела, тем сильнее адсорбция:
K + ‹‹ Са 2+ ‹‹ Al 3+
Усиление адсорбции
Особый интерес представляет адсорбция ионов поверхностью кристалла, в состав которого входят такие же ионы или родственные ионы. В этом случае адсорбцию можно рассматривать как кристаллизацию, т.е.
достройку кристаллической решетки способными адсорбироваться на ней ионами. Это позволило Панету и Фаянсу сформулировать следующее правило:
На кристаллической поверхности адсорбента адсорбируются те ионы, которые способны достраивать кристаллическую решетку и дают труднорастворимое соединение с ионами, входящими в состав кристалла.
Пример: |
|
||||
|
+ K+ + Cl- → |
|
Cl- |
K+ |
|
nAgCl |
nAgCl |
||||
Cl- |
K+ |
||||
|
|
|
|||
|
|
|
|||
[Панет Фридрих Адольф (1887 – 1958), немецкий химик. Первым исследовал абсолютный возраст метеоритов, один из авторов правила Фаянса-Панета.
Фаянс Казимир (1887-1975), американский физико-химик, иностранный членкорреспондент АН СССР с 1924 года, труды в области радиохимии. Установил вместе с Ф. Панетом праило Фаянса-Панета).]
ИОНООБМЕННАЯ АДСОРБЦИЯ
Ионообменная адсорбция – это процесс, при котором твёрдый адсорбент обменивает свои ионы на ионы такого же знака заряда, находящиеся в растворе.
Для ионообменной адсорбции характерно следующее:
эта адсорбция специфична, т.е. к обмену способны только определённые ионы, по своей природе этот процесс приближается к химическим явлениям;
ионообменная адсорбция не всегда обратима;
протекает медленнее, чем молекулярная адсорбция;
при ионообменной адсорбции может меняться рН среды.
Вещества, проявляющие способность к ионному обмену при контакте с растворами электролитов, называются ионитами. Большинство ионитов – твёрдые, нерастворимые, ограниченно набухающие вещества. Иониты состоят из каркаса, несущего положительный или отрицательный заряд, и подвижных противоионов, которые компенсируют своими зарядами заряд каркаса и стехиометрически обмениваются на противоионы раствора электролита.
По знаку заряда обменивающихся ионов иониты делят на катиониты, аниониты и амфолиты.
По химической природе каркаса – на неорганические, органические и минерально-органические. Неорганические и органические иониты могут быть природными (целлюлоза, древесина, торф) и синтетическими (силикагель, Al2O3, наиболее важны ионообменные смолы). Минеральноорганические состоят из органического полиэлектролита на минеральном носителе.
Иониты применяются для очистки, разделения и концентрирования веществ из водных органических и газообразных сред. Например: очистка сточных вод, лекарственных веществ, сахара, выделение ценных металлов
ит. д.
ВОПРОСЫ ДЛЯ САМОКОНТРОЛЯ
(по теме «Поверхностная энергия. Адсорбция»)
1.Какова причина возникновения избыточной поверхностной энергии?
2.Что называется поверхностным натяжением? От чего зависит величина поверхностного натяжения?
3.В чём заключаются причины самопроизвольных поверхностных явлений?
4.Какие поверхностные явления связаны с уменьшением величины межфазной поверхности?
5.Что называется адсорбцией? Чем она обусловлена?
6.Чем можно объяснить, что деревянную палочку диаметром 1 см сломать легко, а стальной стержень такого же диаметра – практически невозможно?
7.Какие вещества называются поверхностно-активными, поверхностно-инактивными?
8.В чём состоят особенности строения молекул ПАВ и ПИВ и их адсорбции?
9.Как зависит поверхностное натяжение от концентрации ПАВ в растворе?
10.Уравнение Гиббса, его анализ. Ориентация молекул в поверхностном слое; структура липидного биослоя.
11.Чем отличается физическая адсорбция от хемосорбции?
12.Что называется поверхностной активностью? Как её можно определить графически и аналитически?
13.В чём заключается правило Дюкло-Траубе?
14.Как графически можно определить предельную адсорбцию?
15.В чём состоят особенности газов и паров на твёрдых поверхностях?
16.Какие участки есть на изотерме Ленгмюра? Какие математические уравнения характеризуют каждый участок?
17.Перечислите основные положения теории Ленгмюра.
18.Как с помощью теории Ленгмюра можно объяснить ступенчатую
адсорбцию?
19.От каких факторов зависит адсорбция на пористых адсорбентах? 20.Какие свойства газов влияют на их адсорбцию.
21. Что является причиной адсорбции растворённых веществ на поверхности твёрдых тел?
22.Какая адсорбция является молекулярной, от каких факторов она зависит?
23.Как зависит молекулярная адсорбция от природы растворённого вещества, растворителя и адсорбента?
24.Перечислите особенности ионной адсорбции. Как она зависит от
размеров и зарядов ионов?
25. Сформулируйте правило Панета –Фаянса.
26.В чём сущность ионообменной адсорбции? Какое состояние называется ионообменным равновесием? Какая величина его характеризует?
27.Какие поверхности называются гидрофильными, гидрофобными?
ЭКСПЕРИМЕНТАЛЬНАЯ ЧАСТЬ
ЗАДАНИЕ № 1
Определение зависимости поверхностного натяжения растворов от длины углеводородной цепи ПАВ сталагмометрическим методом
Цель работы. Изучить влияние длины углеводородной цепи и концентрации ПАВ на величину поверхностного натяжения растворов.
Сущность работы сводится к подсчёту числа капель исследуемых растворов ПАВ и воды, вытекающих из одного и того же объёма сталагмометра. Жидкость засасывается выше верхней метки, и когда её уровень опустится до верхней метки, начинают считать число капель, вытекающей жидкости, до тех пор, пока уровень жидкости достигнет нижней метки.
Капля, вытекающей жидкости, отрывается от трубки сталагмометра под действием силы тяжести собственной массы. Поверхностное натяжение стремится противодействовать вытеканию капли, поскольку образование капли связано с увеличением поверхности жидкости.
Чем больше поверхностное натяжение, тем больше должна быть масса капли, способной преодолеть поверхностное натяжение и оторваться.
Практическая часть
1.Определяют число капель воды, выливающейся из сталагмометра.
2.Затем подсчитывают число капель 0,1 М водных растворов следующих спиртов в указанном порядке: С2Н5ОН, С3Н7ОН, С4Н9ОН, С5Н11ОН.
3.Рассчитывают поверхностное натяжение этих спиртов по формуле
σх = σводы ∙ nводы / nx.
4.Строят кривую зависимости σ от числа углеродных атомов в молекулах спиртов (n атомов углерода).
5.Делают вывод о зависимости поверхностного натяжения водных растворов спиртов от длины углеводородной цепи молекул спирта.
