
677
.pdf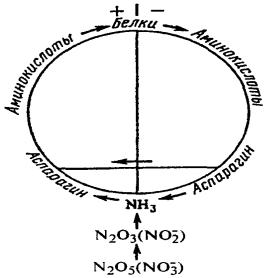
ция сахара и возрастает в процессе сахароварения содержание «вредного» небелкового азота, у картофеля снижается содержание крахмала, в овощной и бахчевой продукции и кормах накапливаются потенциально опасные для человека и животных количества нитратов.
Основные источники азотного питания растений.
Основными источниками азота для растений в естественных условиях служат соли азотной кислоты и аммония, нитриты и органические соединения азота, такие как мочевина и аминокислоты; поглощение идет в виде анионов NO3- и катионов NH4+.
Содержание и формы азота в растениях. Превращения азота в растениях. Нитраты, поступившие в растения, восстанавливаются с участием металлсодержащих ферментов через нитриты до аммиака.
НNO3-→ НNO2-→ (НNO)2→ NH2ОН → NH3 (при восстановлении нитратов до нитритов растениям необходим Мо, до гипонитрита и гидроксиламина – Cu, Fe, Mg, до аммиака – Mg.
Аммиак, поступивший в растение из почвы или образовавшийся в самом растении в результате восстановления нитратов, участвует в образо-
вании аминокислот.
Синтез органических азотистых соединений до белка включительно происходит через аммиак, образованием аммиака завершается и их распад. Аммиак, по образному выражению Д. Н. Прянишникова, есть альфа и омега в обмене азотистых веществ в растениях
(рис. 6).
151

Для самих растений нитраты безвредны и могут накапливаться в их тканях в значительных концентрациях (табл. 57). Нитраты и нитриты в повышенных количествах опасны для теплокровных, вызывают заболевание метгемоглобинемией (вместо гемоглобина в крови образуется метгемоглобин, нарушается снабжение тканей кислородом, развивается синюшность) и могут быть предшественниками канцерогенных соединений – нитрозаминов.
Таблица 57
Группировка растений по способности накапливать нитраты, мг/кг сырой массы (Кидин В.В., 2009)
|
|
Содержание |
Группа |
Культура |
нитратов, |
|
|
мг/кг |
1 |
Томат, перец, физалис, баклажан |
30-150 |
2 |
Тыква, огурец в открытом грунте, кабачок, патиссон |
120-360 |
3 |
Лук-репка на перо, лук-батун, лук-порей, шпинат, чеснок |
140-390 |
4 |
Морковь, свѐкла, редька, репа, редис, хрен, брюква, па- |
350-1350 |
|
стернак |
|
5 |
Укроп, кинза, тмин, мята, горчица, базилик, крыжовник |
320-390 |
6 |
Капуста, салат, петрушка, сельдерей |
480-6760 |
Накопление нитратов в продукции происходит при избыточном азотном питании, при недостатке углеводов и в пасмурную погоду. Индикаторы на нитраты – салат, щавель. В таблицах 58, 59 приведены допустимые уровни содержания нитратов в растениях и кормах.
Таблица 58
Допустимые уровни содержания нитратов в растениях (мг/кг NО3) (Агрохимия 2002)
Продукция |
Открытый грунт |
Защищѐнный грунт |
1 |
2 |
3 |
Картофель |
250 |
|
Капуста белокочанная |
|
|
ранняя (до 01.09) |
900 |
|
поздняя |
500 |
|
|
152 |
|
|
|
Окончание таблицы 58 |
|
|
|
|
|
1 |
2 |
|
3 |
Морковь |
|
|
|
ранняя (до 01.09) |
400 |
|
|
поздняя |
250 |
|
|
Томаты |
150 |
|
300 |
Огурцы |
150 |
|
400 |
Свѐкла столовая |
1400 |
|
|
Лук репчатый |
80 |
|
|
Лук-перо |
600 |
|
800 |
Листовые овощи |
2000 |
|
3000 |
Дыни |
90 |
|
|
Арбузы, виноград, яблоки, груши |
60 |
|
|
Перец сладкий |
200 |
|
400 |
Кабачки |
400 |
|
400 |
Консервированные овощи |
|
50 |
|
Таблица 59
Предельно допустимые концентрации нитратов и нитритов в кормах для сельскохозяйственных животных, мг/кг сырого продукта
Продукция |
NО3 |
NО2 |
Комбикорма для крупного и мелкого рогатого скота |
600 |
10 |
Комбикорма для свиней и птицы |
200 |
5 |
Сено, солома |
500 |
10 |
Зелѐные корма |
200 |
10 |
Картофель |
300 |
10 |
Свѐкла |
800 |
10 |
Силос, сенаж |
200 |
10 |
Зернофураж |
300 |
10 |
Травяная мука |
200 |
10 |
Жмых, шрот |
200 |
10 |
Особенности питания растений аммонийным и нитратным азотом
Д.Н. Прянишников доказал равноценность нитратного и аммиачного питания. При благоприятных условиях лучшей формой является NH3, так как не требуется дополнительная энергия на восстановление нитратов. Преимущественное использование растениями аммонийного или нитратного азота зависит от ряда факторов, важнейшие из которых: биологические особенности культуры, обеспеченность еѐ углевода-
153
ми, реакция среды, наличие кальция, калия и других элементов питания, в том числе микроэлементов.
При недостатке углеводов и, следовательно, органических кетокислот (особенно при прорастании семян, имеющих малый запас углеводов) избыточное поступление аммонийного азота в растения может оказывать отрицательное действие. В этом случае аммонийный азот не успевает использоваться на синтез аминокислот и накапливается в тканях, вызывая «аммиачное отравление» растений. Те растения, в посевном материале которых содержится много углеводов (например, крахмала у картофеля), быстро усваивают поступающий аммонийный азот и хорошо отзываются на внесение аммонийных удобрений.
При нейтральной реакции аммонийный азот усваивается растениями лучше, а при кислой – хуже, чем нитратный. Повышенное содержание кальция, магния и калия создаѐт более благоприятные условия для усвоения аммонийного азота, а при нитратном питании важное значение имеет достаточная обеспеченность фосфором и молибденом. Недостаток молибдена тормозит восстановление нитратов и ограничивает ассимиляцию нитратного азота растениями. В естественных условиях сравнительная ценность для растений нитратных и аммиачных (аммонийных) форм азотных удобрений в значительной степени определяется их превращениями в почве и еѐ свойствами.
Работами Ф.М. Турчина установлено, что аммиачное отравление растений можно предотвратить внесением калийных удобрений. При аммиачном питании происходит усиленное поглощение хлора, при нитратном – кальция. Молодые растения чувствительны к аммиачному отравлению, поэтому лучше при посеве вносить нитратную форму азота.
Синтез некоторых аминокислот идет за счѐт присоединения аммиака к органическим кетокислотам.
154
Аспарагиновая и глутаминовая аминокислоты могут присоединять еще по одной молекуле аммиака, давая амиды – аспарагин и глутамин. Эти соединения служат для детоксикации избыточных количеств аммиака и в качестве источника аминогрупп при синтезе различных аминокислот в реакциях переминирования.
В процессе роста и развития в растениях постоянно синтезируется огромное количество разнообразных белков. Для биосинтеза белков, как и других сложных органических соединений, требуются затраты большого количества энергии. Основные источники еѐ в растениях – фотосинтез и дыхание (окислительное фосфорилирование), поэтому между синтезом белка и интенсивностью дыхания и фотосинтеза существует тесная связь.
Наряду с синтезом белков, в растениях происходит распад их под действием протеолитических ферментов на аминокислоты с отщеплением аммиака. В молодых растущих растениях или органах синтез белков превышает распад, по мере старения процессы расщепления активизируются и начинают преобладать над синтезом.
Общее содержание азота в различных почвах. Содер-
жание азота в почвах зависит от количества гумуса и составляет примерно 1/20 его часть. В черноземных почвах общее содержание азота достигает 0,4-0,5%, а в дерновоподзолистых почвах и сероземах его лишь 0,05-0,15%. Общий запас азота в пахотном слое разных почв колеблется от
600 до 15000 кг/га (табл. 60).
|
|
|
|
|
Таблица 60 |
||
Относительное и валовое содержание азота |
|
||||||
в пахотном слое разных почв (Минеев В.Г., 2006) |
|
||||||
Почва |
|
N |
Почва |
N |
|||
% |
|
тыс. кг/га |
% |
тыс. кг/га |
|||
|
|
|
|||||
Дерново-подзолистая |
0,02-0,05 |
0,6-1,5 |
Чернозем |
0,2-0,5 |
6-15 |
||
песчаная |
|||||||
|
|
|
|
|
|
||
Дерново-подзолистая |
0,05-0,13 |
1,5-4,0 |
Серозем |
0,05-0,15 |
1,5-4,5 |
||
суглинистая |
|||||||
|
|
|
|
|
|
||
|
|
155 |
|
|
|
||
Формы азота в почвах. Основная масса (до 99%) почвенного азота находится в виде органических соединений (белковых и гумусовых веществ), недоступных для питания растений. Скорость минерализации органических соединений азота почвенными микроорганизмами до усвояемых растениями минеральных соединений (аммония и нитратов) зависит от условий аэрации, влажности, температуры и реакции почвы. Поэтому количество минеральных соединений азота в почвах сильно колеблется – от следов до 2-3% общего его содержания.
Превращения азота в почвах. Процессы аммонификации, нитрификации, денитрификации, гумификации и иммо-
билизации. Разложение органических азотистых веществ в почве в общем виде может быть представлено следующей схемой: гуминовые вещества, белки → аминокислоты, амиды → аммиак → нитриты → нитраты → молекулярный азот.
Распад органических азотсодержащих веществ почвы до аммиака называется аммонификацией. Аммонификацию осуществляют разнообразные аэробные и анаэробные почвенные микроорганизмы. Она происходит во всех почвах при разной реакции среды, но замедляется в анаэробных условиях и при сильнокислой и щелочной реакциях. Аммиак взаимодействует с угольной кислотой почвенного раствора, образуя карбонат аммония, a NH4+ поглощается почвой:
2NH3 + Н2СО3 = (NH4)2CO3
Ca
(Почва) СCaa + (NH4)2CO3 ↔ (Почва) NH4 + CaCO3
NH4
Аммонийный азот в почве подвергается нитрификации – окислению до нитратного азота: NH3 +Н2О= NH4ОН -2Н+=
156
NH2ОН -2Н+=НNO +Н2О= NH(ОН)2 -2Н+= НNO2-→NO3- (аммиак окисляется до аммония, затем до гидроксиламмония, далее до гипонитрита, нитрита и нитратов).
Нитрификация происходит в результате деятельности группы специфических аэробных бактерий, для которых окисление аммиака служит источником энергии. Одни из них (Nitrosomonas) окисляют NH4+ до NO2 -, затем другие бактерии (Nitrobacter) окисляют NO2- до NO3-. Оптимальные условия для нитрификации – хорошая аэрация, влажность почвы 60-70% капиллярной влагоѐмкости, температура 25-32°С и близкая к нейтральной реакция (рН 6,2-8,2). Интенсивность нитрификации – один из признаков культурного состояния почвы.
На кислых подзолистых почвах в условиях плохой аэрации, избыточной влажности и низкой температуры процессы минерализации протекают слабо и прекращаются на стадии образования аммония. Нитрификация из-за неблагоприятных условий для деятельности нитрифицирующих бактерий бывает подавлена, нитратов образуется мало.
На окультуренных, хорошо обработанных почвах процессы аммонификации и нитрификации проходят более интенсивно, больше образуется минеральных соединений азота, главным образом нитратов. Известкование кислых почв, систематическое внесение органических и минеральных удобрений, усиливая микробиологическую деятельность в почве, резко повышают интенсивность минерализации органического вещества и образования усвояемых минеральных соединений азота. Последние не накапливаются в почве в больших количествах, так как потребляются растениями и микроорганизмами и частично снова превращаются в органическую форму.
Кроме того, нитратный азот теряется из почвы в результате денитрификации и вымывания его из корнеобитаемого
157
слоя осадками и поливными водами. Потери нитратов за счѐт вымывания из почв тяжелого гранулометрического состава под растениями обычно незначительны (на суглинистых 5- 6 кг/га). Однако на легких, особенно парующих, почвах в увлажненных районах, а также в условиях орошаемого земледелия такие потери могут быть значительными и достигать 25-30 кг/га. К отрицательным последствиям вымывания нитратов относится также загрязнение ими водных источников, в том числе питьевых ресурсов.
В основном потери азота из почвы происходят в газообразной форме в результате денитрификации – (НNO3-→ НNO2 → (НNO)2→ N2О→ N2) процесса дессимиляторного восстановления нитратного азота до молекулярного (N2) либо до газообразных оксидов азота (NO) и (N2O). Общие потери за счѐт денитрификации обычно составляют 10-20 % от дозы азота, внесенного с удобрениями, а средняя величина потерь азота, обеспечиваемая запасами его в почве, достигает 6 кг/га.
Биологическую денитрификацию осуществляет группа денитрифицирующих бактерий. Особенно интенсивно этот процесс идет в анаэробных условиях, при щелочной реакции почвы (рН 7,0-8,2) и в присутствии доступного микроорганизмам органического вещества богатого углеводами. Биологическая денитрификация протекает и в обычных условиях аэрации, реакции среды и увлажнения, поскольку в почвах даже при общих аэробных условиях неизбежно наличие анаэробных микрозон, а диапазон благоприятной реакции среды для развития денитрификаторов довольно широкий.
Наряду с биологической денитрификацией наблюдается косвенная, называемая хемоденитрификацией, которая связана с образованием газообразных оксидов азота и молекулярного азота в результате химических реакций: при разложении
158
промежуточных продуктов нитрификации – нитратов и гидроксиламина (особенно при кислой реакции), при взаимодействии нитритов с NH4+, α-аминокислотами, ионами Fe2+ и Mn2+ и с органическими веществами почвы.
NH3 + НNO2= NH4NO2 → N2+H2O (хемоденитрификация)
Следовательно, в круговороте азота в земледелии процессы нитрификации, наряду с положительным эффектом, имеют и отрицательное значение, так как образующиеся нитраты и нитриты могут вымываться и теряться из почвы в виде газообразных продуктов (N2, N2O, NO) биологической и хемоденитрификации.
Один из продуктов денитрификации (закись азота – N2О) характеризуется продолжительным временем пребывания в атмосфере (114-120 лет) и высоким потенциальным вкладом в развитие «парникового эффекта», который оценивается в 170-310 раз выше по сравнению с диоксидом углерода. Одновременно закись азота является предшественником соединений, взаимодействующих в ходе фотохимических реакций с озоном стратосферы, вызывая его разрушение. В результате ежегодного роста концентрации закиси азота на 0,5-1,2 % создаѐтся серьезная угроза изменения климата и химии атмосферы.
Объемы эмиссии закиси азота тесно связаны с состоянием азотного цикла, характеризуя степень его нарушенности. Чем больше азота вовлечено в биогеохимический круговорот и меньше эффективность его использования в земледелии (что, как правило, наблюдается при поступлении его избытка с высокими дозами азотсодержащих удобрений), тем больше закиси азота выделяется в атмосферу. Таким образом, нерациональное применение удобрений может вносить свой вклад в глобальные проблемы современности, связанные с нарушением газового режима атмосферы.
159
В почве одновременно с минерализацией органического азотсодержащего вещества происходят вторичные процессы синтеза, когда минеральные соединения азота переходят в органические, в белок плазмы микробных клеток. Этот процесс называется иммобилизацией. Предпосылками для процесса иммобилизации являются поступление в почву органических веществ с широким отношением С: N (20: 1 и более). Среднее отношение С: N в плазме разлагающих органические вещества микроорганизмов составляет 10: 1. После отмирания и гумификации белковый азот микроорганизмов становится частично доступным для растений.
Баланс азота в почвах. В расходной части баланса учитывают вынос элементов питания с урожаем основной и побочной продукции, вынос с растительными остатками, вымывание нитратов, эрозию почвы и денитрификацию. Как показали проводимые исследования, из внесѐнных удобрений 30-60% азота используется растениями, 15-30 – аккумулируется в почве, 10-30 теряется в результате денитрификации 1- 5% вымывается в виде нитратов.
Естественное поступление азота осуществляется в результате биологической фиксации, с атмосферными осадками и семенами. В атмосфере над каждым гектаром почвы находится около 80 тыс. т азота, но молекулярный азот воздуха недоступен большинству растений (кроме бобовых). Только небольшое количество связанного азота (до 3-5 кг/га) образуется в самой атмосфере под действием грозовых разрядов и с осадками в виде аммиака, азотистой и азотной кислот поступает в почву.
Единственный естественный источник восстановления почвенных запасов этого элемента – процесс биологической
160
