
Lab_rab_104
.pdf
Государственное образовательное учреждение высшего профессионального образования
«ПЕТРБУРГСКИЙ ГОСУДАРСТВЕННЫЙ УНИВЕРСИТЕТ ПУТЕЙ СООБЩЕНИЯ»
Кафедра «Физика» Лаборатория молекулярной физики.
ОПРЕДЕЛЕНИЕ ТЕРМИЧЕСКОГО КОЭФФИЦИЕНТА ДАВЛЕНИЯ ГАЗА
Методические указания к лабораторной работе № 104
САНКТ-ПЕТЕРБУРГ
2005
Цель работы: опытное определение зависимости давления газа от температуры, вычисление среднего термического коэффициента давления газа (воздуха) в интервале температур от комнатной до 100 оС.
Термический коэффициент давления газа
Если объём некоторой массы газа поддерживать постоянным, то при повышении температуры давление газа в сосуде будет изменяться по линейному закону:
pt = p0 (1+αpt) , |
(1) |
|||
где p0 — давление газа при 0 ºС, pt — давление газа при t ºС, αp — |
|
|||
термический коэффициент давления газа. |
|
|||
Как видно из формулы (1), |
|
|||
αp = |
pt − p0 |
|
(2) |
|
p0t |
||||
|
|
|||
Термический коэффициент давления газа показывает на какую часть увеличивается первоначальное давление газа, находящегося при 0 ºС, при нагревании на 1 ºС при постоянном объёме.
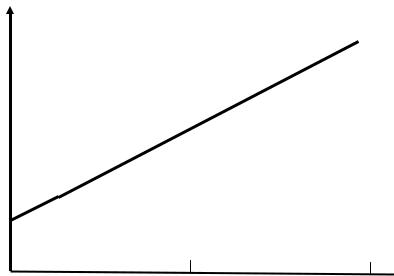
Для вычисления αp по формуле (2) необходимо знать давление p0 при 0 ºС и давление pt . Давление p0 можно найти из графика зависимости
давления от температуры, построенного по измеренным значениям p и t (рис.1). Для этого нужно экстраполировать (продолжить) экспериментальную линию до пересечения с осью ординат (t=0 ºС).
p, кПа
• •
•
•
• •
••
••
p0
t, ºС
0 |
50 |
100 |
Рис.1
Из формулы (1) можно вывести другое выражение для αp , записав
p1 = p0 (1 +αp t1 ) p2 = p0 (1 +αp t2 )
После преобразований получим:
αp = |
p2 − p1 |
(3) |
|
p1t2 − p2t1 |
|||
|
|
Выбрав на графике два значения температуры t1 и t2 (с разницей в 40 – 50 градусов) по оси ординат определяют соответствующие этим температурам давления газа p1 и p2.
Строго говоря, термический коэффициент давления для реальных газов является величиной, зависящей от давления и температуры. Тем не менее для некоторых газов, например для водорода, гелия и азота, значение αp
сохраняет почти постоянную величину для широкого интервала температур. Для идеального газа αp = 1/273 K-1.
Задача эксперимента состоит в измерении давления воздуха в закрытом сосуде при различных температурах.
Описание установки
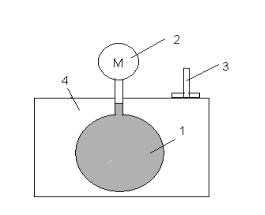
Схема установки для определения термического коэффициента давления газа изображена на рис.2.
Рис. 2
Исследуемый газ находится в стеклянной колбе 1, которая помещена в термостат 4 и соединена трубкой с манометром 2, служащим для определения давления в колбе. Температура определяется с помощью термометра 3, вставленного в тубус на термостате. Манометр измеряет

превышение давления в колбе над атмосферным давлением. Атмосферное давление Н определяется по барометру в мм. рт. ст.
1 мм. рт. ст. = 133 Па.
Показания манометра h выражены в кГс/см2 (техническая атмосфера) 1 кГс/см2= 9,8×104Па.
Давление в колбе p равно сумме показаний барометра и манометра
p=H + h |
(4) |
Порядок выполнения работы
1.Закрыть дверцу термостата. Записать в таблицу показания барометра и начальные показания манометра и термометра.
2.Включить термостат, при этом должна загореться сигнальная лампа. Газ начинает нагреваться.
3.Через каждые 10 0C необходимо записать в таблицу показания термометра t и манометра h в смкГс2 .
4.Вычислить по формуле (4) давление p в колбе при разных температурах и занести в таблицу.
5.Построить график p = f(t) (см. рис.1), определить p0.
6.Вычислить по формуле (3)αp .
7.Оценить погрешность αp результата косвенного измерения αp по формуле
|
|
|
αp =αp |
2 |
|
|
h |
, |
|
(5) |
||||||
|
|
|
p2 |
|
|
|
|
|||||||||
где h – погрешность манометра. |
|
|
|
|
− p1 |
|
|
|
||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||
|
t,ºC |
H, мм |
H, Па |
h, |
кГс |
h, Па |
|
|
p, |
αp , |
αp , |
|||||
|
рт. ст. |
см |
2 |
|
|
|
кПа |
К-1 |
К-1 |
|
||||||
|
|
|
|
|
|
|
|
|
|
|
|
|||||
|
20 |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
30 |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
· |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
· |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
100 |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
Контрольные вопросы:
1.Что определяет термический коэффициент давления?
2.Какой термодинамический процесс исследуется в данной работе? Напишите уравнение этого процесса.
3.Напишите первое начало термодинамики для исследуемого процесса.
4.От чего зависит давление газа с молекулярно-кинетической точки зрения?
5.Почему давление газа растет с увеличением температуры?
6.Получите формулу (5), предполагая, что основную погрешность в
результат вычисления αp по формуле (3) вносит разность давлений
p2-p1.
ОПРЕДЕЛЕНИЕ ТЕРМИЧЕСКОГО КОЭФФИЦИЕНТА ДАВЛЕНИЯ ГАЗА
Методические указания
Составитель: старший преподаватель М.А. Березовец
Рецензент: доцент Р.А. Романова
План 2005 г.
