
- •Санкт-Петербургская государственная медицинская
- •Isbn 5-7243-0283-7 Коллектив авторов, 2009
- •1. Тема 27. Химия крови. Обмен хромопротеинов.
- •3. Конкретные задачи.
- •5. Задание для самоподготовки:
- •Основная литература:
- •6. Вопросы для самоподготовки:
- •Количественное определение в крови метгемоглобина (метод л.Э.Горна).
- •Лабораторная работа № 14 Количественное определение общего билирубина в сыворотке крови по методу Ендрассика и Клехгорна.
- •Выберите правильный ответ
- •Тест 12 выберите все правильные ответы
- •Выберите все правильные ответы
- •Выберите все правильные ответы
- •Тест 29
- •Тест 30 установите соответствие
- •1. Тема 28. “Биохимическая оценка состояния функций печени”
- •2. Цель занятия:
- •3. Конкретные задачи:
- •5. Задание для самоподготовки:
- •Основная литература:
- •6. Вопросы для самоподготовки:
- •7. Этапы занятия, контроль усвоения.
- •Белковые фракции
- •Ответы по теме: Биохимическая оценка состояния функций печени
- •Тестовый контроль по теме: Биохимия гепатоцитов
- •Установите соответствие
- •Ответы по теме: Биохимия гепатоцитов
- •1. Тема 29. Адаптация. Биохимические механизмы детоксикации эндогенных и экзогенных соединений
- •Продолжительность занятия 180 минут
- •3. Конкретные задачи:
- •5. Вопросы для самоподготовки:
- •7.Этапы занятия, контроль усвоения и распределения учебного времени.
- •Биохимические механизмы детоксикации и адаптации
- •Индукторы цитохрома р-450
- •Ингибиторы цитохрома р-450
- •Влияние микронутриентов на метаболизм ксенобиотиков (минеральные компоненты)
- •Роль глутатиона в процессах детоксикации
- •Металлотионеины
- •Тестовый контроль по теме: “Адаптация. Биохимические механизмы детоксикации эндогенных и экзогенных соединений”
- •Глутатион является:
- •Реакции, за счет которых протекает вторая фаза детоксикации ксенобиотиков:
- •Реакции, катализируемые монооксигеназной системой:
- •Микросомальные оксигеназы участвуют в:
- •Феномен «токсификации» наблюдается при метаболизме:
- •Металлотионеины – это белки, которые:
- •Дополните
- •Последовательность стадий в механизме действия цитохрома р-450:
- •1. Тема 30. Физико-химические свойства, нормальные и патологические компоненты мочи, качественный и количественный анализ патологических компонентов мочи.
- •2. Цель занятия:
- •3. Конкретные задачи:
- •5. Вопросы для самоподготовки:
- •6. Задания для самоподготовки:
- •7. Этапы занятия, контроль их усвоения и распределение учебного
- •Лабораторная работа № 15
- •Общие свойства мочи.
- •2. Определение кетоновых тел.
- •3. Определение белка.
- •Количественное определение белка в моче колориметрическим методом с пирогаллоловым красным.
- •Количественное определение глюкозы в моче глюкозооксидазным методом.
- •Тестовый контроль по теме: Физико-химические свойства, нормальные и патологические компоненты мочи, качественный и количественный анализ патологических компонентов мочи.
- •Выберите все правильные ответы
- •Выберите все правильные ответы
- •Тест 19
- •Причиной гемоглобинурии является ______ _______.
- •1. Тема 31. Биохимическая оценка состояния функции почек.
- •Алгоритм решения задач.
- •Нормальные величины
- •Анализ мочи
- •Функциональные пробы
- •Тестовый контроль по теме: Биохимическая оценка состояния функции почек.
- •Нарушение реабсорбции в почечных канальцах характеризуется:
- •Функция ренина заключается в:
- •Острый гломерулонефрит характеризуется:
- •Дополните
- •Ответы по теме: Биохимическая оценка состояния функции почек.
- •Тестовый контроль по теме: Свободнорадикальное окисление. Антиоксидантная система"
- •Реакция, в которой образуется гидроксил-радикал:
- •Наибольшей реакционной способностью обладает:
- •Антиоксиданты следует с осторожностью назначать при:
- •Тест 28
- •Ответы по теме: Свободнорадикальное окисление. Антиоксидантная система".
- •Тестовый контроль по теме: ″Минеральный обмен″.
- •Выберите правильный ответ
- •Установите строгое соответствие
- •Тестовый контроль по теме: Мышцы" Тест 1
- •Ответы по теме: Мышцы"
- •Фермент ацетилхолинэстераза способствует:
- •Ингибиторы ацетилхолинэстеразы способствуют:
- •Эндорфины и энкефалины: а) имеют липидную природу
- •Тестовый контроль по теме: Взаимосвязь обменов"
- •Выберите все правильные ответы
- •Установите соответствие
- •Ответы по теме: ² Взаимосвязь обменов"
- •Программа курса биологической химии.
- •1. Химия белков
- •2. Ферменты
- •3. Витамины, классификация, биологическая роль
- •4. Энергетический обмен.
- •5. Обмен белков
- •6. Химия и обмен углеводов
- •7. Химия и обмен липидов
- •8. Гормоны, классификация, биологическая роль
- •9. Взаимосвязь основных видов обмена:
- •16. Минеральный обмен
- •17. Антиоксидантная система
- •Оглавление
6. Вопросы для самоподготовки:
6.1. Химический состав крови.
6.2. Физико – химические свойства крови.
6.3. Классификация и функции белков крови.
6.4. Характеристика хромопротеинов (строение, свойства, функции).
6.5. Гемсодержащие белки: строение, свойства, функции.
6.6. Гемсодержащие ферменты: строение, свойства, функции. Примеры гемсодержащих ферментов.
6.7. Нормальные и патологические производные гемоглобина, механизм их образования.
6.8. Кооперативный эффект на примере оксигенации гемоглобина. Факторы, влияющие на сродство гемоглобина к кислороду.
6.9. Метгемоглобин: строение, образование, свойства, реакции восстановления.
6.10. Метгемоглобинемии: определение, классификация, лечение. Какие энзимопатии могут быть причиной метгемоглобинемий?
6.11. Гемоглобинопатии (серповидноклеточная анемия) и талассемии.
6.12. Дыхательная функция крови.
6.13.Этапы синтеза гема.
6.14. Порфирии, диагностика порфирий, классификация.
6.15. Этапы распада гемоглобина.
6.16. Что такое прямой и непрямой билирубин: механизмы образования, свойства.
6.17. Диагностическое значение определения общего билирубина и его фракций в сыворотке крови.
6.18. Виды желтух и их дифференциальная диагностика.
6.19. Принцип метода определения билирубина в сыворотке крови.
7. Этапы занятия, контроль усвоения и распределения учебного времени.
|
Этапы занятия |
Форма усвоения |
Время |
|
7.1.Постановка задачи. 7.2. Контроль исходного уровня знаний. 7.3.Разбор теоретического материала. 7.4. Приобретение практических навыков. 7.5. Подведение итогов занятия. |
Излагает преподаватель. Тестовый контроль.
Опрос студентов, дискуссия.
Выполнение лабораторной работы. Излагает преподаватель. |
5 мин. 10
90
70
5 |
Пример билета проверочного контроля:
1) Гемсодержащие ферменты: строение, свойства, функции. Примеры гемсодержащих ферментов.
2) Что такое прямой и непрямой билирубин сыворотки крови, место их образования и диагностическое значение.
Количественное определение в крови метгемоглобина (метод л.Э.Горна).
Цель работы: ознакомиться с методом количественного определения метгемоглобина в крови.
Мотивация: метгемоглобин образуется в результате реакции окисления железа в геме гемоглобина
H bFe+2
e
MetHbFe+3,
т.е. MetHb
образование идет под действием любых
веществ с дефицитом e.
Этому способствует изменение конформации
белковой части молекулы гемоглобина
вследствие окисления ряда функциональных
групп белка. В крови здорового человека
содержание метгемоглобина не более
3%,что достигается равновесием между
реакциями его образования и реакциями
восстановления метгемоглобина. Из
реакций восстановления наиболее
значимыми являются следующие:
bFe+2
e
MetHbFe+3,
т.е. MetHb
образование идет под действием любых
веществ с дефицитом e.
Этому способствует изменение конформации
белковой части молекулы гемоглобина
вследствие окисления ряда функциональных
групп белка. В крови здорового человека
содержание метгемоглобина не более
3%,что достигается равновесием между
реакциями его образования и реакциями
восстановления метгемоглобина. Из
реакций восстановления наиболее
значимыми являются следующие:
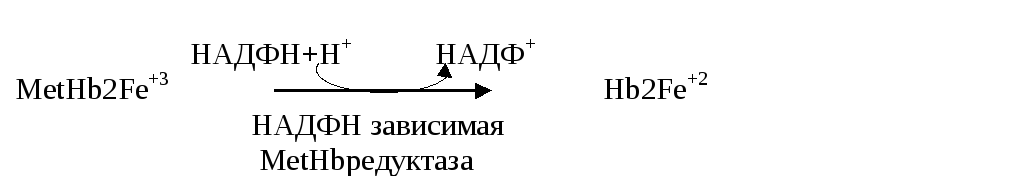
причем, НАДФН+Н+ образуется в ключевых реакциях ПФЦ
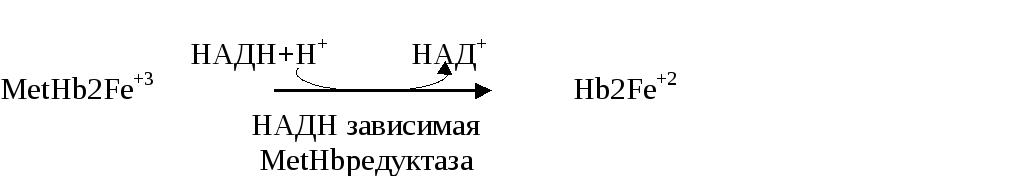
причем, НАДН+Н+ образуется в ключевых реакциях гликолиза.
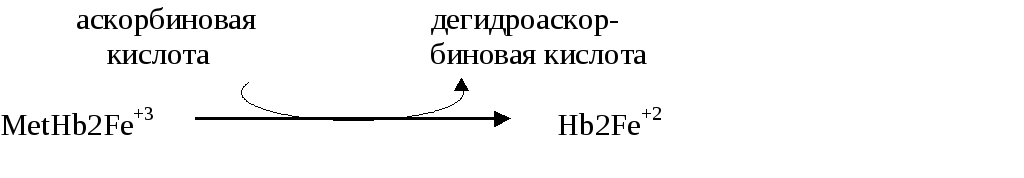 причем,
данная реакция является неферментативной.
Если содержание метгемоглобина в крови
превышает 3%- это называется метгемоглобинемия.
Метгемоглобинемии делятся на врожденные
и приобретенные. Врожденная метгемоглобинемия
имеет место при энзимопатиях и гемобинозах.
Энзимопатии – генетически обусловленные
нарушения синтеза ключевых ферментов,
участвующих в восстановлении МеtHb
или ключевых ферментов ПФЦ, генерирующих
восстановленный НАДФН. Гемоглобинозы
делятся на гемоглобинопатии – генетически
обусловленные нарушения строения
белковой части Hb,
возникающие в результате точечных
мутаций, и талассемии – состояния
развивающиеся в результате генетически
обусловленного снижения синтеза какой
либо из цепей Hb.
причем,
данная реакция является неферментативной.
Если содержание метгемоглобина в крови
превышает 3%- это называется метгемоглобинемия.
Метгемоглобинемии делятся на врожденные
и приобретенные. Врожденная метгемоглобинемия
имеет место при энзимопатиях и гемобинозах.
Энзимопатии – генетически обусловленные
нарушения синтеза ключевых ферментов,
участвующих в восстановлении МеtHb
или ключевых ферментов ПФЦ, генерирующих
восстановленный НАДФН. Гемоглобинозы
делятся на гемоглобинопатии – генетически
обусловленные нарушения строения
белковой части Hb,
возникающие в результате точечных
мутаций, и талассемии – состояния
развивающиеся в результате генетически
обусловленного снижения синтеза какой
либо из цепей Hb.
Приобретенные метгемоглобинемии делятся в зависимости от причины на эндогенные и экзогенные. Эндогенная метгемоглобинемия может возникать при различных патологических состояниях или заболеваниях, которые сопровождаются недостаточностью АОС (например: хронический энтерит, хронический гепатит, сахарный диабет и другие).
Экзогенная метгемоглобинемия возникает в случае избыточного поступления в организм человека окислителей, в том числе и лекарственных препаратов со свойствами окислителей. Так как MetHb теряет способность транспортировать О2, метгемоглобинемия сопровождается признаками гемической гипоксии, которые обусловлены различными нарушениями в обмене веществ. Для профилактики и лечения осложнений необходимо контролировать уровень MetHb в крови.
Быстрым, нетрудоемким методом определения % содержания MetHb в крови является фотоколориметрический метод Л.Э.Горна. Этот метод удобен как для профилактического обследования людей, контактирующих с MetHb образователями, так и в гигиенических исследованиях при производственных и пищевых отравлениях некоторыми химическими соединениями (нитриты,
оксиды азота, пары нитробензола, нитроанилин, гексацианоферрат калия, хлорат калия и др.), при проведении токсикологических исследований на животных.
Принцип метода: метод основан на определении оптической плотности раствора, содержащего метгемоглобин. Метгемоглобин избирательно погло-щает свет с длиной волны 619 нм. Содержание метгемоглобина рассчитывают в процентах, принимая за 100% оптическую плотность раствора полностью окисленного (гексацианоферратом) гемоглобина. Эритроциты разрушают в аммиачной среде.
Ход работы:
В три пробирки отмеривают по 7,3 мл 0,25% раствора аммиака. В две пробирки вносят по 0,2 мл крови, взятой у крысы до затравки. Первая пробирка содержит HbO2 (100%). Во вторую пробирку добавляют 1 каплю насыщенного раствора K3Fe(CN)6, принимая ее за эталон со 100% содержанием MetHb. В третью пробирку отмеривают 0,2 мл крови крысы, отравленной нитритом натрия или другими метгемоглобинообразователями, и определяют в этой крови MetHb.
Пробы оставляют стоять в течение одного часа при комнатной температу-ре, затем растворы фотометрируют, определяя их оптическую плотность. Условия колориметрии: светофильтр красный (длина волны 610 нм), кювета - 10 мм, сравнение против воды.
Для расчета процентного содержания метгемоглобина в исследуемой пробе используют формулу:
Х% MetHb = (D MetHb оп – D HbO2) 100
D MetHb 100% – D HbO2
DHbO2 – оптическая плотность раствора, не содержащего метгемоглобин (кровь, взятая до затравки крысы);
DMetHb100%. – оптическая плотность раствора, содержащего метгемо-глобин в максимальной концентрации;
DMetHbоп – оптическая плотность раствора, содержащего метгемоглобин в неизвестной концентрации (кровь крысы, затравленной нитритом).
