
- •Подзолков Владимир Петрович
- •1.1. Общая анестезия
- •2.5.27. Коарктация аорты
- •Г.И.Цукерман и.И.Скопин
- •Л.А.Бокерия
- •В. И. Бураковский в.С.РаботниковД.Г. Иоселиани
- •7.16.3. Реплантация пальцев
- •7.16.4. Микрохирургия лимфатических путей
- •1. Общие вопросы сердечно-сосудистой хирургии
- •2. Врожденные пороки сердца
- •3. Приобретенные болезни сердца и пе рикарда
- •6. Трансплантация сердца
- •4. Нарушения ритма сердца
- •5. Ишемическая болезнь сердца
- •7. Болезни сосудов
- •2. Congenital heart diseases
- •3. Acquired heart and pericardium diseases
- •4. Rhythm disorders of the heart
- •5. Ischemic heart disease
- •6. Transplantation of the heart
- •7. Vessel diseases
- •26.06.96. Формат бумаги 84x108716- Бумага мелованная офсетная.
Л.А.Бокерия
4.1. ХИРУРГИЧЕСКАЯ АНАТОМИЯ ПРОВОДЯЩЕЙ СИСТЕМЫ СЕРДЦА И СВЯЗАННЫХ С НЕЙ ОБРАЗОВАНИЙ
Основными элементами проводящей системы сердца являются синусно-предсердный узел, межузловые пути, предсер-дно-желудочковый узел, предсердно-желудочковый пучок (пучок Rica) и его ножки. Синусно-предсердный узел—это субэпикардиальная группа высокоспециализированных клеток, расположенных в пограничной борозде в месте соединения верхней полой вены и правого предсердия на передне-медиальной поверхности. Узел имеет яйцевидную форму с широким телом и сужающимся хвостом. Примерные размеры: длина 15 мм, ширина 5 мм, толщина 1,5 мм. Клетки группируются вокруг центральной артерии синусно-предсер-дного узла. Артерия может быть ветвью правой или левой венечной артерии и проходит спереди или сзади от верхней полой вены. Исследованиями последнего времени установлены три различные области, составляющие синусно-предсердный узел, каждая из которых ответственна за отдельную группу нейрогенных или циркуляторных стимулов.
Взаимоотношение этих областей определяет конечное действие синусно-предсердного узла. В естественных условиях (в здоровом организме) только клетки этого узла сердца спонтанно формируют фазу 4 деполяризации, и таким образом синусно-предсердный узел является местом формирования нормального сердечного импульса.
По краю узла расположены клетки миокарда предсердия. Проводниковые клетки с промежуточными структурными характеристиками вкраплены между клетками водителя ритма и обычным миокардом. Они формируют промежуточные диски на границе узла. Другой тип клеток—бледные (диаметр до 15 мк)—из-за низкого содержания миофибрилл напоминают волокна Пуркинье (миоциты сердечные проводящие). Существование этих клеток, однако, признается не всеми авторами. Таким образом, в составе синусно-предсердного узла имеются узловые, «бледные» проводниковые и клетки миокарда предсердия.
В течение нескольких десятилетий идут споры о том, существуют ли специализированные проводящие пути между синусно-предсердным узлом и предсердно-желудочковым узлом—так называемые межузловые пути. Функционально они существуют совершенно определенно. Известно, что возбуждение от синусно-предсердного узла антеградно проходит по пограничному гребню и лимбу овальной ямки (рис. 4.1). Эти мышечные пучки не являются специализированными изолированными трактами проводящей системы, как это имеет место в желудочках сердца. Электрические импульсы проходят через эти предсердные мышечные пучки быстрее, чем в других отделах предсердий, и одновременное повреждение их приводит к блокаде межузловой проводимости.
Предсердно-желудочковый (атриовентрикулярный) узел— это наиболее сложный анатомический отдел проводящей системы. С функциональных позиций предсердно-желудочковый узел является областью, в которой происходит нормальная задержка атриовентрикулярной проводимости. Эта область анатомически связана с группой клеток предсердно-желудочкового соединения; эти клетки гистологически отличаются от клеток сократительного миокарда.
Приблизившись к области предсердно-желудочкового уз-
ла, предсердный импульс пересекает «переходную зону» специализированных клеток, располагающихся в основании межпредсердной перегородки. Эта переходная зона окружает предсердную часть «компактного» отдела предсердно-желудочкового узла, т. е. того отдела, в котором максимально выражена задержка проведения. Нижняя, продольная часть компактного отдела узла пенетрирует центральное фиброзное тело непосредственно кзади от перепончатой части межпредсердной перегородки, превращаясь в предсердно-желудочковый пучок. Предсердно-желудочковый узел с переходной зоной и пенетрирующим пучком располагается в треугольнике Коха (анатомически хорошо различимой области), границы которого составляют сухожилие Тодаро, заслонка венечного синуса (тебезиев клапан) и кольцо трехстворчатого клапана. Треугольник Коха является надежным ориентиром при выполнении операции криодеструкции предсердно-желудочкового узла у больных с наджелудоч-ковыми тахикардиями, если выполнение другой, более оптимальной операции невозможно.
Предсердно-желудочковый узел пенетрирует центральное фиброзное тело в месте сочленения трехстворчатого, митрального и аортального клапана, превращаясь в предсердно-желудочковый пучок. Гистологически трудно определить начало и окончание предсердно-желудочкового пучка. Началом его обычно считается место, где преимущественно встречаются большие клетки типа волокон Пуркинье (миоциты сердечные проводящие), при этом они располагаются параллельно и ориентированы в продольном направлении. Окончанием предсердно-желудочкового пучка является место, где появляются элементы левой и правой ножек. Поэтому размеры его часто вызывают споры. Длина пучка колеблется от 4,5 до 30 мм (средняя величина 10 мм), а диаметр— от 0,7 до 4 мм (средняя величина 1,8 мм).
Анатомия этой области усложняется тем, что соединение правых камер сердца занимает пространственное положение, отличающееся от положения соединения левых камер сердца, а кольцо трехстворчатого клапана ближе к верхушке сердца, чем кольцо митрального клапана. Предсердно-желудочковый пучок проходит вдоль заднего нижнего края перепончатой части межжелудочковой перегородки (рис. 4.2). Правая ножка пучка проходит субэндокардиально и направляется к основанию медиальной сосочковой мышцы, спускается кпереди к верхушке желудочка в составе перегородочно-краевой трабекулы и разветвляется на верхушке, частично пересекая полость желудочка в составе «модераторного тяжа» (рис. 4.3). В нижней части перепончатой межжелудочковой перегородки от предсердно-желудочкового пучка отходит множество отростков, формирующих левую ножку предсердно-желудочкового пучка, которая уходит вниз на левую сторону перегородки и через 1—2 см делится на меньший—передний и больший—задний пучок. Медиальные части каждого из этих пучков формируют в дистальном направлении три сети анастомозов: переднюю, среднюю и заднюю ветви. Если смотреть на межжелудочковую перегородку с левой стороны через аортальный клапан, то наиболее уязвимая зона проводящей системы расположена в непосредственной близости от правой коронарно-некоронар-ной комиссуры (рис. 4.4). Дистальные ветви проводящей системы заканчиваются в пограничной зоне между волокнами Пуркинье и сократительным миокардом, т. е. там, где клетки постепенно теряют форму волокон Пуркинье и при-
473

4.1. Схематическое изображение расположения заднего (1), среднего (2), переднего (3) межузловых путей и межпред-сердного пучка—пучка Бахмана (4).
ОЯ—овальная ямка; СПУ—синусно-предсердный узел; ПЖУ—предсердно-желудочковый узел; ВС—венечный синус.

обретают черты сократительного миокарда желудочков. Особое значение для кардиохирурга имеют взаимоотношения различных структур и пространств, относящихся к соединению межпредсердной и межжелудочковой перегородок, предсердно-желудочковой борозды и фиброзного «скелета» сердца. Наиболее мощным образованием последнего является центральное фиброзное тело, где соприкасаютсяфиброзные кольца митрального, трехстворчатого и аортального клапанов.
Кольца митрального и аортального клапанов в месте своего соединения формируют левый фиброзный треугольник. Левая передняя часть центрального фиброзного телаопределяется как правый фиброзный треугольник. Предсер-дно-желудочковая борозда между двумя треугольникамиявляется частью продолжения между передней створкой митрального клапана и кольцом аортального клапана. Это единственное место в предсердно-желудочковой борозде, где миокард предсердия не состоит в интерпозиции с миокардом желудочка. Поэтому между левым и правым фиброзным треугольниками не бывает добавочных аномальных атриовентрикулярных путей (пучки Кента).
В пирамидальном пространстве, расположенном над приточной перегородкой, находятся задние перегородочные пути при синдроме Вольфа—Паркинсона—Уайта. Основанием (дном) этого пирамидального пространства является верхнезадняя часть межжелудочковой перегородки. Сверху и сбоку оно ограничено расходящимися стенками правого и левого предсердий, а задняя часть покрыта эпикардом,переходящим с предсердия на желудочек над жировой прослойкой атриовентрикулярной борозды.
Пространство содержит терминальную часть венечного синуса, артерию предсердно-желудочкового узла и жировой слой (рис. 4.5). Сложная анатомия этого отдела является непрекращающимся «вызовом» хирургу, стремящемуся прервать добавочное аномальное атриовентрикулярное соединение, проходящее в пирамидальном пространстве.
Волокна (пути), шунтирующие проведение возбуждения по миокарду. В норме миокард предсердия отделен от миокарда желудочков фиброзной тканью. У больных с синдромомВольфа—Паркинсона—Уайта имеется мышечный мостик, структурно идентичный миокарду предсердия. Размеры егоот 1 до 8 мм. Он перекидывается через предсердно-желудоч-ковую борозду, внедряется в миокард желудочка (рис. 4.6) и в определенных условиях является причиной тахикардии по типу повторного входа (риентри). У одного больного возможно наличие нескольких пучков Кента. Пучки Кента встречаются вдоль всего периметра предсердно-желудочковой борозды, за исключением пространства между левым и правым фиброзными треугольниками. W. Sealy,
4.2. Схематическое изображение предсердно-желудочкового узла и проксимального отдела специализированной проводящей системы [James Т., 1961].
Видно взаиморасположение межпредсердной перегородки (МПП), митрального клапана (МК), перепончатой части перегородки (ПЧП) и предсердно-желудочкового узла (А), пучка (Б), его левой (В, Г) и правой ножек (Д). Обе ножки предсердно-желудочкового пучка проходят в составе МЖП: правая субэндокардиально, левая пенетрирует ее, уходя на левую сторону.
474
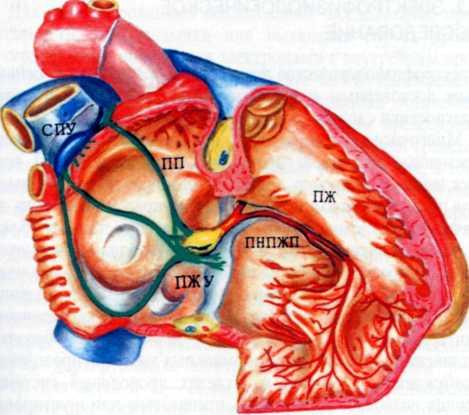

СПУ— синуаю-предсердный узел; ПЖУ— предсердно-желу-дочковый узел; ПНПЖП—правая ножка предсердно-желудочкового пучка. Остальные обозначения те же, что на рис. 4.1.
4.4. Топографическая анатомия левой ножки предсердно-желудочкового пучка [Netter F., 1970].
ЛП—левое предсердие; Л Ж—левый желудочек; А—Б—передняя и задняя ветви левой ножки предсердно-желудочкового пучка; Ао — аорта; ЛС—легочный ствол; ПБ—пучок Бахмана.
J. Gallagher выделяют четыре основные локализации пучков Кента: правостороннюю, левостороннюю, переднюю и заднюю перегородочные.
Тракт Джеймса описан в 1961 г. Это мышечное образование, происходящее из задних отделов межпредсердной перегородки и шунтирующее предсердно-желудочковый узел, внедряется на уровне дистального отдела узла или проксимального отдела предсердно-желудочкового пучка. Некоторые специалисты отрицают возможность его анатомическо-
го существования, которое часто выявляется электрофизио-логически.
Волокна Магейма описаны в 1947 г. Они представлены параспецифическими образованиями, соединяющими ди-стальный отдел предсердно-желудочкового узла или проксимальный отдел предсердно-желудочкового пучка с верхними отделами межжелудочковой перегородки. Тахикардии при наличии волокон Магейма возникают редко, но протекают злокачественно—по типу желудочковых тахиаритмий.

МЖП—межжелудочковая перегородка; ПП и ЛП—правое и левое предсердия; ПЖ и Л Ж—правый и левый желудочки; ТК и МК—трехстворчатый и митральный клапаны; ВПВ и НПВ—верхняя и нижняя полые вены; сТ—сухожилие Тодаро; ЦФТ—центральное фиброзное тело; ВС—венечный синус.
475

4.6. Микропрепарат левостороннего добавочного аномального проводящего пути [Anderson R., Becker A., 1981]. I — предсердие; 2 — .-желудочек; 3 — фиброзное кольцо (ука-laiia стрелкой створка митрального клапана); 4 — пучок Кента.
4.2. ЭЛЕКТРОФИЗИОЛОГИЧЕСКОЕ ИССЛЕДОВАНИЕ
Электрофизиологическое исследование (ЭФИ) стало основным достоверным и окончательным методом топической диагностики сложных нарушений ритма сердца.
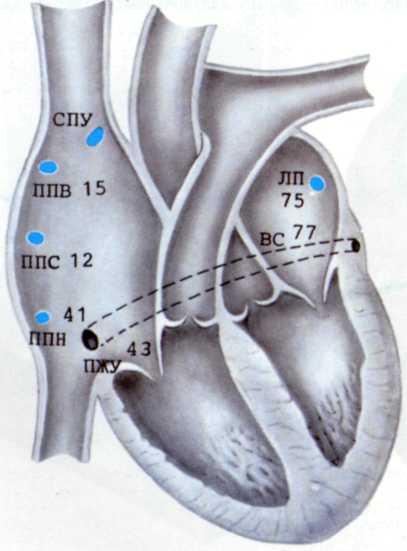
Многочисленными исследованиями были установлены временные интервалы проведения (распространения) возбуждения по миокарду (рис. 4.7). Так. время, необходимое для прохождения импульса от синусно-предсердного узла до начальных отделов пограничной борозды, составляет 15 мс. а до ее конечного отдела 41 мс, до коронарного синуса 77 мс. В предсердно-желудочковый пучок возбуждение приходит через 43 мс. В здоровом сердце время проведения между предсердно-желудочковым пучком и желудочком (интервал Я— V) составляет 40—50 мс. Таким образом, удлинение или укорочение нормальных значений проведения возбуждения в различных отделах проводящей системы сердца позволяет заподозрить препятствие или шунтирование процесса распространения возбуждения в миокарде. Для получения столь ценной информации под рентгенологическим контролем пункционно через вену и/или артерию в сердце вводят 4—5 эндокардиальных электрода, располагая их так. чтобы получить данные о скорости и характере распространения возбуждения (рис. 4.8). Электроды подключают к самописцу и регистрируют электрические потенциалы—электрограммы (ЭГ). осуществляя эндокардиаль-ное картирование (рис. 4.9).
При операциях на открытом сердце исследуют последовательность распространения возбуждения по всему эпикарду—эпикардиальное картирование. Для этого обычно необходимы два электрода: один референтный, показания которого принимаются за нулевое значение, а другой картирующий, позволяющий определить время прихода возбуждения в различные отделы сердца. В условиях операции проводится также трансмуральное (используется игла-электрод с множеством отведений) или эндокардиальное (после вскрытия полостей сердца) картирование.
Электроды. Для эндокардиального картирования наиболее часто применяются биполярные, триполярные или тет-раполярные электроды USCI, как правило, трех размеров: 5F, 6F и 7F. Расстояние между полюсами электрода 1 см. Тетраполярные электроды устанавливают в предсердие и коронарный синус, триполярные—в область предсердно-же-лудочкового узла или предсердно-желудочкового пучка. а биполярные—в желудочки сердца. Некоторые специалисты для электрофизиологического исследования у детей пользуются одним восьми- или девятиполярным электродом, который устанавливают с таким расчетом, чтобы иметь информацию на всем протяжении проводящей системы. Однако разрешающая способность данного способа диагностики несколько ниже, чем при наличии нескольких многополярных электродов.
4.7. Основные позиции электродов при картировании предсердий и средние величины времени прихода (мс) электрического возбуждения от синусно-предсердного узла к этим точкам.
СПУ—синусно-предсердный узел; ЛП—левое предсердие; ППВ, ППС. ППН — верхний, средний и нижний отделы правого предсердия; ВС — венечный синус; ПЖУ — предсердно-желудочковый узел.
476
Для комбинированных исследований (исследование проводимости, гемодинамики или выявления сброса крови в сердце) часто пользуются электродами с внутренним просветом. Такой электрод удобен тем, что можно одновременно исследовать: 1) гемодинамику при аномалии Эбштейна;
записать гисограмму и давление в правом предсердии;
при необходимости использовать проводник или транссе- птальную иглу; 4) исследовать газовый состав крови, в том числе в коронарном синусе для изучения влияния аритмии на сердечный выброс, или определить величину сброса кро ви и т. д.
Для проведения эпикардиального картирования необходимы референтные и картирующие электроды. В качестве референтных мы используем биполярные электроды в форме прищепки для фиксации на предсердия (ушко) и игольчатые в форме «вил» для фиксации на желудочки. Оптимальная форма картирующего электрода—прямая (длиной 8— 10 см для детей и 15—18 см для взрослых). Предложены картирующие электроды в форме кольца, надеваемого на палец, для обследования задней поверхности сердца и некоторые другие формы. При картировании очень важно видеть место, на которое накладывается электрод. «Слепое» картирование всегда может отразиться на результате операции—неустранение или неполное устранение аритмии.
Возбуждение, воспринимаемое электродом, через блок усилителей и преобразователей передается на осциллоскоп и самописец. В этой схеме крайне желательно иметь многоканальный аналог-магнитофон. В последнее время для диагностики сложных аритмий используются компьютеры. Наиболее типичный вариант организации электрофизиологического исследования представлен на рис. 4.10.
Изложенный материал относился к регистрации информации. Само электрофизиологическое исследование предусматривает искусственное создание условий, при которых развиваются нарушения ритма, наблюдаемые у больного. Такие условия моделируются программируемым электрическим стимулятором сердца, который, таким образом, является важнейшим элементом диагностической процедуры. Программируемый электрический стимулятор сердца— сложное в техническом отношении устройство, предназначенное для диагностических и лечебных целей. Режим работы его предусматривает возможность электрической стимуляции сердца в асинхронном режиме и режиме demand (по требованию). Возможна последовательная (секвенциальная) стимуляция. При электрофизиологическом исследовании он позволяет проводить так называемую программируемую стимуляцию сердца, когда на миокард наносится экстрастимул в различные периоды сердечного цикла через определенное количество сердечных сокращений. В результате этого выявляется экстрасистола, приводящая к развитию приступа аритмии. В некоторых случаях есть необходимость «подать» на сердце серию следующих друг за другом стимулов (от 2 до 20 между двумя сокращениями) и т.д. Прибор позволяет проводить частую и сверхчастую стимуляцию. Диагностическое назначение прибора состоит в том, чтобы вызвать, изучить и прекратить имеющуюся у больного тахи-аритмию, а лечебное—в купировании спонтанно развившейся тахикардии.
Измерение интервалов проведения. Регистрация электрограммы предсердно-желудочкового пучка—важнейший метод изучения атриовентрикулярной проводимости, позволя-

4.8. Рентгенограмма грудной клетки больного при электрофизиологическом исследовании сердца.
Расположение пяти электродов в полостях сердца при ЭФИ (переднезадняя проекция). ПП—правое предсердие (верхний отдел); ПЖП—предсердно-желудочковый пучок; ВС—венечный синус; ПЖ и Л Ж—правый и левый желудочек.
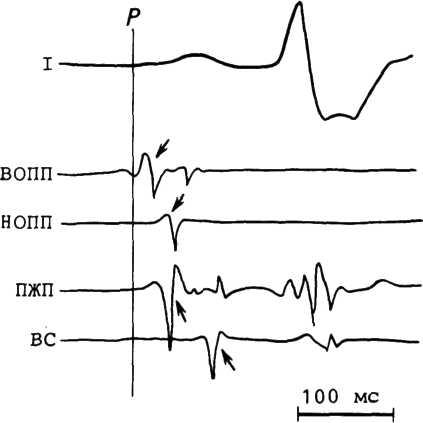
4.9. Электрокардиограмма и электрограммы верхнего (ВОПП) и нижнего (НОПП) отделов правого предсердия, предсердно-желудочкового пучка (ПЖП) и венечного синуса (ВС) при нормальном антеградном распространении возбуждения.
Время локальной активности определяют в момент пересечения изоэлектрической линии первого «быстрого» отклонения электрограммы (указано стрелками). Начало зубца Р в I отведении является точкой отсчета (референтная точка).
477

Спайк предсердно-желудочкового пучка имеет двухфазную или трехфазную форму продолжительностью от 15 до 25 мс. Он располагается между спайками предсердной и желудочковой локальной активности.
Гисография позволяет определить интервалы А — Я и Я— V, установить соотношение спайка предсердно-желудочкового пучка с другими элементами электрограммы. На качество гисограммы влияют частота фильтров и положение электрода относительно узла. Спайк предсердно-желудочкового пучка особенно хорошо проявляется, если он фильтруется при частоте менее 40 Гц и более 500 Гц.
Положение электрода в области предсердно-желудочкового узла смещает спайк пучка и изменяет его амплитуду. Максимального значения он достигает, находясь в дисталь-ном отделе предсердно-желудочкового пучка, что на гисо-грамме соответствует срединному положению спайка между волнами Я и К.
Интервал А — Я—это время проведения импульса от нижних отделов межпредсердной перегородки через предсердно-желудочковый узел в предсердно-желудочковый пучок. Таким образом, этот показатель дает ориентировочное представление о времени проведения возбуждения по предсердно-желудочковому узлу. На значения этого показателя влияет как местоположение электрода, так и эмоциональное состояние больного. При усилении тонуса симпатической нервной системы этот интервал укорачивается, при усилении тонуса парасимпатической системы—удлиняется. Видимо, поэтому так разноречивы в литературе данные о нормальных величинах интервала А — Я: от 45 до 150 мс.
Интервал А — Я приобретает диагностическое значение при электростимуляции и введении лекарств.
Интервал Я—V характеризует время проведения от проксимальных отделов предсердно-желудочкового пучка до миокарда желудочков. Нормальные значения у взрослых колеблются от 35 до 55 мс. Вегетативная нервная система не влияет на длительность этого интервала. Не влияют на него также электрофизиологическое исследование или введение лекарств. Вариант расчета интервалов А—Я и Я— V приведен на рис. 4.11.
Внутрипредсердная проводимость является недостаточно изученным разделом электрофизиологии. Наиболее часто для ее характеристики используется интервал Р—А (от начала волны Р до начала спайка А на гисограмме). Однако волна А может предшествовать зубцу Р. Смещение электрода при регистрации гисограммы книзу искусственно увеличивает интервал. Наконец, интервал Р—А характеризует не всю внутрипредсердную проводимость, а лишь проводимость в нижних отделах правого предсердия.
Поэтому единственным условием для определения характера внутрипредсердной проводимости является наличие нескольких электродов в правом предсердии, в проекции предсердно-желудочкового узла и в венечном синусе. Тогда можно точнее определить последовательность распространения возбуждения по миокарду предсердий.
Программируемая электрическая стимуляция сердца. Учащающая стимуляция и нанесение программированного единичного или множественных экстрастимулов на синусовом или навязанном ритме являются основными методами динамического электрофизиологического исследования.
Такое исследование позволяет: 1) охарактеризовать физиологические свойства проводящей системы, предсердий и желудочков; 2) вызвать аритмию и изучить ее механизм; 3) исследовать влияние лекарств и/или электростимуляции на функцию проводящей системы, предсердий и желудочков, а также определить их эффективность (порознь или вместе) в лечении аритмий.
Стимуляция проводится электрокардиостимулятором, имеющим изолированный источник питания; амплитуда стимулов в 2 раза превышает порог стимуляции.
Учащающая стимуляция позволяет изучить функциональные свойства проводящей системы. Обычно этот вид стимуляции проводят из верхнего отдела правого предсердия вблизи синусно-предсердного узла. Стимуляцию начинают с частоты, несколько превышающей частоту собственного ритма, прогрессивно уменьшая продолжительность цикла на 50 мс и доводя до цикла с минимальным значением 300 мс. Для сохранения стабильности каждого режима стимуляция на каждом новом цикле должна продолжаться не менее 30 с.
Нормальной реакцией проводящей системы на учащающую стимуляцию является постепенное удлинение интер-
478
вала А—Я по мере укорочения продолжительности цикла стимуляции с переходом в атриовентрикулярную блокаду (типа периодов Самойлова—Венкебаха). При этом интервал Я— V не изменяется. Продолжение стимуляции приводит к увеличению степени блокады (2:1,3:1). При отсутствии дополнительных проводящих путей у большинства больных блокада типа периодов Самойлова—Венкебаха развивается при стимуляции с длительностью цикла 500—350 мс. Скорость развития этого феномена зависит от исходной частоты сердечных сокращений и влияния автономной нервной системы. Существует корреляция между интервалом А—Я при синусовом ритме и проявлением периодов Венкенбаха при стимуляции. У больных с удлиненным интервалом А— Я блокада узла развивается при низкой частоте стимуляции, а у больных с укороченным интервалом А—Я—при высокой частоте стимуляции. В целом удлинение интервала А— Я выше 400 мс, когда в результате стимуляции развиваются периоды Венкебаха, является патологическим и отмечается при нарушениях внутриузловой проводимости.
Стимуляция желудочков позволяет изучить ретроградную проводимость по предсердно-желудочковому узлу. По данным различных авторов, она встречается у 40—90% людей.
Считается, что обратная проводимость наиболее часто выявляется при хорошей антеградной проводимости. Это, по-видимому, так, но необходимо помнить, что ретроградная проводимость возникает часто и у больных с полной поперечной блокадой.
Как и при предсердной стимуляции, стимуляцию желудочков начинают с частоты, несколько превышающей частоту исходного ритма. Затем стимуляцию учащают и доводят длительность цикла до 300 мс. Нормальной считается реакция, аналогичная той, которая возникает при стимуляции предсердий. Ретроградная блокада типа периодов Самойлова—Венкебаха и более высокие степени блокады развиваются, однако, при более короткой длине цикла. Экстрасистолы, возникающие при желудочковой стимуляции, называют желудочковыми «эхо». Они возникают при критических степенях задержки желудочково-предсердной проводимости и в ряде случаев свидетельствуют о формировании круга повторного входа в предсердно-желудочко-вом угле в связи с феноменом продольной диссоциации.
Метод является исключительно важным для определения уровня блокады в узле.
Поскольку при ретроградной стимуляции спайк предсер-дно-желудочкового пучка выявляется только в 10% случаев, то в большинстве ориентиром при расчете интервалов проведения служит деполяризация предсердий. Для установления уровня задержки можно, например, использовать данные скрытой ретроградной проводимости. Если при желудочковой стимуляции интервал Я—А не изменяется, значит ретроградный блок находится внутри узла. Аналогичную пробу можно провести с атропином.
Определение рефрактерных периодов. Рефрактерность миокарда определяется его способностью реагировать на экстрастимул. Она может быть относительной, эффективной и функциональной.
Относительный рефрактерный период (ОРП)—период полного восстановления, или зона, в течение которой проведение тестирующего и основного (собственного) импульсов идентично. Электрофизиологически—это наиболее продол-
жительный интервал между ответом на тестирующий стимул и спонтанным (либо навязанным) электрическим ответом соответствующего отдела сердца.
Эффективный рефрактерный период (ЭРП)—наиболее продолжительный спаренный интервал между основным ритмом и тестирующим стимулом, не вызвавшим ответа. Поэтому его следует измерять проксимальнее рефрактерной ткани.
Функциональный рефрактерный период (ФРП)—минимальный интервал между двумя последовательно проведенными импульсами. Это значит, что поскольку функциональный рефрактерный период измеряет выходные показатели ткани сердца, то и определять его нужно дистальнее этой ткани. Поэтому, например, определение эффективного рефрактерного периода ткани возможно, если функциональный рефрактерный период проксимальных его отделов будет меньше, чем эффективный рефрактерный период ди-стальных. Таким образом, эффективный рефрактерный период системы Гиса—Пуркинье можно измерить лишь в том случае, если он превышает функциональный рефрактерный период предсердно-желудочкового узла.
Концепция измерения рефрактерных периодов применима к любому отделу проводящей системы. При электрофизиологическом исследовании она определяется нанесением экстрастимулов. Одиночные предсердные или желудочковые экстрастимулы наносятся с непрерывно уменьшающимся спаренным интервалом до тех пор, пока не прекратится ответ ткани. Поскольку рефрактерность ткани сердца зависит от длины цикла, то ее следует измерять при фиксированной (навязанной) частоте в физиологических пределах (1000—600 мс), чтобы исключить влияние синусовой аритмии и/или спонтанно возникших экстрасистол. Для нормализации рефрактер-ности, которая обычно завершается к 4—5-му собственному сокращению, экстрастимул наносится через каждые 8—10 спонтанных либо навязанных сокращений.

4.11. Пример расчета интервалов на гисограмме с использованием записи электрокардиограммы в отведении К,. Стрелками обозначено начало зубца Р и спайки деполяризации предсердия (А), предсердно-желудочкового пучка (Н) и желудочков (V). Интервал Р—А составляет 35 мс, А — Н— 90 мс, Н—V—40 мс, ПП—правое предсердие; ВС—венечный синус; ПЖП—предсердно-желудочковый пучок.
479
Интраоперацнонное исследование—картирование сердца.
Электрические процессы в сердце характеризуются большим динамизмом последовательности распространения возбуждения по миокарду. Аритмии приводят к нарушению этого динамизма с образованием аритмогенных участков или зон миокарда. Это значит, что к той области сердца, в которой возникает аритмия, возбуждение приходит раньше или позже, чем ко всем остальным отделам. Чтобы локализовать это место, необходимо иметь нулевой сигнал (референтная точка), обычно регистрируемый из легко доступного отдела с устойчивыми характеристиками (ушко предсердия, выходной отдел правого желудочка или место, наиболее близко расположенное к источнику аритмии). Затем картирующим электродом по определенной схеме измеряют время прихода возбуждения в различные отделы сердца и рассчитывают разницу между референтным сигналом и сигналом, регистрируемым в каждой из этих точек. Зоны максимальной разницы и являются очагом аритмии.
Получение информации наиболее благоприятно на фоне той аритмии, которая имеется у больного (конкретные примеры методов картирования сердца приведены в разделе тахиаритмии).
Приводимые в этом разделе электрофизиологические критерии и способы их определения лишь очень кратко характеризуют современное состояние клинической электрофизиологии сердца. Они нужны для диагностики и объяснения механизмов аритмий, а также для подбора лекарственной терапии и хирургического лечения.
4.3. БРАДИАРИТМИИ
Физиологические пределы частоты сердечных сокращений у взрослого здорового человека в состоянии покоя могут колебаться от 60 до 100 в минуту. Несмотря на то что эти цифры, безусловно, носят очень ориентировочный характер, они приняты в практической медицине и позволяют иметь надежный ориентир в подходе к определению понятия бра-дикардия и тахикардия. Таким образом, у людей с числом сердечных сокращений менее 60 имеется брадикардия, а с числом более 100—тахикардия.
За последние годы в лечении брадиаритмий достигнуты большие успехи в основном благодаря развитию исключительно эффективных, долговечных и хорошо управляемых электрокардиостимуляторов. Введение микропроцессоров в эти аппараты позволило расширить их фунциональные возможности. Комбинация операций в некоторых самых современных стимуляторах превышает 5 000 000.
Развитие методов электрофизиологии позволяет подробно исследовать состояние всей проводящей системы. При таком подходе можно очень точно локализовать уровень поражения проведения возбуждения по миокарду. Однако только накопление и обобщение коллективного опыта таких исследований позволит определить тактику лечения в спорных случаях.
В настоящее время совершенно определенной является тактика лечения лишь при состояниях, характеризующихся приступами Морганьи—Адамса—Стокса или при наличии у больного трифасцикулярной блокады. В остальных случаях (тахи-брадисиндром, остановка предсердия, атриовент-рикулярная блокада II степени) подходы различны. Если читатель обратится к материалам последних международ-
ных конгрессов по электростимуляции, то увидит, что некоторые авторы больным с «малой» симптоматикой (слабость, легкое головокружение) имплантируют стимуляторы. При этом учитываются физиологические системы. Другие авторы являются сторонниками традиционных подходов (см. выше).
Наиболее частыми причинами брадиаритмий являются атриовентрикулярная блокада и слабость синусно-предсер-дного узла (более 95%). Реже встречаются нарушения сино-атриальной проводимости, предсердно-узловой (атриовент-рикулярной) проводимости и полной межузловой проводимости (остановка предсердий).
Этиология. Слабость синусно-предсердного узла или прекращение его функции (остановка) может быть следствием вовлечения этого узла в ишемиче-ский, склеротический или воспалительный процесс. У большинства больных выявляется ИБС (35—51%). К другим наиболее частым причинам слабости синусового узла относят кардиопатию, гипертоническую болезнь, ревматизм, сифилис, ВПС. Имеются также отдельные сообщения о таких заболеваниях, как туберкулезный перикардит, тиреотоксикоз, амилоидоз сердца, дифтерия.
Признаки синдрома на ЭКГ могут быть обусловлены влиянием лекарств: дигиталис, хинидин, новокаинамид, ана-прилин. У 40% больных не удается установить этиологию заболевания.
В основе другой распространенной патологии с вовлечением синусового узла — синоатриальной блокады сердца—могут быть такие причины, как: 1) воспаление при активном ревмокардите либо другие формы миокардита; хирургическая травма; 2) дегенеративный процесс (например, постдифтеритический фиброз), коронарный атеросклероз; 3) ишемия, обусловленная инфарктом миокарда в результате окклюзии артерии, питающей синусно-предсер-дный узел.
Хроническая остановка предсердия—состояние, при котором отсутствует электрическая активность миокарда предсердий в течение месяцев или лет, что обычно наблюдается в терминальных стадиях многих заболеваний. Чаще других это бывает при инфаркте миокарда. Причиной остановки предсердий является гипоксия или гиперкалиемия.
Более подробно изучена этиология атриовентрику-лярной блокады. В ее основе может быть ряд заболеваний—склеродегенеративная болезнь, ИБС, лекарственная интоксикация, в частности антиаритмическими препаратами, воспалительные состояния при ревмокардите и миокардите, ВПС. Наиболее часто атриовентрикулярная блокада возникает вследствие трех первых причин.
Склеродегенеративная болезнь характеризуется прогрессирующим замещением фиброзной тканью специализированных мышечных клеток проводящей системы. При гисто-патологическом исследовании выявляется, что фиброз может начинаться как в области окончаний ветвления ножек предсердно-желудочкового пучка, т. е. дистально, так и в проксимальных отделах системы Гйса — Пуркинье, а затем охватывает всю специализированную проводящую систему. Оказалось, что и электродеструкция предсердно-желудочкового узла, направленная на создание искусственной полной поперечной блокады сердца у больных с наджелудо-чковыми тахикардиями, характеризуется аналогичными изменениями. Когда поражение проводящей системы первично, болезнь не распространяется на сократительный миокард и коронарные сосуды. Заболевание носит хронический характер, и полная поперечная блокада обычно развивается только в пожилом возрасте. При ИБС блокада сердца является результатом снижения перфузионного объема крови к специализированной проводящей системе. Так как предсер-дно-желудочковый узел кровоснабжается артерией этого узла, то уменьшение кровотока по ней ведет к нарушениям узловой проводимости. Предсердно-желудочковый пучок и проксимальные отделы правой и левой ножек предсердно-
480
желудочкового пучка кровоснабжаются первой большой перегородочной ветвью левой венечной артерии. Снижение кровотока по этой артерии может приводить к нарушению проводимости в кровоснабжаемой зоне.
Препараты наперстянки и анаприлин уменьшают проводимость по предсердно-желудочковому узлу. В больших дозах, особенно при передозировке, они могут вызвать нарушения проводимости, вплоть до блокады сердца.
Клиника и диагностика слабости сннусно-предсердного узла. Синдром встречается одинаково часто у мужчин и женщин, обычно у людей старше 70 лет, но может быть и у детей.
Симптоматика этого синдрома обычно обусловлена снижением перфузии жизненно важных органов, особенно мозга и сердца.
Мозговые проявления являются отличительным признаком симптоматики. У больного внезапно появляются головокружения, предобморочные состояния или обморок. Этому могут предшествовать жалобы на повышенную утомляемость, раздражительность, ухудшение памяти. Больные со слабостью синусно-предсердного узла предрасположены к системной эмболизации, что связывают со сменой ритма предсердий. Типичны жалобы на одышку, боли и проявления застойной недостаточности. У больных может быть отек легкого, если слабость синусно-предсердного узла сочетается с тахикардией.
На ЭКГ выявляется синусовая брадикардия (у 90%). У некоторых больных, если наблюдается тахибрадисиндром, регистрируется тахикардия. На ЭКГ можно также выявить признаки инфаркта миокарда, блокаду ножек предсердно-желудочкового пучка, гипертрофию миокарда. Однако и нормальная ЭКГ не исключает наличия у больного слабости синусно-предсердного узла. Поэтому необходимо учитывать наиболее типичные клинические проявления: обморок, предобморочные состояния, легкие головокружения, сердцебиения. Обморочные состояния обычно требуют проведения дифференциальной диагностики. Следует провести тщательный анализ приема сердечных препаратов, так как слабость синусового узла может отчетливо проявляться при лечении другой патологии; сердечной недостаточности, ИБС, возвратных тахиаритмий.
Физикальное обследование дает мало информации для выявления нарушений ритма. Оно, однако, очень важно для исключения других причин обморочных состояний (аортальный стеноз, идиопатический гипертрофический субаортальный стеноз, миксома левого предсердия). Часто стандартная ЭКГ с длительной записью может прояснить ситуацию. Однако аритмия, обусловленная слабостью узла, на ЭКГ может отсутствовать, что требует проведения дополнительных исследований.
Исключительно информативным методом исследования является холтеровское мониторирование—непрерывная запись ЭКГ на минимагнитофон в течение 24—26 ч с последующим анализом. Даже в отсутствие клинических признаков удается определить характерные изменения на ЭКГ, что позволяет у больных с жалобами на обмороки или предобморочные состояния установить правильный диагноз. Однако чаще всего у больного имеется и клиническая симптоматика, и характерные изменения ЭКГ, выявляемые методом холтеровского мониторирования.
Существует также несколько методов «провокации» для выявления слабости синусно-предсердного узла.
Если после массажа каротидного синуса возникает пауза длительностью более 3 с, то такую реакцию синусно-предсердного узла можно считать неадекватной и подозревать болезнь синусно-предсердного узла. Хотя этот признак не является специфическим, он позволяет заподозрить болезнь и продолжить обследование. Пробу следует проводить при непрерывной записи ЭКГ, соблюдая меры предосторожности, имея под рукой все необходимое для реанимации.
Проба Вальсальвы используется для дифференциальной диагностики слабости синусно-предсердного узла и физиологической синусовой брадикардии. У больных с поражением узла частота сердечных сокращений не меняется. При физиологической синусовой брадикардии происходит ожидаемое учащение ритма в фазу 2 (вдоха) и замедление ритма в фазу 4 (выдоха). Пробы на учащение ритма также можно использовать в процессе обследования больного.
Для исключения парасимпатических влияний как причины синусовой брадикардии внутривенно вводят атропин (1—2 мг). Если после этого число сердечных сокращений не превышает 90 в минуту, а время восстановления синусно-предсердного узла останется прежним, можно говорить об органической природе заболевания.
Предсердная стимуляция для определения времени восстановления синусно-предсердного узла является важнейшим методом установления диагноза. Время восстановления изучают при частой стимуляции (90—150 в минуту), временно подавляющей функцию синусно-предсердного узла. Интервал между последним стимулом и первой волной Р после прекращения стимуляции определяет искомое время. Если в результате стимуляции возникает остановка предсердия, то интервал определяется от последнего стимула до узлового сокращения. В норме время восстановления синусно-предсердного узла колеблется от 0,8 до 1,1 с (в среднем 0,9 с). Интервал более 1,6 с следует относить к патологической величине. У больных со слабостью синусно-предсердного узла он составляет 1,6—7 с.
Таким образом, несмотря на то что такие методы исследования, как массаж каротидного синуса, проба Вальсальвы, введение атропина и время восстановления синусно-предсердного узла, имеют очень большое значение, тем не менее они приобретают истинно диагностическое значение лишь тогда, когда на ЭКГ регистрируется характерный ритм.
По клиническому течению больных со слабостью синусно-предсердного узла можно разделить на три группы. К первой группе относятся те, у которых, несмотря на выраженную брадикардию (35—40 в минуту), сердечный выброс достигает нормальных значений за счет резкого возрастания ударного выброса. Благодаря этому клиническая симптоматика, обусловленная гипоперфузией жизненно важных органов, не развивается. Такие больные в лечении не нуждаются.
Во вторую группу отнесены больные с так называемой малой симптоматикой. Эти больные отмечают небольшую отечность в области лодыжек, которая легко устраняется минимальными дозами диуретиков, предъявляют жалобы на неприятное чувство замедления, ускорения сердечных сокращений или ощущение нерегулярного сердечного ритма. Они также не нуждаются в специфическом лечении. Им проводится симптоматическая терапия. К третьей группе
487

4.12. Зависимость спонтанной частоты сердечных сокращений от уровня блокады проводящей системы сердца. 1 — ниже предсердно-желудочкового пучка; 2 — на его уровне; 3 — на уровне предсердно-желудочкового узла.
отнесены больные с выраженной, или «типичной», симптоматикой.
Больные жалуются на обмороки, потерю сознания, головокружение, боли в сердце, утомляемость, снижение работоспособности, ухудшение памяти (проявления недостаточности кровообращения или синдрома низкого сердечного выброса). Эта группа больных нуждается в электростимуляции, дополняемой при необходимости лекарственным лечением. Для таких больных физиологическая стимуляция является предпочтительной, поскольку проводимость в пред-сердно-желудочковом узле сохранена.
Клинические проявления при полной поперечной блокаде зависят от типа и длительности расстройств сердечной функции, а также от состояния мозгового кровообращения. Мозговая симптоматика может варьировать от легкого недомогания и головокружения, которые могут быть преходящими, до потери сознания с судорогами или без них. Последнее наблюдается при остановке желудочков или частоте сердечных сокращений менее 20 в минуту. Изредка наблюдается фибрилляция желудочков. Эта аритмия может быть самостоятельной или сочетаться с другими нарушениями сердечного ритма. Однако у больных с церебральным атеросклерозом блокада сердца с частотой менее 40 сердечных сокращений в минуту может сопровождаться клинической картиной мозговой недостаточности. Одновременно появляются симптомы сердечной недостаточности (быстрая утомляемость, одышка). При физикальном обследовании кардинальным признаком полной поперечной блокады сердца (кроме редкого ритма) является изменение интенсивности I тона. Он выслушивается лучше всего над верхушкой, а изменение его тональности связано с изменением соотношений в работе между предсердиями и желудочками. Часто выслушивается самостоятельный тон предсердий. Венозное давление повышено. Пульсация шейных вен не совпадает с сокращениями желудочков; появляются характерные «пушечные волны» на шее в случаях, когда волна Р попадет на ЭКГ в интервал QRST (это время, когда предсердие сокращается при закрытом трехстворчатом клапане).
Атриовентрикулярную блокаду классифицируют с учетом локализации и тяжести поражения. Так, I тип блокады относится к поражению самого узла, а II тип—к инфрано-дальному сегменту. Тяжесть блокады выражают в степенях: 1°, 2° или 3° (полная поперечная блокада). Наиболее значительно уровень поражения влияет на частоту сердечных сокращений. При блокаде I типа (блокада узла) число сокра-
щений сердца колеблется от 30 до 60. При блокаде II типа, если зона повреждения расположена в предсердно-желудоч-ковом пучке, число сокращений составляет 28—48 в минуту, а если ниже—от 4—5 до 40 (рис. 4.12).
Первая степень блокады протекает благоприятно и на ЭКГ характеризуется удлинением интервала Р—Q более 0,21 с, отсутствием сопутствующих поражений (блокады ножек).
При II степени блокады отмечается задержка проведения некоторых предсердных сокращений. На ЭКГ она может быть двух типов.
Тип I блокады Самойлова—Венкебаха или тип I Мобитца характеризуется нарастающим удлинением интервала Р— Q, в результате чего наступает блокада и волна Р появляется после комплекса QRS, а затем все повторяется. При типе II блокады Самойлова—Венкебаха или типе II Мобитца блокированной волне Р предшествует интервал Р— Q, который относительно постоянен (как и первый проходящий импульс после блокированного). Однако при типе II вероятность развития полной поперечной блокады выше, чем при типе I. Поэтому больным с блокадой типа II необходимо проводить интенсивную антиаритмическую терапию.
При III степени атриовентрикулярной блокады (полная поперечная блокада) определяется полная независимость активности предсердий и желудочков: предсердия сокращаются с частотой 60—100 в минуту, желудочки—20—50. Полная поперечная блокада может развиться и на фоне мерцания предсердий. Постоянная (хроническая) полная поперечная блокада может периодически прерываться возвращением синусового ритма с частотой предсердно-желудочкового проведения 1:1. При внезапном начале полной поперечной блокады возможна длительная желудочковая асистолия, предшествующая появлению очага желудочкового водителя ритма. В специальной литературе этот период называют «прогреванием» водителя ритма. Такой пароксиз-мальный эпизод, называемый синдромом Морганьи—Ада-мса—Стокса, представляет наибольший риск для больного, поскольку сопровождается головокружением, синкопе и внезапной смертью. Больной может быть сильно травмирован из-за падения в период синкопе. Еще более опасна фибрилляция желудочков из-за нестабильности миокарда. Поэтому наличие хотя бы одного приступа синкопе в анамнезе является показанием к имплантации стимулятора.
При приобретенной блокаде в 85% случаев имеют место нарушения внутрижелудочковой проводимости. При врожденной блокаде длительность и форма комплекса QRS не изменены. Иногда этот комплекс сохраняет нормальный вид. Широкий комплекс QRS при блокаде можно объяснить необычной локализацией водителя ритма, а также различными комбинациями блокады ножек предсердно-желудочкового пучка. Изменение в последующем конфигурации комплекса QRS у этих больных обычно связано с изменением места расположения водителя ритма. При врожденной блокаде водитель ритма локализован в предсердно-желу-дочковом пучке, поэтому комплекс QRS узкий (рис. 4.13).
Какова реальная угроза больному с полной поперечной блокадой и откуда она исходит? Самая большая опасность—это фибрилляция желудочков. Она может быть следствием нерегулярности желудочкового ритма, что зависит от многих причин. Нерегулярность ритма возникает тогда, когда положение водителя ритма неустойчиво, води-
482

Уровень блокады изображен сплошной линией, водитель ритма — кружочком. ПЖУ — предсердно-желудочковый узел; ЦФТ—центральное фиброзное тело; ПЖП—предсердно-желудочковый пучок; ЛН и ПН—левая и правая ножка предсердно-желудочкового пучка.
тель ритма перемещается из одного фокуса на другой, когда есть желудочковые экстрасистолы или имеется конкуренция двух или более водителей ритма. Подобная электрическая нестабильность отмечается при мерцательной аритмии с проведением отдельных наджелудочковых импульсов или после оживления больного в период приступа Морганьи— Адамса—Стокса с последующим развитием желудочковой тахикардии.
Показания к имплантации стимулятора. К имплантации электрокардиостимуляторов имеются ограниченные показания: 1) эпизодическая, частая или фиксированная атриовент-рикулярная блокада, сопровождающаяся эпизодами асистолии или желудочковой тахикардии; 2) слабость синусно-предсердного узла (дисфункция узла), проявляющаяся эпизодами синусовой брадикардии, остановки функции узла или наджелудочковой тахикардии. Все остальные показания не превышают 10% случаев имплантации стимуляторов.
Изменение подхода к лечению больных с полной поперечной блокадой хорошо известно. Если наблюдается полная поперечная блокада при обратимых состояниях (выраженная лекарственная интоксикация, инфаркт задней стенки миокарда и т. д.), то необходимо имплантировать кардиостимулятор, несмотря на отсутствие симптоматики. Напротив, при врожденных блокадах появление симптомов служит показанием к использованию искусственного водителя ритма, поскольку многие подобные больные длительно не предъявляют жалоб и ведут активный образ жизни. При брадиаритмической форме мерцания предсердий стимулятор имплантируют в том случае, если пауза превышает 3 с или если число сердечных сокращений постоянно менее 50 в минуту.
Дисфункция синусно-предсердного узла редко приводит к летальному исходу; полная поперечная блокада, наоборот, дает очень высокий процент летальности. Поэтому больным с дисфункцией синусно-предсердного узла стимулятор имплантируют в том случае, если появляется соответствующая симптоматика или нарушается нагнетательная функция сердца. Иногда больной не осознает клинических симптомов дисфункции, но их замечают окружающие. В этих случаях следует имплантировать электрокардиостимулятор.
Сложно однозначно ответить на вопрос о том, при какой
продолжительности паузы без сопутствующих признаков или симптомов следует проводить электрокардиостимуляцию. Обычно если была хотя бы одна пауза в 3 с и более, то стараются зафиксировать такую паузу еще несколько раз и затем имплантируют стимулятор. Вообще синусно-пред-сердный узел чувствителен ко многим лекарствам, особенно к бета-блокаторам, а также к дисбалансу электролитов. Поэтому, если имеются эпизоды остановки синусно-предсердного узла во время сопутствующего заболевания, следует повременить с имплантацией электрокардиостимулятора. Кроме того, бывает так, что нарушение баланса электролитов и обусловленную этим остановку синусно-предсердного узла не удается устранить лекарственными средствами и приходится прибегать к имплантации искусственного водителя ритма. Бессимптомная синусовая бради-кардия, особенно во время сна, даже если число сердечных сокращений уменьшается до 30 в минуту и/или сочетается с ускоренным желудочковым ритмом, не является показанием к имплантации электрокардиостимулятора.
Массаж области каротидного (сонного) синуса— это простой и быстрый способ получения ответа на интересующий вопрос. Сначала надо аускультативно и с помощью метода допплерографии убедиться в полной проходимости сонной артерии, так как частичная окклюзия этого сосуда может привести к неврологическим расстройствам. Индуцированная пауза более чем 3 с или появление полной поперечной блокады может коррелировать с недиагностированным синкопе. Положительная проба на гиперчувствительность каротидного синуса у больных с характерными симптомами является показанием к имплантации электрокардиостимулятора. Больные с синусовой брадикардией при частоте сердечных сокращений более 40 в минуту, не сопровождающейся дальнейшим замедлением ритма или остановкой синусно-предсердного узла, обычно жалоб не предъявляют. Но это не правило. У некоторых людей при этой же частоте сердечных сокращений имеются признаки уменьшенного сердечного выброса, апатии, быстрой утомляемости и даже малая психическая симптоматика, обусловленная синусной брадикардией. Несмотря на то что у этих больных нет прямого риска для жизни, они нуждаются в имплантации электрокардиостимулятора.
483
Для выявления больных с неадекватной стимуляцией желудочков исключительно информативной является временная стимуляция предсердий. Желудочковая стимуляция даже при достаточной частоте сердечного ритма снижает сердечный выброс, создает обратные предсердно-желудочковые соотношения и вызывает появление неприятных ощущений «пушечных волн» на шее и в груди. Так как 2/3 больных с хронически редким синусовым ритмом испытывают дискомфорт от такой ретроградной проводимости, по-видимому, будут расширены показания к применению двухкамерных электрокардиостимуляторов. Надо помнить, однако, что ретроградная проводимость хорошо переносится даже тогда, когда антеградная проводимость частично или полностью нарушена. Состояние антеградной проводимости по ЭКГ не позволяет однозначно оценить ретроградную проводимость. Если у больного часто появляются эпизоды остановки синусно-предсердного узла, то при сохранности ат-риовентрикулярной проводимости следует подумать о необходимости искусственной ЭКС из предсердия. Если это не удается и необходима желудочковая стимуляция, то ЭКС проводят на том же ритме, который защищает от асистолии и синкопе, но в обьином состоянии подавлен.
Больные с атриовентрикулярной блокадой I степени обычно не нуждаются в специальном лечении.
Больные с блокадой II типа, или типа II Мобитца, нуждаются в электростимуляции, даже если отсутствует клиническая симптоматика. Однозначно не определена тактика у больных с бифасцикулярной блокадой (двусторонняя блокада ножек предсердно-желудочкового пучка). По-видимому, больные с бифасцикулярной блокадой, у которых нет неврологической симптоматики, но есть клинические признаки, позволяющие заподозрить высокий риск развития фибрилляции или внезапной смерти, и у них документируется высокая степень блокады одним из нижеперечисленных методов: холтеровское мониторирование, проба с физической нагрузкой и гисография, при которой интервал Н— К^70 с, нуждаются в имплантации стимулятора.
Показанием к имплантации является симптоматика, а не гисограмма. Для больных с синдромом Морганьи—Адам-са—Стокса электрокардиостимуляция является методом выбора.
Электрическая стимуляция сердца. Электрокардиостимуляция—выдающееся достижение человечества второй половины XX в. В настоящее время в мире ежегодно имплантируется до 300000 стимуляторов. Причем выполненная своевременно, по строгим показаниям, с учетом особенностей уровня поражения проводящей системы электрическая стимуляция позволяет больному вернуться к социально полноценному образу жизни.
Впервые идею искусственного водителя ритма реализовал Hyman в 1930 г. Аппарат был использован для стимуляции предсердия и запускался рукояткой магнитогенератора с прерывателем. Прибор был передвижным и использовался у постели больного. В 1950—1951 гг. W. Bigelow разработал электрокардиостимулятор для увеличения частоты сокращений сердца под гипотермией. В 1952 г. P. Zoll убедительно продемонстрировал клинические возможности электрической стимуляции у больных с полной поперечной блокадой сердца. Стимуляция осуществлялась непосредственно через грудную клетку. Интерес хирургов к этой проблеме резко возрос в связи с развитием проблемы «открытого» сердца и возникновением такого осложнения, как полная поперечная блокада при операциях по поводу приобретенных поро-
ков сердца. С. Lillchei (1963) показал, что прямую стимуляцию сердца можно осуществлять электродом, имплантируемым в желудочек. Однако длительная стимуляция оказалась невозможной из-за инфицирования электрода.
В 1958 г. S. Furman впервые использовал метод чрезвеноз-ной стимуляции сердца от громоздкого устройства, работавшего от электрической сети. Электрод проводился через верхнюю полую вену и устанавливался в основание правого желудочка. Таким образом, был разработан простейший метод электрокардиостимуляции. В 1959 г. P. Senning, а в 1960 г. W. Chardack описали полностью имплантируемые электрокардиостимуляторы. Таким образом, появились исключительно благоприятные условия для развития электрокардиостимуляции. Однако только в 1970 г. были созданы герметичные аппараты, а позже литиевые батареи со сроком работы 7—10 лет, что позволило приступить к массовому выпуску надежных и долговечных устройств.
4.3.1. НОМЕНКЛАТУРА И СОВРЕМЕННАЯ ТЕХНОЛОГИЯ ЭКС
В международной практике используется 5-буквенный номенклатурный код, который представляет собой современную разработку рабочих групп Североамериканского общества по стимуляции и электрофизиологии (NASPE) и Британской группы по стимуляции и электрофизиологии (BPEG) и известен как общий код NBG-NASPE/BPEG (табл. 4.1). Как правило, используют первые 3 буквы, а букву R (IV позиция)—для программируемых ЭКС с изменяющейся частотой ритмовождения—VVIR, DDDR (адаптация по частоте). Буква V в коде NBG связана с антитахикардическими функциями.
Исходя из понимания исключительной важности наличия номенклатурных документов, относящихся к разработке показаний к имплантации ЭКС и выбору типа и режима ритмовождения, для кардиологов и кардиохирургов, рабочая группа (комиссия по брадиаритмиям) Комитета экспертов Минздравмедпрома Российской Федерации и Российской АМН по имплантируемым антиаритмическим устройствам и электрофизиологии (КОМЭКСА) утвердила рекомендации для имплантации ЭКС при брадикардиях [Бокерия Л. А. и др., 1994].
Первые модели ЭКС работали в асинхронном режиме (VO0) и проводили стимуляцию с фиксированной частотой. В 1965 г. появились первые модели ЭКС, способные определять собственную деятельность сердца и работать в режиме demand, т. е. «по требованию» (VVI). Мультипрограммные стимуляторы обеспечили широкий набор характеристик, необходимых для изменения электрических параметров ЭКС при изменяющемся взаимодействии мышцы сердца и самого ЭКС. Следующее поколение стимуляторов обеспечило физиологический характер электрокардиостимуляции (режимы VAT, VDD, AAI и DDD) путем автоматического контроля частоты и(или) увеличения степени наполнения желудочков сердца за счет синхронного сокращения предсердий (вклад предсердий). Физиологическая стимуляция нормализует сердечный выброс и значительно увеличивает функциональные возможности пациента. Интересно, что первый клинический опыт применения физиологических стимуляторов относится к 1962 г., когда пытались использовать Р-синхронизирован-ные ЭКС. Однако бывшие тогда в наличии и работавшие в режиме VAT стимуляторы не обладали способностью определять желудочковую активность. Поэтому желудочковая экстрасистола вполне могла привести к желудочковой
484
Таблица 4.1. Единый код ЭКС—номенклатура NBG-NASPE/BPEG

стимуляции в уязвимый период. Для исключения возможных проблем, связанных со стимуляцией в режиме VAT, были созданы более совершенные ЭКС, работающие в режиме VDD.
Недостатком такого режима стимуляции является отсутствие возможности стимуляции предсердий при отсутствии предсердной активности, что исключает положительный фактор предсердно-желудочковой синхронизации. В настоящее время наиболее совершенная система стимуляции— это полностью автоматизированная электростимуляция сердца в режиме DDD, позволяющая сохранить предсердно-желудочковую синхронизацию при урежении ритма сердца ниже установленного предела. Однако и этот режим недостаточен при хронотропной недостаточности миокарда. Примером является слабость синусового узла, когда не отмечается спонтанного учащения сердечного ритма в ответ на физиологическую нагрузку. Только включение в электронную систему ЭКС специальных детекторов (сенсоров), реагирующих на различные сигналы, отличные от Р-волны и увеличивающие соответственно частоту, оптимизирует физиологическую стимуляцию.
В настоящее время ряд зарубежных фирм использует сенсоры, реагирующие на нагрузку (механические сотрясения) («Medtronic», «Siemens-Elema»), частоту дыхания и минутный объем дыхания («Telectronics», «Biotec»), коэффициент dp/dt правого желудочка («Medtronic») и изменение температуры центральной венозной крови («Biotronik»), вызванный интервал Q—T («Vitatron») и другие параметры. В самое последнее время появились ЭКС, имеющие по два сенсора в одном устройстве («Topaz» фирмы «Vitatron»), что позволяет нивелировать недостатки односенсорного ЭКС. Новымв этом направлении стало использование сочетания функции адаптации по частоте с двухкамерным (секвенциальным) режимом стимуляции. Комбинация сенсора, работающего по нагрузке и позволяющего быстро достичь оптимальной частоты, и включение второго сенсора, работающего поинтервалу Q—Т или минутному объему вентиляции (при продолжении нагрузки или в фазе восстановления), позволя-
ют добиться оптимума частоты ритма в любую фазу нагрузки.
Самые последние разработки ЭКС, работающих в режиме DDDR, способны определять наличие у больного мерцания и трепетания предсердий и автоматически переключаться на другой, безопасный и тоже частотно-адаптируемый (желудочковый) режим стимуляции (WIR). Таким образом, исключается возможность поддержания наджелудочковой та-хиаритмии.
Рекомендации рабочей группы АНА/АСС включают 3 класса показаний к имплантации ЭКС: класс I—условия, при которых существует единое мнение о необходимости обязательной имплантации ЭКС; классII—условия, при которых часто имплантируют ЭКС, но существует ряд разногласий относительно необходимости их имплантации; классIII—условия, при которых существует единое мнение об отсутствии необходимости имплантации ЭКС. Усовершенствованные рекомендации рабочей группы АНА/АССприняты за основу нашей комиссией, за исключением рекомендаций к имплантации ЭКС при изолированной хронической предсердно-желудочковой блокаде II и III степеней, даже асимптомной, так же как и при блокаде II степени (Мобитца I), возникающей неоднократно в течение дня и ночи. Аналогичный подход характерен для большинстваевропейских групп.
Мы суммировали рекомендации, предложенные рабочей группой АНА/АСС и рядом европейских рабочих групп по электрокардиостимуляции, согласно шести основным категориям: I. Приобретенная предсердно-желудочковая (атрио-вентрикулярная—АВ) блокада у взрослых, включая блокаду, развившуюся в результате операции на сердце или искусственно созданную для лечения тахиаритмии;II. АВ-блока-да после инфаркта миокарда; III. Хроническая би- и трифас-цикулярная блокада; IV. Дисфункция синусно-предсердного узла (СПУ);V. Синдром повышенной чувствительности ка-ротидного синуса и нейрососудистые синдромы; VI. Электрокардиостимуляция при брадиаритмиях у детей, включаябрадиаритмии после операции на сердце.
485
4.3.1.1. Показания к имплантации ЭКС
I. Приобретенная предсердно-желудочковая блокада
у взрослых.
Класс I (абсолютные показания):
1а. ППБ сердца любой анатомической локализации, постоянная или преходящая с клиническими проявлениями симптоматической брадикардии (головокружение, обмороки, сердечная недостаточность и др.).
16. ППБ сердца с эктопическими ритмами или другими условиями, которые требуют применения препаратов, подавляющих автоматизм спонтанных водителей ритма, и приводят в результате к симптомной брадикардии.
1в. ППБ сердца с периодами асистолии более 3 с или выскальзывающим ритмом менее 40 в минуту, даже если ППБ бессимптомная.
1г. ППБ сердца после аблации предсердно-желудочково-го соединения и в случае миотонической дистрофии.
Симптомная брадикардия при АВ-блокаде II степени, постоянная или перемежающаяся, вне зависимости от типа или анатомического места блокады.
Фибрилляция предсердий, или трепетание предсердий, или редкие случаи наджелудочковой тахикардии, сочетаю щиеся с АВ-блокадой и симптомной брадикардией.
Асимптомная АВ-блокада II степени (Мобитца I или II) или III степени, постоянная или перемежающаяся, на уровне или ниже пучка 1иса (по данным гисографии).
Класс II (относительные показания):
1. Асимптомная ППБ сердца, постоянная или перемежа ющаяся, выше уровня пучка Гиса с числом сокращений желудочков более 40 в минуту.
2. Симптомная изолированная АВ-блокада I степени. Класс III (противопоказания):
Асимптомная изолированная блокада I степени.
Асимптомная АВ-блокада II степени выше пучка Гиса.
II. Инфаркт миокарда. Класс I:
Устойчивая АВ-блокада II степени или ППБ сердца, возникшая после инфаркта миокарда с блокадой в системе Гиса—Пуркинье.
Преходящая возникшая АВ-блокада и сочетающаяся блокада ножек пучка Пгса.
Класс II:
1. Устойчивая АВ-блокада, возникшая в АВ-узле.
Класс III:
Преходящие нарушения АВ-проведения при отсутствии дефектов внутрижелудочкового проведения.
Преходящая АВ-блокада с преходящей блокадой пе редней ветви левой ножки пучка Гиса (БПВЛНПГ).
Приобретенная БПВЛНПГ при отсутствии АВ-блока- ды.
Устойчивая АВ-блокада I степени при наличии блокады ножек пучка Гиса, которая не проявлялась ранее.
III. Би- и трифасцикулярная блокада. Класс I:
Симптомная брадикардия, сочетающаяся с бифасцику- лярной блокадой с перемежающейся ППБ сердца.
Би- и трифасцикулярная блокада с перемежающейся блокадой II степени без клинических проявлений симптом ной брадикардии.
Чередующаяся блокада ножек пучка 1иса.
Индуцированная стимуляцией АВ-блокада с анатоми ческой локализацией ниже уровня пучка Гиса.
Класс II:
1. Обморочные состояния (синкопе), не доказанные тем, что они обусловлены ППБ сердца у больных с би- и трифас- цикулярной блокадой, когда другие причины синкопе удает ся идентифицировать.
2. Значительное удлинение интервала Н— V (> 100 мс). Класс III:
Блокада ножки пучка Гиса без АВ-блокады или клини ческих симптомов.
Блокада ножек пучка Гиса с АВ-блокадой I степени без клинических симптомов.
IV. Синдром слабости синусового узла. Класс I:
1. Документированная симптомная брадикардия на фоне приема кардиотропных препаратов или без их приема.
Класс II:
1. Недостаточно документированная связь между клиническими симптомами и брадикардией у больных с синдромом слабости синусового узла и спонтанным или обязательным приемом кардиотропных препаратов (частота сердечных сокращений менее 40 в минуту).
Класс III:
Асимптомная синусовая брадикардия, включая боль ных, у которых выраженная брадикардия (частота сердеч ных сокращений менее 40 в минуту) обусловлена длитель ным приемом кардиотропных препаратов.
Дисфункция синусового узла с документированной бра дикардией, которая не является причиной клинических про явлений симптомов брадикардии.
V. Синдром повышенной чувствительности каротидного синуса и нейрососудистые синдромы.
Класс I:
1. Повторяющиеся обмороки, вызванные воздействием на область каротидного синуса (минимальное давление на область каротидного синуса вызывает асистолию более 3 с в случае, если не введены какие-либо препараты, которые подавляют функцию СПУ и АВ-узла).
Класс II:
Повторяющиеся обмороки без явных провоцирующих факторов, но у пациентов с гиперчувствительной реакцией сердечно-сосудистой системы.
Обмороки, обусловленные брадикардией, воспроизво димой откидыванием головы вверх с введением или без введения изопротеренола (или других провоцирующих фак торов), при которых временная электрокардиостимуляция сердца и повторное проведение провоцирующих тестов мо гут установить показания к имплантации постоянного ЭКС.
Класс III:
Гиперчувствительная реакция сердечно-сосудистой сис темы при стимуляции области каротидного синуса, но без клинических проявлений.
Отсутствие явных клинических симптомов при гиперчув ствительности каротидного синуса в ответ на стимуляцию области каротидного синуса.
Повторяющиеся обмороки или менее выраженные кли нические симптомы на фоне отсутствия признаков гиперчув ствительности каротидного синуса.
486
Одним из важных обстоятельств при определении показаний к имплантации ЭКС является соотнесение клинических симптомов с брадикардией. Симптоматическая брадикар-дия, имеющая клинические симптомы, связанные с редким ритмом, проявляется головокружением, предобморочным состоянием или обмороками (пресинкопе или синкопе), резким снижением толерантности к физической нагрузке или застойной сердечной недостаточностью.
Мы суммировали общепринятые показания к обязательной имплантации ЭКС при брадикардиях (класс I), относительные показания или однозначно неопределенные показания к постоянной электростимуляции сердца (класс II) и представили противопоказания к постоянной электрокардиостимуляции (класс III).
Далее нам представляется необходимым дать ряд комментариев по каждой из 6 категорий, которые определены как основные при разработке рекомендаций к постоянной электрокардиостимуляции.
I. Стимуляция при приобретенной АВ-блокаде у взрослых
При наличии клинических проявлений симптоматичной брадикардии, связанных с АВ-блокадой, показана постоянная электрокардиостимуляция независимо от уровня блокады (ниже или выше пучка Гйса). Это увеличивает продолжительность жизни больных с ППБ и обмороками. Нет доказательств увеличения продолжительности жизни у пациентов с АВ-блокадой I степени. Прогноз при АВ-блокаде II степени с периодами Самойлова—Венкеаха, обусловленной нарушениями проведения в АВ-узле, и прогноз только при данной форме АВ-блокады, как правило, благоприятный. При блокаде II степени (типа Мобитца), обусловленной нарушениями проведения в пучке Гиса или ниже него, прогноз неясный; отмечаются тенденция к развитию ППБ и частые клинические проявления симптомов брадикардии. Даже «асимптомным пациентам» с нарушениями проведения импульса в области пуча Гйса или ниже него необходимо имплантировать ЭКС.
П. Стимуляция при АВ-блокаде и инфаркте миокарда Прогноз у больных данной группы в основном зависит от величины некроза миокарда, степени дисфункции левого желудочка и характера нарушений проведения во внутриже-лудочковой части проводящей системы сердца, а не от АВ-блокады как таковой. Временная электростимуляция сердца, к которой часто прибегают врачи, не означает, что больному обязательно будет имплантирован ЭКС. Пациенты с постоянной АВ-блокадой I степени и блокадой ножек пучка Гиса, которая не была документирована до развития инфар-гга миокарда, не нуждаются в имплантации ЭКС. Постоянная электрокардиостимуляция больным инфарктом миокарда, у которых повреждение проводящей системы возникло в результате инфаркта миокарда, является, таким образом, отсроченной, а режим стимуляции определяется клиническими проявлениями.
III. Стимуляция при хронической би- и трифасцикулярной блокаде
В ряде исследований было показано, что симптомная АВ-блокада у больных с двух- и трехпучковой блокадой с типичной клинической картиной характеризуется высокой смертностью, в том числе высоким риском внезапной смерти. Поэтому наличие обмороков у больных с двух- и трехпуч-ковой блокадой должно служить показанием к имплантации ЭКС. Альтернирующая блокада ножек пучка Пгса является показателем нарушения проведения в обеих ножках и также служит показанием к постоянной электрокардиостимуляции. В настоящее время не найдено клинических, электрокардиографических или электрофизиологических критериев, идентифицирующих пациентов высокого риска в группе больных с блокадой ножек пучка Гйса. Вместе с тем не выявлено и достоверной корреляции между величиной
интервалов Р—R и Н—V и вероятностью развития ППБ и внезапной смерти. Значение интервала Н—К>100 мс у «асимптомных пациентов» является показанием к имплантации ЭКС, так как увеличение интервала Я— V, как правило, сочетается с основным заболеванием мышцы сердца, а следовательно, и с высоким риском внезапной смерти.
Проведение чреспищеводной или эндокардиальной стимуляции предсердий также позволяет выявить нарушения проведения в дистальном отделе пучка Гйса и определить показания к постоянной электрокардиостимуляции.
IV. Стимуляция при дисфункции СПУ
Дисфункция СПУ включает синусовую брадикардию, остановку СПУ, синусно-предсердную блокаду, синдром тахи-брадикардии. Важно документировать связь клинических симптомов с одной из форм дисфункции СПУ, так как симптомы, как правило, преходящи. У спортсменов повышенный тонус блуждающего нерва может обусловить развитие преходящей, но выраженной брадикардии либо даже асистолии с длительностью до 2,8 с. У пациентов с остановкой СПУ и синдромом тахи-брадикардии прогноз менее благоприятный, чем у больных с изолированной синусовой брадикардией. Наличие синдрома тахи-брадикардии часто является показанием к электростимуляции сердца, особенно если пациент нуждается в приеме антиаритмических препаратов в связи с пароксизмальной тахиаритмией.
У пациентов с дисфункцией СПУ предсердная и бифокальная стимуляция сердца увеличивает продолжительность жизни. При изолированной дисфункции СПУ достаточно имплантации предсердного электрода и стимуляции в режиме AAI. В случае предполагаемых нарушений АВ-проведе-ния, в том числе при приеме антиаритмических препаратов для достижения нормосистолии у больных с фибрилляцией и трепетанием предсердий, используют в первом случае бифокальную стимуляцию (DDD), а во втором—желудочковую частотно-адаптируемую (VVIR).
V. Стимуляция при повышенной чувствительности каро- тидного синуса и нейрососудистых синдромах
Синдром повышенной чувствительности каротидного синуса (синдром каротидного синуса) проявляется выраженной рефлекторной реакцией при воздействии на область каротидного синуса. Он характеризуется остановкой СПУ и(или) асистолией, когда развивается АВ-блокада длительностью более 3 с и(или) отмечается клинически значимое снижение артериального давления. Постоянная электрокардиостимуляция показана этим больным, несмотря на то что она устраняет только брадиаритмический компонент данного синдрома. Урежение ритма или асистолия может быть эффективно предотвращена методом постоянной электрокардиостимуляции. Оптимальным является режим DDI, особенно в сочетании с гистерезисом по частоте. Электрокардиостимуляция не показана пожилым больным и пациентам, длительно принимающим гликозиды. У таких больных незначительное воздействие на область каротидного синуса может вызвать значительные изменения частоты сердечных сокращений и артериального давления.
VI. Электрокардиостимуляция у детей
Показания к постоянной электрокардиостимуляции у детей соответствуют таковым у взрослых с той существенной оговоркой, что у детей необходима еще более уточненная диагностика клинических проявлений (симптомов). Следует шире пользоваться холтеровским мониторированием и электрофизиологическим исследованием брадикардии. Наиболее часто показанием к имплантации ЭКС у детей служит синдром тахи-брадикардии, особенно если прием антиаритмических препаратов является обязательным. Частота этого синдрома в последние годы возросла в связи с широким внедрением в клиническую практику операций в областях, прилегающих к СПУ (операции по методу Сен-нинга или Мастарда при транспозиции крупных сосудов, операции по методу Фонтена при атрезии трехстворчатого клапана, единственном желудочке).
При АВ-блокадах у детей следует стремиться к бифокальной стимуляции, чтобы сохранить синергизм функций пред-
487
сердий и желудочков. Это особенно важно при нормальных размерах желудочков.
Необходимо еще раз подчеркнуть, что приведенные рекомендации с учетом рекомендаций ряда рабочих групп Европы и Северной Америки будут совершенствоваться и в будущем. Изменение показаний будет формироваться при появлении новых поколений ЭКС, а также данных об отдаленных результатах их использования, продолжительности и качестве жизни пациентов. Важно помнить, что у постели больного окончательное решение принимает врач, и задача состоит в том, чтобы он руководствовался общепринятыми критериями для имплантации постоянных водителей ритма.
4.3.1.2. Выбор режима электрокардиостимуляции
После принятия решения о необходимости имплантации ЭКС следующим шагом является выбор режима электростимуляции, а следовательно, типа ЭКС. В табл. 4.2 представлены основные характеристики различных режимов стимуляции.
DDDR-стимуляторы—наиболее совершенные универсальные стимуляторы, которые позволяют добиться оптимального режима стимуляции, в том числе с режимом адаптации по частоте, как в зависимости от активности предсердий (хронотропный фактор предсердий), так и независимо от нее. Предлагаемые алгоритмы стимуляции являются оптимальными и, возможно, идеальными на сегодняшний день. Стоимость ЭКС, возможности их выбора в той или иной стране мира, необходимость в сохранении физической активности или строгий постельный режим в связи с основным заболеванием в значительной степени влияют на выбор режима и типа ЭКС.
Таблица 4.2. Характеристика различных режимов электрокардиостимуляции
|
|
|
Активация |
Зависимая |
Независя- |
|
Режим электро- |
|
желудочков |
от актив- |
щая от ак- |
|
кардиостимуля- |
АВ-синхро- |
через нор- |
ности пред- |
тивности |
|
ции |
низация |
мальную |
сердий час- |
предсердий |
|
|
|
проводя- |
тотная |
частотная |
|
|
|
щую систему |
адаптация |
адаптация |
|
AAI |
+ |
+ |
_ |
|
|
VVI |
|
|
|
|
|
AAIR |
+ |
+ |
|
+ |
|
VVIR |
|
— |
_ |
+ |
|
VAT/DDI |
± |
± |
— |
— |
|
DDIR |
± |
+ |
— |
+ |
|
DDD |
+ |
± |
+ |
_ |
|
DDDR |
+ |
+ |
+ |
+ |
Нарушения АВ-проведення. ППБ сердца остается основным показанием к постоянной электрокардиостимуляции(режим WI) в нашей стране. На схеме 4.1 представлен алгоритм выбора режима электростимуляции сердца при ППБ. При наличии хронической формы фибрилляции предсердий или остановки предсердий используется обычно режим WI. Если спонтанный (выскальзывающий) ритм не учащается при нагрузке, предпочтение отдают стимуляции с адаптацией по частоте—WIR.
СХЕМА 4.1. ВЫБОР РЕЖИМА ЭЛЕКТРОКАРДИОСТИМУЛЯЦИИ ПРИ ПОЛНОЙ ПОПЕРЕЧНОЙ БЛОКАДЕ

Наличие синусового или предсердного ритма с адекватной хронотропной реакцией при необходимости AV-синхрониза-ции позволяет использовать электрокардиостимуляцию в режиме VDD. В этом случае имплантируют один эндокар-диальный электрод, который позволяет провести стимуляцию желудочков и полноценно определять электрическую активность предсердий. РежимDDDRрекомендован присочетании ППБ и дисфункции СПУ, когда синусовый узел не отвечает адекватно частоте сердечных сокращений в ответ на метаболические потребности организма или имеется хро-нотропная недостаточность.
Дисфункция СПУ. При дисфункции СПУ должна проводиться стимуляция предсердия, так как хорошо известныосложнения, обусловленные развитием пейсмекерного синдрома (более чем у 30% больных) при стимуляции в режиме VVI, так же как и рост числа тромбоэмболических осложнений и развитие хронической формы фибрилляции предсердий. На схеме 4.2 представлен алгоритм для выбора оптимального режима электростимуляции сердца при дисфункции СПУ.
В случае хронической мерцательной аритмии или асистолии предсердий показан режим WI или WIR. При бради-кардии и остановке СПУ необходимо проведение физиологической электрокардиостимуляции. При нормальной функции АВ-узла (точка Венкебаха>140 в минуту) рекомендуется предсердная стимуляция, так как развитие АВ-блока-ды не превышает 5—8% в сроки наблюдения более 3 лет. Если необходима стимуляция в режимеDDD, то желательно использовать стимуляторы, имеющие функцию гистере-
488
СХЕМА 4.2. ВЫБОР РЕЖИМА ЭЛЕКТРОКАРДИОСТИМУЛЯЦИИ ПРИ ДИСФУНКЦИИ СПУ

Хронотропная недостаточность. Под термином «хронотропная недостаточность» обычно понимают неадекватный ответ СПУ или (в случае ППБ) водителей ритма из нижележащих отделов проводящей системы сердца в ответ на нагрузку или другие метаболические потребности организма. Исследования последних лет показали, что 40% пациентов с имплантированными ЭКС испытывают в определенной степени хронотропную недостаточность и нуждаются в физиологической, в частности частотно-адаптируемой, электрокардиостимуляции. Пока еще нет однозначного ответа на вопрос, уменьшает или нет частоту развития пред-сердных тахиаритмии стимуляция в режиме AAIR или DDDR. Вероятно, на фоне приема антиаритмических препа-
ратов данная проблема может иметь положительное решение. Однако только анализ отдаленных результатов, полученных на большой группе больных, позволит провести сравнительный анализ режимов DDD и DDDR электрокардиостимуляции и их влияния на частоту возникновения предсердных тахиаритмии.
Рефлекторно обусловленные вазомоторные обмороки. На схеме 4.3 представлен алгоритм решения при выборе режима электрокардиостимуляции при вазовагальных (нейросо-судистых) обмороках и синдроме каротидного синуса. Ясно, что только больных с кардиоингибирующими формами данного синдрома можно эффективно лечить методом электростимуляции. Около 70% больных с синдромом каротидного синуса могут иметь рефлекторную АВ-блокаду. Поэтому наряду со стимуляцией в режиме WI все большему числу больных имплантируют DDD-стимуляторы. В ряде случаев при сочетании вазомоторных (вазодилатационных) форм обмороков, когда отмечают кардиоингибиторный элемент, эффективность электрокардиостимуляции будет определяться степенью преобладания того или иного компонента вазомоторного обморочного состояния.
Необходимо подчеркнуть, что при выборе режима стимуляции следует учитывать индивидуальность каждого больного. Ясно, что в схему нельзя включить все клинические ситуации, но основные правила при выборе режимов постоянной электрокардиостимуляции должны быть соблюдены. Соблюдение приведенных ниже принципов позволит до-
489
СХЕМА 4.3. ВЫБОР РЕЖИМА ЭЛЕКТРОКАРДИОСТИ
МУЛЯЦИИ ПРИ РЕФЛЕКТОРНО ОБУСЛОВЛЕННЫХ
ОБМОРОКАХ

биться оптимального режима электрокардиостимуляции сердца.
Стимуляция предсердия и определение его активности крайне важны, если сохранена активность СПУ.
WI и VVIR являются режимами выбора у больных с хронической фибрилляцией и остановкой («молчание») предсердий.
При хронотропной недостаточности миокарда показан режим стимуляции с адаптацией по частоте.
«Синдром кардиостимулятора» и «тахикардия кардио стимулятора» могут быть в большинстве случаев устранены специальным режимом электростимуляции.
Наиболее простой режим—VVI—в основном реко мендуют больным с низкой физической активностью, при болезни, приковывающей пациента к постели, при отсутст вии необходимости в частом включении ЭКС.
Имплантация ЭКС наряду с купированием симптомов брадиаритмии должна способствовать улучшению качества и продолжительности жизни.
После ознакомления с рекомендациями относительно постоянной электрокардиостимуляции при брадиаритмиях и выбора оптимального ее режима важно решить основной вопрос: как применить предлагаемые рекомендации к каждому конкретному больному?
До принятия решения об имплантации постоянного ЭКС и выбора режима электростимуляции необходимо обязательно установить причинную связь клинических симптомов с документированной брадиаритмией, а также определить: 1) место нарушения проведения и(или) формирования импульса; 2) надежность и гемодинамическую эффективность
спонтанного (выскальзывающего) ритма; 3) наличие или отсутствие хронотропной недостаточности; 4) наличие или отсутствие наджелудочковых тахиаритмий.
Правильно собранный анамнез, функциональные методы исследования, ЭКГ в 12 отведениях, холтеровское монито-рирование, нагрузочные и медикаментозные пробы как не-инвазивные методы исследования позволяют почти всегда ответить на поставленные вопросы. В частности, неинвазив-ные методы исследований в ряде случаев помогают установить область АВ-блокады (табл. 4.3). Необходимо иметь в виду, что только чреспищеводное или инвазивное электрофизиологическое исследование может выявить причину преходящих клинических симптомов, предположительно связанных с брадиаритмиями (это особенно справедливо для случаев дисфункции СПУ, когда методом мониторирования не удается зарегистрировать их причинную связь); исключить тахиаритмий как причину симптомов; выбрать оптимальный режим электрокардиостимуляции (оценив функцию СПУ и АВ-проведения).
Та б л и ц а 4.3. Неинвазивная дифференциальная диагностика интранодальной и инфранодальной АВ-блокады
|
Условие исследования |
АВ-проведение при АВ-блокаде | |
|
интранодальной |
инфранодальной | |
|
Нагрузка Изопротеренол [1—3 мкгДкг • мин) ] Атропин (1—2 мг) Вагусные пробы |
Улучшается Ухудшается |
Может ухудшиться Не изменяется или парадоксально улучшается |
Активный образ жизни. Стимулятор, воспринимающий импульс предсердия и стимулирующий желудочек, целесообразен для больных, привыкших к активному образу жизни. Предсердно-желудочковый секвенциальный стимулятор осуществляет предсердно-желудочковую синхронизацию, но не увеличивает частоту сердечных сокращений при физической нагрузке (рис. 4.14, 4.15).
Новые предсердные стимуляторы позволяют увеличить число сокращений желудочков до 150—175 в минуту в ответ на спонтанное учащение ритма предсердий. Врач выбирает один из верхних пределов пульса в зависимости от образа жизни больного.
Ранее, когда число предсердных сокращений превышало верхний предел устройства, ответ предсердной синхронизации переставал срабатывать, что приводило к значительному снижению числа сокращений желудочков. Новейшие конструкции ЭКС отвечают по типу феномена Самойлова— Венкебаха и сохраняют число сокращений На верхнем пределе или близко к нему. Такое число сокращений предсердий необходимо, чтобы исключить внезапное снижение «желудочкового ответа» у больных, занимающихся теннисом, бегом или плаванием.
Дисфункция миокарда. В настоящее время у больных с нарушением функции миокарда используются предсердно-же-лудочковые секвенциальные стимуляторы, а также предсер-
490


(200 мс), отсчитываемого от времени деполяризации предсердий (Si).
дные электрокардиостимуляторы. Функция миокарда может быть нарушена и у детей, и у взрослых. У детей функция миокарда изменена в результате операции на сердце при сложных пороках. У большой группы больных с дисфункцией синуснопредсердного узла, нарушением атриовентрику-лярной проводимости или при их сочетании дисфункция миокарда обусловлена пороком клапана, дефектом перегородки или повторными хирургическими вмешательствами.
В настоящее время благодаря внедрению неинвазивных методов уделяется больше внимания тому, насколько двухкамерный стимулятор улучшает «производительность» сердца у таких больных. Однако и ранее было известно, что при выраженной дисфункции двухкамерные стимуляторы малоэффективны. Необходимо выяснить, насколько синхронизация с предсердием благоприятна для таких больных, поскольку возрастает частота сокращений в ответ на изменение активности больного.
Снижение комплайенса сердца. У больных со сниженным комплайенсом сердца гемодинамика нередко улучшается при восстановлении функции предсердия. У больных с иди-опатическим гипертрофическим субаортальным стенозом и полной поперечной блокадой (последняя иногда развивается после операции иссечения подклапанного стеноза) стимуляция желудочков редко улучшает состояние. Она становится значительно лучше при восстановлении функции предсердия, поскольку резко возрастает сердечный выброс. Это возможно сделать с помощью бифокального электрокардиостимулятора. Аналогичное положение у больных и с другой патологией—гипертрофической кардиомиопатией, у которых гемодинамическое улучшение также достигается при физиологической и двухкамерной ЭКС.
«Пейсмекерный синдром». Синдром электрокардиостимулятора подробно описан нами в разделе осложнений. Он встречается чаще у взрослых, но наблюдается и у детей, несмотря на то что дети не замечают отрицательного действия электрокардиостимулятора (так называемые «пушечные волны» на шее). Взрослые больные, напротив, отмечают снижение давления, неприятные ощущения при растяжении яремных вен при желудочковой стимуляции, вплоть до синкопе. Двухкамерная стимуляция существенно улучшает состояние больных, хотя она, конечно, не является абсолютной гарантией устранения указанных симптомов.
Сопутствующие желудочковые или наджелудочковые аритмии. В педиатрической практике у больных со сниженной насосной функцией миокарда часто отмечается желудочковая экстрасистолия. Использование двухкамерных стимуляторов у этой категории больных часто приводит к купированию экстрасистолии. Вероятно, это связано с нормализацией продолжительности предсердно-желудочкового проведения и уменьшением комплайенса желудочка. Подавление сопутствующей желудочковой или наджелудочковой аритмии может стать важнейшим показанием к применению двухкамерного стимулятора. Показания к постоянной или долговременной электростимуляции у детей отличаются от показаний у взрослых.
При врожденной полной поперечной блокаде показанием к имплантированию электрокардиостимулятора детям служат: 1) обмороки или повторные головокружения; 2) выполнение операции по поводу сопутствующей патологии сердца; 3) застойная сердечная недостаточность, обусловленная медленным ритмом и не поддающаяся устранению лекарственной терапией; 4) низкий сердечный выброс во
497
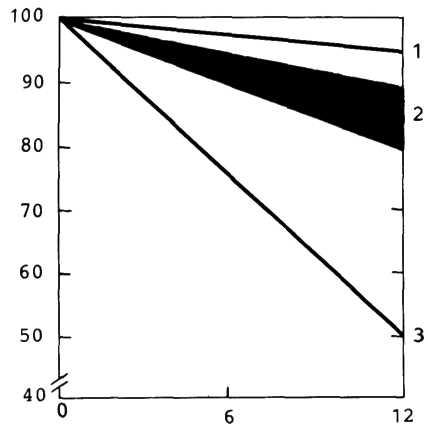
4.16. Актуарные кривые выживаемости здоровых (1) и больных с приобретенной (хронической) полной поперечной блокадой при хирургическом (2) и консервативном (3) лечении. По оси абсцисс — время наблюдения за больными в месяцах; по оси ординат — выживаемость в процентах.
время нагрузки, выявляемой при велоэргометрии; 5) широкий (более 0,8 с) комплекс QRS, в том числе у новорожденных с частым предсердным (более 140 в минуту) и редким желудочковым (менее 50 в минуту) ритмом в связи с неблагоприятным прогнозом естественного течения заболевания.
Операционная полная поперечная блокада является наиболее частым, хотя в ряде случаев и спорным показанием для постоянной ЭКС. Послеоперационная летальность без лечения в этой групле больных колеблется от 60 до 100%. Поэтому большинство авторов рекомендуют имплантировать стимулятор, если полная поперечная блокада, возникшая во время операции, сохраняется 2 нед, а суточное мони-торирование показывает, что частота сердечных сокращений не превышает 50 в минуту. Целесообразно также провести гисографию, которая подтвердит наличие блока на уровне предсердно-желудочкового пучка или дистальнее его.
Слабость синусно-предсердного узла часто возникает у детей после коррекции ВПС. Преходящие формы слабости узла у детей могут быть обусловлены влиянием кардиопле-гического раствора или манипуляциями вблизи него. Дисфункции, обусловленные названными причинами, могут пройти без последствий в ближайшие дни после операции. У больных с постоянной и выраженной формой слабости синусно-предсердного узла следует провести холтеровское мониторирование и электрофизиологическое исследование. Показанием к операции служат обморочные состояния, документированные случаи выраженной брадиаритмии.
Физиологическая стимуляция у детей предпочтительнее по многим причинам. Во-первых, поскольку им производят миокардиальную стимуляцию, то можно хорошо фиксировать предсердный электрод. Это имеет основное значение в надежной работе аппарата. У детей нет мерцания или трепетания предсердий, что также является благоприятным фактором. Во-вторых, сохранение нормального сердечного
выброса, достигаемое при физиологической стимуляции,— это важнейший фактор роста и развития ребенка. Такая стимуляция также служит эффективной мерой профилактики пейсмекерного синдрома.
Операция. Существуют два принципиально различных способа хирургического лечения. При закрытом способе электроды проводят через вену (под рентгенологическим контролем) и таким образом осуществляют эндокардиаль-ную стимуляцию. При открытом способе делают торакото-мию и электрод или электроды имплантируют в миокард. Эндокардиальный метод применяют у взрослых, миокар-диальный—у детей.
Для эндокардиальной стимуляции доступ к сердцу осуществляют через одну из трех вен: наружную, внутреннюю яремную вену или головную вену. В исключительных случаях, если облитерированы названные вены, пунктируют подключичную вену. После установления электрода определяют порог стимуляции. Затем имплантируют стимулятор в подключичной области и проверяют эффективность его работы.
Торакальный доступ к сердцу используется у детей. Оптимальным является левосторонний доступ в четвертом межреберье, позволяющий в условиях хорошо видимой поверхности левого желудочка фиксировать электрод. Многие авторы предпочитают подреберный (эпигастральный) доступ. При бифокальной стимуляции делают срединную стер-нотомию или правостороннюю торакотомию. При этом предсердный электрод укрепляют следующим образом: в межкавальном промежутке острым путем (1,5 см) разделяют жировой слой. После обнажения миокарда в последний ввинчивают электрод и дополнительно фиксируют П-образ-ным швом, восстанавливающим целостность эпикардиаль-ного жира. Желудочковый электрод фиксируют обычным способом.
Подкожное ложе должно быть достаточно точно рассчитано, чтобы исключить произвольное вращение стимулятора; оно должно быть дренировано в первые сутки после операции через катетер, проведенный в самостоятельный разрез, находящийся около основного разреза. Профилактически следует назначить терапию антибиотиками.
Мы придаем важное значение дооперационной нормализации гемодинамики. Эффективна дооперационная стимуляция через временный эндокардиальный электрод. Благодаря этому послеоперационный период протекает гладко. Эта стимуляция позволяет снять явления застойной сердечной недостаточности и таким образом выполнить операцию больному, хорошо подготовленному к ней. Временный электрод также позволяет поддержать оптимальную частоту сердечных сокращений в период основных манипуляций на сердце.
Выживаемость больных после имплантации электрокардиостимулятора. Хорошо известно, что прогноз у больных, которым электрокардиостимулятор имплантирован в связи с полной поперечной блокадой, хороший (рис. 4.16). Лишь только наличие ранее перенесенного инфаркта миокарда отражается на продолжительности жизни у этой группы больных. Если нет инфаркта миокарда или ИБС, больные с полной поперечной блокадой сердца после имплантации стимулятора живут в среднем 12 лет. К сожалению, такой прогноз не относится к больным, которым ЭКС проводится в связи с атриовентрикулярной блокадой II степени. Изложенное относится не только ко всей суммарной группе больных, но даже и к больным с блокадой II степени, не
492
перенесших инфаркт миокарда и не страдающих ИБС. Примерно 50% подобных больных умирают в течение 6 лет после имплантации стимулятора. Причиной ранней смерти является тяжелое поражение миокарда, как правило, некоро-нарогенного генеза.
Продолжительность жизни больных, которым электрокардиостимуляция проводилась в связи с нарушениями си-ноатриального проведения, включая больных с тахи-бради-синдромом, существенно не отличается от продолжительности жизни больных с полной поперечной блокадой. После установления электрокардиостимулятора она составляет 8—9 лет. Однако продолжительность жизни в этой популяции больных резко снижается, если имеется сопутствующая желудочковая тахикардия. Наличие такого осложнения, как желудочковая тахикардия, приводит к смерти 50% больных в течение одного года после имплантации стимулятора. Таким образом, сопутствующая желудочковая тахикардия при брадиаритмиях является более серьезным фактором снижения продолжительности жизни, чем возраст или коронарная болезнь.
В одной из работ последнего времени [Houser R. et al., 1983] эти выводы подтверждены наблюдениями за 968 больными в течение 18 лет. Сроки выживаемости составили среди больных с полной поперечной блокадой 11,8 года, с атриовентрикулярной блокадой II степени—6,3 года, с синусовой брадиаритмией—8,8 года (средние сроки по всей серии 8,9 года).
Факторами, снижающими продолжительность жизни, по степени важности являются желудочковая тахикардия, возраст при имплантации стимулятора, ранее перенесенный ннфаркт миокарда, застойная сердечная недостаточность, ; ВПС, хроническая почечная недостаточность.
Вопросы технического обеспечения ЭКС. Тестирование [ имплантированных систем. Наиболее эффективным I методом тестирования имплантированной системы является I использование анализатора электрокардиостимуляторов, Ёюторый искусственно воспроизводит функции восприятия и навязывания ритма электрокардиостимулятора. \, Измерение пороговой энергии стимуляции необ-■родимо для определения потенциала навязывания ритма на ■вкшице электрод—миокард. Электрическая энергия выходного устройства стимулятора, формирующая импульс боль-Вого, характеризуется двумя компонентами. Это компонент Клшвтуды (напряжение или ток) и компонент времени (ши-Кдо импульса, т. е. продолжительность). Порогом энергии Ешуляции считают то минимальное значение напряжения Нр тока, которое при заданной ширине импульса начинает ■^поляризацию сердца.
ИЬшример, имплантируемый электрод рассчитан на шири-^■импульса 0,5 мс и порог напряжения менее 0,5 в, если при Кой ширине импульса требуется порог напряжения более Щл, то этот вариант стимуляции желудочков считается неудовлетворительным. Предсердный «имплантат» со стан-Вцхгными электродами при ширине импульса 1 мс рассчи-Нрв на порог напряжения менее 1 в, порог более 2 в является «удовлетворительным. Низкий порог гарантирует соответствующую безопасность сохранения порога при посте-Квном и длительном контакте на границе электрод— ми-^■рд. Можно построить кривую сила—продолжительность проверкой повторных измерений порога, меняя ^Еину импульса. Сопротивление определяют показателем
отношения напряжения к силе тока. При этом напряжение должно быть близким к величинам на выходном устройстве электрокардиостимулятора. Так, расчетное сопротивление при 5 в должно быть в пределах 300—800 Ом.
Сигналы деполяризации сердца, волна Р или волна R проходят через соединение электрод—миокард, трансформируются в воспринимающем устройстве. Измерение амплитуды и частоты определяемых сигналов важно для того, чтобы подобрать оптимальный режим воспринимающего (сенсорного) устройства. Для измерения этих свойств используют калиброванные эндокардиальные электрограммы и анализаторы систем ЭКС. Амплитуда эндокардиального сигнала предсердия более 1,5 мв, а желудочка—4 мв достаточна для сенсорного устройства; сигнал длительно сохраняется, несмотря на изменение структуры эндокарда в месте имплантации электрода.
Анализаторы систем ЭКС способны определить соответствующие сигналы с эндокарда и воспроизвести их амплитуду. Калиброванная эндокардиальная электрограмма необходима тогда, когда анализатор не может определить сигнал. Однако обычно анализатор ЭКС и воспроизводит электрограмму, и анализирует ее.
Имплантация двухкамерных стимуляторов с использованием анализатора ЭКС дает идеальную возможность для анализа эндокардиальных сигналов каждой камеры, изучения атриовентрикулярной проводимости и ретроградной проводимости. Ретроградный анализ важен при использовании современных предсердно-синхронизированных стимуляторов (VAT, VDD, DDD), поскольку недостаточный учет ретроградной активности может привести к развитию тахи-аритмии, индуцированной стимулятором. Такое исследование невозможно провести в кабинете зондирования или в операционной, не снабженной электрофизиологическим оборудованием. Простейшая система тестирования двухкамерного электрокардиостимулятора может быть создана, если поставить временные электроды в предсердие и желудочек и через тестирующий кабель соединить их с анализатором работы электрокардиостимулятора и электрически изолированным монитором ЭКГ. Больной также должен быть электрически изолирован. Такое оборудование позволяет проводить стимуляцию одной камеры, запись и анализ электрограммы другой.
Таким образом, по мере разработки и внедрения новых уменьшенных и более современных стимуляторов и электродов снижаются препятствия к имплантации предсердных и двухкамерных стимуляторов. Эти преимущества существенным образом отражаются на хирургической технике и отдаленных результатах.
ЭКС зависит от способности стимулятора деполяризовать область вокруг головки электрода, которая была бы достаточной, чтобы начать деполяризацию всего сердца. Минимальный достаточный стимул, вызывающий сокращение сердца, называют порогом стимуляции. Он выражается в единицах напряжения тока или энергии. Порог стимуляции—феномен активный, а не статический и имеет определенные характеристики.
1. Продолжительность (длительность) импульса однонаправленно влияет на порог стимуляции и зависит от амплитуды тока: чем больше длительность, тем меньше ток и наоборот. Однако при уменьшении продолжительности импульса до 0,2—0,4 мс порог не создается
493
независимо от силы тока. Аналогично этому уменьшение силы тока ниже определенных значений (подпороговое) приводит к тому, что удлинение продолжительности импульса не приведет к деполяризации сердца. Возможности получения пороговых значений создаются при длительности импульса 0,5—2 мс. Поэтому во всех клинических стимуляторах эта величина колеблется от 0,6 до 2,7 мс.
Поверхность и конфигурация электрода имеет большое значение. Электроды с большой поверхно стью вызывают деполяризацию миокарда при меньших зна чениях силы тока, чем электроды с малой поверхностью. Соответственно этому сферические электроды обладают мак симальным по длительности постоянным порогом стимуля ции, цилиндрические—минимальным.
Контакт электрода с миокардом важен в том отношении, что порог стимуляции возрастает как функция расстояния между электродом и сокращающимся миокар дом. Увеличение этого расстояния возникает в результате воспаления в месте введения электрода (особенно сильно оно выражено на 5—10-й день). Порог стимуляции может возрастать в 10 раз. К 3—4 нед воспаление затихает, а порог стимуляции снижается до значений, превышающих истин ные (исходные) в 2—5 раз. Затем это значение длительно удерживается. При маленьких размерах электродов хрони ческий порог стимуляции значительно превышает этот пока затель в остром периоде. Аналогично этому увеличение продолжительности импульса приводит к уменьшению со отношения между порогом постоянной и временной стиму ляции, несмотря на то что чем короче импульс, тем эконом нее потребление энергии питания.
Анодная стимуляция потребляет энергии в 16 раз больше, чем стимуляция от катода. Поэтому в настоящее время все стимуляторы осуществляют катодную деполяризацию миокарда. Более того, анод на сердце может вызывать его фибрилляцию, что неоднократно наблюдалось при биполярной стимуляции, когда оба электрода имплан тировали в миокард.
Следует избегать монофазной стимуляции, так как в месте приложения развивается выраженный фиброз, кото рый не наблюдается при двухфазном импульсе. Все совре менные стимуляторы используют двухфазный стиму- ляционный сигнал.
Сон, прием пищи, физические нагрузки, гипоксия из меняют порогстимуляции. Наиболее сильно это прояв ляется во сне, когда порог стимуляции возрастает на 30— 40%. Почти на такую же величину увеличивает этот показа тель прием пищи, а физическая активность, напротив, сни жает порог стимуляции на 10—25% по сравнению с данны ми, полученными в покое. Гипоксия и гиперкапния также увеличивают порог деполяризации миокарда.
Нарушения электролитного обмена, как из вестно, могут менять работу стимулятора. При этом влия ние уровня сывороточного калия часто несущественно. Гора здо важнее соотношение внутри- и внеклеточного калия. Медленная инфузия калия даже при нормальном его содер жании приводит к уменьшению порога стимуляции. Быст рое повышение концентрации внеклеточного калия приво дит к увеличению порога стимуляции. Изменение концент рации кальция не влияет на этот показатель.
Лекарственные препараты по-разному меняют порог ЭКС. Симпатомиметики (кроме изадрина) повышают
возбудимость миокарда и снижают порог стимуляции. Иза-дрин также не противопоказан, однако у некоторых больных он вызывает парадоксальную реакцию. Глюкокортикоиды снижают порог стимуляции, а минералокортикоиды, напротив, повышают его. Антиаритмические препараты (хинидин, новокаинамид, ритмилен, пропранолол, изоптин) в терапевтических дозах на 10—15% увеличивают порог стимуляции. Этот эффект усиливается при появлении побочного действия лекарств. Напротив, лидокаин понижает порог стимуляции.
Нарушения функции электрокардиостимулятора. 1. Уреже-ние частоты работы стимулятора—наиболее частая причина смены электрокардиостимулятора. Современные аппараты рассчитаны на устойчивый 7—8-летний период функционирования батареи. Однако иногда уже к исходу первого года ритм урежается до 58—60 мин и возникают конкурентные отношения собственного ритма и ритма аппарата, особенно при физической активности. Если стимулятор не имеет программируемого устройства, позволяющего увеличить частоту, то его надо заменить.
Учащение работы стимулятора—более редкое осложнение. Обычно после имплантации стимуляторов отмечается увеличение или уменьшение частоты на 2—3 импульса в минуту по сравнению с должным. Затем работа стимулятора стабилизируется и сохраняется в этом пределе весь период, вплоть до истощения запаса питающего элемента.
В редких случаях, однако, особенно при раннем истощении батареи, частота его может возрасти, что ведет к развитию желудочковой тахикардии. Такая ситуация является очень тревожной и требует неотложной операции, чтобы предупредить фибрилляцию желудочков.
Иногда в программируемых стимуляторах, особенно в новых моделях, возможно спонтанное изменение программы (перепрограммирование) в сторону учащения. В этих случаях наружным устройством—программатором—следует изменить интервал стимулирования, что достаточно для нормализации работы устройства.
Неустойчивые ритмы отличаются внезапной сменой и чередованием урежения и учащения ритма. Такие изменения могут быть предвестником более серьезной поломки аппарата. Если эти изменения не связаны с перемещением аппарата в ложе, то его следует заменить.
В некоторых моделях стимуляторов, имеющих литиевые батареи (последние считаются лучшим источником питания), обнаруживается повышенная чувствительность к изменению температуры окружающих тканей. В этих устройствах, по-видимому, имеются минимальные отклонения от стандарта. Изменения частоты сердечных сокращений на 1—2 в минуту допустимы и не требуют смены стимулятора.
В практике ЭКС встречаются нарушения чувствительности (восприимчивости), когда в результате недостаточного подавления пейсмекеров типа demand отсутствует деполяризация желудочков. Это может быть обусловлено недостаточностью чувствительности к волнам Р или Т, перемежающимся разобщением надорванных эпикардиаль-ных электродов, электромагнитными помехами или подавлением потенциалами мышц. Недостаточная восприимчивость волны Р обычно обусловлена смещением эндокарди-ального предсердного электрода.
В связи с улучшением условий экранирования стимуляторов электромагнитные помехи мало влияют на их работу.
494
Наиболее частой причиной появления помех стали в последнее время микроволновые печи, диатермия, промышленные радарные установки, ретрансляционные радио- и телебашни. «Подавление» работы стимулятора потенциалами мышц в основном отмечается при использовании униполярных стимуляторов.
В связи с тем что у людей с имплантированным электрокардиостимулятором источник собственного ритма часто бывает подавлен (пейсмекерная, или ЭКС-зависимость), нарушение работы воспринимающего устройства может иметь серьезные последствия и привести даже к синкопе. Поэтому у таких больных смена электрокардиостимулятора абсолютно необходима и часто выполняется по жизненным показаниям. Простейшее решение, если это стимулятор demand и в экстренных случаях можно перевести работу стимулятора в асинхронный режим с фиксированной частотой с помощью наружного магнитного переключателя.
Одновременное повреждение восприятия и захвата сигнала деполяризации может быть результатом смещения и отхода от эндокарда электрода, повреждения последнего на протяжении, плохого контакта между стимулятором и электродом, выраженного фиброза в области головки электрода. О воспалительном процессе в первые дни после имплантации упоминалось выше. Смещение эн-докардиального электрода возникает в любое время, но наиболее часто это происходит в первые 3 дня, а затем в течение первого месяца. Разрыв или поломка электрода, а также фиброз в месте контакта отмечаются в более поздние сроки.
Следует подчеркнуть, что нарушения чувствительности и захвата редко бывают полными, скорее они носят перемежающийся характер.
Нарушения чувствительности наиболее часто наблюдаются при использовании электродов с малой поверхностью, а также у больных с фиброзом миокарда. Они чаще возникают при использовании биполярных стимуляторов, поскольку униполярные системы подают в стимулятор более крупные по размерам сигналы.
Часто причиной нарушения чувствительности являются сопутствующие желудочковые экстрасистолы с укороченным интервалом сцепления. Нетипичная морфология деполяризации и малая выраженность такой экстрасистолии приводят к неспособности стимулятора воспринять комплекс. В таких случаях возникает конкуренция ритмов.
Потеря способности «захватывать» сигнал также носит интермиттирующий характер и обычно связана либо со смещением катода, либо с разрывом электрода. В изолированном виде этот феномен может быть причиной перфорации сердца эндокардиальным электродом с повышением порога стимуляции, фиброза вокруг электрода, гипер- или гипокалиемии, токсического действия лекарств, блока на входе, т. е. в месте крепления электрода к желудочку. Рецидив дооперационной симптоматики особенно отчетливо проявляется у ЭКС-зависимых больных.
Стимуляция грудной мышцы происходит тогда, когда наблюдается утечка энергии в месте соединения электрода со стимулятором. Иногда это возникает при использовании униполярного устройства в результате его поворота таким образом, что стимул «попадает» прямо на мышцу. Одной из частых причин стимуляции диафрагмы или межреберных мышц является перфора-
ция эндокардиальным электродом стенки правого желудочка. При этом выявляются потеря «захвата» сигнала аппаратом и признаки блокады правой ножки предсердно-желудоч-кового пучка. Изолированная блокада правой ножки у больного со стимулятором не означает, перфорации стенки правого желудочка.
Следует, однако, отметить, что стимуляция диафрагмы и межреберных мышц описана и без повреждения целостности правого желудочка. Она иногда отмечается при мио-кардиальной стимуляции у больного в горизонтальном положении, а при изменении положения исчезает. Здесь имеют значение взаимоотношения фиксированного миокардиаль-ного электрода и диафрагмы.
Смещение электрокардиостимулятора наблюдается редко и отмечается обычно у пожилых больных в связи с потерей эластичности кожи и ее тургора. Резкое смещение аппарата книзу вызывает смещение эндокардиаль-ного электрода или даже его перелом. Иногда возможен поворот стимулятора, что приводит к потере энергии в месте соединения электрода и аппарата.
Шумовая симптоматика в сердце, обусловленная стимулятором, описывается очень редко, но если она возникает, то может быть обусловлена перфорацией межжелудочковой перегородки или структур трехстворчатого клапана эндокардиальным электродом. Иногдау больных выслушивается высокочастотный пресистоличе-ский щелчок, наблюдаемый при диафрагмальной или межреберной стимуляции.
Пейсмекерный синдром характеризуется такими симптомами, как головокружение, утомляемость, обморок или пульсация вен шеи, сочетающимися с гипотонией, и обусловлен работой электрокардиостимулятора. Обычно он наблюдается у больных, которым проводится желудочковая стимуляция (VVI), и купируется после перехода на физиологическую стимуляцию: бисеквенциальную (DVI) или автоматическую (DDD).
Существует два объяснения возникновения пейсмекерного синдрома. Во-первых, сохранная желудочково-предсердная проводимость сопровождается ретроградной активацией предсердий и их сокращением в то время, когда предсердно-желудочковые клапаны закрыты. Это приводит к венозной регургитации в системных и легочных венах и гемодинами-ческой недостаточности наполнения. Установлено также, что такой застой крови ослабляет рефлекторную активность общепериферического сопротивления и давления крови. В соответствии с другой точкой зрения этот синдром вызывается нарушением атриовентрикулярной синхронизации. Но, по-видимому, синдром вызывают оба фактора. Причем при ретроградной желудочково-предсердной проводимости больше страдают больные с нормальной функцией желудочков, а нарушение предсердно-желудочковой синхронизации более выраженно отражается на гемодинамике больных со сниженным комплайенсом.
С целью профилактики синдрома электрокардиостимулятора необходимо уметь «распознать» больных, у которых имплантация стимулятора может привести к его развитию. Его можно выявить при имплантации электрокардиостимулятора и не требуется дооперационного гемодинамического или полного электрофизиологического обследования.
Во время операции устанавливают желудочковый электрод и проводят электрическую пробу. Артериальное давле-
495
ние измеряют при «собственном» ритме больного и затем «навязывая» ему несколько более частый ритм в режиме demand (WI). Если у больного в период стимуляции артериальное давление падает на 20 мм рт. ст. и более, то это значит, что риск развития синдрома электрокардиостимулятора очень высок. Чем больше снижается артериальное давление при пробной стимуляции, тем более выраженными будут симптомы синдрома электрокардиостимуляции в последующем в режиме WI. Следовательно, больному показана физиологическая стимуляция. Теоретически гемодина-мические рефлексы возникают, по-видимому, у всех больных с имплантированными стимуляторами. Однако эти изменения выражены неодинаково у разных больных, и снижение давления компенсируется и при стимуляции в режиме demand.
Дополнительной мерой контроля, позволяющей выявить ретроградную (желудочково-предсердную проводимость), является установка временного предсердного электрода. Его можно провести либо через то же пункционное отверстие, через которое проведен желудочковый электрод, либо через подключичную вену противоположной стороны. Проводя стимуляцию сердца через желудочковый электрод, определяют наличие ретроградной проводимости. Если у больного при стимуляции в режиме VVI давление не падает и нет признаков ретроградной проводимости, предсердный электрод удаляют и имплантируют стимулятор в режиме WI. Поиски наиболее оптимальных методов прогноза пейсме-керного синдрома продолжаются. Если у больного сохранена ретроградная (V— А) проводимость даже без снижения артериального давления, некоторые хирурги сами ставят физиологические стимуляторы. Они уверены, что при переходе из горизонтального положения в вертикальное давление неизбежно снизится и у больного появятся симптомы синдрома электрокардиостимулятора. Можно использовать вращающийся стол, позволяющий придать больному в процессе тестирования сидячее положение и положение стоя и таким образом определить изменения артериального давления при желудочковой стимуляции. Еще более достоверную информацию можно получить, если больному провести катетеризацию легочной артерии. Тогда можно определить сердечный выброс и давление заклинивания при «собственном ритме» больного и при желудочковой стимуляции и сопоставить эти данные с данными при физиологической стимуляции в режиме предсердной (DDD) или бисеквенциаль-ной стимуляции (DVI).
Диагностика синдрома электрокардиостимулятора у больных с имплантированным электрокардиостимулятором. Если больной с имплантированным стимулятором предъявляет жалобы, характерные для пейсмекерного синдрома, то первое, что нужно сделать, это измерить артериальное давление в положении лежа, сидя и стоя. При этом если установлен программируемый стимулятор, то его следует перепрограммировать так, чтобы у больного некоторое время был синусовый ритм, и в этот период вновь измерить артериальное давление в положении лежа, сидя, стоя.
Проведенное тестирование может выявить гипотензию, обусловленную электрокардиостимуляцией, в таких случаях возможны различные решения. Если «собственный ритм» больного постоянный, то можно уменьшить частоту ритма от стимулятора, что снижает частоту искусственного водителя ритма. Можно также использовать феномен гистерези-
са, позволяющий удлинить интервал после воспринимаемого (спонтанного) комплекса QRS на интервал больший, чем следующий за электрическим стимулом. Это помогает значительно уменьшить проявления конкуренции в работе пей-смекера и собственного ритма больного. Внедрение в клиническую практику метода холтеровского мониторирования позволяет использовать этот метод с одновременной регистрацией артериального давления.
Другой неинвазивный метод—повышение значимости многоканальной электрокардиографии и тщательности изучения деполяризации предсердий, возникающей в ответ на стимуляцию желудочков. Запись потенциалов с поверхности может дать информацию о наличии ретроградной проводимости. Однако не у всех больных можно получить точную информацию о наличии ретроградной проводимости.
Если диагноз пейсмекерного синдрома сомнителен, а состояние больного этого требует, следует провести инвазив-ное исследование в условиях стационара. Устанавливают временный предсердный и постоянный желудочковый электроды на стороне, противоположной стороне ранее имплантированного электрода. Электроды соединяют с устройством, позволяющим проводить последовательную стимуляцию. Сначала определяют ретроградную проводимость. Затем в режиме желудочковой (VVI), секвенциальной (DVI) или предсердной стимуляции (DDD) определяют и сравнивают динамику артериального давления. Если артериальное давление снижается при желудочковой стимуляции и не изменяется при физиологической, убирают ранее имевшийся стимулятор и налаживают последовательную стимуляцию с использованием двухкамерного аппарата. До внедрения стимуляторов типа DDD с удлиненным программируемым рефрактерным периодом предсердий для исключения тахикардии пейсмекерного генеза стимуляторы последовательного действия (DVI) использовались у больных с сохранной ретроградной проводимостью. Новейшие стимуляторы DDD легко приспосабливаются к тому, чтобы избежать такой тахикардии путем удлинения рефрактерного периода предсердий.
4.4. СИНДРОМЫ ПРЕДВОЗБУЖДЕНИЯ ЖЕЛУДОЧКОВ
В 1930 г. L. Wolff, J. Parkinson, P. White описали электрокардиографический синдром, включающий функциональную блокаду ножки предсердно-желудочкового пучка и короткий интервал Р—R, который наблюдается у молодых, физически здоровых людей, периодически страдающих приступами пароксизмальной тахикардии. Как было выяснено вскоре, синдром WPW может приводить к смерти.
Синдром предвозбуждения желудочков является удобной «моделью» для изучения ритмов повторного входа (риент-ри). Характерная морфология зубца QRS, которая наблюдается при предвозбуждении желудочков, возможность выполнения внутрисердечного исследования, включая специализированную проводящую систему сердца, проведение программированной стимуляции сердца, развитие эпикарди-ального картирования сердца, наличие хирургической техники, необходимой для прерывания аномальных проводящих путей, и выявляемость определенного анатомического субстрата синдрома на патологоанатомическом материале,
496
способствовали более тщательному изучению синдромов предвозбуждения.
Определение и классификация. Предвозбуждение—термин, впервые использованный R. Ohnell (1944), относится к случаям, когда из-за наличия анатомического «шунта» часть или весь миокард желудочка активируется импульсом, возникшим в предсердии и достигшим этого участка раньше, чем возбуждение, приходящее в желудочек через нормальную (специализированную) проводящую систему. Эту концепцию предвозбуждения распространяют и на тех больных, у которых аналогичное анатомическое сообщение и сопутствующая аритмия сочетаются с нормальной ЭКГ (добавочные аномальные пути проводят возбуждение только в обратном ретроградном направлении).
В 1975 г. европейская группа по изучению предвозбуждения разработала классификацию синдромов предвозбуждения (рис. 4.17). К ним относятся: 1) предсердно-желудочко-вые соединения, формирующие прямую связь между предсердием и желудочком; 2) нодовентрикулярные волокна, соединяющие предсердно-желудочковый узел с миокардом желудочков; 3) фасцикуловентрикулярное соединение системы Гиса—Пуркинье с миокардом желудочков; 4) обходные (шунтирующие) предсердно-желудочковый узел пути. Функционирующие предсердно-желудочковые соединения (пучок Кента) дают классическую картину синдрома WPW, а нодовентрикулярные и фасцикуловентрикулярные тракты (волокна Магейма)—варианты синдрома WPW. Обходные пути (шунты) предсердно-желудочкового узла (тракт Джеймса) формируют так называемый синдром L—G—L (Lown— Ganong—Levine).
Эти синдромы характеризуются коротким интервалом P—R, аномальным комплексом QRS и их анатомическим субстратом. Наиболее частый вариант этих синдромов— синдром Вольфа—Паркинсона—Уайта. Однако могут быть варианты, включающие короткий интервал Р—R, аномальный комплекс QRS или полностью неизменную электрокардиограмму.
В соответствии с терминологией, предложенной этой же группой под термином «соединение», обычно используется общий термин для описания аномальных проводящих путей, которые проникают в «работающий» (сократительный) миокард. Термин «тракт» используется для описания аномальных проводящих путей, которые внедряются в специализированную проводящую систему сердца. Поскольку нормальное и аномальное функциональное проявление синдрома всегда основывается на точных анатомических субстратах, следует быть очень осторожным при экстраполяции функциональных проявлений на анатомический субстрат. При синдроме предвозбуждения выявление прямых анатомических признаков с помощью обзорных методов (визуально) затруднительно. Поэтому для клинических целей целесообразно использовать функциональные проявления, которые идентифицируют области, где получена корреляция между структурой и функцией (рис. 4.18).
Функциональные определения предвозбуждения. Добавочные предсердно-желудочковые мышечные соединения, известные в литературе под названием «пучки Кента», начинаются в миокарде и внедряются в сокращающийся миокард. Их называют также мышечными мостиками, поскольку они перекидываются через атриовентрикулярную борозду.
Добавочные предсердно-желудочковые соединения распо-

4.17. Анатомические субстраты синдромов предвозбужде-ния, рекомендованные Европейской группой по изучению пред-возбуждения.
I — путь предпочтительного внутриузлового проведения; 2 — задний межузловой тракт; 3 — нодовентрикулярный путь; 4 — атриовентрикулярный путь; 5 — атриопучковый путь; 6 — фасцикуловеитрикулярный путь; ПЖУ—предсердно-же-лудочковый узел; ПЖП—предсердно-желудочковый пучок; ЛН и ПН—левая и правая ножки предсердно-желудочкового пучка.
лагаются в свободной стенке (париетально) или в перегородке. Аномалия характеризуется полным шунтированием функции предсердно-желудочкового узла. Поэтому потенциал (спайк) предсердно-желудочкового пучка может быть смещен в желудочковую часть электрограммы, что приводит к дальнейшему стиранию исходной картины (Л-волна) и расширению комплекса QRS. Если в предсердно-желудоч-ковом пучке возникает экстрасистола, комплекс QRS нормализуется. Он нормализуется также при развитии рецип-рокной тахикардии, в результате которой добавочный путь «начинает работать» в ретроградном направлении, замыкая таким образом круг повторного входа (риентри). Аналогичная картина (нормализация QRS) наблюдается при электростимуляции предсердно-желудочкового пучка.
Особенности усиления проводимости в предсердно-желудо-чковом узле. Несмотря на большие достижения клинической электрофизиологии сердца, основные противоречия, сохраняющиеся и до настоящего времени, касаются нарушения проводимости внутри предсердно-желудочкового узла. Как известно, в здоровых сердцах имеются межузловые пути, предсердные тракты, которые в конечной своей части огибают предсердно-желудочковый узел, приближаются к трехстворчатому клапану и пенетрируют нижнюю часть узла. Таким образом, межузловые пути потенциально представляют собой частичный шунт этого узла. Напротив, волокна, отходящие от предсердия к предсердно-желудочковому пучку (предсердно-узловые волокна) и полностью шунтирующие узел, встречаются очень редко. У ряда больных при стимуляции предсердий предсердно-желудочковая проводимость не удлиняется. Это явление было охарактеризовано рядом авторов как «ускоренная внутриузловая проводи-
497

Цифрами обозначены интервалы времени (мс) на гисограмме.
мость». Предполагается, что аномалия проведения между предсердием и предсердно-желудочковым пучком может иметь место в следующих случаях: 1) предсердно-гисовский интервал (А — Н) на синусовом ритме меньше 60 мс (нижний предел нормы); 2) соотношение проводимости между предсердием и предсердно-желудочковым пучком равно 1:1 на фоне стимуляции правого предсердия при длительности цикла менее 300 м/с; 3) удлинение интервала А — Н незначительное и не превышает 100 мс при стимуляции правого предсердия с длительностью цикла 300 мс.
Добавочное нодовентрикулярное соединение и фасцикуло-вентрикхлярное добавочное соединение известны в литературе как волокна Магейма. По анатомо-функциональным признакам мы выделяем две подгруппы волокон.
Добавочные нодовентрикулярные соединения начинаются от предсердно-желудочкового узла и внедряются в миокард желудочка. Электрофизиологически при обследовании больных, имеющих такое соединение, наблюдается короткий интервал Н— V (менее 30 мс). сочетающийся с измененным комплексом QRS. В зависимости от того, где соединение внедряется в желудочек, морфология комплекса QRS может напоминать блокаду ножки предсердно-желудочкового пучка либо может появиться Д-волна. Может наблюдаться нормальное соотношение интервала Р— R, когда из-за низкого внедрения соединения в миокард желудочка задержка проведения в предсердно-желудочко-вом узле отсутствует. В этом случае при стимуляции предсердий значительно увеличивается проведение возбуждения между предсердием и желудочком. Поскольку добавочный путь начинается проксимальнее предсердно-желудочкового пучка, то при стимуляции области пучка или возникновении стволовых экстрасистол комплекс QRS нормализуется.
В последние годы появились сообщения об электрофизиологическом «субстрате» так называемых атриофасцикуляр-ных волокон, которые, вероятно, играют основную роль в формировании круга «нодовентрикулярной» тахикардии [Zipes D., 1994]. Гистологические подтверждения наличия дополнительных путей, соединяющих боковую стенку правого предсердия с правой ножкой пучка Гиса, т. е. атриофас-цикулярных трактов, в литературе пока не представлены.
У больных с фасцикуловентрикулярным соединением добавочные волокна соединяют специализированную проводящую систему желудочков (предсердно-желудоч-ковый пучок или его ножки) с миокардом желудочка. Как и в предыдущем случае, отмечаются нормальное значение интервала Р— R. задержка проведения возбуждения проксимальнее предсердно-желудочкового пучка при электростимуляции предсердия, а также укорочение интервала Н— V с атипичным комплексом QRS. Однако в отличие от нодо-вентрикулярного соединения стимуляция предсердно-желудочкового пучка или стволовая экстрасистола не нормализуют комплекс QRS, а предсердная стимуляция не приводит к усилению изменений комплекса QRS при наличии у больного фасцикуловентрикулярных соединений.
Синдром Вольфа—Паркинсона—Уайта. Современное представление об анатомическом субстрате и электрофизиологические данные свидетельствуют, что синдром Вольфа— Паркинсона—Уайта обусловлен добавочными проводящими путями. Основным элементом этих путей является сократительный миокард.
Основным методом диагностики синдрома Вольфа— Паркинсона—Уайта остается электрокардиография. Доказательством наличия добавочных проводящих путей служат короткий интервал Р—R (Р—Q), уширенный комплекс QRS и подъем начального сегмента QRS—А-волна. Диагностические проблемы возникают тогда, когда один или даже все перечисленные признаки отсутствуют. Все признаки на ЭКГ обусловлены преждевременным возбуждением участка миокарда, активируемого пучком Кента. В большинстве случаев миокард возбуждается через оба пути: нормальный и аномальный, а результирующая комплекса QRS отражает смещение этих воздействий. Начальная часть QRS—это отражение активации какого-то проксимального отдела желудочка, где внедряется добавочный путь.
Раннее возбуждение миокарда желудочков добавочными проводящими путями происходит потому, что обычные ми-окардиальные клетки пучка Кента проводят быстрее, чем клетки предсердно-желудочкового узла. Однако если пучок-добавочного пути сам по себе активируется позже предсердно-желудочкового узла, то предвозбуждение либо запазды-
498

вает, либо вообще не проявляется, что более характерно для левосторонней локализации пучка Кента, чем для правосторонней.
Наиболее частой формой аритмии является реципрокная тахикардия с антеградным проведением через предсердно-желудочковый узел (пучок Гиса) и ретроградным проведением через добавочный путь (пучок Кента). Пусковым моментом, приводящим к тахикардии, обычно является экстрасистола, возникающая в предсердии, желудочке или же пред-сердно-желудочковом узле. На синусовом ритме импульс проходит одновременно по проводящим путям и по пучку Кента. Для объяснения механизма возникновения реципрокной тахикардии необходимо уяснить некоторые особенности патологической физиологии добавочных проводящих путей. Время, необходимое для восстановления функции проведения по добавочному пути после деполяризации (рефрактерный период), зависит от продолжительности цикла стимуляции или спонтанного ритма. Значение рефрактерного периода может существенно отличаться в зависимости от того, в каком направлении «работает» добавочный путь—в ан-теградном или ретроградном. У больных с реципрокной тахикардией рефрактерный период добавочного пути часто превышает рефрактерный период проводящей системы. Поэтому при появлении предсердной экстрасистолы последняя блокирует проведение по добавочному пути в антеград-ном направлении и дает преимущественное проведение к желудочку через нормальную проводящую систему. Это приводит к нормализации комплекса QRS. Нормальные и добавочные проводящие пути в этот момент диссоциируют, что способствует возникновению круга повторного входа (рис. 4.19). Возбуждение, распространяющееся на желудочек, «застает» добавочный путь в состоянии, при котором он «работает» только в ретроградном направлении, способствуя возвращению импульса обратно в предсердие. Таким образом, возникает круговой ритм с антеградной проводимостью через нормальную проводящую систему (нормальная QRS) и ретроградную проводимость через добавочный проводящий путь. Это и есть ортодромная пароксизмальная тахикардия при синдроме Вольфа—Паркинсона—Уайта.
Реже реципрокный ритм, обусловленный синдромом пред-возбуждения, имитирует желудочковую тахикардию. Это бывает тогда, когда возбуждение в антеградном направле-4 нии проводится через добавочный путь, а в ретроградном—
через предсердно-желудочковый узел. Этот вариант тахикардии назван «антидромная реципрокная тахикардия» и считается редким.
Аритмии, сочетающиеся с синдромом Вольфа—Паркинсона— Уайта. Мерцательная аритмия сопутствует синдрому предвозбуждения в 12—40% случаев, как правило, выявляется у хирургических больных. Высокую частоту сочетания синдрома Вольфа — Паркинсона — Уайта и мерцательной аритмии можно объяснить тем, что в хирургические стационары обычно направляют наиболее тяжелых больных, лечение которых в терапевтических стационарах, несмотря на применение всех имеющихся средств, оказывается неэффективным.
Трепетание предсердий практически не сочетается с синдромом преждевременного возбуждения желудочков. Какие же факторы являются причиной развития мерцательной аритмии при наличии у больного синдрома предвозбуждения?
Добавочные проводящие пути играют определенную роль в поддержании реципрокной тахикардии. Этому может способствовать наличие механических или циркуляторных факторов, приводящих к растяжению или гипоксии предсердий, что в свою очередь приводит к нарушению ритма предсердий. Обычно частота сердечных сокращений при реципрокной тахикардии, сочетающейся с синдромом Вольфа—Паркинсона—Уайта, больше, чем при реципрокной тахикардии, обусловленной кругом повторного входа в предсердно-желудочковом узле. Этот более высокий ритм может предрасполагать к электрической нестабильности, вызывающей мерцание предсердий. В литературе приводится большое количество наблюдений перехода реципрокной тахикардии в мерцательную аритмию. Наличие частых экстрасистол, которые предрасполагают к реципрокной тахикардии, может также явиться начальным этапом заболевания предсердия, что ведет к его мерцанию. Наконец, если имеются добавочные проводящие пути, то единичные или множественные желудочковые экстрасистолы могут изменить ретроградную проводимость. Результирующая волна возбуждения, распространяющаяся ретроградно, «сталкивается» с волной антеградного возбуждения, идущей от синусно-предсердного узла; это приводит к нестандартной деполяризации предсердия и вызывает его мерцание. Аналогичный эффект возможен и тогда, когда волна ретроградного возбуждения «застает» миокард предсердия в уязвимый период—в фазу восстановления.
Фибрилляция желудочков. Наличие мерцательной аритмии при синдроме предвозбуждения—очень серьезный аргумент в пользу хирургического лечения больного, посколь-
499
ку этот вариант аритмии, с одной стороны, сам по себе утяжеляет течение болезни, а с другой—является потенциальным фактором внезапной смерти при синдроме Вольфа—Паркинсона—Уайта. Наличие добавочного пути с коротким рефрактерным периодом, сочетающимся с мерцательной аритмией или с трепетанием предсердий, может приводить к смерти в результате прямого перехода очень частых сокращений предсердий (мерцания) в аналогичные сокращения желудочков (фибрилляция).
На развитие фибрилляции желудочков при сопутствующей мерцательной аритмии у больных с синдромом WPW не влияют пол, возраст больных в момент обследования, их возраст в начале появления симптоматики тахикардии, число лет, прошедших со времени эпизода тахикардии до развития фибрилляции желудочков, или наличие сопутствующих аномалий сердца. Часто бывает так, что первый же эпизод тахикардии переходит в фибрилляцию желудочков, в то время как у большинства больных реципрокная тахикардия существует на протяжении многих лет, а затем неожиданно осложняется фибрилляцией желудочков. И только тщательный анализ электрокардиографической картины вне приступа, во время приступа тахикардии, а также при развитии мерцательной аритмии позволяет выявить группу больных, предрасположенных к фибрилляции желудочков. Оказалось, что к фибрилляции желудочков предрасположены те больные, у которых интервал R—Л в период мерцательной аритмии менее 200 мс. Таким образом, обследуя больных с синдромом предвозбуждения, у которых бывают эпизоды мерцательной аритмии, всегда следует стремиться получить запись ЭКГ и проанализировать предрасположенность больного к развитию желудочковой тахикардии. Однако, по данным литературы, примерно у 10% больных фибрилляция желудочков развивается на фоне реципрокной тахикардии, обусловленной синдромом Вольфа—Паркинсона—Уайта; у этих больных никогда ранее, а также в период развития фибрилляции желудочков не регистрировалась мерцательная аритмия.
Наиболее полное объяснение генеза синдрома предвозбуждения дает теория Джеймса [James Т., 1972], согласно которой для этого заболевания характерна продольная диссоциация проводящей системы сердца. Тахикардия обусловлена механизмом повторного входа (риентри), она возникает при блокаде одного «колена» этого круга.
Синдром Вольфа—Паркинсона—Уайта считается простейшей моделью риентри-тахикардии у человека. Пучок Кента является недостающим звеном анатомического круга повторного входа, в состав которого, кроме него, входят предсердия, предсердно-желудочковый узел и пучок, а также желудочки. При синусовом ритме или при электрической стимуляции предсердий возбуждение проходит и по проводящей системе, и по добавочному пути. Однако, если возникает предсердная экстрасистола, это приводит к различному ответу двух путей проведения. Экстрасистола блокируется в пучке Кента, но проводимость по предсердно-желудочковому узлу сохраняется. Это приводит к тому, что пучок Кента проводит импульс в ретроградном направлении, поскольку он сохраняет способность желудочково-предсердного проведения. При условии, что все компоненты круга повторного входа успеют восстановиться ко времени прихода импульса, функционирующий круг приводит к развитию устойчивой тахикардии. Описанный механизм дока-
зан внутрисердечными электрофизиологическими исследованиями, а также результатами операций, доказывающих возможность полного устранения риентри-тахикардии после прерывания проводимости по пучку Кента.
Ряд авторов, в противоположность мнению большинства сторонников теории врожденного генеза синдрома предвозбуждения, выдвигают версию о приобретенном характере этого заболевания. Позднее проявление болезни (синдрома), однако, не противоречит высказанным ранее предположениям, не исключает врожденного анатомического субстрата тахикардии. Хорошо известно также, что начало аритмии, связанное с синдромом предвозбуждения, требует какого-то изменения в состоянии сердца, например появление экстра-систолии (в случаях реципрокной тахикардии) или мерцательной аритмии, которая чаще всего появляется в более старшем возрасте. Кроме того, чтобы возникла тахикардия по типу риентри, необходима «блокада» проведения импульса в добавочном проводящем пути или нормальном пути проведения. Появление предсердных или желудочковых экстрасистол способствует этому. Патофизиологические изменения, связанные с возрастом, могут играть не последнюю роль в дифференциации качеств нормальных и проводящих путей сердца, что и может явиться причиной того, что тахикардии у больных с синдромом WPW возникают не в раннем возрасте, а в юношеском или даже в период зрелости.
Электрофизиологическое обследование больных с синдромом Вольфа—Паркинсона—Уайта отличается многоплановостью. В процессе обследования необходимо решить, имеется ли предвозбуждение, какова природа сопутствующей аритмии, достаточно точно локализовать место добавочного проводящего пути, доказать роль добавочного пути в развитии тахиаритмии, охарактеризовать «функциональное поведение» добавочного пути и определить эффективность лекарственной терапии для конкретного больного.
При электрофизиологическом обследовании прежде всего следует доказать, что имеется предвозбуждение. Для этого необходимо установить начало Д-волны на стандартной ЭКГ и что она предшествует спайку предсердно-желудоч-кового пучка на электрограмме. На гисограмме при этом выявляется следующая картина. На синусовом ритме комплекс, характеризующий спайк предсердно-желудочкового пучка (Я), находится обычно в начале Д-волны. У здорового человека через 35 мс после этого обычно следует спайк желудочка (V). У больных с синдромом WPW эти два спайка (интервал Я— V) практически накладываются один на другой (Я—К=10-0 мс), что характерно для синдрома предвозбуждения.
Степень предвозбуждения на фоне синусового ритма может увеличиваться, что проявляется удлинением времени проведения через предсердно-желудочковый узел и достигается учащающей стимуляцией сердца из близко расположенной к добавочному проводящему пути зоны. Эти факторы приводят к смещению спайка предсердно-желудочкового пучка в желудочковый компонент комплекса QRS, поскольку желудочек все больше и больше активируется через добавочный путь.
Несмотря на то что у большинства больных электростимуляция усиливает проявления предвозбуждения, однако есть группы больных, у которых предвозбуждение усиливается по мере удлинения продолжительности сердечного со-
500
кращения или на синусовом ритме. Это свидетельствует о том, что физиология синдрома предвозбуждения чрезвычайно сложна.
Есть еще одно исключение, о котором необходимо помнить. Предвозбуждение не всегда выявляется на ЭКГ на фоне синусового ритма при левосторонней локализации пучка Кента. У врача, обследующего больного с возвратными тахикардиями без документированных фактов, предвозбуждения, возникает ряд трудностей. На ЭКГ может появляться нормальный интервал P—Q и нормальный комплекс QRS. Если у такого больного удается записать ЭКГ во время приступа, то нередко можно обнаружить переход реципрокной тахикардии в мерцательную аритмию с быстрым проведением на желудочек и появлением аномального комплекса QRS.
В определенных случаях ЭКС из правого предсердия не выявляет синдрома предвозбуждения. В данном случае это связано с ускоренным проведением по предсердно-желудоч-ковому узлу. Если после этого начать стимуляцию левого предсердия (через венечный синус), то появляется очень ясный признак преждевременного возбуждения желудочков. Электрофизиологическое исследование позволяет изучить функциональные свойства добавочных путей и сопутствующие аритмии. Оно позволяет также определить проведение и рефрактерность структур, составляющих нормальную проводящую систему сердца, а также добавочных путей как в антеградном, так и в ретроградном направлении. Во время этих манипуляций, как правило, удается вызвать тахикардию. При определении рефрактерных периодов ЭКС сердца осуществляется при частоте, которая обычно бывает у больного, а экстрасистолы наносятся с прогрессивным уменьшением продолжительности цикла. При этом становится возможным определить наиболее короткий последовый интервал, при котором предсердная экстрасистола все еще проводится на желудочек через добавочный путь. Эта величина называется эффективным рефрактерным периодом добавочного пути. Получаемая величина довольно точно соответствует кратчайшему интервалу между двумя сокращениями с признаками предвозбуждения, что позволяет выявить больных с опасностью развития желудочковой фибрилляции при наличии предшествующей ей мерцательной аритмии, обусловленной синдромом Вольфа—Паркинсона—Уайта. Практически, однако, это удается не всегда из-за высокой рефрактерное™ мышцы предсердия как таковой. Поэтому справедливо считается, что для определения дополнительных путей с быстрым проведением импульса у таких больных более предпочтительно индуцировать трепетание или мерцание предсердий путем сверхчастой стимуляции предсердий.
Внедрение хирургических методов лечения у больных с синдромом предвозбуждения поставило вопрос о необходимости точной топической диагностики добавочных аномальных проводящих путей. Стандартная электрокардиография позволяет в значительном числе случаев определить местоположение пучка Кента. Однако для хирургических целей дооперационное внутрисердечное электрофизиологическое исследование и особенно интраоперационное исследование являются методом установления точной локализации этого образования.
Метод программируемой электрической стимуляции сердца и регистрация электрограмм во время исследования по-
зволяют точно охарактеризовать состояние нормальных проводящих путей сердца и добавочных проводящих путей у больных с синдромом предвозбуждения, а также установить наличие сопутствующих аритмий. Это же исследование позволяет определить эффективность воздействия различных антиаритмических препаратов на функциональные свойства добавочных проводящих путей. В идеальном случае, конечно, желательно для выбора лекарственной терапии электрофизиологическое исследование проводить всем больным.
Мы считаем, что целесообразнее использовать этот же метод для изучения естественного течения синдрома предвозбуждения. Он позволит ответить на вопрос о том, в какой степени бессимптомные синдромы с коротким рефрактерным периодом и способные потенциально давать быструю проводимость по добавочному предсердно-желудочковому пути требуют профилактического проведения антиаритмической терапии. Другими словами, ставится вопрос, насколько оправдан профилактический прием препаратов больными с высоким риском внезапной смерти. Совершенно понятно, что такое исследование должно проводиться в тех случаях, когда у больных, несмотря на проводимую антиаритмическую терапию, сохраняются приступы тахиаритмий. Особое внимание следует обратить на тех, у которых приступы тахикардии сочетаются со снижением артериального давления, ухудшением гемодинамики. Требуют обязательного обследования больные с тахиаритмиями с высокой вероятностью внезапной смерти, обусловленной быстрой проводимостью по добавочному предсердно-желу-дочковому пути в момент развития мерцательной аритмии, поскольку такое обследование позволяет сделать единственный правильный вывод о спасении этих больных. Мы считаем, что абсолютным показанием к проведению электрофизиологического обследования является молодой возраст больных, когда возвратные аритмии требуют непрерывного применения антиаритмических препаратов, что ухудшает анатомическое и функциональное состояние миокарда. У таких больных хирургическое лечение, несомненно, предпочтительнее перед другими методами.
Лечение. При лекарственной терапии следует основываться на механизме аритмии и особенностях фармакокинетики препаратов. Следует учитывать наличие сопутствующих аритмий, особенности проводимости и рефрактерности предсердия, желудочка, нормального и добавочного проводящих путей в антеградном и ретроградном направлениях.
У больных с реципрокной тахикардией начало аритмии обычно возможно при наличии экстрасистолии (предсер-дной, узловой или желудочковой), вызывающей диссоциацию процесса активации нормального и добавочного проводящих путей из-за разности рефрактерных периодов, что приводит к формированию круга риентри. Поэтому профилактическая терапия может быть направлена на уменьшение числа экстрасистол или на изменение рефрактерных периодов таким образом, чтобы интервал, следующий за экстрасистолой, способной вызвать диссоциацию, становился короче. Лечение можно направить непосредственно на механизм, с помощью которого формируется аритмия.
Большинство лекарств обладает многофакторным воздействием на организм больного, например такой широко распространенный препарат, как хинидин. Он применяется во
501

всех странах мира. С одной стороны, хинидин удлиняет продолжительность эффективного рефрактерного периода добавочного пути, а с другой—замедляет проведение в нескольких элементах круга тахикардии.
В целом, однако, воздействие лекарства на проводимость и рефрактерность является однотипным. У больных с рефрактерной аритмией целесообразно избрать следующий путь. Электрофизиологическое обследование больных дополняется серийным тестированием лекарств и ежедневным подтверждением эффективности или неэффективности этой терапии при помощи электрода, оставленного в сердце. Лекарства затем систематически тестируются, причем можно тестировать не только один препарат, но и несколько, в результате удается найти оптимальный состав антиаритмической терапии. При этом оценка терапии, проводимая при электрофизиологическом исследовании, проводится следующим образом: терапия предупреждает тахикардию, уре-жает частоту приступов, замедляет тахикардию или неэффективна. В последнем случае абсолютно показано хирургическое вмешательство.
Показания к хирургическому лечению. Отбор больных на операцию определяется многими факторами. К ним относятся возраст больного и его общее состояние, характер тахикардии, наличие или отсутствие сопутствующих аномалий сердца, которые сами по себе требуют хирургического вмешательства, характер добавочного предсердно-желудоч-кового пути и его доступность, уменьшение симптомов болезни в результате лекарственной терапии и т. д. Консервативную терапию необходимо проводить до операции. Однако у многих больных лекарственная терапия безуспешна. В частности, встречаются больные, которые плохо переносят антиаритмические препараты, иногда даже такие, которые могли бы быть наиболее эффективными. Особую сложность представляет лечение до операции детей. Из литературы известно также, что многие антиаритмические препараты обладают сильным побочным действием. Это вынуждает
в определенном проценте случаев определять показания к операции в молодом возрасте.
Хирургическое лечение. Первая удачная операция у больного с синдромом Вольфа—Паркинсона — Уайта была выполнена в 1968 г. в Дьюкском медицинском центре W. Sealy. Успех первой операции, как это часто бывает, оказался возможным в результате исключительно правильного подбора больного. У этого больного был правосторонний пучок Кента, благодаря чему оказалось возможным на сокращающемся сердце выделить правую венечную артерию на участке, где проходил этот добавочный путь, и затем рассечь его.
Доступ к добавочным путям со стороны эпикарда длительное время считался нерациональным. Вероятно, это справедливо при расположении пучка Кента с левой стороны. В этом случае он проходит под коронарным синусом и левой коронарной артерией. Отделение их на сокращающемся сердце, несомненно, представляет большие сложности. Что касается перегородочной локализации, то доступ к ней со стороны эпикарда оказался еще более трудным. В 1974 г. W. Sealy и соавт. разработали метод устранения добавочных предсердно-желудочковых путей, используя доступ к сердцу со стороны эндокарда. Метод получил наибольшее распространение. Однако первые результаты операции во всех клиниках сопровождаются недостаточно надежной ликвидацией добавочных предсердно-желудочковых путей (от 10 до 20%), большой частотой развития полной поперечной блокады (до 20%). другими хирургическими осложнениями (кровотечение). Поэтому поиск более простых и надежных способов устранения добавочных проводящих путей активно продолжается.
Однако не может быть однотипного подхода к хирургическому лечению синдромов предвозбуждения. Во-первых, при синдроме Вольфа—Паркинсона—Уайта мышечный мостик, пучок Кента проходят в эпикарде. Поэтому, кроме перегородочной локализации, в остальных позициях он бо-
502
лее доступен снаружи (в частности, для его устранения электрошоковым воздействием). При перегородочной локализации, вероятно, наиболее целесообразна операция, разработанная Сили. Остановимся кратко на методах оперативного устранения добавочных проводящих путей.
Эндокардиальные методы доступа к сердцу. Операция выполняется в условиях ИК и кардиоплегии (на остановленном сердце).
Срединная продольная стернотомия. Укрепляют два референтных электрода: при правосторонней локализации на ушко правого предсердия и выходной отдел правого желудочка, при левосторонней—на ушко левого предсердия и на доступную бессосудистую зону левого желудочка. Затем «навязывают» ритм на предсердие с частотой, превышающей исходную на 10—15%. Это позволяет, с одной стороны, усилить предвозбуждение, а с другой— проводить картирование в однотипных условиях. Картируют предсердно-желудочковую борозду, разделенную на 30 точек—по 15 точек на передней и задней поверхности (рис. 4.20) со стороны желудочка. При этом в месте локализации пучка Кента (или пучков Кента) электрограмма будет опережать референтную не менее чем на 50 мс (рис. 4.21). После этого, т. е. когда локализована желудочковая зонапредвозбуждения, приступают к локализации предсердной зоны предвозбуждения. Это достигается либо программированной стимуляцией, либо частой стимуляцией. Картируют оба предсердия вдоль предсердно-желудочковой борозды в 30 точках, симметричных точкам на желудочковой стороне. Локализация зоны максимального предвозбуждения характеризуется опережением прихода возбуждения в эту зону по отношению к референтной точке. Затем тахикардию с помощью одного из двух методов прекращают. Индукция и купирование тахикардии доказывают механизм риентри, а после операции программируемая стимуляция используется для определения ее эффективности.
После этого можно приступить к операции прерывания проводимости по пучку Кента. В аорту, полые вены вводят канюли и подключают АИК, охлаждают больного и останавливают сердце. При правосторонней локализации предсердие широко вскрывается почти на всем протяжении атри-овентрикулярной борозды, чтобы хорошо видеть трехстворчатый клапан. Место соединения правого желудочка и предсердия образует острый угол, что отделяет эту часть сердца от эпикарда. Задача хирурга состоит в том, чтобы на расстоянии примерно 4 см (по 2 см с каждой стороны пучка Кента) отделить изнутри предсердие от желудочка в проекции предсердно-желудочковой борозды. Для этого делают
разрез эндокарда отступя 1—1,5 мм от клапанного кольца, а затем рассекают подлежащий мышечный слой и отделяют от мышечного слоя предсердия и желудочка жир эпикарда(рис. 4.22).
Если после полного разделения предсердия и желудочка предсердие отвести кверху, то откроется «крыша» желудочка. В этом месте могут оставаться отдельные волокна пучка Кента. Поэтому мышечную часть желудочковой поверхности дополнительно осторожно коагулируют. На этом манипуляции по устранению пучка Кента заканчиваются. Восстанавливают целостность созданного дефекта одноряднымнепрерывным швом. Ушивают дефект эпикарда и разрез предсердия также однорядным швом. Восстанавливают сердечную деятельность. При адекватно выполненной операции Д-волна исчезает, что является первым признаком отсутствия предвозбуждения. Затем проводят учащающую стимуляцию и определяют проводимость по предсердно-желудоч-ковому узлу—точку Венкебаха. После устранения пучка Кента она возникает при частоте сердечных сокращений 150—170 в минуту. Затем картируют сердце. Для этого при устойчивом синусовом ритме начинают стимуляцию предсердий с частотой ритма, превышающей исходную на 10—15%, и проводят картирование желудочковой стороны атрио-вентрикулярной борозды. Ранее выявляющиеся точки опережения прихода возбуждения не регистрируются. Все участки эпикарда желудочковой поверхности деполяризуются с одинаковой скоростью.
Невозможность индукции ЭКС тахикардии также является доказательством эффективности выполненной операции.
При левосторонней локализации добавочного проводящего пути доступ к пучку Кента аналогичен доступу к митральному клапану (в межкавальном промежутке). У больных с синдромом WPW сердце обычно нормальных размеров. Поэтому разрез межпредсердной перегородки следует продлить на легочные вены. Тем не менее обзор кольца митрального клапана не всегда бывает достаточным. В этих случаях улучшить доступ к клапану можно смещением всего сердца кверху. Разрез эндокарда в месте расположения пучка Кента делают отступя от кольца митрального клапана 1—1,5 мм (рис. 4.23). Разрезают подлежащий мышечный слой на всем протяжении (весь разрез около 4 см). Подэпи-кардиальная клетчатка содержит левую венечную артерию и венечный синус. Мы предпочитаем обнажать эти сосуды частично, чтобы затем под контролем зрения их отвести. Освобождают края предсердия и желудочка от жира, тщательно отрезают каждое волоконце, соединяющее предсердие и желудочек. Очищенные поверхности краев предсердия

1—II отведение ЭКГ; 2—референтная электрограмма (реф ЭГЖ) из области выходного отдела правого желудочка; 3—электрограмма (би ЭГЖ) из 13-й точки (правая задне-пристеночная локализация). Картирующая ЭГ опережает референтную на 120 мс.
503


4.23. Схематическое изображение устранения левого пристеночного добавочного атриовентрикулярного пути. Доступ к сердцу в межкавалыюм промежутке. ВС—венечный синус; ВА—венечная артерия; ЛП—левое предсердие; Л Ж—левый желудочек; МК—митральный клапан.
и желудочка аккуратно коагулируют. При этом наружный слой эпикарда повреждать не следует. Он служит достаточно эффективным барьером для профилактики кровотечения. Рану левого предсердия ушивают однорядным непрерывным швом, а разрез межпредсердной перегородки—двухрядным швом. Проводится тщательная профилактика воздушной эмболии. «Согревают» больного и восстанавливают сердечную деятельность. После нормализации гемодинамики и отключения АИК осуществляют контроль за эффективностью проведенной операции.
Особенностью операции при переднеперегородочной локализации пучка Кента являются наличие в составе подэпи-кардиального жира правой коронарной артерии и необходимость предпринимать дополнительные меры предосторожности, чтобы ее не повредить. При заднеперегородочной локализации пучок Кента проходит в очень сложных анатомических структурах—заднем пирамидальном пространстве. Основным элементом, вокруг которого проводятся манипуляции, является коронарный синус.
После выполнения операции при перегородочных локализациях пучка Кента контроль за устранением предвоз-буждения такой же, как и при других локализациях, описанных выше.
Изложенные методы операций были в основном разработаны W. Sealy. Они являются общепринятыми. К сожалению, некоторые из них технически очень сложны, особенно при левосторонней и заднеперегородочной локализациях пучка Кента.
Эпикардиальный доступ. Одним из методов, уменьшающих риск хирургического вмешательства, является эпикардиальная электродеструкция. Этот метод в деталях разработан в ИССХ им. А. Н. Бакулева АМН СССР. Применение ее основано на том, что пучок Кента расположен эпикардиально. Локальное электрошоковое воздействие вызывает ограниченную электрокоагуляцию и разрыв тканей
504
с последующим замещением жировой и мышечной ткани нежным соединительнотканным рубцом.
Операция проводится по следующей схеме. После рассечения грудины и вскрытия перикарда осуществляют картирование для установления локализации пучка Кента, вызывают и прерывают тахикардию, определяют точку Венкебаха, антеградную и ретроградную проводимость. Затем вводят канюлю в аорту и полую вену, подключают АИК и начинают перфузию (при температуре 37 "С, что позволяет сохранить ЭКГ с характерными признаками предвозбуждения). В зоне расположения пучка Кента (после пережатия полых вен) через наконечники шаровой конфигурации диаметром 5 мм наносят электроразряды (рис. 4.24). С предсердной стороны атриовентрикулярной борозды наносят обычно 3— 4 разряда с энергией 50 Дж, достаточной для разрушения пучка Кента. Однако в некоторых случаях этой энергии мало. При «глубоком» залегании пучка Кента или разветвленном его варианте мы наносим такое же количество разрядов на желудочковый конец атриовентрикулярной борозды с энергией 150—200 Дж.
Эффект операции определяется незамедлительно по исчезновению Д-волны. Примерно в 10—15% случаев после электровоздействия развивается преходящая полная поперечная блокада. Она продолжается не более 2—5 мин. В этих случаях ИК продолжается и после восстановления синусового ритма проводится проба на эффективность операции, как указано выше. На этом операция заканчивается.
Преимущества этой операции очевидны. Однако решить вопрос о том, насколько она целесообразна при всех локализациях пучка Кента, можно лишь в результате анализа большого числа наблюдений. Пока в пользу этой операции свидетельствуют предельная простота ее выполнения, исключение ряда осложнений, свойственных кардиоплегии, а также безопасность.
Хирургическая коррекция других форм синдромов предвозбуждения. Тракт Магейма по анатомическому расположению хотя и отличается от пучка Кента, однако оперативное пособие при его устранении сходно с таковым при синдроме Вольфа—Паркинсона—Уайта. Нодовентрикулярная тахикардия у больных с трактом Магейма обусловлена механизмом риентри с вовлечением в круг предсердно-желудочково-го узла.
Операция выполняется в условиях нормотермической перфузии. Перед началом ИК вызывают тахикардию и картируют желудочек. При этом область тракта Магейма в перегородке активируется наиболее рано. Картирование приходится выполнять после подключения ИК. Если добавочный путь локализован, устранить его можно двумя путями: послойным рассечением эндокарда и миокарда предсердия или криовоздействием при температуре -60 С в течение 2 мин. Показателем адекватности воздействия являются прекращение тахикардии и невозможность повторного приступа. Наименее разработанной является операция при наличии у больного нодовентрикулярного или фасцику-ловентрикулярного тракта. Когда это соединение начинается от предсердно-желудочкового узла, можно предположить, что оно локализовано в правом желудочке. Если оно начинается от предсердно-желудочкового пучка, то локализуется одинаково часто как в правом, так и в левом отделе. Топическая диагностика затруднительна. Поэтому мы выполняем операцию по определенной схеме.

4.24. Схематическое изображение метода эпикардиального электровоздействия на пучок Кента.
Разряд с энергией в 50 Дж со стороны предсердного отдела пучка Кента и в 150 Дж со стороны желудочкового конца пучка Кента в месте приложения наконечника вызывает ограниченную коагуляцию и некроз ткани. Это приводит к прекращению проводимости по пучку Кента и выключению составного элемента риентри. П—предсердие; Ж—желудочек; ПЖБ—предсердно-.желудочковая борозда; В А—венечная артерия; 3—зона электродеструкции; ДПЖС—дополнительное предсердно-желудочковое соединение.
После вскрытия перикарда проводят полное картирование сердца на синусовом ритме, чтобы выявить преждевременную активность. Затем эту процедуру выполняют на фоне индуцированной тахикардии. При этом зона предвозбуждения может регистрироваться в зоне внедрения волокон Магейма в сократительный миокард. Обычно эта область граничит с межжелудочковой перегородкой. Вот почему на современном этапе наших знаний и диагностических возможностей на операционном столе должна быть выполнена процедура по устранению этого тракта с обеих сторон межжелудочковой перегородки. Приводим пример из нашей практики.
Операция сделана 5-летней девочке. Основным проявлением болезни была непрерывно рецидивирующая желудочковая тахикардия. При внутрисердечном электрофизиологическом исследовании установлено, что у больной имеется добавочное нодовентрикулярное соединение. Из-за непрерывно рецидивирующих приступов тахикардии с ухудшением гемодинамики и неэффективности консервативной терапии была рекомендована операция.
При картировании на операционном столе установлено, что наиболее ранняя активность фиксируется в перегородке. После подключения АИК при нормальной температуре было вскрыто правое предсердие и произведены эндокардиаль-ные разрезы и криовоздействие, которые должны были изолировать тракт Магейма, если бы он располагался справа. Проведение программированной стимуляции показало, что добавочный путь не устранен: тахикардия сохранилась. Операция продолжалась в условиях И К. Температура тела больного снижена до 28 С. После кардиоплегии вскрыта меж-
505
предсердная перегородка изнутри, благодаря чему стал доступен митральный клапан и часть левого желудочка. Сделан разрез и осуществлено криовоздействие, изолирующее тракт Магейма слева. Ушит разрез перегородки, а затем предсердия. Восстановлена сердечная деятельность. Восстановился синусовый ритм. Тесты на вызывание тахикардии отрицательные. Операция закончена обычным путем. В последующие два года у больной приступов не наблюдалось.
В настоящее время рано говорить о результатах хирургического лечения синдромов предвозбуждения. Суммарный опыт операций при синдроме Вольфа—Паркин-сона—Уайта не превышает 1000 операций. Количество операций при тахикардиях, обусловленных наличием трактов Магейма или Джеймса, вообще исчисляется единицами. Результаты хирургического лечения непрерывно улучшаются. Большое значение имеет локализация пучка Кента. При правосторонней пристеночной локализации получены почти 100% оптимальные результаты во всех специализированных отделениях.
При левосторонней пристеночной локализации положительные результаты составляют 90—95%, при перегородочной—80—95%. В этой последней группе больных чаще бывают полная поперечная блокада и повторные операции. Это связано с близким расположением пучка Кента к пред-сердно-желудочковому узлу.
Вместе с тем адекватное устранение добавочных проводящих путей полностью излечивает больного, освобождает его от приступов и приема антиаритмических препаратов.
4.5. НАДЖЕЛУДОЧКОВАЯ ТАХИКАРДИЯ
Наджелудочковая тахикардия характеризуется учащением сердечного ритма более 100 ударов в минуту с неизмененной формой комплекса QRS.
Изложение данного раздела мы условно разделили на две части. В первой освещены наджелудочковые тахикардии (ри-ентри-тахикардии): синусно-предсердная, внутрипредсерд-ная и внутриузловая предсердно-желудочковая, так называемая пограничная тахикардия, а также эктопическая предсердная тахикардия. Во второй дан анализ современного состояния проблемы изучения трепетания предсердий.
Клиническое течение всех наджелудочковых тахикардии определяется состоянием сердечного выброса в момент приступа. Последний, особенно при отсутствии сопутствующей кардиальной патологии, зависит от числа желудочковых сокращений. Поэтому самочувствие больного бывает однотипным при разных тахикардиях. Механизмы развития могут отличаться. Выявление их важно для выбора методов лечения.
Несмотря на то что тахикардия как патологическое состояние была известна еще в прошлом веке, истинное разграничение тахиаритмий на наджелудочковые и желудочковые стало возможным лишь после появления электрокардиографии. Неудивительно, что и в настоящее время бывают ситуации, когда только квалифицированное электрофизиологическое исследование позволяет определить, находится ли очаг аритмии выше или ниже предсердно-желудочкового узла.
Мерцательная аритмия (фибрилляция предсердий) впервые упоминается в научной литературе в работе Вулпиана (1874), который наблюдал ее в эксперименте на собаке и назвал mouvement fibrillaire. В клинической практике эта патология впервые упомянута Герингом в 1908 г. под названием pulsus irregularis perpetuus. Он отметил отсутствие волны Р,
но не сумел доказать идентичность этой аритмии с мерцательной аритмией. В 1909 г. Левайс, а также Ротбергер и Вантерберг первыми в клинической практике описали мерцательную аритмию как исключительно частую патологию. Трепетание предсердий в эксперименте на собаках впервые наблюдал Мак-Виллиам в 1887 г. Клиническое описание данной патологии впервые приведено Джолли и Ритчи в 1911 г. Синусно-предсердная риентри-тахикардия впервые описана более 40 лет назад Баркером и соавт. (1943). Однако диагностика этого заболевания и в настоящее время очень трудна и возможна только с помощью программируемой электрической стимуляции сердца.
Внутриузловая (атриовентрикулярная) риентри-тахикардия была описана в 1913 г. Mines. Тогда же он высказал предположение, что этот механизм является основной причиной наджелудочковых тахикардии. Уже в 60-е годы XX в. были установлены факты продольной диссоциации предсер-дно-желудочкового узла на два пути, приводящей к поддержанию тахикардии. Этот механизм оказался наиболее типичным при наджелудочковых тахикардиях у людей. Эктопические тахикардии, в основе которых лежит механизм повышенного автоматизма, описали Венкебах и Витенберг в 1927 г.
В структуре заболеваемости частота наджелудочковых тахикардии составляет 4/5 от всех тахиаритмий. Она регистрируется у 1,1% всех госпитализируемых больных. Абсолютные значения распространенности отдельных форм наджелудочковых тахикардии изучены недостаточно полно. Большую роль должен сыграть метод холтеровского мони-торирования в амбулаторных условиях. Он значительно повышает процент выявляемое™ тахиаритмий.
Из возвратных наджелудочковых тахиаритмий наиболее часто встречается узловая тахикардия, затем синусовая и, наконец, внутрипредсердная. Мерцательная аритмия—наиболее частая форма тахиаритмий. Мерцательной аритмией страдает 0,4% всего населения земного шара. Особенно часто мерцательная аритмия наблюдается при заболеваниях, способствующих увеличению размеров левого предсердия (митральный стеноз, ДМПП). У этого контингента больных частота мерцательной аритмии достигает 25—40% [Coumel P., 1984].
Этиология. Наджелудочковые тахикардии могут проявляться на фоне ревмокардита, ишемической болезни сердца, гипертонической болезни, тиреотоксикоза, эмболии легочной артерии, ВПС (ДМПП), пролапса митрального клапана, острого перикардита, острого инфаркта миокарда. Часто наджелудочковая тахикардия является симптомом синдрома предвозбуждения желудочков. В наименее выраженной форме наджелудочковая тахикардия является индивидуальной реакцией на гипервентиляцию, эмоциональный стресс, алкогольную интоксикацию, частое курение, прием кофе.
Патогенез наджелудочковых тахикардии. В основе большинства наджелудочковых тахикардии лежит механизм повторного входа возбуждения (риентри). Примерно в 70% случаев в круг повторного входа вовлечен предсердно-желу-дочковый узел, в 20% — одновременно синусно-предсер-дный узел и предсердие, в 6—9% — только синусовый узел, в 1—4% — только предсердие.
Узловая предсердно-желудочковая риентри-тахикардия возникает при продольной диссоциации предсердно-желудоч-кового узла на два пути: медленный путь (а-путь) и быстрый (Р-путь) (рис. 4.25). Рефрактерный период медленного пути короче, чем быстрого. Во время синусового ритма импульс из предсердия проходит по быстрому пути и вызывает формирование единичного комплекса QRS. Распространяясь по медленному пути, импульс достигает предсердно-желудочкового пучка вскоре после того, как произошла его деполяризация и установилась рефрактерность от воздействия импульса, пришедшего по быстрому пути. При возникновении предсердной экстрасистолы импульс блокирует-
506

Повторный вход возбуждения обусловлен продольной диссоциацией предсердно-желу-дочкового узла на а- и fi-nymu (двойные пути). Объяснение в тексте.
ся в быстром пути из-за его более длинной рефрактерности, но продвигается по медленному пути. В тех случаях, когда движение импульса по медленному пути настолько замедленно, что другой, быстрый путь успевает восстановиться, на ЭКГ отмечается лишь так называемая предсердная эхо-инвертированная волна Р после комплекса QRS.
Ранняя предсердная экстрасистола также блокируется в быстром пути; но продвижение импульса по медленному пути еще более замедляется, что создает условия для ретроградной активности р-пути. Поэтому на ЭКГ регистрируется эховолна предсердия. Однако из-за большей продолжительности времени проведения в антеградном направлении время восстановления а-пути становится достаточным. Импульс из быстрого пути вновь входит в а-путь и развивается тахикардия. Концепция двойных путей проведения в пред-сердно-желудочковом узле и взаимосвязь процессов проводимости и рефрактерности—двух путей внутриузлового проведения — доказаны в клинических условиях методом программируемой электрической стимуляции сердца.
Механизм повторного входа возбуждения в синуснопред-сердном соединении принципиально схож с тем, который наблюдается в предсердно-желудочковом узле. В синусно-пред-сердном узле при определенных условиях развивается функциональная диссоциация с блокадой синоатриального проведения, что может приводить к развитию тахикардии. Имеются клинические наблюдения, доказывающие, что предсердная экстрасистола приводит к развитию синусовой тахикардии.
Органическим субстратом, принимающим участие в формировании круга риентри. является зона между синусно-предсердным узлом и пограничным гребнем, содержащая синоатриальные перинодальные волокна. В этой зоне происходит задержка входа и выхода волны нормального возбуждения. Доказана также возможность функциональной диссоциации пучка Бахмана в возникновении риентри и рецип-рокной наджелудочковой тахикардии.
Как и при синусовой риентри-тахикардии, при внутри-предсердной тахикардии повторного входа возбуждения возникновение и продолжение тахикардии возможны на фоне атриовентрикулярной блокады, что указывает на то, что в ее формировании могут не участвовать отделы проводящей системы, располагающиеся ниже предсердно-желудоч-кового узла. Внутрипредсердная тахикардия всегда развивается на фоне органических изменений миокарда предсердия. Время проведения импульса по предсердию во время приступа отличается от времени, регистрируемого при синусовом ритме или антеградной стимуляции. Время активации верхнего отдела предсердия, области венечного синуса
и предсердно-желудочкового пучка при тахикардии может отличаться, что исключает участие этих отделов в тахикардии, но устанавливает пассивную активацию этих участков из зоны риентри. Особое значение при исследовании следует уделять изучению зубца Р на ЭКГ. При синусовой или внутрипредсердной тахикардии характерной особенностью являются идентичность волны Р во время синусового ритма и тахикардии, нормальное значение интервала А—Н. Частота сокращений сердца обычно меньше, чем при реципрокной тахикардии предсердно-желудочкового узла. Характерной особенностью наджелудочковой риентри-тахикардии является возможность ее индукции или купирования предсерд-ной или желудочковой экстрасистолой при программированной стимуляции (табл. 4.4). Если это происходит при критическом значении интервала Р—R, то, следовательно, в круг вовлечен предсердно-желудочковый узел. Длительность цикла при возникновении пароксизма всегда одна и та же.
Продолжительность цикла тахикардии остается одной и той же в течение всего приступа.
Если при пароксизме тахикардии зубец Р экстрасистолы не отличается от предыдущего, фиксируемого при синусовом ритме, то причиной возникновения пароксизма можно считать автоматическую (эктопическую) активность миокарда предсердий. Если же зубец Р экстрасистолы и предыдущего сокращения не похожи, то следует думать о механизме риентри. Очень важна для диагностики конфигурации зубца Р и комплекса QRS. Так, отсутствие зубца Р во время приступа тахикардии свидетельствует о риентри в предсердно-желудочковом узле. Сказанное справедливо и для случаев инвертированного зубца Р. У больных с нормальным значением интервала Р—R во время основного ритма тахикардия является либо повторным входом возбуждения в синусно-предсердном узле, либо внутрипредсердной тахикардией. Полезны для дифференциальной диагностики лекарственные и физиологические пробы. Так, если при надавливании на каротидный синус тахикардия сохраняется, но развивается и атриовентрикулярная блокада, то участие предсердно-желудочкового узла в риентри-тахикардии маловероятно. Если эта проба прекращает приступ тахикардии, то можно думать об участии в круге
507
Таблица 4.4. Дифференциальная диагностика наджелудочковых риентри-тахикардий (НЖТ)

Диагноз эктопической тахикардии (табл. 4.5) ставят, если: 1) тахикардия начинается спонтанно с «разогрева», т. е. периода учащения ритма в начале пароксизма; 2) тахикардию невозможно вызвать или прекратить программированной стимуляцией; 3) при электрофизиологическом исследовании не удается установить наличие двойного проведения (двойных путей).
Таблица 4.5. Дифференциальная диагностика риент-ри- и эктопической предсердной тахикардии

Клиника. Клинически пароксизмы предсердной тахикардии начинаются и обрываются внезапно и могут продолжаться от нескольких секунд до нескольких часов или дней. Частота сердечных сокращений во время приступа различна и может колебаться от 160 до 260 в минуту. В анамнезе у больного бывает упоминание о предсердных экстрасистолах, частота которых со временем увеличивается и однажды провоцирует приступ тахикардии. Приступы могут возникать эпизодически (один раз в неделю, .месяц или еще реже) или очень часто (несколько раз в день). Во время приступа желудочковые сокращения носят регулярный характер.
Симптоматика типична для любого быстрого ритма и зависит от состояния сердечной мышцы, способности последней приспосабливаться к тахикардии, от продолжительности приступа, эмоционального состояния больного. Короткие пароксизмы могут даже не беспокоить больного, он лишь отмечает сердцебиение.
При длительных приступах с большой частотой желудочковых сокращений, особенно при наличии порока сердца или ИБС, симптоматика становится ярко выраженной. Она характеризуется различной степенью дискомфорта или даже болями за грудиной, одышкой, слабостью, головокружением, обмороком.
Признаки пароксизмальной тахикардии обусловлены - ускоренным правильным ритмом. Пульс быстрый, слабого наполнения. В этот период возможны падение артериального давления, острое развитие недостаточности кровообращения и сердечной недостаточности. Такая симптоматика и присоединяющаяся стенокардия особенно часто наблюдаются на фоне ИБС. Типична полиурия, которая наблюдается во время приступа тахикардии. Повышенный диурез (до 8 л) появляется сразу после начала пароксизма и может длиться 30—90 мин. Он обусловлен подавлением секреции АКТГ. Влияние тахикардии на сердечную гемодинамику зависит от частоты сердечных сокращений, продолжительности приступа, сохранения синхронизации функции предсердий и желудочков, а также от сопутствующей кардиальной патологии. В здоровом сердце тахикардия с сохранением антеградного проведения с частотой сердечных сокращений не более 140 в минуту приводит к увеличению сердечного выброса. При дальнейшем учащении ритма период наполнения желудочков укорачивается, а ударный выброс уменьшается. При сопутствующей патологии снижение сердечного выброса происходит и при менее выраженной тахикардии. Таким образом, наджелудочковая тахикардия без органической патологии сердца первоначально незначительно изменяет сердечный выброс. Однако длительный пароксизм ухудшает гемодинамику. Постепенно снижается систолическое, диа-столическое и пульсовое артериальное давление, увеличивается левопредсердное давление и падает ударный выброс. В отличие от этого при тахикардии, обусловленной физиче-
508
ской нагрузкой, ударный выброс не изменяется или возрастает, что приводит к значительному увеличению сердечного выброса.
На ЭКГ комплексы QRS обычно не расширены, число сердечных сокращений 160—240 в минуту. Волна Р очень характерна по конфигурации—она обычно наслаивается на волну Т предыдущего сокращения, поэтому их трудно различить. В этих случаях, чтобы установить характер ЭКГ, необходимо зафиксировать либо начало тахикардии, либо ее конец. Если это не удается, можно сделать массаж каротид-ного синуса, что очень часто дает возможность установить генез предсердных аритмий. Дальнейшее смещение волны Р и ее слияние с комплексом QRS наблюдаются при узловой, «пограничной» тахикардии. При пароксизмальной наджелудочковой тахикардии комплекс QRS обычной продолжительности. Возможно, однако, его расширение, если импульс поступает в проводящую систему в период относительной рефрактерное™. Это может усложнить диагностику предсердной тахикардии. Дифференциальная диагностика такой тахикардии с желудочковой тахикардией приобретает исключительно важное значение, так как методы лечения и прогноз различны. У больных, предрасположенных к развитию наджелудочковой тахикардии, на фоне синусового ритма обычно выявляются частые или спаренные предсер-дные экстрасистолы.
Большое значение имеет переходный период между приступом и синусовым ритмом, поскольку в это время возможно развитие либо асистолии, либо преходящей желудочковой тахиаритмии. Период переходной аритмии зависит от метода восстановления исходного ритма (массаж каротид-ного синуса, электрическая дефибрилляция). Переходная ЭКГ может иметь различный вид: 1) асистолия до 6 с с восстановлением синусового ритма; 2) едва уловимое замедление ритма, за которым следует внезапный переход к нормальному ритму; 3) внезапное восстановление ритма; 4) замедление, асистолия и затем восстановление ритма; 5) желудочковая тахикардия; 6) предфибрилляторная желудочковая аритмия и экстрасистолия с дальнейшей нормализацией ритма. Врач должен помнить об этом полиморфизме изменений ЭКГ ритма, чтобы не растеряться и не сделать ошибки.
Многоочаговая, или хаотическая, предсердная тахикардия—это тахикардия с частотой более 100 в минуту, изменяющейся формой зубца Р и интервалов Р—R, Р—Р и R—R, она обычно наблюдается у людей старшего возраста с сопутствующей патологией (чаще всего с легочным сердцем). Многоочаговая тахикардия может быть предвестником мерцательной аритмии, с которой ее часто путают. Она может сочетаться с атриовентрикулярной блокадой I—II степени, особенно развивающейся в результате приема препаратов дигиталиса. Эту тахикардию очень важно отличать от мерцательной аритмии, поскольку дигиталис эффективен при мерцании и не эффективен при хаотической предсердной тахикардии.
Ритм обычно не очень частый, но трудно поддается коррекции. Тахикардия устойчива не только к ваготоническим и холинергическим препаратам, хинидину, новокаинамиду, лидокаину, изоптину, но и плохо купируется электрической дефибрилляцией.
Возвратная предсердная тахикардия характеризуется короткими пароксизмами предсердной тахикардии
(3—8 сокращений), изредка прерываемыми 1—2 синусными сокращениями. Она еще более рефрактерна к лекарственной терапии, чем непрерывно рецидивирующая предсердная тахикардия.
Диагностика. Пароксизмальную наджелудочковую тахикардию можно заподозрить у больного, предъявляющего жалобы на внезапное учащение работы сердца, внезапно начинающиеся и внезапно прекращающиеся пароксизмы. Наличие предсердных экстрасистол на фоне регулярной тахикардии с частотой 160—240 в минуту дополняет диагноз пароксизмальной наджелудочковой тахикардии. Изменения ЭКГ характерны: 1) зубец Р во время приступа отличается от такового при синусовом ритме, приближается и/или сливается с предшествующей волной Т; 2) ритм во время приступа правильный; 3) комплекс QRS обычно не изменен (иногда возможна аберрация); 4) первое нормальное сокращение после пароксизма возникает после паузы. Иногда бывает трудно определить истинный механизм тахикардии либо из-за очень быстрого ритма и недостаточной выраженности предсердного комплекса на ЭКГ, либо из-за широких комплексов QRS. В этом случае полезно сделать массаж каротидного синуса. Электрофизиологическое исследование позволяет, во-первых, установить механизм тахикардии (эктопическая или риентри), а во-вторых, определить уровень нахождения аритмогенной зоны. Если при программируемой стимуляции или сверхчастой стимуляции удается «запустить» или прекратить тахикардию, то риентри-тахикар-дия считается доказанной.
Для доказательства уровня аритмогенной зоны в сердце вводят несколько электродов, располагающихся в области синусно-предсердного узла, верхнего, среднего и нижнего отделов правого предсердия, левого предсердия (венечный синус), в проекции предсердно-желудочкового пучка. Это позволяет локализовать область, из которой раньше всего регистрируется электрограмма, а также определить, участвует ли синусно-предсердный или предсердно-желудочковыи узел в круге повторного входа возбуждения.
Естественное течение наджелудочковых тахикардии изучено недостаточно. Оно резко осложняется и ухудшает прогноз при: а) длительных приступах (несколько часов и более); б) сопутствующем поражении миокарда, наличии порока сердца или ишемической болезни сердца; в) наличии приступов, несмотря на проводимую терапию; г) появлении загрудинных болей, вплоть до коллапса в момент тахикардии.
Показания к операции ограничены. Только при рефрак-терности к лекарственной терапии ставят вопрос о хирургическом лечении больного с наджелудочковой тахикардией.
Лечение. Следует подходить дифференцированно к лечению больного во время приступа и в межприступном периоде. Приступ тахикардии можно устранить вагусной пробой, внутривенным введением антиаритмического препарата, программированной стимуляцией, наконец, электрической дефибрилляцией.
Консервативное лечение направлено на удлинение проводимости в предсердно-желудочковом узле, изменяющем его рефрактерность. При всех уровнях возникновения наджелудочковой тахикардии такое лечение может иметь самостоятельное или существенное вспомогательное значение.
В межприступном периоде можно рекомендовать: антита-хикардитические стимуляторы, трансвенозную катетерную
509
электродеструкцию предсердно-желудочкового узла (создание полной поперечной блокады с имплантацией ЭКС), хирургическое лечение—закрытые (трансвенозный доступ к сердцу) и открытые операции.
К числу новейших методов лечения рефрактерной и лекарственной терапии наджелудочковой тахикардии относят антитахикардитические стимуляторы. Их действие не излечивает больного, но снимает пароксизмы. Для определенной группы больных (больные старческого возраста, с тяжелыми сопутствующими заболеваниями сердца или других органов) применение таких стимуляторов вполне оправдано.
Хирургическое лечение. При органической синусовой тахикардии в настоящее время используют один из основных методов лечения: создают полную поперечную блокаду с имплантацией электрокардиостимулятора или производят резекцию синусно-предсердного узла с начальным отделом пограничного гребня. Разумеется, эта операция физиологична и позволяет сохранить антеградный, предсердный ритм. Все больные, у которых с помощью электрофизиологических методов достоверно установлено происхождение аритмии из синусового узла, в связи с чем выполнена резекция этого узла, хорошо себя чувствовали в течение 8 лет (максимальный срок наблюдения). Они вели привычный образ жизни, не принимали лекарств, у них отмечалась эквивалентная реакция на физическую нагрузку. Аналогичные данные получены в хирургической клинике Дьюкского медицинского центра [Lowe J., 1990], где за больными наблюдали в течение 7 лет. В тех случаях, если выполнить резекцию синусно-предсердного узла с пограничным гребнем не удается, прибегают к созданию полной поперечной блокады. Для этих больных очень важно подобрать оптимальный режим стимуляции. У большинства из них размеры сердца не увеличены и желудочковая стимуляция в режиме «де-манд» может быть недостаточна для поддержания системы кровообращения. У таких больных следует стремиться к проведению стимуляции в частотно-зависимом режиме (см. «Брадиаритмии»).
При локализации очага аритмий в предсердиях или меж-предсердной перегородке независимо от того, наблюдается тахикардия повторного входа возбуждения или эктопическая тахикардия, могут быть выполнены следующие операции:
трансвенозная аблация (деструкция) путем радиоча стотного воздействия, получившая наименование «радиоча стотная аблация»;
изоляция, резекция, криодеструкция или лазерная фото- аблация этой зоны под контролем зрения; электрическая изоляция того предсердия, в котором находится очаг арит мии, а при ее безуспешности выполнение операции «кори дор» или «лабиринт»;
изоляция предсердно-желудочкового узла или криовоз- действие либо лазерное воздействие на него с созданием полной поперечной блокады и последующей имплантацией электрокардиостимулятора. При нормальных размерах же лудочков сердца следует стремиться к имплантации частот но-зависимого электрокардиостимулятора.
При узловых тахикардиях наиболее эффективна операция устранения шунтирующих волокон, позволяющая сохранить естественный синусовый ритм. Эта операция, получившая название «изоляция предсердно-желудочкового узла», безопасна и дает прекрасные отдаленные результаты. Имеются
сообщения о выполнении радиочастотной аблации шунтирующих волокон в электрофизиологическом кабинете. К сожалению, такая процедура часто заканчивается возникновением полной поперечной блокады и имплантацией электрокардиостимулятора.
Идея использования у больных с наджелудочковыми- та-хикардиями закрытых методов лечения получает все большее распространение. В данном случае речь идет о тахикардиях, локализующихся в свободной стенке предсердий, меж-предсердной перегородке или ушках предсердия. Лечение проводят непременно в электрофизиологическом кабинете при выполнении программируемой электрической стимуляции сердца или других электрофизиологических исследований, позволяющих установить локализацию очага аритмии. Первоначально проводят топическую диагностику аритмо-генного очага. Если удалось установить его локализацию, то в предполагаемой области выполняют радиочастотную аб-лацию, что приводит к подавлению патологического очага, нормализации ритма и ЭКГ. Наиболее легко подавляются эктопические фокусы, располагающиеся в ушках предсердий. В тех случаях, когда радиочастотная аблация неэффективна, сохраняется рефрактерность к лекарственной терапии, а опасность выполнения открытой операции превышает допустимый риск, производят закрытую трансвенозную ка-тетерную деструкцию предсердно-желудочкового узла. Эта процедура приводит к созданию полной поперечной блокады. Затем имплантируют электрокардиостимулятор.
Хирургические методы лечения наджелудочковой тахикардии разработаны в конце 70-х годов. Рассмотрим важнейшие из них. Как правило, операции выполняют в условиях искусственного кровообращения, однако при доступности эктопического очага (ушко правого или левого предсердия, свободная стенка), когда можно обойтись без искусственного кровообращения, операция может быть выполнена без него. Главное—локализовать очаг тахикардии. Это достигается эпикардиальным картированием. Вызывают тахикардию программированной стимуляцией или сверхчастой стимуляцией.
Предсердие условно разделено на 64 зоны. Последовательно картируют оба предсердия. Электрограмма аритмо-генной зоны «опережает» электрограмму референтной области на 80—130 мс. Локализованную зону аритмии можно резецировать или устранить ее активность криовоздействи-ем. Обе процедуры полностью устраняют тахикардию. Повторяют процедуру «провокации» тахикардии частой стимуляцией или программированной стимуляцией. Это дает возможность оценить адекватность «разрушения» арит-могенной зоны, а также выявить другие источники тахикардии.
Приводим клинический пример.
Больной И., 13 лет, предъявлял жалобы на постоянное сердцебиение, слабость, головокружение, одышку при физической нагрузке. Он наблюдался и лечился во многих стационарах страны: педиатрических, кардиологических, хирургических. Была диагностирована непрерывно рецидивирующая наджелудочковая тахикардия. При электрофизиологическом исследовании установлено, что она имеет эктопический генез (не купировалась и не вызывалась программируемой стимуляцией). Антиаритмическая терапия с применением препаратов широкого спектра действия в течение более одного года была безуспешной. Предложена операция. Во время операции было проведено эпикардиаль-ное картирование, позволившее локализовать очаг арит-
570

Очаг аритмии локализован в основании ушка левого предсердия ( — 103 мс). Ао — аорта; ТР — легочный ствол; VCS—верхняя полая вена; VCI—нижняя полая вена; LAA—ушко левого предсердия; RAA — ушко правого предсердия; CS—венечный синус; PV—легочные вены.
мии,— эктопический фокус располагался в основании ушка левого предсердия (рис. 4.26). В условиях нормотермиче-екого ИК эктопический очаг был подавлен криовоздействи-ем при температуре — 60° С в течение 2 мин. Послеоперационный период протекал гладко. Последующее обследование в течение 2 лет свидетельствовало об эффективности выполненной операции—состояние больного улучшилось, у него сохранялся синусовый ритм.
Изоляция предсердно-желудочкового узла при узловой тахикардии. В 1984—1985 гг. D. S. Johnson и D. L. Ross, сотрудники университетской клиники Сиднея (Австралия), предложили операцию по радикальному устранению узловой риентри-тахикардии. Они выделили два типа шунтирующих волокон при этом виде тахикардии: тип А (супермедиальное расположение зоны ранней активации по отношению к предсердно-желудочковому узлу) и тип Б (постлатеральное расположение зоны ранней активации по отношению к предсердно-желудочковому узлу в устье коронарного синуса).
Операцию выполняют в условиях срединной стернотомии. У всех больных осуществляют интраоперационное картирование области расположения предсердно-желудочкового узла в условиях нормотермического искусственного кровообращения после вскрытия стенки правого предсердия. Особенно внимательно проводят картирование области треугольника Коха на индуцированной тахикардии. В результате этого удается установить область раннего ретроградного прорыва возбуждения. По завершении картирования больного охлаждают до 30—28° С, останавливают сердце с помощью кристаллоидной кардиоплегии и выполняют операцию изоляции узла от шунтирующих волокон. Непременным условием успешного выполнения операции является использование оптических очков с увеличением не менее 2,5.
Таким образом, при любом типе узловой предсердно-желудочковой тахикардии доступ к предсердно-желудочко-
вому узлу через правое предсердие. Мы проводим канюля-цию верхней полой вены непосредственно на уровне впадения в нее непарной вены, т. е. выше синусно-предсердного узла. Нижнюю полую вену канюлируем в ее устье через правое предсердие непосредственно над межпредсердной перегородкой. Для обеспечения хорошего обзора разрез предсердия производим на всем протяжении предсердно-желу-дочковой борозды, отступя от нее примерно 1,5 см. В модифицированном нами варианте операции изоляция предсердно-желудочкового узла предполагает проведение разреза от правого фиброзного треугольника на расстоянии примерно 1,5 см от кольца трехстворчатого клапана и параллельно ему до устья коронарного синуса, а затем к кольцу трехстворчатого клапана перпендикулярно ему. В пределах этого разреза рассекают эндокард и подлежащее мышечное образование на глубину не менее 3 мм с таким расчетом, чтобы обнажить межпредсердную перегородку и по возможности удалить жировую ткань, окружающую сосудисто-нервные образования в пределах треугольника Коха. Тщательно изолируют артерию, питающую предсер-дно-желудочковый узел. При использовании оптических линз тело узла на остановленном сердце хорошо видно под эндокардом. Это позволило нам расширить уровень изоляции узла и уменьшить количество послеоперационных рецидивов. Дополнительно к первому разрезу мы выполняем разрез непосредственно по кольцу трехстворчатого клапана и таким образом изолируем тело предсердно-желудочкового узла от шунтирующих волокон и с дистальной стороны. На рис. 4.27 представлены варианты оперативного вмешательства, предложенные D. S. Johnson и D. L. Ross (а—г) и вариант операции, выполняемой нами (д).
Операция электрической изоляции левого предсердия. Эту операцию производят в тех случаях, когда эктопических очагов несколько и они локализованы в левом предсердии или известно, что очаг находится в левом предсердии, но его
511

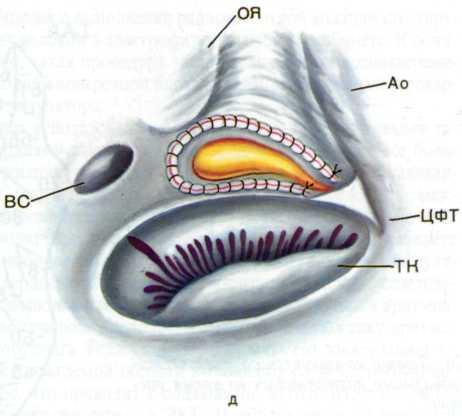
4.27. Операция изоляции предсердно-желудочкового узла при узловой риентри-тахикардии.
Методика Джонсона — Росса: а — / этап расслоения зндоми-окарда с отведением стенки правого предсердия для доступа к заднему перегородочному пространству. TV—трехстворчатый клапан; RVFW—стенка правого желудочка; C.S.— коронарный синус: Т of T—сухожилие Тодаро; б — // этап расслоения эндомиокарда С обнажением жизненно важных образований заднего перегородочного пространства. Перино-дальные ткани предсердно-желудочкового узла могут быть видимы. При выраженном .жировом слое следует выделить артерию узла и отвести ее кпереди. AVN— пространство предсердно-желудочкового узла; CFB— центральное фиброзное тело; LAS—перегородка левого предсердия; в—расслоение эндомиокарда при типе А узловой тахикардии. Резецируют мышечный массив над перегородкой левого предсердия с переходом на центральное фиброзное тело; г—расслоение при типе Б узловой тахикардии. Освобождают от .жира свободную стенку правого желудочка до предсердно-желудочкового узла. Под артерией узла освобождают все жировое пространство вплоть до правой коронарной артерии; д — схематическое изображение операции изоляции предсердно-желудочкового узла в модификации Л. А. Бокерия. Разрез эндомиокарда начинают от центрального фиброзного тела (ЦФТ). продолжают, отступя от проекции узла примерю 1,5 см, к верхнему краю коронарного синуса и от него к фиброзному кольцу трехстворчатого клапана (ТК). Выделяют артерию узла и под ней освобождают от жира все пространство, а в зонах, не содержащих жира, делают разрез глубиной до 3 мм. Затем разрез проводят по фиброзному кольцу в медиальную сторону и под контролем оптических линз доводят до тела узла. В пределах этого разреза освобождают подлежащие ткани. В результате формируется изолированный блок тканей, не содержащих элементов, соединяющих эту область с окружающей тканью. Восстановление целостности достигается использованием пролена 6/0.
512
не удалось точно лоцировать. Операция была предложена в эксперименте одним из крупнейших специалистов в области аритмологии J. Сох в 1980 г. Первая успешная операция в клинике был выполнена в ИССХ им. А. Н. Бакулева. Вмешательство выполняют в условиях искусственного кровообращения и холодовой кардиоплегии. После остановки сердца производят разрез в межкавальном промежутке, аналогичный разрезу, используемому для обеспечения доступа к митральному клапану (рис. 4.28). Мягко отводят межпредсердную перегородку и далее проводят атриотомию кпереди, вдоль пучка Бахмана к кольцу митрального клапана, строго слева от правого фиброзного треугольника (см. рис. 4.28, а). Передний разрез левой атриотомии завершен. Обращаем внимание на то, что этот разрез проходит через фиброзное кольцо митрального клапана, основная масса левого предсердия теперь отделена спереди от остального сердца (см. рис. 4.28, б). Трансмуральную атриотомию левого предсердия затем продолжают кзади до уровня коронарного синуса. Далее разрез идет по эндокарду, переходя через кольцо митрального клапана кзади, точно слева от межпредсердной перегородки. Это то место, где имеется проведение между правым и левым предсердием в отноше-
4.28. Схематическое изображение операции электрической изоляции левого предсердия. Объяснение в тексте.
нии 1:1 из-за наличия межпредсердного мышечного соединения, проходящего в составе коронарного синуса (см. рис. 4.28. в).
Завершающим моментом электрической изоляции левого предсердия является криовоздействие (-60 С в течение 2 мин) в задней части атриотомии. Оно направлено на прекращение деятельности межпредсердных волокон, проходящих в составе коронарного синуса. Аналогичное криовоздействие проводят с эпикардиальной стороны предсер-дно-желудочковой борозды на противоположной стороне коронарного синуса, чтобы подавить активность межпредсердных эпикардиальных проводников. Затем все разрезы ушивают в обратной последовательности и осуществляют восстановление сердечной деятельности с профилактикой воздушной эмболии по принятой методике. В тех случаях, когда в дополнение к этой операции выполняют вмешательство на митральном клапане, последовательность этапов варьирует: при пластической операции сначала выполняют пластику митрального клапана, а затем все компоненты операции изоляции, а при протезировании клапана в полном объеме производят операцию изоляции левого предсердия, а затем имплантацию клапана и ушивание разреза в межкавальном промежутке.
Операция электрической изоляции обоих предсердий (операция «коридор»). Основное назначение этой операции, идея
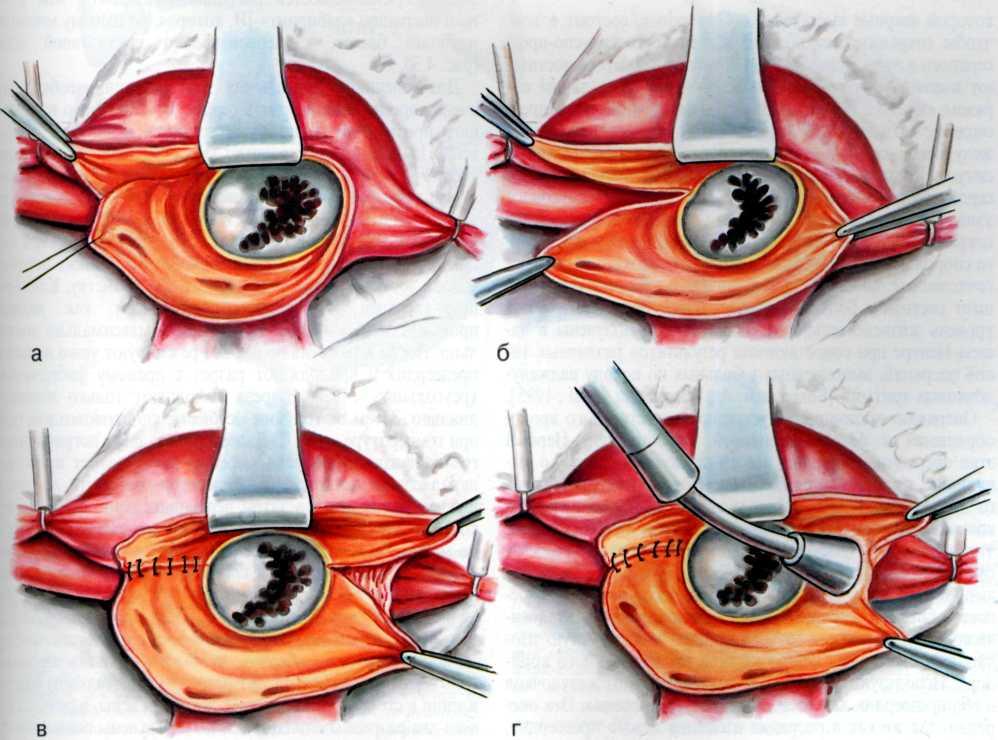
513

4.29. Схематическое изображение операции «коридор». Между синусным узлом и предсердно-желудочковым умом остается узкая полоска миокарда, сохраняющая физиологическую проводимость от синусного узла к желудочкам. СУ—синусный узел; ПП—правое предсердие; ТК—трехстворчатый клапан; АВУ—атриовсптрикулярный (предсер-дно-желудочковый) узел; МК—митральный клапан; ЛП— левое предсердие; КС—коронарный синус.
которой впервые высказана G. Guiraudone, состоит в том, чтобы сохранить синхронную деятельность синусно-пред-сердного и предсердно-желудочкового узлов. Этого достигают изоляцией правого и левого предсердий, и, таким образом, остается небольшой участок мышечной части предсердия, позволяющий обеспечить сокращения обоих желудочков сердца, синхронизированные с сокращениями синусового узла. Таким образом, нагнетательная функция сердца будет обеспечена по условиям работы синусового узла, т. е. естественного водителя ритма; предсердия будут сокращаться в собственном ритме. Операция вызывает много споров как не очень физиологичная (J. Сох), однако многочисленные данные свидетельствуют о том, что она улучшает состояние больного и обеспечивает физиологический уровень жизнедеятельности. Такие данные получены в нашем Центре при сопоставлении результатов различных типов операций, выполненных у больных по поводу наджелу-дочковых аритмий [Бокерия Л. А., Ревишвили А. Ш., 1995]. Операцию производят в условиях искусственного кровообращения и фармакохолодовой кардиоплегии. Первый этап операции—изоляция левого предсердия, которую выполняют, как описано ранее. Второй этап—изоляция правого предсердия. Разрез в форме подковы, опирающейся на кольцо трехстворчатого клапана, проводят таким образом, чтобы отделить свободную стенку правого предсердия от синусно-предсердного узла, как показано на рис. 4.29. После выполнения всех этих манипуляций восстанавливают целость обоих предсердий. Затем проводят электрофизиологическое исследование, подтверждающее электрическую изоляцию предсердий и формирование так называемого коридора. Используют по два электрода на один из желудочков и оба предсердия для последующего тестирования. Эта операция, так же как и операция изоляции левого предсердия,
может быть компонентом реконструктивных вмешательств на клапанах сердца или выполняемых по поводу врожденных пороков сердца, при которых требуется одномоментная коррекция порока сердца и наджелудочковой аритмии.
Операция «лабиринт». Эта операция, предложенная J. Сох, в отличие от предыдущих операций по изоляции одного или обоих предсердий предполагает возможность сохранения синусового ритма или антеградной проводимости во всем сердце. Разработка этой операции стала возможной в результате установления в последние годы того факта, что мерцательная аритмия также относится к тахикардиям типа риентри. но формируется по большому кругу (макрориент-ри) (рис. 4.30, а). Основной смысл операции, позволяющей добиться сохранения антеградной проводимости у больных с наиболее сложными нарушениями ритма, в том числе с мерцательной аритмией, состоит в том. что при ее правильном выполнении вместо трех межузловых путей, функционирующих между синусно-предсердным и предсердно-желудочковым узлами, начинает функционировать один, охватывающий весь миокард обоих предсердий. Операция позволяет установить правильный ритм у лиц с хронической мерцательной аритмией, у некоторых из которых это мерцание продолжалось до 30 лет. Операцию выполняют в условиях искусственного кровообращения и фармакохолодовой кардиоплегии. Некоторые этапы, предшествующие вскрытию левых отделов сердца, могут быть произведены на сокращающемся сердце. В настоящее время существует несколько разновидностей операции «лабиринт». Мы опишем операцию «лабиринт»-Ш. которая, по нашему мнению, наиболее близка к первоначально высказанной идее (рис. 4.30, б).
Для успешного выполнения этой операции необходимо очень хорошо мобилизовать сердце. С этой целью на большом протяжении скелетируют верхнюю и нижнюю полые вены. Выделяют пространство между правой легочной артерией и верхним полюсом межпредсердной перегородки таким образом, чтобы ретрокардиальное пространство из этого доступа стало хорошо видно. В области межкаваль-ного промежутка на большом протяжении—от нижней полой вены до правой нижней легочной вены—также освобождают доступ к ретрокардиальному пространству. Канюля-цию верхней полой вены производят как можно проксимальнее, а нижней полой вены—максимально диста-льно. После пережатия полых вен резецируют ушко правого предсердия и продолжают разрез к правому фиброзному треугольнику. Часть разреза выполняют только эндокар-диально. Затем в этой зоне осуществляют криовоздействие при температуре -60 С. Далее вдоль заднего пограничного гребня вскрывают правое предсердие и разрез проводят параллельно межпредсердной перегородке почти до устья нижней полой вены, а затем перпендикулярно фиброзному кольцу трехстворчатого клапана. Ту часть разреза, которая не может быть выполнена трансмурально, завершают эн-докардиальным разрезом и криовоздействием. Затем в меж-кавальном промежутке делают разрез левого предсердия, аналогичный тому, который производят при формировании доступа к митральному клапану. Разрез продолжают кпереди под аорту таким образом, чтобы изолировать легочные вены. Этот разрез завершают разрезом в дистальном направлении в сторону левой нижней легочной вены, в результате чего два разреза соединяются и легочные вены оказываются
514

сердия; СПУ—синусно-предсердный узел; ЛВ — легочные вены; АВУ—атриовентрикуляриый узел; слева вверху — область криодеструкции; б — операция «лабиринт» в трехпро-екционном изображении сердца no J. L. Сох. Хорошо видны разрезы. Обязательна криодеструкция в области коронарного синуса с внутренней и внешней сторон для прерывания проводимости по межпредсердным волокнам. Сохраняется тканевый мостик в области атриовентрикулярного узла, который позволяет проводить электрический импульс от предсердия на желудочки. Единственным полностью изолированным участком предсердия являются легочные вены; в — операция «лабиринт» III.
515
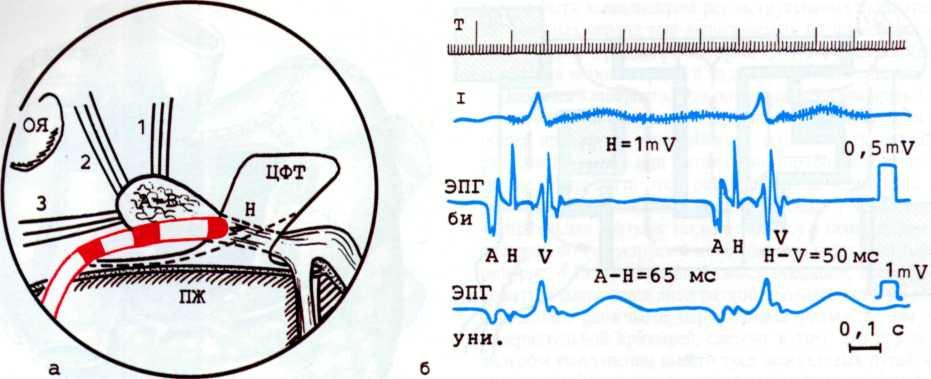
а—электрод, установленный в проекции предсердпо-желудо-чкового узла или предсердно-желудочкового пучка, служит для нанесения электрического разряда, приводящего к перерыву проведения на уровне электровоздействия: б— ЭКГ и ЭПГ при проведении электродеструкции. Электрограмма предсердно-желудочкового пучка зарегистрирована в биполярном (би) и униполярном режиме (уни).
изолированными. Ушко левого предсердия вворачивают внутрь, резецируют и разрез от него продолжают к нижнему краю верхней левой легочной вены.
После этого межпредсердную перегородку в межкаваль-ном промежутке в нижней ее трети рассекают через нижний край овальной ямки и продолжают разрез к митральному клапану, в сторону задней ее створки. Операция может быть дополнена вмешательством на клапанах сердца или перегородках в связи с их дефектами у взрослых больных. Все разрезы ушивают в обратной последовательности; восстанавливают сердечную деятельность.
В доступной нам литературе сообщается примерно о 300 операциях. Все авторы, накопившие достаточный опыт выполнения этой операции без риска для больного, очень высоко ценят ее физиологичность.
Создание полной поперечной блокады на открытом сердце. Эту операцию в настоящее время производят в дополнение к операциям, выполняемым при клапанной патологии или врожденных пороках сердца у взрослых. Для создания блокады можно использовать лазерное воздействие или крио-воздействие.
В последние годы полную поперечную блокаду создают трансвенозным способом, используя метод фульгурации (электродеструкции) либо радиочастотной аблации. В сердце вводят два эндокардиальных электрода. Один, биполярный, устанавливают в правом желудочке. Он служит для «навязывания» ритма после создания блокады. Другой, тет-раполярный, устанавливают в области предсердно-желудочкового пучка (рис. 4.31). В этом месте наносится электрический разряд энергией 250—300 Дж, приводящий к развитию полной поперечной блокады. Электрод служит анодом, пла-
стинка дефибриллятора под спиной больного—катодом. В зависимости от уровня блокады число сокращений желудочков различное—от полной асистолии до 60 в минуту (рис. 4.32) (следует стремиться к созданию высокой блокады). В течение 2—3 дней ЭКС осуществляют через эндокардиаль-ный электрод от наружного стимулятора. Убеждаются, что блокада дает стойкий эффект, и после этого имплантируют постоянный стимулятор. При радиочастотной аблации пучка Гиса процедуру выполняют под местной анестезией и подают на дистальный полюс электрода для аблации разночастот-ную энергию 20—30 Вт в течение 30—60 с.
Осложнения после операций устранения очага наджелудо-чковой тахикардии не описаны. Однако число наблюдений незначительно. По нашему мнению, в небольшом проценте случаев следует ожидать рецидивы тахикардии эктопического генеза.
При искусственном создании полной поперечной блокады или электродеструкции предсердно-желудочкового узла трансвенозным методом описаны единичные наблюдения рецидива тахикардии. В этих случаях процедуру повторяют на уровне предсердно-желудочкового пучка. Другое осложнение этой операции—«отказ» электрокардиостимулятора. Реальная угроза для жизни больного создается при очень редком сердечном ритме (5—10 в минуту), что допускается теоретически, однако в литературе не описано. Непосредственные и отдаленные результаты по данным литературы хорошие.
4.6. ТРЕПЕТАНИЕ ПРЕДСЕРДИЙ
Трепетание предсердий—электрокардиографический термин, который характеризует так называемые волны трепетания, представляющие собой регулярные двухфазные осцилляции одинаковой формы. Частота сокращений предсердий при этом колеблется от 200 до 400 в минуту и сочетается с различной степенью блокады сердца. Изоэлектрическая линия на ЭКГ отсутствует, а трепетание предсердий лучше всего определяется в отведениях II, III, aVF и V,.
Трепетание предсердий проявляется как установившееся нарушение ритма или, чаще, как пароксизмальное. преходящее состояние.
516
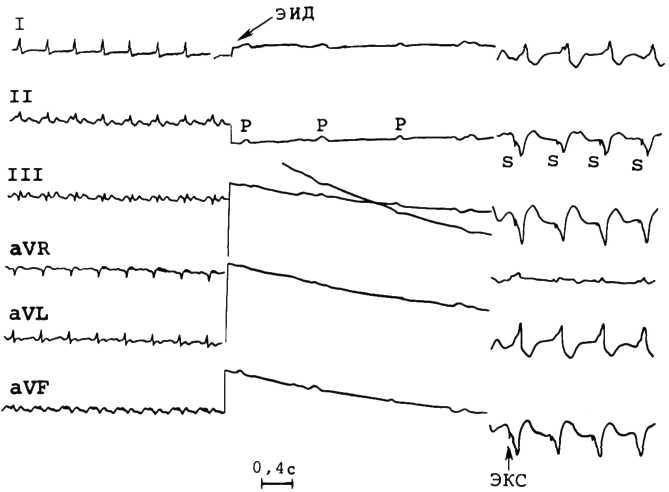
Этнология и предрасполагающие факторы. Трепетание предсердий может сочетаться с любым сердечным заболеванием, но наиболее часто оно наблюдается при ревматическом поражении митрального клапана. Трепетание предсердий нередко наблюдается при ИБС, артериальной гипертен-зии, при перикардитах, ВПС, особенно пролапсе митрального клапана, кардиомиопатиях. Трепетание предсердий осложняет течение синдрома тахикардии-брадикар-дии при слабости синусно-предсердного узла.
Патогенез. В основе трепетания предсердий могут лежать два механизма: механизм повторного входа возбуждения (риентри) или эктопический очаг. При повторном входе возбуждения активация предсердия происходит в основном вокруг кольца ткани между двумя полыми венами. Импульс распространяется в одном направлении в замкнутом пространстве, образуя непрерывный цикл. Это движение теоретически можно прекратить, если изменить рефрактерность любой части круга. На этом принципе основано применение хинидина при трепетании предсердий. В настоящее время есть разнообразные доказательства механизма риентри при трепетании предсердий. С. Leier (1978) убедительно показал, что у людей, страдающих зтой патологией, имеется поражение проводящей системы предсердий.
Классификация. В классической литературе выделяют типичную (общую) и нетипичную (редкую) формы трепетания предсердий. Деление это зависит от морфологии волн трепетания предсердий. Для типичной формы характерно наличие отрицательных волн F, для нетипичной—положительных. Предполагается, что различны субстраты активации предсердий. При общем типе трепетания активация предсердий происходит против часовой стрелки: каудоцефальная активация нижних отделов перегородки и левого предсердия и цефалокаудальная—правого предсердия. При нетипичной форме трепетания распространение процесса активации имеет обратное направление. Различие в активации предсердий не объясняет механизма аритмии, поэтому большого практического значения не имеет. Согласно другой теории, трепетание предсердий обусловлено быстрой сменой ритма из эктопического (одного) фокуса предсердия. При этом разница между трепетанием предсердий и эктопической пред-сердной тахикардией состоит в скорости импульсации из
фокуса. В пользу этой теории приводят и клинические наблюдения. У ряда больных на ЭКГ возникновению трепетания предсердий предшествуют одна или две спаренные пред-сердные экстрасистолы. Нужны веские аргументы, чтобы установить истину. Возможно, однако, что оба механизма взаимодействуют и формируют этот вид аритмии.
J. Wfells и соавт. (1979) различают два типа трепетания предсердий: I (классический) и II (выделенный по электрофизиологическому принципу) [Wfells J. et al, 1979]. В классификации не учитываются морфология и полярность волн трепетания предсердий на ЭКГ. Оба типа характеризуются исключительно постоянной морфологией волн F от сокращения к сокращению, полярностью, амплитудой и продолжительностью цикла. Отличие I от II типа состоит в том, что I тип трепетания удается купировать частой предсер-дной стимуляцией из верхних отделов правого предсердия. В некоторых случаях учащающая стимуляция предсердий приводит к переходу I типа трепетания во II тип; II тип трепетания предсердий переходит в I тип спонтанно. Кроме электрофизиологической характеристики, эта классификация предусматривает и точный критерий выраженности тахикардии: при I типе трепетания число сокращений предсердий колеблется от 240 до 340 в минуту, при II типе—от 340 до 433 в минуту. Авторы не исключают, что нижний и верхний пределы трепетания предсердий могут быть и иными. Но частота сокращений 340 в минуту служит важным электрофизиологическим критерием разделения двух типов этой формы тахиаритмии.
Клиника. Выраженность симптоматики при трепетании предсердий зависит от следующих причин: а) тяжести основного заболевания сердца, вызвавшего трепетание; б) частоты желудочковых сокращений; в) продолжительности аритмии. Симптоматика варьирует от нерезко выраженных приступов головокружения до отека легких с гипотонией и остановкой сердца.
При заболеваниях, сопровождающихся гипертрофией левого желудочка, возможна утрата роли предсердий в напол-
517
нении желудочков кровью со снижением сердечного выброса более чем наполовину от исходной величины. К таким заболеваниям относятся гипертоническая болезнь, клапанный или подклапанный аортальный стеноз, гипертрофическая кардиомиопатия. Частота желудочковых сокращений имеет важное значение при определении тяжести состояния больного. При частоте сокращений свыше 150 в минуту симптоматика становится более отчетливой. Выраженная недостаточность кровообращения развивается очень быстро при проведении импульсов с предсердий на желудочки в отношении 1:1. Это и неудивительно: примерно в 85% больных число сокращений предсердий превышает 300 в минуту, а нередко достигает 350 в минуту. Состояние больного, наоборот, значительно улучшается при переходе трепетания предсердий в мерцание, поскольку при этом уменьшается число желудочковых сокращений.
Диагностика. Диагностируют трепетание предсердий обычно на основании типичной картины ЭКГ, на которой регистрируется предсердная активность в форме зубов акулы или в форме пилы. Вектор направлен книзу, поэтому трепетание особенно хорошо видно в отведениях II, III, aVF и нередко V^ Изоэлектрическая линия не фиксируется. Ат-риовентрикулярная проводимость изменяется по-разному, но наиболее часто она составляет 2:1. При этом число сокращений предсердий в минуту составляет 300, а желудочков—150. Поэтому, когда на ЭКГ число сокращений сердца составляет 150 в минуту всегда следует исключить у больного трепетание предсердий. Это особенно важно, когда волны трепетания маскируются комплексом QRS или зубцом Т.
Иногда при трепетании предсердий возможно проведение импульса из предсердий в желудочки по предсердно-желудоч-ковому узлу в соотношении 1:1. При аберрации проведения из-за очень высокой частоты сокращений желудочков такую форму трепетания предсердий нередко принимают за желудочковую тахикардию. Не исключается наличие у одного и того же больного трепетания предсердий и желудочковой тахикардии. В частности, такое возможно в случаях, когда больного с трепетанием предсердий начинают лечить не препаратами, удлиняющими проведение по предсердно-желудочковому узлу, как, например, дигиталис, а хинидином. Поэтому у больного с тахикардией 260—300 в минуту при регулярном (правильном) ритме трепетание предсердий необходимо дифференцировать с пароксизмальной предсердной тахикардией. Последняя характеризуется меньшей частотой сокращений (160—240 в минуту). Пищеводное отведение ЭКГ позволяет отдифференцировать зубец Р предсердной тахикардии от волн F трепетания предсердий. При трепетании предсердий нет изоэлектрической линии на ЭКГ, а при предсердной тахикардии она сохранена. Целесообразно использовать тест стимуляции каротидного синуса. При проведении массажа каротидного синуса блуждающий нерва усиливает блокаду проведения по предсердно-желудочковому узлу, и типичная картина волн F становится отчетливой. При предсердной тахикардии массаж каротидного синуса «срабатывает» по закону «все или ничего». Обычно тахикардия внезапно обрывается и восстанавливается синусовый ритм или эта процедура на нее никак не влияет.
Все остальные виды тахикардии, в том числе и желудочковая, не представляют сложностей при проведении дифференциальной диагностики трепетания предсердий.
Электрофизиологическое исследование при трепетании предсердий позволяет: 1) изучить состояние проводимости по предсердию и определить субстрат трепетания; 2) разработать метод, устанавливающий пути активации трепетания; 3) установить электрофизиологический механизм трепетания и клиническое значение этого состояния у больного; 4) определить возможность прекращения трепетания электрической стимуляцией; 5) отдифференцировать трепетание предсердий от желудочковой тахикардии в сложных случаях.
Отсутствие изоэлектрической линии на ЭКГ не позволяет иметь референтную точку, которая могла бы служить источником отсчета распространения возбуждения по предсердию. Только тогда, когда удается снять трепетание путем учащающей стимуляции, а затем вызвать его программируемой стимуляцией (одиночным стимулом), удается установить место, где «зарождается» эта тахикардия.
Электрофизиологическое исследование позволяет установить, что у таких больных имеется нарушение внутрипред-сердной проводимости. У большинства больных внутрисер-дечное исследование позволяет выявить изменение рефрак-терности миокарда предсердий и функции синусно-предсердного узла.
Лечение. Многие годы для лечения трепетания предсердий используют ряд фармакологических препаратов и электрическую дефибрилляцию сердца. Необходимо соблюдать основной принцип лечения—последовательность: сначала назначить лекарственную терапию, а затем дефибрилляцию, однако он в интересах больного не всегда соблюдается. При трепетании предсердий с проведением импульса 1:1 показана электрическая дефибрилляция. Дефибрилляцию выполняют и при меньшем числе желудочковых сокращений с быстро нарастающей сердечной недостаточностью. При устойчивом состоянии больного начинают лечение с больших доз препаратов дигиталиса из расчета 0,05 мг/кг, чтобы уменьшить проводимость по предсердно-желудочковому узлу. Если эффект проявился в переходе трепетания предсердий в мерцание, лечение дигиталисом дополняют хинидином. Обратная последовательность назначения препаратов недопустима, так как может привести к развитию желудочковой тахикардии.
В последние годы для лечения трепетания предсердий в сочетании с препаратами дигиталиса назначают анапри-лин (обзидан, индерал, пропранолол). Он уменьшает число сокращений желудочков. Следует, однако, помнить, что этот препарат является р-блокатором и может усугубить сердечную слабость, бронхиальную астму, хронические об-структивные легочные заболевания. Поэтому мы рекомендуем использовать его лишь после насыщения организма сердечными гликозидами. В последнее время при тяжелом течении заболевания, когда консервативное лечение неэффективно, электрическая дефибрилляция кратковремен-на, а клиника заболевания остается выраженной, используют хирургическое лечение.
Результаты хирургического лечения зависят от многих причин. Одним из основных условий получения хороших результатов радикального лечения является установление механизма трепетания предсердий. При типичной форме трепетания предсердий, которое обусловлено механизмом повторного входа возбуждения, можно очень точно локализовать очаг трепетания предсердий и с помощью криовоз-действия или лазерной фотоаблации полностью его пода-
578
вить. Как правило, этот очаг расположен в зоне, ограниченной устьем нижней полой вены, коронарным синусом, нижним краем овальной ямки и межкавальным промежутком с латеральной стороны. Примерно у 80% больных в течение 5 лет после радикального воздействия на очаг трепетания предсердий сохраняется синусовый ритм. В тех случаях, когда трепетание предсердий имеет нетипичную форму или сочетается с мерцательной аритмией, можно выполнить операцию по созданию поперечной блокады с имплантацией частотно-зависимого стимулятора, операцию электрической изоляции по типу «коридор» или «лабиринт».
Прогноз. Прогноз при трепетании предсердий зависит от проводимости по предсердно-желудочковому узлу (частота пульса). Имеет значение характер основного заболевания, эффективность терапии которого уменьшает частоту приступов тахикардии и ее выраженность. Прогноз лучше в молодом возрасте и у лиц с неосложненными формами болезни.
Устранение очага трепетания предсердий, особенно при ее идиопатической форме, позволяет максимально увеличить продолжительность жизни больных.
При искусственном создании полной поперечной блокады актуарная выживаемость в течение 10 лет составляет 75%.
4.7. ЖЕЛУДОЧКОВЫЕ ТАХИКАРДИИ
Желудочковая тахикардия—патологическое состояние, клинические проявления которого обусловлены низким сердечным выбросом.
При желудочковой тахикардии частота сердечных сокращений превышает 100 в минуту. Функция синусового узла сохранена, он функционирует самостоятельно или вовлекается в ритм желудочков при ретроградной проводи-. мости.
Частота. Желудочковые тахикардии бывают врожденными и приобретенными. Врожденные желудочковые тахикардии встречаются в 15% случаев, приобретенные—в 85%.
Желудочковые тахикардии чаще встречаются у мужчин (69%), чем у женщин (31%). Большинство случаев приходится на возраст от 40 до 70 лет.
Пароксизмальная рецидивирующая желудочковая тахикардия обычно выявляется на фоне какого-то другого тяжелого сердечного заболевания, наиболее часто ИБС. Примерно 35% больных с желудочковой тахикардией имеют в анамнезе инфаркт миокарда, а у 60% больных течение острого инфаркта миокарда в разные периоды болезни осложняется желудочковой тахикардией. Еще выше процент желудочковой тахикардии у больных с хронической аневризмой сердца.
Второй очень частой причиной желудочковой тахикардии является интоксикация препаратами дигиталиса (25%). В частности, при лечении других форм тахиаритмий может возникнуть исключительно опасная форма желудочковой тахикардии типа «пируэт». В последнее время, особенно в связи с внедрением в клиническую практику метода эхо-кардиографии и улучшением диагностики, высокий процент желудочковой тахикардии (до 10% случаев) выявляется при пролапсе митрального клапана. Также часто причиной желудочковой тахиаритмий называют кардиомиопатию и несколько реже—ревмокардит, гипертонию, амилоидоз.
Примерно у 5—17% больных причина заболевания сердца, приведшая к развитию желудочковой тахикардии, не выявляется. В этих случаях говорят о психосоматической природе, однако эмоциональный стресс как причина желудочковой тахикардии описывается в литературе исключительно редко. Желудочковые тахикардии представляют большую опасность для жизни.
Этиология и патогенез. Для практических целей выделяют четыре основные группы причин, вызывающих желудочковые тахикардии. В первую группу выделяют постинфарктные желудочковые тахикардии. Ко второй группе относят тахикардии, обусловленные Рубцовыми изменениями миокарда вследствие перенесенной операции на сердце (обычно по поводу врожденной патологии), локализованного грану-лематоза (саркоидоз, дисплазия желудочков, истонченный «бумажноподобный» желудочек). В третью группу объединены тахикардии при диффузном поражении миокарда. Это может быть гипертрофия миокарда в результате аортального стеноза либо алкогольная или вирусная кардиомиопа-тия. К четвертой группе относят тахикардии, первичную фибрилляцию желудочков, развивающиеся при физической нагрузке. Ни в анамнезе, ни в момент исследования изменения на ЭКГ не регистрируется. В большинстве случаев выявляют тотальную окклюзию коронарных сосудов. В формировании тахикардии основное значение имеет фактор электрической нестабильности, приводящий к изменению времени проведения возбуждения в зонах, определяемых как аритмогенные и являющихся причиной желудочковой тахикардии.
Классификация. Для желудочковой тахикардии, как и для других видов тахикардии, нет общепринятой классификации. Для ее характеристики в основном описывают особенности ритма либо механизм, вызывающий тахикардию.
Ритмы тахикардии: пароксизмальная, непароксизмальная, устойчивая, возвратная, медленная тахикардия, мономорф-ная, полиморфная, типа «пируэт» (torsade de pointes).
Механизмы желудочковой тахикардии: риентри, повторный вход возбуждения, эктопический «триггерный».
Патологическая анатомия. С современных позиций врожденная желудочковая тахикардия—аритмогенная дисплазия, в основе которой лежит генетический фактор. Аномалия структуры миофибрилл сократительного миокарда, которая выявляется при аритмогенной дисплазии, наблюдается даже у эмбрионов. Заболевание часто носит семейный характер. Аритмогенная дисплазия как заболевание проявляется с течением времени, не сразу. Этот период совпадает со временем замещения миофибрилл жировой тканью. Процесс захватывает медиомуральный и субэпикардиальные слои. Это позволяет заподозрить травматическое повреждение, обусловленное сокращениями сердца. Когда патологический процесс завершен, нормальная структура сохранена только в субэндокардиальном слое. Все остальные слои замещены жировой тканью. При микроскопическом исследовании отмечаются истончение стенки желудочка и разрастание слоя эпикардиального жира. Гистологическое исследование выявляет зоны вкрапления нормальных или частично дегенери-рованных фибрилл. Последние, имеющие несколько причудливую форму с перемежающимися нормальными очертаниями миокарда, являются основой формирования «задержанной» проводимости и круга повторного входа возбуждения (риентри). При этом структура сохранена только в субэпикардиальном слое, в эндомиокардиальном слое выявляют неспецифические изменения.
519

Измененный миокард отмечен точками и отделен от здорового зоной недеполяризованных волокон, за исключением участков проведения возбуждения (1,2). Из ишемизированной зоны в область здорового миокарда проходят один (а) или два (б) пути проведения возбуждения. Поэтому возможны одна или две зоны активации неизмененного миокарда. В зависимости от скорости проведения возбуждения и длины проводящего пути развиваются два вида тахикардии: моиоморф-ная или полиморфная. Представлен вариант тахикардии (в), когда, несмотря на наличие двух путей проведения, из здоровой ткани в измененный миокард отмечается лишь один «прорыв» возбуждения. В связи с наличием двух различных путей проведения в ишемизированной ткани длительность цикла тахикардии может меняться без изменения ее «морфологии». Аналогичный результат имеет место, если в измененном миокарде изменяется скорость проведения возбуждения от сокращения к сокращению (г).
При электрофизиологическом исследовании в зоне дисп-лазии регистрируется задержанная, двойная и фрагментиро-ванная активность. Частая стимуляция приводит к возрастанию спаренных потенциалов. Такая реакция миокарда этой зоны объясняет механизм повторного входа возбуждения, так как задержанная активность превосходит рефрактерный период здоровой ткани. Наиболее приемлемой теорией, объясняющей механизм повторного входа при аритмогенной дисплазии желудочков, в настоящее время считается та, согласно которой измененный миокард проводит возбуждение только в одном направлении. Таким образом возникает механизм с блокадой проведения возбуждения в обратную сторону, что очень напоминает механизм повторного входа возбуждения при синдроме Вольфа—Паркинсона—Уайта.
Патологическая анатомия инфаркта миокарда и постинфарктного периода описана в литературе очень подробно. До настоящего времени, однако, неясно, почему у одних больных тахикардия развивается, а у других нет. Есть объяснение причин возникновения устойчивой и неустойчивой тахикардии, а также самого механизма желудочковой тахикардии коронарогенного генеза. Исследованиями последнего времени установлено, что при формировании патологического процесса в эпикардиальном слое развивается желудочковая тахикардия по типу кратковременных пароксизмов или «пробежек». Устойчивая желудочковая тахикардия возможна при трансмуральном поражении миокарда с образованием фиброза миокарда. Фиброз становится «твердым остовом», по краям которого происходит неравномерное растяжение миокарда. Электрическая нестабильность этой зоны обусловлена наличием островков нормальных миоци-
тов в зоне акинезии. Таким образом, аритмогенный субстрат напоминает тот, который выявляется при аритмогенной дисплазии. Вот почему при аневризме сердца или рубцовых изменениях очаг аритмии всегда локализован на границе здорового и перерожденного миокарда. При этом в островках миоцитов формируется анатомический субстрат желудочковой тахикардии.
При моделировании желудочковой тахикардии особое внимание обращают на внутримиокардиальную проводимость. При этом необходимо иметь в виду такие важные факторы, как наличие одного или одновременно двух источников возбуждения в желудочках. Значение внутримиокар-диальной проводимости для формирования количества очагов тахикардии и направления волны возбуждения видно на рис. 4.33. В отличие от пути проведения, соединяющего зоны с быстрой и медленной проводимостью только в одной точке, проведение возбуждения из пораженной ткани в здоровую возможно по двум разным зонам. В ряду случаев возникновение нестабильности миокарда приводит к изменению места наиболее ранней активации здоровой ткани, что изменяет частоту сокращений сердца во время тахикардии и комплекс QRS. Этих изменений не происходит, если свойства проведения нового пути идентичны свойствам старого, несмотря на то что траектории их прохождения могут отстоять друг от друга на значительном расстоянии.
Аналогичным образом наличие двух точек контакта между здоровой тканью и тканью с замедленной проводимостью не приводит к изменению комплекса QRS во время тахикардии. Если свойства проводимости нового пути аналогичны свойствам.ранее существовавшего, то ритм не изменится, а ЭКГ останется прежней. Подобное происходит и при изменении траектории прохождения пути, но она сохраняется в зоне поражения. В этом случае меняется ритм, а характер ЭКГ остается прежним.
Локализация очага желудочковой тахикардии. У больных ИБС область возникновения желудочковой тахикардии независимо от характера ЭКГ локализована либо в левом желудочке, либо в межжелудочковой перегородке с левой стороны.
Если нет ИБС, очаг может быть локализован как в правом желудочке, так и в левом. Так, у больных с послеоперационным рубцом миокарда правого желудочка (тетрада Фалло) тахикардия развивается в правом желудочке в его выходном отделе. У больных с кардиомиопатией она обычно локализована в левом желудочке или в перегородке. Без органических поражений сердца аритмогенная зона находится в правом желудочке. Идиопатическая желудочковая тахикардия
520
с комплексом QRS типа блокады левой ножки предсердно-желудочкового пучка на ЭКГ происходит из правого желудочка, изредка из межжелудочковой перегородки.
4.7.1. «ВРОЖДЕННАЯ» ЖЕЛУДОЧКОВАЯ ТАХИКАРДИЯ
Основной формой «врожденной» желудочковой тахикардии является аритмогенная дисплазия желудочков. Типичным проявлением заболевания являются повторные эпизоды желудочковой тахикардии, наблюдаемые преимущественно в юношеском возрасте. Аритмогенная дисплазия встречается у мужчин примерно в 2 раза чаще, чем у женщин. В большинстве случаев патологический процесс локализован в правом желудочке. Поэтому заболевание называют аритмоген-ной дисплазией правого желудочка. Однако наличие такой дисплазии и в левом желудочке, и в перегородке сердца не исключается.
На ЭКГ у больных во время приступа желудочковой тахикардии регистрируется блокада левой ножки предсер-дно-желудочкового пучка. Это обусловлено задержкой распространения возбуждения на левый желудочек. Ось сердца меняется в зависимости от того, где находится участок дисплазии. Если он находится в выходном отделе правого желудочка, то ЭКГ имеет нормальную ось или смещена вправо. Если зона аритмии располагается на диафрагмаль-ной поверхности и на верхушке правого желудочка, то на ЭКГ регистрируется левограмма.
При синусовом ритме выявляются признаки, характерные для поражения правых камер сердца: увеличение зубца Р более чем на 2,5 мм, инверсия сегмента 57* в отведения V,—V5 и задержка проведения возбуждения по правому желудочку. Этим проявлениям часто сопутствует блокада правой ножки предсердно-желудочкового пучка с низким вольтажем, быстрой фазой смены потенциалов. Исследованиями последнего времени было установлено, что это обусловлено блокадой париетальной ножки без определенной альтерации ножек предсердно-желудочкового пучка.
В /з случаев наблюдается очень специфический признак—феномен желудочкового поствозбуждения—волна эпсилон, которая располагается после комплекса QRS до начала сегмента ST. Этот так называемый задержанный потенциал лучше всего регистрируется при картировании сердца (рис. 4.34). Локализация этого потенциала во время внутрисердечного исследования позволяет очень точно определить топику поражения.
При рентгенологическом исследовании выявляется умеренное, диффузное увеличение сердца, преимущественно между дугой аорты и левым желудочком. Легочный рисунок не изменен. Кардиоторакальный индекс обычно менее 0,6. При эхокардиографическом исследовании видно изолированное расширение правых камер сердца, особенно правого желудочка. Увеличивается соотношение правый желудочек левый желудочек. При рентгеноконтрастном внутрисердеч-ном исследовании—вентрикулографии—выявляется увеличение полостей правых отделов, особенно правого желудочка. Одновременно отмечается снижение сократительной функции этой камеры сердца. Изменения локализованы преимущественно в выходном отделе и проявляются в форме небольших дивертикулов. Такие же дивертикулы могут ло-кализовываться на верхушке правого желудочка и на задне-диафрагмальной поверхности его стенки, непосредственно под трехстворчатым клапаном. Описанные аномалии могут носить изолированный характер или быть во всех трех отмеченных отделах, они формируют своеобразный треугольник дисплазии (рис. 4.35). Специфическим ангиографи-ческим признаком заболевания является длительная задержка контрастного вещества в обозначенных местах, которая может продолжаться до 20 сокращений сердца и более. Кон-трактильный статус области дисплазии существенно отличается от такового в других отделах правого желудочка, которые быстро освобождаются от контрастного вещества.
Электрофизиологическое исследование у таких больных следует проводить после уточнения положения этих дивертикулов с помощью ангиокардиографического исследования. Это позволяет при электрофизиологическом исследовании очень детально изучить зону дисплазии. В том случае, если больному с помощью ранее выполненных исследований удалось локализовать очаги дисплазии. проведение катетера в эти участки позволяет точно отдифференцировать их значение в происхождении тахикардии. На электрограммах регистрируется так называемый задержанный потенциал активности, который располагается на сегменте ST, предшествуя зубцу Т. Если из этого участка проводить стимуляцию желудочков, то интервал между стимулом и сокращением желудочка может достигать 80 мс. В этой зоне порог стимуляции очень высокий. Следует отметить, что такие методы электрофизиологического исследования, как программируемая или частая стимуляция, не вызывают и не прекращают желудочковую тахикардию. Вызвать тахикардию у этих больных вообще бывает трудно. Поэтому программируемую стимуляцию следует проводить из несколь-

Задержанный и фрагментированный потенциалы (обозначены стрелками). Порог стимуляции в этой зоне очень высокий. АДПЖ—арит-могенна.ч дисплазия правого желудочка. Норма— здоровый миокард.
527

4.35. Ангиокардиограмма (а) и ее схема (б) при аритмоген-ной дисплазии правого желудочка.
«Дивертикулы», которые могут быть источником тахикардии, обычно локализованы в выходном отделе (3), но могут располагаться и на верхушке (2,а,б), и на диафрагмальной поверхности желудочка под трехстворчатым клапаном (1). Дивертикулы во всех трех участках называют треугольником дисплазии.
ких мест правого желудочка, используя различные методики электрофизиологического исследования. Однако достаточно желудочковую тахикардию вызвать однократно, чтобы в последующем ее можно было вызвать легко.
4.7.2. «ПРИОБРЕТЕННАЯ» ТАХИКАРДИЯ
Наиболее частой причиной ее развития, как указывалось выше, является ИБС. Желудочковая тахиаритмия, сочетающаяся с ИБС, может иметь в своей основе три очень важных этиологических механизма: автоматический желудочковый фокус (эктопический очаг), круг повторного входа возбуждения (риентри) и триггерный автоматизм. Долгое время считалось, что желудочковая тахиаритмия, сочетающаяся с ИБС, первично обусловлена автоматическим фо-
кусом из-за чрезмерной возбудимости миоцитов, располагающихся по краям плохо перфузируемой зоны миокарда— рубца или аневризмы. Экспериментальными исследованиями и клиническими наблюдениями в 70-х годах было установлено, что в большинстве случаев желудочковая тахиаритмия, сочетающаяся с коронарной болезнью сердца, имеет в своей основе механизм повторного входа возбуждения. Круг повторного входа может быть обусловлен либо механизмом микрориентри, когда в него включается очень незначительное количество клеток миокарда, либо макрори-ентри, когда в круг включаются элементы специализированной проводящей системы сердца и свободная стенка желудочка. В развитии рефрактерной желудочковой тахиаритмии не установлено значения триггерного механизма.
С практической точки зрения в клинической классификации этиологических типов рефрактерной ишемической желудочковой тахикардии можно выделить две группы: эктопические аритмии и аритмии повторного входа (риентри). Совершенно эмпирически эктопической желудочковой тахикардией считается такая, которую нельзя вызвать и прекратить програми-рованной электрической стимуляцией сердца и другими электрофизиологическими методами, в частности сверхчастой стимуляцией. Тахикардию повторного входа возбуждения можно вызвать и прекратить, используя электрофизиологические методы. Несмотря на то что существует различная реакция на программируемую стимуляцию при эктопической и риентритахикардии, тем не менее все еще не удалось доказать наличие одного или другого механизма. Тем не менее существующая классификация принята повсеместно, поскольку она позволяет, с одной стороны, определить показания к хирургическому лечению, а с другой—надеяться на успех такого лечения в одном случае и не рассчитывать в другом. Поскольку эктопическая тахикардия не вызывается электрофизиологическими методами и легко подавляется общей анестезией, ее трудно индуцировать во время операции.
Клиника. Клинические проявления желудочковой тахикардии аналогичны проявлениям других форм тахикардии, но выраженность их больше, так как значительнее нарушается гемодинамика и тахикардия развивается на фоне другого серьезного сердечного заболевания.
Больные жалуются на загрудинные боли, одышку, син-копальные состояния. Периодически возможны обмороки с переходом в гемодинамический шок. При кратковременных приступах тахикардии некоронарогенного происхождения больные жалуются на сильное сердцебиение, общую слабость, загрудинные боли. Если приступ затягивается, появляется одышка. Течение заболевания осложняется появлением нарушений функций жизненно важных органов (почки, сердце, мозг) и прогноз становится неблагоприятным: возможна внезапная смерть.
Физикальные признаки во время желудочковой тахикардии вариабельны и существенным образом зависят, во-первых, от функции предсердий в этот период, а во-вторых, от сопутствующей сердечной патологии. Если при желудочковой тахикардии возникает предсердно-желудочковая диссоциация, то аускультативно отмечают изменение интенсивности I тона, интермиттирующие тоны Короткова (изменение систолического артериального давления от сокращения к сокращению), прерывистые пушечные волны а на сфигмограмме, регистрируемой в области яремной вены. Все это является результатом разобщения функций предсердий и же-
522

лудочков. А если желудочковая тахикардия сочетается с ретроградной проводимостью в отношении 1:1, то наблюдаются постоянное усиление 1 тона и постоянная волна а на кривой венозного давления.
При исследовании гемодинамических изменений было выявлено, что при одной и той же частоте наджелудочковой и желудочковой тахикардии сердечный выброс, коронарный кровоток и среднее артериальное давление изменяются одинаково. Однако желудочковую тахикардию больные переносят труднее. Обычно желудочковая тахикардия приводит к снижению артериального давления (рис. 4.36). Продолжение приступа вызывает различные нарушения кровообращения. Приступы желудочковой тахикардии особенно опасны у «коронарных» больных, у которых снижение коронарного кровотока на фоне его исходной недостаточности может иметь фатальные последствия. Пароксизм тахикардии приводит к снижению не только сердечного выброса, но и мозгового и печеночного кровотока. Сказанное, по-видимому, объясняет, почему эта тахикардия развивается у больных с выраженной патологией миокарда и часто сочетается с тяжелыми изменениями гемодинамики.
Электрокардиографические признаки довольно типичны, но не являются абсолютно патогномоничными: I) желудочковый комплекс уширен (0,14 с и более); 2) желудочковые сокращения правильные, частота их обычно колеблется от 140 до 250 в минуту; 3) предсердно-желудочковая диссоциация отчетливо выражена и характеризуется тем, что предсердия сокращаются реже, чем желудочки. Однако эта диссоциация не позволяет исключить полностью узловой ритм с аберрантной проводимостью; 4) изменения комплекса QRS часто аналогичны таковым при предшествующей или последующей желудочковой экстрасистолии на ЭКГ; 5) диагноз становится более определенным, когда на ЭКГ удается обнаружить редкие узкие комплексы QRS. Это так называемые сокращения захвата, проводимые с предсердия. Они возможны, если возбуждение с предсердий приходит в тот момент, когда ни узел, ни желудочки не находятся в состоянии рефрактерное™. Комплекс QRS в такой период занимает промежуточное положение между нормальным сокращением и комплексом тахикардии. Эти
сокращения исключительно точно характеризуют желудочковую тахикардию.
Выделяют три типа ЭКГ при желудочковой тахикардии. При I типе желудочковая тахикардия имеет устойчивый характер, а все желудочковые комплексы совершенно однотипны. Число сердечных сокращений колеблется от 140 до 250 в минуту, имеется высокая вероятность перехода в фибрилляцию желудочков. Ко II типу относят повторные тахикардии в форме групповых экстрасистол от 3 до 6 комплексов. Они могут продолжаться неопределенное время—от нескольких минут до нескольких месяцев. К III типу относят ускоренный идиовентрикулярный ритм—так называемую медленную желудочковую тахикардию. Частота сердечных сокращений составляет 100—140 в минуту. Обычно тахикардия наблюдается на фоне острого инфаркта миокарда и обусловлена образованием задержанной активности в сети волокон Пуркинье (в последующем возможно формирование эктопического фокуса). Она продолжается обычно в течение 30 сокращений сердца (блок входа возбуждения носит непостоянный характер).
Такой тип тахикардии описан также при дигиталисной интоксикации, ревмокардите, миокардите, гипертонической болезни.
При анализе ЭКГ желудочковую тахикардию нередко принимают за наджелудочковую или узловую. Причиной такой ошибки бывает уширенный комплекс QRS.
При наджелудочковой тахикардии широкий комплекс QRS обусловлен неполным восстановлением волокон проводящей системы желудочков ко времени прихода следующего импульса из предсердия или предсердно-желудочкового узла. Поэтому для того чтобы отдифференцировать наджелудочковую тахикардию от желудочковой, надо иметь в виду, что наджелудочковая тахикардия: 1) начинается с предсер-дной или узловой экстрасистолы; 2) интервал QRS—Р очень короткий; 3) конфигурация QRS не изменена; 4) аритмию можно прекратить, надавливая на каротидный синус.
Дифференциальный диагноз. Желудочковую тахикардию трудно отличить от наджелудочковой тахикардии с аберрантной проводимостью. Поэтому в критических случаях всегда необходимо электрофизиологическое исследование.
523
Оно позволяет установить, в каком отделе сердца находится источник возбуждения сердца. В остальных случаях электрокардиографические критерии и выявление основного заболевания позволяют точно отдифференцировать желудочковую тахикардию от наджелудочковой.
Естественное течение и прогноз. Несмотря на актуальность этого вопроса, данные литературы скудные. По-видимому, это обусловлено трудоемкостью исследования и сложностью обоснования получаемых результатов. Кроме того, необходимы такие сложные и не всегда доступные методы, как внутрисердечное электрофизиологическое исследование, ангиография, в том числе коронарография, холтеровское мониторирование, исследование гемодинамики.
При ИБС желудочковая тахикардия наиболее опасна, если она появляется в остром периоде инфаркта миокарда. Так, когда устойчивая желудочковая тахикардия появляется в течение первых 8 нед после развития инфаркта миокарда, то летальность достигает 85%. Максимальная продолжительность жизни составляет при этом 4 года, а средняя—только 0,7 года. Если желудочковая тахикардия впервые появляется через 2 мес от времени развития инфаркта миокарда, то летальность также очень высока, но не превышает 50%. Продолжительность жизни колеблется от 0 до 13 лет, составляя в среднем 2,8 года.
При идиопатической желудочковой тахикардии без лечения 78% больных умирают в первые 4 года от времени появления первого приступа. Лекарственная терапия позволяет увеличить продолжительность жизни в среднем до 8,8 года.
В настоящее время хорошо известно, что на исход заболевания не влияют длительность интервала Q—Г, конфигурация комплекса QRS, наличие блокады левой или правой ножки предсердно-желудочкового пучка. Лишь патология, вызывающая тахикардию, а точнее объем поражения миокарда сказываются на длительности жизни, поскольку отражается на продолжительности приступа и частоте сокращений сердца во время тахикардии и состояния гемодинамики во время него. Прогноз ухудшается при удлинении приступа и особенно при возвратных тахикардиях.
Электрофизиологическое исследование. Хирургическому лечению больного с желудочковой тахикардией должно предшествовать полное внутрисердечное обследование— рентгеноконтрастное и электрофизиологическое. Это относится в равной мере и к больным с врожденной патологией, приводящей к развитию желудочковой тахикардии, и к больным, у которых тахикардия является следствием приобретенного заболевания сердца. Ангиокардиографиче-ское исследование (в том числе коронарография) дает возможность решить вопрос о необходимости операции и ее объемах при патологии, вызвавшей тахикардию. Так называемая врожденная желудочковая тахикардия может быть обусловлена аритмогенной дисплазией желудочков, опухолью желудочка в период новорожденное™, пролапсом митрального клапана, болезнью Уля, аномалией Эбштейна. Эти болезни диагностируются методами ангиокардиографии и эхокардиографии. При рефрактерной ишемической желудочковой тахикардии коронарография и вентрикулография позволяют определить объем хирургического вмешательства. Внутрисердечное дооперационное электрофизиологическое исследование преследует цель установить, что: 1) аритмия является желудочковой, а не наджелудочковой;
2) аритмию можно вызвать и прекратить программированной электрической стимуляцией сердца, что доказывает наличие механизма повторного входа; 3) установить, что желудочковая тахиаритмия начинается из области патологически измененного миокарда (дисплазия, опухоль, инфаркт миокарда или аневризма сердца); 4) выполнить катетерное картирование, чтобы предельно точно локализовать специфическую область в пределах границы патологически измененной и здоровой ткани—непосредственный источник желудочковой тахикардии.
Дооперационное электрофизиологическое обследование больных с рефрактерной желудочковой ишемической тахикардией позволяет установить, что желудочковая тахикардия может быть нескольких типов. Наиболее часто она имеет единственный морфологический субстрат и начинается из определенного места в левом желудочке. Эта моно-морфная желудочковая тахикардия обычно достаточно продолжительна, что позволяет выполнить эндокардиальное картирование для определения места ее происхождения. Реже мономорфная желудочковая тахикардия недостаточно устойчива, что не позволяет провести полное обследование больного в дооперационном периоде.
В этих случаях используют специальные приемы, чтобы локализовать очаг тахикардии (электрическая стимуляция из различных отделов с одновременной записью всех 12 отведений ЭКГ и сопоставление ее с ЭКГ при ранее зарегистрированном приступе). Другой тип желудочковой тахикардии, который обычно сочетается с ИБС,—это полиморфная желудочковая тахикардия. К этому типу относится тахикардия, которая начинается из нескольких областей левого желудочка, что проявляется различными типами тахикардии. Сюда же относятся и тахикардии, которые начинаются из левого желудочка, но электрофи-зиологически характеризуются «пируэтом» (рис. 4.37). Полиморфная желудочковая тахикардия также может быть устойчивой или неустойчивой, но обычно она переходит в желудочковую фибрилляцию. Переход тахикардии в желудочковую фибрилляцию во время внутрисердечного исследования может быть обусловлен первичной электрической нестабильностью сердца или связан с гемодинами-ческими нарушениями, типичными для желудочковых тахикардии. Третий тип рефрактерной ишемической желудочковой тахикардии—это первичная фибрилляция желудочков, которая возникает при внутрисердечном электрофизиологическом исследовании. Фибрилляция желудочков возникает без предшествующей тахикардии, а синусовый ритм без предвестников переходит в желудочковую фибрилляцию при программированной электрической стимуляции или при кратковременной сверхчастой ЭКС.
Лечение парокензмальной желудочковой тахикардии. В типичных случаях подход к лечению желудочковой тахикардии определяется клиническим состоянием больного и предрасполагающими факторами (аритмогенная дисплазия, ИБС и т. д.). Последовательность лечения желудочковой тахикардии включает использование лекарств, электрическую дефибрилляцию, программированную электрическую стимуляцию сердца, включая автоматическую дефибрилляцию от имплантированных кардиостимуляторов, хирургическое лечение.
При консервативном лечении препаратом выбора является лидокаин. Он эффективен, безопасен, легко вводит-
524

ся (внутривенно) и быстро насыщает миокард. В терапевтических дозах не ухудшает сократительной функции миокарда, как это нередко бывает при использовании других антиаритмических препаратов. Вводят внутривенно струйно из расчета 1 мк/кг (в течение -3—4 мин). Эффект наступает через 2 мин и продолжается 20 мин. В дальнейшем внутривенное введение продолжают со скоростью 1—4 мг в минуту. При неэффективности лидокаина следует использовать новокаинамид. В острых случаях его вводят внутривенно по 100 мг каждые 5 мин (не более 25 мг в минуту) (до 1000 мг). Этот препарат, однако, более эффективен как профилактическое средство.
В последние годы из антиаритмических препаратов широко применяют амиодарон (кордарон) 5 мг/кг внутривенно медленно в 250 мл 5% раствора глюкозы. У больных с рефрактерной желудочковой тахикардией он позволяет перевести быструю форму тахикардии (180—240 в минуту) в медленную (120—130 в минуту).
Если, несмотря на введение антиаритмических препара-i тов, особенно лидокаина, состояние больного не улучшает-ся, следует провести электрическую дефибрилляцию сердца. |Эта процедура эффективна в 90% случаев. К сожалению, {Часто дефибрилляция приводит лишь к кратковременной рмализации ритма сердца с последующим возобновлени-: пароксизма. В таких случаях электрическую дефибрил-
i приходится повторять неоднократно. f В тех случаях, когда лекарственная терапия и электрошо-воздействие неэффективны, необходимо срочно провести программированную электрическую стимуляцию. Для го под рентгенологическим контролем в желудочек вво-г тетраполярный электрод, который позволяет проводить | стимуляцию сердца, и одновременную регистрацию элек-Цюграмм.
! Пароксизм тахикардии снимают либо учащающей, либо fcc-граммированной стимуляцией. ■ Для прекращения тахикардии достаточно провести стиму-нщию желудочков с частотой, превышающей пароксизм на Ж-30 в минуту, в течение 10—15 с, а затем внезапно «обожать» стимуляцию. Метод бывает успешным примерно случаев. Поскольку электрическая дефибрилляция Вучащающая стимуляция являются наиболее эффективны-^р методами прекращения желудочковой тахикардии, в на-[ предпринимаются попытки для создания им-руемых систем, основанных на этих принципах. В ли-приводятся единичные случаи использования ощей стимуляции при желудочковой тахикардии от ированных стимуляторов. Последние стимуляторы, ^конструкции которых использованы микропроцессоры окомпьютеры), реагируют фактически на совершенно
определенную тахикардию и имеют программу учащающей стимуляции и внезапного «обрыва» стимуляции. Метод электрической дефибрилляции в имплантированных системах также нашел применение в опытных разработках. Идея его применения основана на следующем принципе. Электрическая активность ткани в месте стимуляции, удаленная от очага тахикардии, недостаточна для проведения возбуждения в этот очаг. При развитии тахикардии стимулятор посылает «дефибриллирующий» импульс с такой силой тока, которая достаточна для того, чтобы он проник в очаг аритмии. Этого импульса бывает достаточно для прекращения тахикардии.
Основной недостаток имплантированных систем состоит в том, что они не предупреждают приступ тахикардии. Поэтому показания к их применению ограничены.
Показания к хирургическому лечению. Основными показаниями к хирургическому лечению больных с ишемической желудочковой тахиаритмией являются: 1) рефрактерность лекарственного лечения; 2) непереносимость больным эффективного консервативного лечения; 3) тяжелое соматическое состояние больного; 4) нестабильная стенокардия, необходимость аортокоронарного шунтирования у больного с сочетанной желудочковой тахикардией; 5) застойная сердечная недостаточность, обусловленная аневризмой левого желудочка, требующей резекции, которая сочетается с желудочковой тахикардией.
Основные противопоказания к хирургическому лечению рефрактерной ишемической желудочковой тахиаритмии определяются при электрофизиологическом исследовании: 1) неиндуцируемая желудочковая тахикардия; 2) непродолжительная полиморфная желудочковая тахикардия; 3) эктопическая желудочковая тахикардия; 4) тахикардия третьего типа с переходом в первичную фибрилляцию желудочков. Независимо от анамнеза больного и несмотря на наличие зарегистрированной на ЭКГ желудочковой тахикардии, от операции следует воздержаться, если аритмия не может быть индуцирована во время эндокардиального катетерного электрофизиологического исследования, поскольку вызвать ее во время операции, по-видимому, невозможно. Аналогичным образом следует подходить к случаям с неустойчивой полиморфной желудочковой тахикардией. Возможность индукции этой тахикардии и определения места ее происхождения сомнительна.
Необходимо, однако, отметить, что если неустойчивая полиморфная желудочковая тахикардия угрожает жизни больного, то операцию можно выполнить, используя один из методов эндокардиальной деструкции очага аритмии, не требующих применения интраоперационного картирования. Не рекомендуется оперировать больных с эктопической же-
525
лудочковой тахикардией, поскольку результаты хирургического лечения оказались неудовлетворительными. Точно так же, по-видимому, не следует прибегать к хирургическому лечению тахикардии, протекающей в форме первичной желудочковой фибрилляции.
Правда, один электрофизиологический прием, активно изучаемый в настоящее время, может уменьшить число противопоказаний. Он относится к случаям, когда у больного имеется приступ зарегистрированной желудочковой тахикардии на ЭКГ в 12 отведениях. Эту запись можно сделать вне стационара или во время короткого приступа при электрофизиологическом исследовании. В этом случае допустимо проведение учащающей стимуляции с частотой истинной желудочковой тахикардии из различных отделов сердца с записью ЭКГ в 12 отведениях (стимуляционное картирование). Такое картирование позволяет очень точно локализовать аритмогенный участок. Тогда у больных с желудочковой тахикардией по жизненным показаниям можно сделать операцию. Если тахикардия не индуцируется, можно воспользоваться методом стимуляционного картирования. Этот метод можно применить и во всех других случаях, если больного с желудочковой тахикардией необходимо оперировать в связи с другой патологией (аортокоронарное шунтирование, аневризмэктомия, протезирование клапана).
Хирургическое лечение. Радикальное хирургическое лечение желудочковых тахиаритмий начато в конце 70-х годов, когда были предложены патогномоничные методы операций. Методы лечения коронарогенной тахикардии принципиально не отличаются друг от друга, но в специальной литературе каждый из них принято называть раздельно по имени автора. G. Guiraudon (1978) предложил метод круговой эндокардиальной вентрикулотомии. Н. Harken (1979) и соавт. разработали операцию эндокардиальной резекции миокарда, a J. Могап (1982) модифицировал ее, назвав расширенной резекцией эндокарда. J. Сох и соавт. (1983) при желудочковых тахикардиях выполняют операцию эндокардиальной криодеструкцией. До появления прямых методов устранения желудочковой аритмии применялись операции грудной симпатэктомии, аортокоронарного шунтирования, резекции стенки желудочка, включая инфарцированный миокард или аневризмэктомию и аортокоронарное шунтирование в сочетании с резекцией стенки желудочка. J. Сох, проанализировав результаты 171 непрямой операции (по данным литературы), установил, что операционная летальность составляет 27%; в 17% случаев операция была безуспешной. Таким образом, суммарный положительный результат непрямых операций был 56%. Неудовлетворенность хирургов результатами непрямой хирургической техники, с одной стороны, и достижения клинической электрофизиологии—с другой, привели к развитию электрофизиологической техники устранения желудочковых тахикардии. Это в свою очередь стимулировало развитие прямых хирургических методов лечения этого тяжелого заболевания.
Несколько иначе совершенствовалась хирургическая техника врожденной желудочковой тахикардии, обусловленной аритмогенной дисплазией правого желудочка. Она была описана G. Fontaine и G. Guiraudon (1976), которые изучили механизмы развития тахикардии ив 1976 г. разработали метод простой вентрикулотомии при лечении больных с желудочковой риентритахикардией.
Радикальные операции. Прямое хирургическое вме-
шательство в очаге аритмии может быть успешным в двух случаях—при изоляции или разрушении очага аритмии. Хирургическая изоляция устраняет патологическое воздействие аритмии, так как ограничивается ее выход в проводящие пути. После выполнения такой операции аритмия может возникнуть с той же частотой, как и до операции, но она ограничена сравнительно маленькой областью сердца и не может выйти за пределы области, ограниченной скальпелем хирурга. Таким образом, сердце не вовлекается в этот процесс. Прямое разрушение очага аритмии (деструкция) возможно методом хирургической резекции или термического воздействия (криодеструкция, электродеструкция, лазердест-рукция).
В 1978 г. французский хирург G. Guiraudon предложил и разработал метод операции круговой эндокардиальной вентрикулотомии для больных с рефрактерной ишемической желудочковой тахикардией. Он предположил, что круговая эндокардиальная вентрикулотомия может либо изолировать аритмогенный очаг миокарда от всего сердца, либо разрушить желудочковую тахикардию путем хирургического разреза по меньшей мере одного колена круга повторного входа возбуждения. Однако установлено, что циркулярная резекция миокарда вызывает глубокие изменения регионарного кровотока, особенно в субэндокардиальном слое. Развивается ишемия, которая приводит к повреждению большинства нормальных, неизмененных полей электрической активности в окружающем миокарде. Поэтому предполагают, что круговая эндокардиальная резекция миокарда приводит к изменению локальной проводимости в аритмогенной области, что таким образом достаточно для прерывания круга риентри. Несмотря на то что такой механизм абсолютно эффективен для прерывания тахикардии, тем не менее снижение регионарного миокардиального кровотока приводит к непосредственной депрессии региональной функции миокарда в любой окружающей ткани, ранее не содержащей фиброза. Изменения региональной функции могут остаться без последствий, если имеющаяся у больного аневризма или инфаркт невелики. Но если иссекаемая область миокарда имеет значительные размеры, то в послеоперационном периоде наблюдается снижение нагнетательной функции сердца.
В 1979 г. Н. Harken для лечения рефрактерной ишемической желудочковой тахикардии предложил метод резекции эндокарда. Для выполнения такой операции необходимо точно локализовать аритмогенную зону у больных с инфарктом миокарда или аневризмой сердца. Такое интра-операционное картирование возможно, если во время операции удается вызвать тахикардию, по продолжительности достаточную для проведения электрофизиологического исследования. Таким образом, если во время операции удается вызвать устойчивую желудочковую тахикардию, которая не приводит к резкому ухудшению гемодинамики, то установление истинного очага аритмии с последующим его иссечением может считаться наилучшим способом лечения желудочковой тахиаритмий.
Точный механизм действия эндокардиальной резекции не известен, но предполагается, что во время операции резецируется весь круг повторного входа возбуждения, вызывающий желудочковую тахикардию. Если у больного невозможно выполнить процедуру картирования на операции (не индуцируется тахикардия, сильно нарушена гемодинамика),
526
то делают расширенную эндокардиальную резекцию с учетом механизма желудочковой тахикардии.
Прямые операции на эндокарде для лечения ишемической желудочковой тахикардии намного эффективнее, чем непрямые. По последним данным, обобщающим мировой опыт 160 операций, положительные результаты получены у 87% больных, неудовлетворительные—у 1%. Операционная летальность составила 12%.
Несмотря на улучшение результатов операции после внедрения методов круговой эндокардиальной вентрикулото-мии, эндокардиальной резекции миокарда или расширенной эндокардиальной резекции, ни один из перечисленных методов не может быть использован абсолютно у всех больных. Использование перечисленных методов затруднительно, если желудочковая тахикардия начинается в передней или задней сосочковой мышце или в задней части выходного отдела межжелудочковой перегородки. Резекция эндокардиального фиброза, распространяющегося на сосочковую мышцу, приводит к необходимости замещения митрального клапана, несмотря на то что клапанный аппарат может быть абсолютно сохранным.
Если желудочковая тахикардия возникает в верхнем отделе межжелудочковой перегородки в области соединения фиброзных колец митрального и аортального клапанов, то возникают различные технические проблемы. Первая состоит в трудности картирования этих больных, поскольку даже тогда, когда желудочковая тахикардия является устойчивой, приходится сердце «вывихивать» из перикарда. А это, как правило, останавливает приступ. Продольную вентрикуло-томию левого желудочка можно сделать между основанием задней сосочковой мышцы и задним отделом межжелудочковой перегородки, а картирование эндокарда задних отделов межжелудочковой перегородки должно выполняться после задней вентрикулотомии. При такой значительной ретракции сердца обычно развивается выраженная аортальная недостаточность, что в свою очередь отражается на точности выявления места (источника) аритмии. Другая техническая проблема, связанная с использованием эндокардиальной резекции, состоит в том, что возможен разрыв клапана аорты или митрального клапана во время самой процедуры эндокардиальной резекции. Во избежание повреждения клапанов делается экономная резекция зоны эндокардиального фиброза (в пределах 3—5 мм над клапанными кольцами), что, однако, не всегда приводит к прерыванию тахикардии.
Исходя из того, что перечисленные выше методы, с одной стороны, не всегда безопасны, а с другой—могут быть недостаточно эффективными для лечения рефрактерной ишемической желудочковой тахикардии трудной анатомической локализации, возникла идея в качестве основного элемента прерывания тахикардии, возникающей в задней или передней сосочковой мышце, а также высоко в межжелудочковой перегородке, использовать метод эндокардиальной гриодеструкции.
Ход операции не отличается от такового при эндокардиальной резекции или круговой резекции миокарда. Во время ИК на вскрытом сердце производится картирование и устанавливается место, откуда происходит желудочковая тахикардия. Затем эту зону замораживают криодеструктором. Очень важно использовать специальный игольчатый электрод—термистор для измерения температуры в толще ми-
окарда. Электрод проводят в зону возникновения тахикардии. Записывая интрамуральную электрограмму в период приложения замораживателя, можно вовремя остановить процесс криодеструкции, если температура здоровых тканей начинает приближаться к критической. Температурный режим в период криодеструкции должен зависеть от того, при каком состоянии миокарда выполняется эта работа. Известно, что оптимальное воздействие криодеструкции бывает в режиме -60° С. При применении криодеструкции на работающем сердце (температура миокарда 37° С) на наконечник подается температура -100° С. Если же эта процедура выполняется в условиях кардиоплегии, когда температура сердца составляет 8—10° С, то температура наконечника составляет - 70° С.
Важно правильно выбрать метод операции в зависимости от локализации зоны тахикардии. Существующий опыт позволяет рекомендовать эндокардиальную резекцию для лечения всех случаев рефрактерной ишемической желудочковой тахикардии. Однако эта операция возможна не у всех больных. Поэтому интраоперационная тактика зависит от двух факторов: 1) от интраоперационной электрофизиологической характеристики желудочковой тахикардии и 2) от хирургической анатомии (локализации) желудочковой тахикардии. Интраоперационное электрофизиологическое проявление тахикардии может быть трех типов: 1) устойчивая мономорфная желудочковая тахикардия; 2) неустойчивая мономорфная желудочковая тахикардия; 3) полиморфная желудочковая тахикардия.
Устойчивая мономорфная желудочковая тахикардия легко картируется во время операции и место ее происхождения находят легко. Точная локализация неустойчивой моно-морфной желудочковой тахикардии во время операции может быть чрезвычайно затруднительной и возможна при использовании многоканальной одномоментной регистрации электрограмм со всей поверхности сердца. В целом для этих типов аритмий допустимо использовать методы с менее уточненной методикой интраоперационного поиска, чем в предыдущем случае (когда аритмия во время операции является устойчивой и легко локализуется).
Если аритмогенный участок локализован в передней стенке левого желудочка, а тахикардия устойчива и имеет моно-морфный характер, то наилучшей операцией является прицельная (локальная) эндокардиальная резекция. Если тахикардия неустойчива и ее трудно картировать, по-видимому, можно ограничиться операцией круговой эндокардиальной резекции, чтобы избежать рецидива тахикардии в послеоперационном периоде. Если же тахикардия имеет полиморфный характер, то мы рекомендуем резецировать всю зону эндокардиального фиброза и дополнить его эндокардиальной криодеструкцией в той области, где отмечается наибольшая степень фрагментации электрической активности, выявляемой при картировании сердца на синусовом ритме. Хирургическая тактика при тахикардии из передней и боковой стенок левого желудочка, несмотря на свою доступность, зависит от двух факторов: во-первых, от того, как легко она вызывается и, во-вторых, насколько полно возможно картирование. С учетом этого решается вопрос об операции. Если в процесс вовлечена передняя сосочковая мышца, то независимо от того, носит тахикардия устойчивый характер или она неустойчива, следует выполнить эндокардиальную криодеструкцию основания сосочковой
527
мышцы. Когда тахикардия этой области носит полиморфный характер, следует резецировать весь эндокардиальный фиброз, распространяющийся с аневризмы, и произвести криодеструкцию на 2/3 ее величины, начиная от основания сосочковой мышцы. Если аритмогенная зона обнаружена в задней сосочковой мышце, то предпочтительнее выполнить процедуру криодеструкции. Однако если тахикардия не носит постоянного характера и нет полной уверенности в том, что аритмогенная зона находится в задней сосочковой мышце, то следует выполнить круговую эндокарди-альную вентрикулотомию вокруг всей границы фиброза задней стенки левого желудочка, сосочковой мышцы, межжелудочковой перегородки по задней ее поверхности. Круговая эндокардиальная вентрикулотомия проводится медиально к кольцу аортального клапана и латерально к кольцу митрального клапана и по глубине распространяется примерно на 5 мм. Наконец, проводят эндокардиальную криодеструкцию по краям зоны круговой эндокардиальной вентрикуло-томии для полной электрической изоляции всей зоны измененного миокарда.
При полиморфной желудочковой тахикардии, исходящей из задней стенки левого желудочка, выполняют аналогичную операцию. Однако если аритмогенную зону удается локализовать очень точно в задней стенке левого желудочка, то можно сделать эндокардиальную резекцию. В случае неустойчивой тахикардии, возникающей из этой области, можно выполнить эндокардиальную резекцию и круговую эндокардиальную вентрикулотомию как первичную процедуру с дополнительной эндокардиальной кри-одеструкцией, выполняемой недалеко от аортального и митрального клапанов. Если источник тахикардии возникает в межжелудочковой перегородке по задней поверхности левого желудочка, можно выполнить эндокардиальную резекцию.
В области кольца аортального клапана дополнительно проводят криодеструкцию. В тех случаях, когда источник тахикардии в пределах задней части перегородки со стороны левого желудочка локализовать не удается, следует резецировать весь участок фиброза и дополнить операцию эндокардиальной криодеструкцией вдоль аортального и митрального клапанов.
Таким образом, выбор метода операции для каждого конкретного больного с рефрактерной ишемической желудочковой тахикардией должен быть обоснован анатомическими и электрофизиологическими характеристиками, полученными в процессе дооперационного внутрисердечного электрофизиологического исследования и интраоперационного картирования. При этом очень важно выполнить операцию на фоне индуцированной желудочковой тахикардии, чтобы сразу же после этого сделать все электрофизиологические пробы, которые позволят судить об эффективности или безуспешности выполненной операции.
Если операция выполняется без кардиоплегической остановки сердца, то это позволяет исключить многие факторы, которые могут временно маскировать желудочковую тахикардию (гипотермия, кардиоплегия). Если у 20% больных после операции не удается вызвать тахикардию, то через 7—10 дней тахикардия индуцируется у каждого пятого оперированного больного. Число рецидивов резко уменьшилось при выполнении операций на сокращающемся сердце.
Приводим краткое описание клинического наблюдения
успешного хирургического лечения больной с рефрактерной к консервативной терапии желудочковой тахикардией.
Больная Ш., 62 лет, переведена в отделение нарушений ритма сердца ИССХ им. А. Н. Бакулева АМН СССР из НИИ скорой помощи им. Н. В. Склифосовского, где в течение 3 сут не удавалось купировать приступ пароксизмаль-ной желудочковой тахикардии и был поставлен вопрос о немедленной хирургической операции.
При поступлении состояние больной тяжелое. Жалобы на резко учащенное сердцебиение, головокружение, слабость, позывы на мочеиспускание. Из расспроса больной и беседы с лечащим врачом установлено, что год назад больная перенесла обширный трансмуральный инфаркт миокарда, осложнившийся аневризмой сердца. Впоследствии было пять эпизодов желудочковой тахикардии, четыре из них удалось купировать лишь электрической дефибрилляцией. В межприступный период состояние относительно удовлетворительное. Лечение хорошо купирует проявления ИБС, но не предупреждает приступов тахикардии.
Кожные покровы влажные. Умеренная иктеричность склер. Пульс частый (200 в минуту), ритмичный, ослаблен. АД 100/85 мм рт. ст. В легких дыхание проводится равномерно с обеих сторон, выслушиваются застойные хрипы в нижних отделах. В проекции верхушки сердца выслушивается систолический шум, проводящийся в подмышечную область. Печень выходит из-под нижнего края реберной дуги на 4,5 см. Живот мягкий, участвует в акте дыхания.
Приступ тахикардии был купирован программированной стимуляцией и проведено обследование. На ЭКГ ритм синусовый, 60—80 в минуту. Рубцовые изменения в передне-перегородочно-верхушечной области с признаками аневризмы. На ФКГ амплитура I тона в первой и второй точках снижена. Шумы не зарегистрированы. Рентгенологически определяется нарушение сократительной функции миокарда. Аневризма в области верхушки и передней стенки левого желудочка. Эхокардиография: створки митрального клапана тонкие, не изменены, открытие их полное. Митральный клапан смещен к задней стенке левого желудочка. Аневризма левого желудочка. Во время холтеровского мониториро-вания выявлена бифокальная левожелудочковая экстраси-столия по типу единичной, би- и тригеминии. Радионуклид-ное исследование (сцинтиграфия миокарда): характер перераспределения препарата позволяет предположить наличие в верхушке и в переднеперегородочной области постинфарктного кардиосклероза, а в области заднебоковой стенки — очаги ишемии. При приеме нитроглицерина сцин-тиграфическая картина не меняется. Проведены коронаро-графия и вентрикулография.
Отмечается выраженная патология коронарных артерий. Левая коронарная артерия в дистальном отделе сужена на 50%. Передняя межжелудочковая ветвь (ПМЖВ) и огибающая ветвь (ОВ) левой коронарной артерии в проксимальных отделах сужены более чем на 75%. Правая коронарная артерия (ПКА) сужена на трех уровнях более чем на 75%. При контрастировании левого желудочка отмечается анев-ризматическое выпячивание передневерхушечной области левого желудочка. Регургитация контрастного вещества в полость левого предсердия (+ +). Общая фракция выброса левого желудочка 0,20, фракция сокращающейся части 0,31. После приема нитроглицерина отмечается улучшение сокращения по заднебазальной стенке левого желудочка. Общая фракция выброса возросла до 0,27, а фракция сокращающейся части до 0,39.
На основании данных объективного обследования был поставлен диагноз: хроническая ИБС. Атеросклероз коронарных сосудов с сужением ПМЖВ, ОВ и ПКА более чем на 75%. Постинфарктный кардиосклероз с образованием аневризмы по переднеперегородочно-верхушечной области с переходом на боковую стенку. Митральная недостаточность (+ +). Пароксизмальная желудочковая тахикардия, рефрактерная к лекарственной терапии. Недостаточность кровообращения ПА стадии.
При выборе тактики лечения мы были вынуждены принимать во внимание ряд соображений. Консервативное лечение с применением антиаритмических препаратов оказалось
528
безрезультатным, а приступы пароксизмальной тахикардии носили упорный характер и снимались лишь электрической дифибрилляцией. Таким образом, встал вопрос о хирургическом лечении. В пользу операции было также следующее: наличие у больной хронической аневризмы левого желудочка, множественные стенозы коронарных артерий, умеренная митральная недостаточность. Анализ коронарографии показал, что ПМЖВ и ОВ левой коронарной артерии проходят в рубце аневризмы и эффект от шунтирования этих артерий будет минимальным. Наличие стеноза ПКА на трех уровнях делает нецелесообразным шунтирование и этой артерии. А если не шунтировать артерии, перенесет ли больная операцию? По-видимому, удовлетворительная реакция на нитроглицерин до определенных пределов позволит компенсировать коронарный кровоток нитратами. Вопрос относительно коррекции митрального клапана решали непосредственно во время операции после пальцевой ревизии клапана. Принято решение сделать этой немолодой больной операцию, направленную на устранение тахикардии и аневризмы, не изменив при этом коронарного кровотока. Это было сложное, не оптимальное, но вынужденное решение. По-видимому, такие ситуации нередко встречаются при коррекции сочетанной патологии.
Во время операции доступ к сердцу осуществлен путем срединной стернотомии. Сердце значительно увеличено в размерах за счет аневризматического образования по пе-реднебоковой стенке левого желудочка. Выраженный спаечный процесс. Сердце полностью выделено из сращений (вынужденная процедура для проведения картирования сердца). Проведено эпикардиальное картирование на синусовом ритме, а затем при индуцированной желудочковой тахикардии (тахикардия вызвана и прекращена програмированной электрической стимуляцией сердца). При картировании на синусовом ритме выявлена обширная зона «задержанной активности». После индукции тахикардии была локализована аритмогенная область в 41—42—43-й точках желудочков сердца. В этих зонах возбуждение опережало приход возбуждения в референтную область на 90—100 мс (рис. 4.38). Далее была проведена ревизия коронарных артерий и пальцевая ревизия митрального клапана. Обнаружена умеренная центральная регургитация, обусловленная растяжением кольца клапана. ПМЖВ и ОВ втянуты в аневризматический рубец, в ПКА определялся кальциноз на протяжении. Введены канюли в аорту и полые вены. Начата гипотермическая перфузия при температуре 25° С. Продольным разрезом вскрыт левый желудочек через аневризматическое выпячивание. Зона наиболее раннего возбуждения локализована в переходной области — на границе фиброза и здоровой ткани. Произведена резекция аневризмы, а затем трехкратное воздействие на аритмогенную область в течение 3 мин (каждое) при температуре 70е С. Дополнительно произведен разрез глубиной 3 мм для ограничения всей зоны фиброза. Разрез левого желудочка ушит П-образным и непрерывным швом.
Больная согрета. Сердечная деятельность через синусовый ритм восстановлена одним разрядом дефибриллятора. Отключен АИК. Проведено электрофизиологическое исследование. В послеоперационном периоде желудочковая тахикардия не индуцируется. Послеоперационное течение без особенностей. Заживление послеоперационной раны первичным натяжением. Через год после операции приступов желудочковой тахикардии не наблюдалось. Больная принимает сустак-мите по 2,6 мг и дигоксин по 0,00125 г 3 раза в день. Состояние удовлетворительное. Она активна, выполняет значительный объем физической работы дома и на даче.
Одновременно с этим в последние годы значительно изменились представления об отдаленных результатах хирургического лечения больных, у которых снижена сократительная функция миокарда. Это привело к тому, что в хирургии злокачественных желудочковых аритмий, сочетающихся с аневризмой сердца, большое значение стали придавать реконструкции левого желудочка, что в свою очередь усилило насосную функцию сердца и привело к улучшению качества жизни и увеличению ее продолжительности.
В современном понимании у такого больного необходимо нормализовать миокардиальный кровоток в бассейнах пораженных артерий, восстановить насосную функцию сердца и устранить субстрат тахиаритмий. Анализ отдаленных результатов хирургического лечения злокачественных желудочковых аритмий на нашем материале свидетельствует о том, что методика хирургического лечения оказывает выраженное влияние на результаты такого лечения. Из 35 наблюдавшихся нами больных 13, которые были оперированы в 1981—1988 гг., пластику левого желудочка после аневризм-эктомии производили по обычной методике с использованием линейного шва, а очаг аритмии устраняли криовоздей-ствием в аритмогеннои зоне. Другим 13 больным, которых оперировали в 1989— 1990 гг., выполняли циркулярную эн-докардиальную резекцию с криодеструкцией аритмогеннои зоны, а для пластики аневризмы использовали прием Жате-не, позволяющий сузить отверстие, образовавшееся в результате резекции аневризмы, примерно на 7з> с наложением двух полукисетных швов и последующим их затягиванием. Уменьшенный таким образом дефект ушивали по обычной методике. Наконец, начиная с 1991 г. мы прооперировали 10 больных, которым произвели расширенную резекцию фиброзно измененного эндокарда и криодеструкцию аритмогеннои зоны с одновременной реконструкцией левого

529




I—продольное вскрытие аневризмы левого желудочка на всем протяжении до границы с непораженными тканями; II—тщательное отсепаровывание всего эндокардиального фиброза с апикального отдела межжелудочковоп перегородки; III—сужение устья аневризматического мешка: а — поперечный срез сердца на уровне аневризмы сердца. Накладывают два полукисетных шва с внутренней поверхности свободной стенки левого желудочка и межжелудочковой перегородки; б — после затягивания швов диаметр устья аневризматического мешка уменьшается до 2,0—2,5 см и устье смещается к верхушке левого .желудочка; IV— пластика дефекта заплатой, сформированной из фиброзного эндокарда и расположенной перпендикулярно продольной оси левого желудочка. Правый и левый желудочки имеют собственные независимые верхушки. Ао — аорта; JIA —легочная артерия; ПП—правое предсердие; ПЖ—правый желудочек; ЛЖ—левый желудочек; ПАЛЖ—постинфарктная аневризма левого желудочка; ПМЖВ—передняя межжелудочковая артерия; ПКА—правая коронарная артерия; ИМП — область фиброзной ткани межжелудочковой перегородки, вовлеченной в аневризматический процесс; ФЭ— фиброзный эндокард; ЗФЭ— заплата, сформированная из фиброзного эндокарда.
530
желудочка и шунтированием всех хирургически суженных артерий, в том числе ПМЖВ, даже если она попадала в рубец. Эта методика требует некоторого пояснения. В 1984 г. V. Dor предложил операцию эндовентрикулярной циркулярной пластики с исключением акинетической перегородки. На первом этапе своей деятельности этот хирург считал достаточным для устранения сопутствующей тахикардии выполнять резекцию фиброзно измененного эндокарда. Позже для устранения аритмии он стал выполнять крио-деструкцию в двух противоположных местах отслоенного эндокарда. Методика, использованная нами у больных, оперированных с 1991 г., сочетает комбинацию ряда приемов Jatene и Dor, а также принципы электрофизиологической хирургии.
После стернотомии и вскрытия перикарда выполняют картирование сердца для установления зоны тахикардии. Подключают аппарат искусственного кровообращения, охлаждают больного до 28—26° С и останавливают сердце с помощью кристаллоидной фармакохолодовой кардиопле-гии. В продольном направлении широко вскрывают аневри-зматический мешок (рис. 4.39). Принципиально важен следующий этап операции. От медиального края разреза от-сепаровывают фиброзно измененный эндокард на всем протяжении пораженной части межжелудочковой перегородки до здорового миокарда. Затем аналогичным образом отслаивают эндокард от латерального края разреза. После завершения этой процедуры формируют два полукисетных шва Жатене (не затягивают) и выполняют криовоздействие в зоне аритмии. Далее швы затягивают по методике Жатене, а из листков отсепарованного фиброзного эндокарда формируют лоскут для закрытия дефекта. Диаметр лоскута, как правило, не превышает 2,5 см. Ориентации лоскута следует уделять особое внимание: он должен занимать строго перпендикулярное положение относительно продольной оси левого желудочка. Фиброзно измененный эндокард нельзя использовать в качестве заплаты в тех случаях, когда апикальный отдел межжелудочковой перегородки кальцинирован. {. В этом случае мы применяем дакроновый протез, на внут-[ ренней поверхности которого фиксируем аутоперикард.
Завершив операцию по устранению аневризмы сердца, [производят шунтирование коронарных артерий. После выполнения всей операции по восстановлению сердечной дея-|тельности проводят электрофизиологическое исследование
для установления адекватности устранения желудочковой тахикардии. Описанная выше операция в настоящее время, по-видимому, является оптимальной у больных с постинфарктными аневризмами сердца, сочетающимися со злокачественными желудочковыми аритмиями сердца. Использованная нами методика реконструкции геометрии левого желудочка позволяет значительно повысить сократительную функцию миокарда. С одной стороны, операция, в результате которой фиброзно измененный эндокард отслаивается на всем протяжении перегородки, исключает из сокращения левого желудочка ослабленный участок перегородки, с другой стороны, прием Жатене позволяет сформировать новую верхушку левого желудочка и таким образом создать принципиально новые условия для изгнания крови из левого желудочка. Оставшийся участок перегородки в правом желудочке не оказывает выраженного влияния на его сократительную функцию. Шунтирование ПМЖВ позволяет улучшить кровоснабжение функционирующего участка межжелудочковой перегородки. Наконец, электрофизиологическое исследование дает возможность эффективно бороться с аритмией.
Осложнения после операции. Основным осложнением операции следует считать неустранение очага аритмии. Рецидив тахикардии в раннем послеоперационном периоде, как правило, приводит к смерти. Другим грозным осложнением является острая сердечная недостаточность, которая наиболее часто наблюдается при круговой эндокардиальной резекции по методу 1ирадона.
К другим осложнениям относятся осложнения, связанные с неадекватной защитой миокарда, неадекватной реваскуля-ризацией, повышенной травматичностью миокарда и т. д. Вот почему только в стационарах, где хирурги имеют большой опыт практической работы, можно получить результаты, отражающие широкие возможности кардиохирургии в лечении желудочковой тахикардии.
Непосредственные и отдаленные результаты. Суммарный клинический опыт, имеющийся в литературе, свидетельствует о том, что наилучшие результаты достигаются при резекции всего фиброзного эндокарда. При этом госпитальная летальность составляет 12, а поздняя—10%. Пятилетняя актуарная выживаемость составляет 68%, а для больных I и II класса, по классификации Нью-йоркской ассоциации кардиологов,— 78 %.
5
Ишемическая болезнь
сердца
