
книги / Физика металлов
..pdf3. ТЕОРИИ ЭЛЕКТРОНОВ И СТРОЕНИЕ АТОМА
Электронные теории описывают свойства металлических тел на основании моделей состояний электронов в этих телах. Состояние электронов анализируется исходя из представлений
остроении металлов.
Кконцу XIX века был накоплен достаточно большой экспериментальный материал о физических свойствах металлов: выяснилось, что они обладают высокой тепло- и электропроводностью, характерным металлическим блеском, были определены значения теплоемкости и т.д.
По закону Ома даже при самых малых значениях напряжения на участке металлического проводника возникает пропорциональный этому напряжению ток с коэффициентом пропорциональности 1 / R, причем эта пропорциональность сохраняется
и при высоких значениях напряжения. Если бы электроны были связаны с атомами, то существовало бы пороговое значение напряжения, при котором возникает ток, или при малых значениях напряжения электросопротивление было бы больше, чем при больших. Отсутствие этих явлений свидетельствует о том, что электроны в металле ведут себя как свободные.
Ричард Толмен и Томас Стюарт в своих опытах, исходя из представления о свободе электронов, предположили, что при торможении проводника электроны в нем должны двигаться по инерции. Они исследовали катушку из металлической проволоки (медной, алюминиевой и серебряной), которая приводилась во вращение вокруг своей оси, а затем резко тормозилась. Чувствительный гальванометр на концах катушки в момент торможения вращения показывал прохождение тока.
Таким образом, к началу XX века сложилось представление об электронах в металлах как о свободных частицах, а об электрическом токе – как о направленном и упорядоченном
31
движении заряженных частиц под действием внешнего электрического поля.
Эрнст Резерфорд в своих опытах убедительно показал, что атомы состоят из ядра и электронной оболочки. Ядро несет положительный заряд, а электронная оболочка – отрицательный.
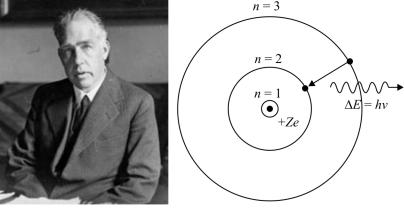
Теоретическое обоснование атомной модели Резерфорда было дано Нильсом Бором. С позиций классической электродинамики электрон, который двигается вокруг ядра, должен непрерывно излучать энергию и в результате потери энергии упасть на ядро. Бор предположил, что электроны двигаются по стационарным орбитам, где они не излучают энергию, однако при переходе с орбиты на орбиту они могут излучать или поглощать энергию. В качестве стационарных орбит Бором приняты окружности, на которых момент количества движения, т.е. момент импульса, равен целому числу приведенных постоянных Планка:
mevr = n=.
а |
б |
Рис. 19. Датский физик Нильс Бор (а)
и его теоретическое описание строения атома (б) [7]
32
Бор применил эти допущения с использованием ряда представлений классической физики, в том числе положения о равенстве кулоновской силы притяжения электрона к ядру и центробежной силы вращающегося электрона, и вывел уравнения для стационарной орбиты и энергии электрона на этой орбите:
|
r |
= |
4πε 0 =2 |
n2 |
и E = − |
Ze2 |
, |
|
|
8πε 0 r |
|||||
|
n |
|
Zmee2 |
|
|
||
где n – |
номер орбиты; |
|
|
|
|||
ћ – |
приведенная постоянная Планка; |
|
|||||
me – масса электрона; |
|
|
|
||||
e – |
заряд электрона; |
|
|
|
|||
Z – |
количество протонов в ядре; |
|
|||||
ε0 – |
диэлектрическая постоянная. |
|
|||||
Теория Бора объяснила дискретность энергетических состояний атомов, наличие спектров излучения с применением квантовых представлений о наличии стационарных состояний электронов и скачкообразном переходе между ними. В то же время эта теория не смогла объяснить различную интенсивность спектральных линий, она работает только для водородоподобных атомов и не смогла полностью уйти от классических представлений, так как включает классической уравнение движения электрона и квантовое уравнение стационарных орбит [7]. Теория Нильса Бора привела к появлению квантовой механики.
В современной физике электронное строение атомов и кристаллов описывается в рамках квантовой механики, которая основана на ряде принципов. Основные из них:
1. Корпускулярно-волновой дуализм: вещество обладает двойственной природой – одновременно может проявлять себя и как частица, и как волна. Этот принцип описывается уравнением Луи де Бройля:
33

λ = h , mv
где h – постоянная Планка;
v– скорость электрона.
2.Принцип неопределенности Гейзенберга: невозможно одновременно точно определить координаты и импульс частицы. Этот принцип описывается выражением
∆ x∆ ≥p = , 2
где ∆x – погрешность при определении координаты; ∆p – погрешность при определении импульса.
3. Уравнение Шредингера. Движение и положение элементарной частицы в пространстве носит вероятностный характер и описывается с помощью волновой функции распределения вероятностей:
|
= |
|
∂ 2ψ |
|
∂ ψ 2 |
∂ ψ |
2 |
|
|
+ U ψ = Eψ , |
||
− |
|
|
|
|
+ |
|
|
+ |
|
|
|
|
|
∂ x |
2 |
∂ y |
2 |
z |
2 |
||||||
|
2m |
|
|
|
∂ |
|
|
|
||||
где ψ – волновая функция (пси).
Полная энергия электрона состоит из кинетической и потенциальной и зависит от значения волновой функции в пространстве, т.е. носит вероятностный характер.
4. Принцип запрета Паули: в одном квантовом состоянии не может находиться более одного электрона. Следствием этого принципа является наличие электронных оболочек в атоме, что делает возможным разнообразие химических элементов и их соединений.
Квантовое состояние описывается четырьмя квантовыми числами:
1. Главное квантовое число n. Определяет энергию элек-
трона (n = 1, 2, 3, …).
34
2.Орбитальное квантовое число l. Определяет форму ор-
битали: l = (n – 1).
3.Магнитное квантовое число m. Показывает ориентацию орбит в пространстве: m = ±l.
4.Спиновое квантовое число s. Характеризует вращение электрона вокруг своей оси: s = ±½.
Теории электронного строения металлов
В развитии представлений об электронном строении металлов можно выделить три основные этапа.
1. Классическая электронная теория (П. Друде и Л. Ло-
ренц, начало XX века) [19]. Классическая теория основана на предположении, что валентные электроны в металле являются свободными частицами, которые могут свободно перемещаться во всех направлениях. Они являются одинаковыми твердыми сферами, двигающимися по прямым линиям до столкновения друг с другом или ионами кристаллической решетки, время контакта частиц пренебрежимо мало по сравнению со временем «свободного» движения.
При отсутствии внешнего электрического поля электроны перемещаются хаотически. В случае возникновения внешнего электрического поля на каждый электрон начинает действовать сила – еЕ и электрон приобретает составляющую скорости в направлении – Е. При этом происходит постепенное смещение всех хаотически движущихся электронов в направлении поля, возникает результирующий перенос заряда – электрический ток.
Плотность тока можно определить как произведение количества электронов n0, их заряда e и средней скорости их упорядоченного движения v :
j = n0e v ,
причем средняя скорость упорядоченного движения
35

v = − eE τ , 2m
где Е – приложенное напряжение; m – масса электрона;
τ– время прогона электрона между двумя столкновениями. Отсюда
j = ne2 τ E = σ Е. 2m
Таким образом, проводимость
σ = ne2 τ . 2m
Среднее время прогона электрона между двумя столкновениями можно представить в виде
τ = |
l |
|
, |
|
ν 2тепл+ ν |
2 |
|||
|
|
где ν тепл – скорость теплового движения электронов.
Средняя кинетическая энергия теплового движения электронов
Е |
= |
3 |
kT = |
mν 2тепл |
, |
|
||||
|
|
|
|
|||||||
к e |
2 |
|
|
|
|
2 |
|
|
||
|
|
|
|
|
|
|
||||
отсюда |
|
|
|
|
|
|
|
|
|
|
|
vтепл = |
|
3kT |
. |
|
|
||||
|
|
|
|
|
||||||
|
|
|
|
|
|
m |
|
|
||
При комнатной температуре v |
тепл |
≈ 106 |
м/с, а ν = 6 10−4 |
м/с. |
||||||
|
|
|
|
|
|
|
|
|||
Следовательно, скоростью упорядоченного движения можно пренебречь. Тогда
36

τ = l , v
где l – длина среднего пробега электрона между двумя столкновениями.
Вэтом случае проводимость
σ= ne2l . 2mv
Классическая электронная теория имеет следующие недостатки:
1.По данным теории длина свободного пробега электрона равна 10–8 –10 –9 м, т.е. электрон пролетает без столкновения до нескольких сотен межатомных расстояний, что не соответствует действительности.
2.Температурная зависимость электросопротивления, полученная в рамках теории, не соответствует экспериментальным
данным: теоретически ρ T , а экспериментально ρ Т.
3.Теория оказалась внутренне противоречивой, так как высокие тепло- и электропроводность определяются из соображения, что электроны – это свободные частицы в рамках кристалла.
Ареальные значения теплоемкости можно получить при условии, что валентные электроны входят в состав атомов, т.е. не вносят вклад в теплоемкость. Электроны также должны вносить вклад в теплоемкость: теоретически для одновалентного металла – 4,5 R, для двухвалентного – 6 R, а экспериментально – 3 R.
2.Квантовая теория свободных электронов (А. Зом-
мерфельд). Эта теория основана на тех же экспериментальных фактах, что и классическая теория электронов. Однако состояние электронов описывается с помощью волновых функций, а распределение электронов по состояниям – законами квантовой статистики.
37

Энергетический спектр электронов. Энергию электрона как микрочастицы можно выразить через кинетическую составляющую:
Ек e = mν ср2 .
2
После подстановки скорости из уравнения Луи де Брой-
ля ( λ = |
h |
) в уравнение для кинетической энергии частицы |
||||||
mν |
||||||||
|
|
|
|
|
|
|
||
получим: |
|
|
|
|
|
|
||
|
|
Е |
= |
h2 |
. |
|
|
|
|
|
|
|
|||||
|
|
к e |
2λ 2 m |
|
||||
Если в это выражение ввести волновое число k = |
2π |
, |
||||||
λ |
||||||||
|
|
|
|
|
|
|
||
которое показывает, сколько раз длина волны данного волнового процесса укладывается на отрезке длинной 2π, получим:
Рис. 20. Зависимость энергии электрона от значений волнового вектора
Ек e = =2 k 2 .
2m
Если построить график для энергии электронов от волнового вектора (рис. 20), то мы увидим один существенный недостаток теории – энергетический спектр свободной микрочастицы непрерывен и, следовательно, все кристаллы в этом случае должны быть проводниками.
Функция распределения Ферми – Дирака. Распределе-
ние электронов по состояниям определяется тем, что энергия всей электронной подсистемы должна быть минимальной. В со-
38
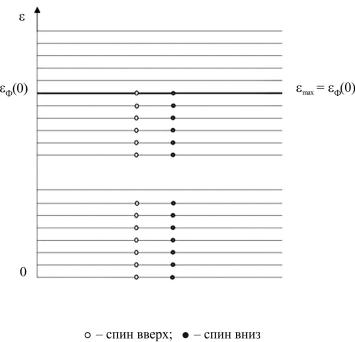
ответствии с принципом запрета Паули в одном квантовом состоянии не может находиться более одного электрона. При заполнении уровней с меньшей энергией электроны заполняют более высокие энергетические уровни.
В k-пространстве каждому энергетическому состоянию электрона соответствует значение вектора k. Поверхности с одинаковой энергией электронов в k-пространстве называются поверхностями Ферми, а максимальная энергия занятых электронами состояний называется энергией Ферми и обозначается как ε Ф .
Вся электронная оболочка в данном случае располагается внутри сферы с радиусом kФ – сфера Ферми, что соответствует состоянию наименьшей энергии.
Схема положения электронов на электронных орбитах по энергиям показана на рис. 20.
Рис. 20. Распределение электронов по орбиталям при абсолютном нуле:
39

Сравнивая полученный результат с распределением Ферми – Дирака при T = 0, приходим к выводу, что максимальная энергия электронов Emax совпадает с энергией Ферми ε Ф (0).
Функция распределения Ферми – Дирака имеет вид
|
f (ε )= 1 / exp ((ε − ε |
Ф |
) / kT )+ 1 , |
|
|
|
|
где ε – |
энергия электрона; |
|
|
k – |
постоянная Больцмана; |
|
|
T – |
абсолютная температура. |
|
|
Распределение функции Ферми – |
Дирака по энергиям в за- |
||
висимости оттемпературы приведено на рис. 21.
Рис. 21. Распределение функцииФерми– Диракавзависимости оттемпературы: 1 – 0 К; 2, 3 и4 – болеевысокие температуры[20]
При увеличении температуры (от 1 до 4) происходит вырождение, или размытие, функции Ферми, другими словами, термическое разрыхление электронной оболочки. Зона термического разрыхления с ростом температуры увеличивается. Вырождение электронного газа происходит при температуре Ферми, когда энергия теплового движения электронов соизмерима с энергией Ферми [20]:
θ Ф= ε Ф / k.
40
