
- •Газовые смеси
- •1.1. Основные признаки газовых смесей
- •1.2. Основные понятия и определения газовых смесей
- •1.3. Способы задания состава смеси реальных газов
- •1.4. Смеси идеальных газов
- •1.4.1. Характеристические функции и функции состояния газовых смесей
- •1.4.1.1. Удельные значения функций и параметров смеси газов
- •По аналогии с внутренней энергией можно получить формулу для удельной энтальпии смеси газов iсм , Дж / кг:
- •1.4.1.2. Мольные значения функций и параметров смеси газов
- •1.4.2. Парциальное давление.
- •1.4.3.Парциальный объем.
- •1.4.4. Задание состава смеси идеальных газов объемными долями.
- •1.4.5. Формулы пересчета для различных способов задания состава газовых смесей
- •1.4.6. Кажущаяся молекулярная масса смеси газов
- •1.4.7. Газовая постоянная смеси газов
- •1.4.8. Плотность смеси газов
- •1.4.9. Энтропия смеси идеальных газов
- •1.4.10. Теплоемкость газовой смеси
- •1.4.11. Коэффициент теплопроводности, коэффициент динамической вязкости газовой смеси.
- •1.4.11.1. Бинарные смеси
- •1.4.11.2. Многокомпонентные смеси
- •2. Смешение газов
- •Смешение газовых потоков
- •Температура смеси газовых потоков
- •Объемный расход смеси газовых потоков
- •2.2.3. Частные случаи смешения газовых потоков
- •Содержание
1.4.7. Газовая постоянная смеси газов
Удельная газовая постоянная однородного газа, заменяющего смесь, называется газовой постоянной смеси Rсм, Дж / (кг·К):
 ,
,
или окончательно
![]() .
.
Через мольные доли газовая постоянная смеси вычисляется следующим образом:
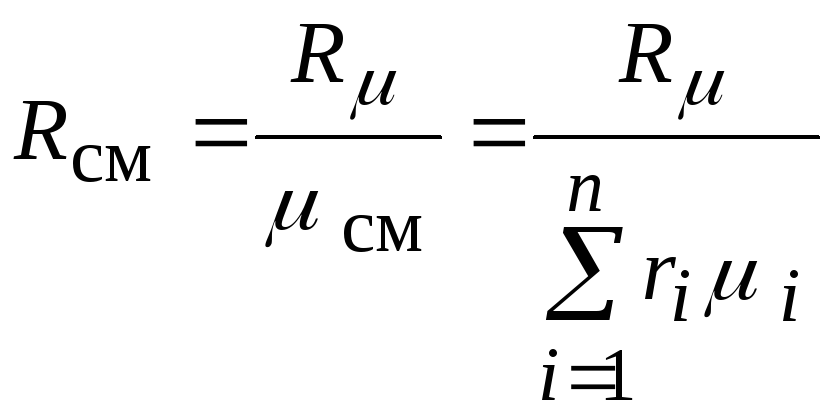 ,
или окончательно
,
или окончательно
 .
.
С использованием
![]() можно получить формулу для вычисления
парциального давления идеального газа
можно получить формулу для вычисления
парциального давления идеального газа
![]() через его массовую долю.
через его массовую долю.
Т. к. ![]() и
и ![]() ,
,
то разделив эти выражения друг на друга получим:
![]() ,
,
откуда ![]()
Из последнего выражения можно получить удобную формулу, связывающую мольные и массовые доли идеального газа.
Т. к. ![]() ,
,
то ![]()
1.4.8. Плотность смеси газов
Плотность однородного газа, заменяющего смесь, называется плотностью смеси:
![]()
В справочниках обычно приводится без объяснений следующая формула для плотности смеси:
![]()
В то же время в технической литературе встречаются формулы вида
![]()
С вычислением
плотности смеси через плотности
компонентов связано наибольшее число
студенческих ошибок. Дело в том, что
значение плотности
![]() -го
компонента можноформальнополучить из двух формул:
-го
компонента можноформальнополучить из двух формул:
![]()
![]()
и ![]()
![]()
Т.
к.
![]() ,
то значения
,
то значения![]() и
и![]() заметно отличаются друг от друга.
заметно отличаются друг от друга.
Проясним вопрос с вычислением плотности смеси.
По определению
![]() и
и![]() ,
тогда
,
тогда![]() .
.
Но
![]() и
и![]()
Т.
о. в последней формуле плотность i-го
газа![]() вычисляется как плотность этого газа,
находящегося в количестве
вычисляется как плотность этого газа,
находящегося в количестве![]() килограммовв объеме
килограммовв объеме![]() (парциальном объеме) при давлении
смеси
(парциальном объеме) при давлении
смеси ![]() и температуре смеси
и температуре смеси ![]() .
.
Такое толкование плотности компонентов смеси используется, в частности, при расчетеобъемов продуктов сгорания топлива.
Если плотность
i-го газа в смеси
вычислять через его парциальное давление![]()
![]() ,
то
,
то 
Т.
о. в этой формуле плотность i-го
газа![]() - это плотность газа массой
- это плотность газа массой![]() ,
находящегося вобъеме
,
находящегося вобъеме ![]() (объем
смеси) при его парциальном давлении
(объем
смеси) при его парциальном давлении ![]() и температуре
и температуре![]() (температуре смеси).
(температуре смеси).
Такое толкование плотности компонентов смеси, в частности, используется при определении абсолютной и относительной влажности воздуха.
1.4.9. Энтропия смеси идеальных газов
Как указано в
параграфе 1.4.1., энтропия 1 кг
![]() -
компонентной смеси идеальных газов
(удельная энтропия смеси)Sсм
, Дж / (К · кг), определяется по
следующей формуле:
-
компонентной смеси идеальных газов
(удельная энтропия смеси)Sсм
, Дж / (К · кг), определяется по
следующей формуле:
![]() ,
,
где: ![]() -
энтропия 1 кгi-го газа.
-
энтропия 1 кгi-го газа.
Из курса общей термодинамики известно:
![]() ,
,
где: ![]() -
массовая изобарная теплоемкостьi-го
газа.
-
массовая изобарная теплоемкостьi-го
газа.
Окончательно
удельная энтропия
![]() -компонентной
смеси может быть вычислена по следующей
формуле:
-компонентной
смеси может быть вычислена по следующей
формуле:
![]()
1.4.10. Теплоемкость газовой смеси
По определению, теплоемкость - это количество теплоты, которое необходимо для изменения температуры единицы количества вещества
(
![]() )
на один градус.
)
на один градус.
Т. к. температура всех газов в смеси одинакова, то теплоемкость смеси, складывается из теплоемкостей всех компонентов, взятых в долях, соответствующих способу задания смеси:
![]() - массовая (удельная)
теплоемкость, Дж / (кг·К);
- массовая (удельная)
теплоемкость, Дж / (кг·К);
![]() - мольная теплоемкость,
Дж / (кмоль·К);
- мольная теплоемкость,
Дж / (кмоль·К);
![]() - объемная
теплоемкость, Дж / (м3·К).
- объемная
теплоемкость, Дж / (м3·К).
где: ![]() - массовая, мольная и объемная теплоемкостиi-го компонента.
- массовая, мольная и объемная теплоемкостиi-го компонента.
