
Лекция 9 Энтропия. Второе начало термодинамики
5.6.Второе начало термодинамики. Тепловой двигатель
Первое начало термодинамики представляет собой по сути обобщение закона сохранения энергии на тепловые явления. Оно устанавливает количественные соотношения между превращениями одних видов энергии в другие.
В отличие от него второе начало определяет условия, при которых возможны эти превращения, а также возможные направления протекания процессов. Оказывается, не все процессы, разрешенные первым началом, возможны.
Первое начало термодинамики запрещает создание вечного двигателя I рода, т.к. при этом нарушается закон сохранения энергии:
невозможен PERPETUUM MOBILE первого рода, т.е. такой периодически действующий двигатель, который совершал бы работу в большом количестве, чем получаемая им извне энергия.
Второе же начало термодинамики исключает возможность создания двигателя второго рода, т.е. такого периодически действующего двигателя, который получал бы тепло от одного резервуара и превращал бы это тепло полностью в работу.
Существует несколько формулировок второго начала.
1. Клаузиус (1850): невозможен самопроизвольный переход тепла от менее к более нагретому телу, или невозможны процессы, единственным конечным результатом которых был бы переход тепла от менее к более нагретому телу.
Тот факт, что, например, в холодильнике совершается переход тепла от холодильной камеры в комнату, не противоречит этому утверждению, поскольку этот процесс не является самопроизвольным: для его осуществления потребляется электрическая энергия.
2. Кельвин (1851): невозможны процессы, единственным конечным результатом которых было бы превращение тепла целиком в работу.
Казалось бы, что этому противоречит, например, процесс изотермического расширения идеального газа, где все полученное газом тепло превращается в работу. Однако это не единственный конечный результат процесса: при этом происходит изменение объема газа.
Заметим, что слово единственный в обеих формулировках является весьма существенным, без него они теряют смысл.
Приведенные формулировки второго начала эквивалентны, из одной неизбежно следует другая. В самом деле, если бы можно было осуществить процесс, запрещенный по Кельвину, то тепло, отнятое от какого-либо тела, можно было полностью превратить в работу, а затем, превратив эту работу целиком в тепло (трением), передать это тепло другому телу с более высокой температурой. В результате мы имели бы процесс, невозможный по Клаузиусу.
Если бы не второе начало, можно было легко решить энергетическую проблему — построить двигатель, который отнимал бы тепло из океанов и целиком превращал его в работу. Подобный двигатель по своим практическим последствиям представлял бы PERPETUUM MOBILE второго рода (в отличие от вечного двигателя — PERPETUUM MOBILE первого рода). При современном потреблении энергии человечеством температура океанов за 1000 лет уменьшилась бы не более чем на один кельвин.
Это позволяет перефразировать формулировку Кельвина так: перпетуум-мобиле 2-го рода невозможен, или невозможно создать тепловой двигатель с КПД η = 1. Напомним, КПД теплового двигателя η = А/Q, где Q — сообщенное двигателю тепло, А— произведенная им работа.
По существу все процессы в макросистемах являются необратимыми (строго говоря, таковыми являются и процессы, которые мы называли обратимыми — это идеализация, удобная для решения многих важных вопросов).
Возникает принципиальный вопрос: в чем причина необратимости? Это выглядит особенно странно, если учесть, что все законы механики обратимы во времени. И тем не менее, никто не видел, чтобы, например, разбившаяся ваза самопроизвольно восстановилась из осколков. Этот процесс можно наблюдать, если предварительно засняв на пленку, просмотреть ее в обратном направлении, но никак не в действительности.
Если происходит какой - либо тепловой процесс, то обратный процесс, т.е. процесс, при котором система проходит те же тепловые состояния, но только в обратном порядке, как правило, невозможен, т.к. тепловые процессы, вообще говоря, являются необратимыми.
Если, например, привести в соприкосновение два тела с разными температурами, то тепло пойдет от более нагретого тела к холодному, а обратный процесс, как известно невозможен, т.е. процесс необратим.
В той или иной степени необратимыми являются все происходящие в природе тепловые процессы, однако в некоторых случаях степень необратимости может оказаться столь незначительной, что процесс можно с достаточной точностью считать обратимым. Для достижения обратимости следует по возможности исключить в системе всякие процессы, имеющие характер приближения к тепловому равновесию (переход тепла от более нагретого тела к холодному, трение между телами и т.д). Примером обратимого процесса является адиабатическое расширение или сжатие газа. Характерная особенность обратимых процессов - их медленность - процесс должен быть настолько медленным, чтобы участвующие в процессе тела успевали в каждый момент времени оказываться в состоянии равновесия, соответствующим имеющимся в этот момент внешним условиям. Т.е. обратимый процесс - это непрерывная последовательность равновестных состояний.
Всякий реальный процесс осуществляется не бесконечно долго, а с конечной скоростью, поэтому он не может быть полностью обратимым. В системе тел, находящихся в равновесии, без внешнего вмешательства никаких процессов происходить не может, т.е. с помощью тел, находящихся в тепловом равновесии, нельзя произвести никакой работы, т.к. работа связана с механическим движением, т.е. с переходом внутренней энергии в кинетическую энергию.
С этой посылкой связано еще одна формулировка второго начала термодинамики:
невозможно получить работу за счет энергии тел, находящихся в тепловом равновесии.
Итак, работу можно произвести только с помощью системы тел, не находящихся в тепловом равновесии.
Любой двигатель представляет собой систему, которая совершает многократно некий круговой процесс (цикл).
В ходе цикла рабочее вещество сначала расширяется до объема V2 , а затем сжимается до первоначального объема V1. При расширении рабочему веществу сообщается тепло Q1 , а при сжатии отбирается тепло Q`2 . Работа A, совершаемая за цикл, равна площади цикла на диаграмме в координатах pV (рис.5.6): A=Q1 - Q2 / .
 Периодически
действующий двигатель, который совершает
работу за счет получаемого из вне тепла,
называется тепловой машиной. Не
все получаемое системой тепло Q1
идет на получение полезной работы, часть
его Q2
/
должна быть возвращена во внешнюю
среду. Очевидно, чем меньше Q2
/
, тем машина выгоднее, поэтому коэффициент
полезного действия тепловой машины
определяется выражением:
Периодически
действующий двигатель, который совершает
работу за счет получаемого из вне тепла,
называется тепловой машиной. Не
все получаемое системой тепло Q1
идет на получение полезной работы, часть
его Q2
/
должна быть возвращена во внешнюю
среду. Очевидно, чем меньше Q2
/
, тем машина выгоднее, поэтому коэффициент
полезного действия тепловой машины
определяется выражением:
![]()
![]() .
(5.12)
.
(5.12)
З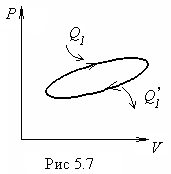 начение
η=
1 запрещено вторым началом термодинамики.
Если цикл, изображенный на рис. 5.6,
обратить, то получится цикл холодной
машины. Она отбирает от тела с температурой
T2
тепло Q2
,и отдает телу с более высокой температурой
T1
тепло Q1/
.
начение
η=
1 запрещено вторым началом термодинамики.
Если цикл, изображенный на рис. 5.6,
обратить, то получится цикл холодной
машины. Она отбирает от тела с температурой
T2
тепло Q2
,и отдает телу с более высокой температурой
T1
тепло Q1/
.
Для работы теплового двигателя необходимо наличие двух резервуаров - с более высокой температурой T1 - нагреватель, он передает рабочему телу двигателя тепло Q1 , и с менее высокой температурой T2 , холодильник, которому двигатель отдает тепло Q2 / .
Для цикла на рис.5.7 если процесс совершается по часовой стрелке, то работа, производимая двигателем за цикл, А > 0.
П
V![]() — поглощенное
тепло,
— поглощенное
тепло,
![]() - отдаваемое тепло (Q
- отдаваемое тепло (Q![]() >0).
Опыт показывает, что тепло
>0).
Опыт показывает, что тепло
![]() неизбежно существует в любом
тепловом двигателе (как тепловой «шлак»).
По первому началу термодинамики за
цикл приращение внутренней
неизбежно существует в любом
тепловом двигателе (как тепловой «шлак»).
По первому началу термодинамики за
цикл приращение внутренней
энергии рабочего вещества ΔU = 0, поэтому
А
=
![]() -
-![]() .
.
Запреты, устанавливаемые вторым началом термодинамики, становятся понятными с открытием новой термодинамической величины — энтропии — и раскрытием ее физического смысла.
