
- •Ш. А. Пиралишвили, н. А. Мочалова, с. В. Веретенников термодинамика. Технические приложения
- •Рыбинск 2007
- •1.1. Способы задания газовой смеси
- •1.4. Энтропия газовой смеси
- •1.5. Задание для самостоятельного решения
- •1.6. Пример выполнения индивидуального задания
- •2. Процессы смешения
- •2.1. Процессы смешения в постоянном объеме
- •2.2. Задание для самостоятельной проработки
- •2.3. Пример выполнения расчета
- •2.4. Смешение в потоке
- •2.5. Индивидуальные задания по расчету
- •2.6. Пример выполнения индивидуального задания
- •2.7. Смешение при заполнении объема
- •2.8. Индивидуальное задание на расчет процесса смешения при заполнении объема
- •2.9. Пример выполнения индивидуального задания по расчету процесса смешения при заполнении объема
2.8. Индивидуальное задание на расчет процесса смешения при заполнении объема
Типичная
задача может быть сформулирована
следующим образом в резервуаре
содержащем
![]() м3
находится некоторый известный газ при
определенном давлении
м3
находится некоторый известный газ при
определенном давлении
![]() и температуре
и температуре![]() по
трубопроводу в него подается в течении
времени
по
трубопроводу в него подается в течении
времени![]() газ того же (или другого) химического
состава с расходом
газ того же (или другого) химического
состава с расходом![]() кг/с
при давлении
кг/с
при давлении![]() и
температуре
и
температуре![]() .
Гидравлические потери отсутствуют.
Считая газ идеальным определить параметры
образовавшейся смеси, рассчитать
энтропии и эксергию компонентов до
смешения и газовой смеси, определить
потери эксергии при смешении и построить
эксергетическую диаграмму.
.
Гидравлические потери отсутствуют.
Считая газ идеальным определить параметры
образовавшейся смеси, рассчитать
энтропии и эксергию компонентов до
смешения и газовой смеси, определить
потери эксергии при смешении и построить
эксергетическую диаграмму.
2.9. Пример выполнения индивидуального задания по расчету процесса смешения при заполнении объема
Условие задачи.
В
резервуаре объемом 5 м3
находится кислород под давлением 300 кПа
и температуре 47 °С.
По трубопроводу в резервуар после
открытия крана начинает поступать
углекислый газ под давлением
![]() МПа
и температуре
МПа
и температуре![]() °С
в течении 5 с с расходом 0,12 м3/с.
Считая газ идеальным, рассчитать
параметры газа после смешения. Найти
приращение энтропии, потери эксергии
и построить эксергетическую диаграмму.
Скорость течения углекислого газа
10 м/с.
°С
в течении 5 с с расходом 0,12 м3/с.
Считая газ идеальным, рассчитать
параметры газа после смешения. Найти
приращение энтропии, потери эксергии
и построить эксергетическую диаграмму.
Скорость течения углекислого газа
10 м/с.
|
Дано:
|
|
|
Р,
Т,
|
|
Задача на термодинамику идеальных газов. В процессе решения необходимо использовать уравнение Клапейрона-Менделеева, уравнения сохранения массы и энергии, первое и второе начало термодинамики, уравнение Гюи-Стодолы для расчета потерь эксергии на основании чего построить эксергетическую диаграмму процесса смешения при заполнении резервуара с кислородом, втекающим в него углекислым газом.
Решение.
Рассчитаем объем углекислого газа, поступившего в резервуар за заданный промежуток времени прокачки
![]() м3.
м3.
Воспользуемся законом сохранения и найдем массу газовой смеси в резервуаре
![]() .
.
Массы компонентов можно найти из уравнения Клапейрона-Менделеева в
предположении идеальности смешивающихся газов:
![]() .
.
Тогда масса углекислого газа, поступившая в резервуар, будет равна:
![]() кг.
кг.
Масса кислорода, содержащегося в баллоне до смешения:
![]() кг.
кг.
Таким образом, масса газовой смеси будет равна:
![]() кг.
кг.
Найдем массовые доли компонентов, входящих в смесь:
для кислорода
![]() ,
,
для углекислого газа
![]() .
.
Проверим баланс по сумме массовых долей
![]()
![]() .
.
Баланс сошелся.
Объемные доли компонентов можно найти по известным массовым долям, воспользовавшись соотношением:
![]() .
.
Кажущуюся молекулярную массу смеси определим, воспользовавшись очевидной зависимостью:
![]() .
.
Найдем газовые постоянные кислорода и углекислого газа:
![]() Дж/(кг×К);
Дж/(кг×К);
![]() Дж/(кг×К).
Дж/(кг×К).
После подстановки получим:
![]() кг/моль.
кг/моль.
Тогда объемная доля кислорода равна:
![]() ;
;
объемная доля углекислого газа;
![]() .
.
Проверка
![]() .
.
Газовая постоянная смеси равна
![]() Дж/(кг·К).
Дж/(кг·К).
Найдем по таблицам Приложения 2 удельные теплоемкости для кислорода и углекислого газа:
![]() кДж/(кг×К);
кДж/(кг×К);
![]() кДж/(кг×К);
кДж/(кг×К);
![]() кДж/(кг×К);
кДж/(кг×К);
![]() кДж/(кг×К).
кДж/(кг×К).
Запишем закон сохранения энергии для смешивающихся компонентов и газовой смеси:
![]()
или
![]() .
.
Откуда температура полученной в резервуаре смеси будет равна:
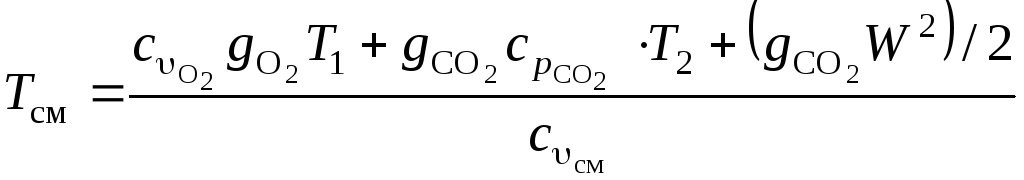 .
.
Теплоемкость
газовой смеси
![]() найдем по известной зависимости,
полученной для расчета газовых смесей:
найдем по известной зависимости,
полученной для расчета газовых смесей:
![]()
![]() кДж/(кг×К).
кДж/(кг×К).
После подстановки в предшествующую формулу, найдем результирующую температуру газовой смеси:
![]() К.
К.
Это значение необходимо уточнить, пересчитав теплоемкости компонентов и теплоемкость смеси, при температуре смеси и методом последовательных приближений, добиться требуемого совпадения выбора теплоемкостей как функции от температуры с рассчитанным значением температуры смеси.
Конечное
давление смеси
![]() можно найти из уравнения Клапейрона-Менделеева:
можно найти из уравнения Клапейрона-Менделеева:
![]() Па
= 0,5 МПа.
Па
= 0,5 МПа.
Вычислим энтропии компонентов в состоянии до смешения и энтропию газовой смеси после окончания процесса, заполнения объема.
Для расчета энтропии воспользуемся зависимостями, приведенными в первой главе пособия при расчете газовых смесей.
Энтропия газов до смешения:
кислорода:
![]()
![]() Дж/К
Дж/К
углекислого газа:
![]()
![]() Дж/К.
Дж/К.
Энтропия системы до смешения равна сумме энтропий кислорода и углекислого газа:
![]() Дж/К.
Дж/К.
Удельная энтропия системы до смешения:
![]() Дж/(кг·К).
Дж/(кг·К).
Найдем энтропию образовавшейся газовой смеси как сумму энтропии компонентов, входящих в нее
![]() .
.
Энтропия кислорода:
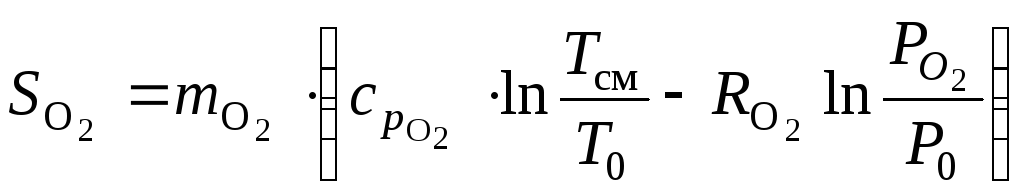 .
.
Энтропия углекислого газа:
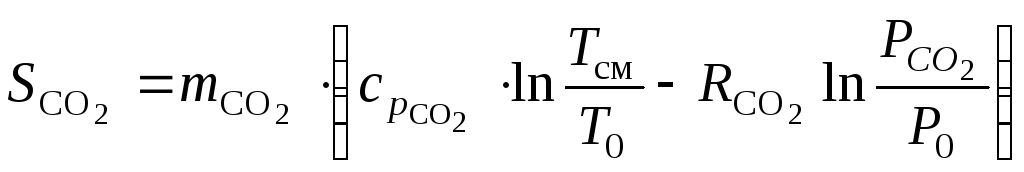 .
.
Найдем парциальное давление кислорода и углекислого газа в смеси:
![]() кПа;
кПа;
![]() кПа.
кПа.
Следовательно,
![]() Дж/К;
Дж/К;
![]() Дж/К.
Дж/К.
Тогда энтропия образовавшейся газовой смеси будет равна
![]() Дж/К.
Дж/К.
Найдем приращение энтропии за счет необратимости процесса смешения
![]() ;
;
![]() Дж
= 2,8 кДж.
Дж
= 2,8 кДж.
Потери эксергии De за счет необратимости процесса смешения найдем воспользовавшись уравнением Гюи-Стодолы
![]() кДж.
кДж.
Эксергию покоящегося газа можно найти, воспользовавшись известным соотношением [4]:
![]() ,
,
где
![]() – параметры системы (газа) соответствующие
состоянию окружающей среды;
– параметры системы (газа) соответствующие
состоянию окружающей среды;![]() – начальные параметры системы.
– начальные параметры системы.
Для потока газа эксергию 1 кг движущейся среды можно рассчитать, воспользовавшись зависимостью для потока [4]
![]() .
.
Дальнейшее
решение можно строить, предполагая газ
идеальным, а энтропию при
![]() К
равной нулю. В рассматриваемом примере
используем таблицы термодинамических
параметров газа по Ривкину [9], приведенных
в Приложении настоящего пособия.
К
равной нулю. В рассматриваемом примере
используем таблицы термодинамических
параметров газа по Ривкину [9], приведенных
в Приложении настоящего пособия.
Найдем значения удельной эксергии и эксергии m кг исходных систем до смешения.
Для
состояния, соответствующему нормальным
физическим условиям из таблиц Приложения
выпишем значения внутренней энергии
![]() .
.
![]() кДж/кг,
кДж/кг,
а
также их значения для начальной
температуры
![]() К:
К:
![]() кДж/кг.
кДж/кг.
Такие
же данные выпишем и для диоксида углерода
(СО2),
![]() К;
К;![]() кДж/кг;
кДж/кг;![]() кДж/кг;
для начального состояния
кДж/кг;
для начального состояния![]() К;
К;![]() кДж/кг;
кДж/кг;![]() кДж/кг.
кДж/кг.
Тогда
величина эксергии кислорода (![]() кг)
до смешения составит величину
кг)
до смешения составит величину
![]() .
.
Удельный объем кислорода при нормальных физических условиях
![]()
![]() кДж.
кДж.
Рассчитаем эксергию диоксида углерода
![]() .
.
Подставим численные значения
![]() кДж.
кДж.
Суммарная эксергия компонентов до смешения равна
![]() кДж.
кДж.
Найдем
эксергию газовой смеси, образовавшейся
в процессе смешения. Параметры газовой
смеси:
![]() °С,
°С,
![]() МПа.
МПа.
Удельные объемы компонентов после смешения:
– кислорода
![]() м3/кг;
м3/кг;
– диоксида
углерода
![]() м3/кг.
м3/кг.
Из
таблиц Приложения 2 выпишем значения
внутренних энергий при
![]() °С;
°С;
![]() кДж/кг;
кДж/кг;![]() кДж/кг.
кДж/кг.
Эксергия 18 кг кислорода в смеси равна
![]() .
.
После подстановки численных значений получим
![]()
![]() кДж.
кДж.
Эксергия диоксида углерода в смеси
![]()
![]() .
.
После подстановки численных значений получим
![]()
![]() кДж.
кДж.
Эксергия смеси, равна сумме эксергий компонентов
![]() кДж.
кДж.
Потери эксергии в процессе смешения составят
![]() кДж.
кДж.
