
Майданник -Педиатрия / Педиатрия_Майданник
.pdfлудочка. При втором типе дискретного субаортального стеноза фиброз- но-мышечное кольцо, расположенное под клапаном аорты, имеет толщину до 1 см и находится ниже, чем мембрана при первом типе заболевания, вовлекается в процесс и передняя створка мембранного клапана. При этом типе дискретного субаортального стеноза развиваются выраженное сужение выносящего тракта и гипертрофия левого желудочка. Существует еще одна разновидность сужения выносящего тракта левого желудочка диффузного характера — так называемое «туннелеподобное» сужение. Заболевание относится к быстро прогрессирующим аномалиям и может быть причиной смерти в раннем детском возрасте.
Быстрое прогрессирование заболевания и неблагоприятный исход обусловлены другими сопутствующими дефектами развития сердца: открытым артериальным протоком, коарктацией аорты, дефектом межжелудочковой перегородки, стенозом устья легочной артерии. Дискретный стеноз аорты часто осложняется бактериальным эндокардитом, что приводит к развитию регургитации и последующего протезирования клапана аорты.
Данные объективного исследования различных типов дискретного субаортального стеноза во многом идентичны. Определяются усиленный верхушечный толчок, систолическое дрожание над основанием сердца. Прослушивается систолический шум, который по тембровым характеристикам не отличается от такового при стенозе аорты и гипертрофической кардиомиопатии, он локализуется максимально на верхушке и в четвертом межреберье. При функциональных пробах изменения интенсивности систолического шума аналогичны таковым при стенозе аорты. Важным диагностическим признаком является определение протодиастолического шума полевому краю грудины, обусловленного аортальной регургитацией. У некоторых больных мезодиастолический шум может выслушиваться над верхушкой сердца, его появление связано с относительным стенозом митрального клапана вследствие ограничения движения передней створки митрального клапана.
При эхокардиографии не всегда удается выявить субаортально расположенную мембрану или фиброзно-мышечное кольцо. Существенным эхокардиографическим признаком является раннее систолическое прикрытие клапана аорты. Систолическое прикрытие характерно и для больных с гипертрофической кардиомиопатией. Однако при гипертрофической кардиомиопатии оно происходит в середине систолы, а при дискретном стенозе — в начале диастолы и связано с турбулентным движением крови при нарушении движения створок аорты.
Наиболее важным дифференциально-диагностическим критерием является наличие переднесистолического движения передней створки митрального клапана, асимметричная гипертрофия межжелудочковой перегородки, которые не встречаются при дискретном стенозе. Кроме того, у больных с гипертрофической кардиомиопатией при функциональных пробах, влияющих на систолический объем левого желудочка и сократимость его миокарда, меняется градиент внутрижелудочкового давления, при дискретном стенозе площадь суженного отверстия остается неизменной.
251
Гипертрофическая кардиомиопатия наблюлается при многих наследственно обусловленных нарушениях обмена веществ, митохондриалыюй патологии, нейромышечных и эндокринных заболеваниях, в частности при таких, как болезнь Помпе, болезнь Кори (или Фербеса), синдром Гурлера, синдром Хантера и др.
ЛЕЧЕНИЕ. Представляет большие трудности. Основная цель медикаментозной терапии — уменьшение систолической обструкции кровотока, улучшение диастолического наполнения левого желудочка и устранение аритмии. Для этого могут быть использованы бета-адрено- блокаторы, блокаторы кальциевых каналов и антиаритмические препараты.
Бета-адреноблокаторы (индерал, обзидан, пропранолол) способствуют увеличению наполнения левого желудочка, в какой-то мере уменьшают градиент давления и оказывают антиаритмическое действие.
Антагонисты кальция (нифедипин, коринфар, верапамил, изоптин) также благоприятно влияют на диастолическую функцию левого желудочка. Следует учесть, что антагонисты кальция типа нифедипина могут увеличить градиент давления ввиду выраженного сосудорасширяющего эффекта и их следует применять с осторожностью.
Для устранения нарушений ритма сердца у больных гипертрофической кардиомиопатией используют кордарон и аймалин. Для защиты от бактериального эндокардита показана профилактика антибиотиками.
Больным с гипертрофической кардиомиопатией противопоказаны кардиотонические средства (сердечные гликозиды) вследствие возможного увеличения систолической обструкции кровотока. Следует также избегать применения вазодилататоров и мочегонных средств или использовать их осторожно при лечении сопутствующей системной гипертензии или других заболеваний у больных с обструкцией выносящего тракта.
В последние годы применяется хирургическое лечение гипертрофической кардиомиопатии — иссечение части межжелудочковой перегородки. Операция показана больным с обструктивной формой заболевания и высоким градиентом давления (более 45 мм рт. ст.), если медикаментозная терапия не приносит желаемого результата.
РЕСТРИКТИВНАЯ КАРДИОМИОПАТИЯ. Это первичное или вторичное заболевание миокарда, характеризующееся диастолической дисфункцией, отсутствием дилатации или гипертрофии желудочка, наличием повышенного системного и легочного венозного давления.
Рестриктивная кардиомиопатия занимает особое место среди всех заболеваний миокарда и встречается редко.
ЭТИОЛОГИЯ. Причиной рестриктивной кардиомиопатии считают фибропластический эндомиокардит Леффлера, наблюдающийся при гиперэозинофилии различного происхождения (эозинофильный васкулит, идиопатический гиперэозинофильный синдром и т.д.).
Еще одна форма, относящаяся к заболеваниям этого класса, — эндокардиальный фиброэластоз, который выявляется у новорожденных и детей раннего возраста. Заболевание почти всегда заканчивается их смертью от недостаточности кровообращения. В этих случаях эндокард резко утолщен вследствие разрастания коллагена, сердце имеет форму шара.
252
Поражение сердца рестриктивного типа может наблюдаться при фиброзе миокарда и эндокарда у больных склеродермией. Рестриктивные процессы характерны и для инфильтративных заболеваний — амилоидоза, гемохроматоза, опухоли сердца.
ПАТОГЕНЕЗ. В патогенезе рестриктивной кардиомиопатии наибольшее значение имеет эндомиокардиальный фиброз, вызванный гиперэозинофилией, которая обусловлена следующими механизмами:
1) повышенным потреблением продуктов, содержащих серотонин (бананы и др.);
2)дефицитом витамина Е;
3)обструкцией лимфатических путей сердца;
4)нарушением иммунитета;
5)паразитарной инфекцией, сопровождающейся эозинофилией.
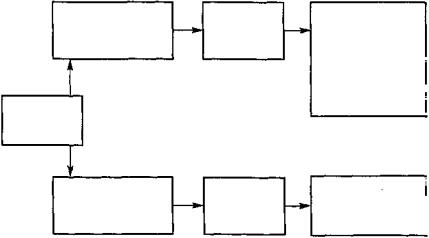
В результате указанных механизмов миокард становится ригидным, наблюдается снижение растяжимости миокарда, в результате чего ограничивается наполнение левого желудочка, уменьшается ударный объем, появляется слабость, усталость и развивается сердечная недостаточность (рис. 36). Сократительная функция левого желудочка не изменена или резко снижена, но систолическая функция желудочков в норме.
Важным звеном патогенеза рестриктивной кардиомиопатии является повышение диастолического давления в желудочках (рис. 36), повышение системного и легочного венозного давления с последующим развитием венозного застоя и появлением клинических признаков правожелудочковой недостаточности (набухание яремных вен, гепатомегалия, асцит, периферические отеки). При этом повышается давление в предсердиях, в последующем развивается их гипертрофия. Сердечная недостаточность у таких больных не сопровождается дилатацией сердца.
Увеличение |
|
Выбухание |
|
диастолического |
Венозный |
||
яремных |
|||
давления |
застой |
||
вен |
|||
в желудочках |
|
||
|
Гепатомегалия |
||
|
|
||
|
|
Асцит |
|
|
|
Периферические |
|
|
|
отеки |
Ригидный
миокард
Снижение |
Снижение |
Слабость |
растяжимости |
ударного |
|
желудочков |
объема |
Усталость |
Рис. 36. Патофизиология рестриктивной кардиомиопатии
253
КЛИНИКА И ДИАГНОСТИКА. В развернутой стадии рестриктивнои кардиомиопатии наблюдается одышка, отеки, асцит, гепатомегалия, выбухание яремных вен (из-за повышения венозного давления), а также выявляются признаки застоя в сосудах малого круга кровообращения. Границы сердца незначительно или умеренно смещаются.
На ЭКГ зубец Ρ высокий (перегрузка правого предсердия), комплекс QRS часто не изменяется, сегмент ST снижается, зубец Τ инвертируется. Часто встречаются блокада левой ножки пучка Гиса и нарушения ритма сердца.
На рентгенограмме грудной клетки в типичных случаях сердце обычных размеров, но может выявляться незначительная или умеренная кардиомегалия, обусловленная увеличением размеров правого или левого предсердия, а также уменьшение пульсации сердца и признаки венозного легочного застоя.
При допплер-эхокардиографии желудочки обычных размеров с неизменной систолической функцией. Иногда определяется выпот в перикарде, утолщение эндокарда и незначительное уменьшение полости желудочка. Значительные структурные изменения клапанов сердца в большинстве случаев отсутствуют. Инфильтративное поражение миокарда может быть ошибочно расценено как гипертрофия желудочка. Диаметр левого желудочка увеличивается в раннюю диастолу, но дальнейшего увеличения в середине и в конце диастолы не наблюдается.
ДИФФЕРЕНЦИАЛЬНАЯ ДИАГНОСТИКА. Клиническая картина рестриктивнои кардиомиопатии весьма сходная с констриктивным перикардитом. Наличие указаний в анамнезе на туберкулез, травму, предшествующий перикардит и системные заболевания, которые могут вовлекать в процесс перикард, делает наиболее вероятным диагноз констриктивного перикардита. Если имеются данные о воздействиях в прошлом радиации, можно думать о констриктивном перикардите или о сочетании констриктивного перикардита с рестриктивнои кардиомиопатией. Перенесенные операции на сердце свидетельствуют в пользу констриктивного перикардита. Объективные признаки амилоидоза, гемохроматоза или других инфильтративных заболеваний, а также соответствующие данные анамнеза говорят о наличии рестриктивнои кардиомиопатии.
ЛЕЧЕНИЕ. На ранних стадиях заболевания применяют преднизолон или другие стероидные гормоны. При развитии сердечной недостаточности лечение направлено на уменьшение ее проявлений. Можно использовать мочегонные средства, но их избыточное применение способно привести к неблагоприятным последствиям. Лекарства с положительным инотропным действием неэффективны, а вазодилататоры следует использовать с большой осторожностью, чтобы избежать ухудшения желудочкового заполнения. Предполагается, что препараты из группы блокаторов кальциевых каналов, возможно, способны увеличивать растяжимость желудочка в диастолу, но доказательства этого в настоящее время неубедительны.
254
МИОКАРДИОДИСТРОФИИ
Термин «миокардиодистрофия» был введен в клиническую практику Г.Ф. Лангом в 1936 году. В настоящее время миокардиодистрофию рассматривают как невоспалительное повреждение миокарда, которое сопровождается ослаблением его сократительной функции. Понятие «миокардиодистрофии» является собирательным, объединяющим различные по этиологии поражения миокарда. Общим является то, что во всех случаях изменяется нормальное течение обменных процессов в миокарде с последующим нарушением его функций.
Однако дистрофические изменения в миокарде не всегда являются единственным и основным патологическим процессом. Очевидно, при недостаточном кровоснабжении или воспалении миокарда нарушаются обменные процессы, которые приводят к дистрофии. Трофика нарушается и вследствие истощения усиленно работающего миокарда при пороках, гипертонической болезни и т.д. Но в таких случаях для характеристики патологического процесса θ целом дистрофические изменения не являются ведущими и не должны учитываться в номенклатуре.
В соответствии с этими представлениями миокардиодистрофии принято разделять на две группы:
1)миокардиодистрофии в широком смысле, или интракардиальные;
2)миокардиодистрофии в узком смысле, или экстракардиальные. Когда дистрофия миокарда сопутствует основному патологическому
процессу в сердце и является его следствием, речь идет об интракардиальной дистрофии.
В таком понимании миокардиодистрофия является патофизиологической основой нарушения функции миокарда с развитием нарушений сердечного ритма и сердечной недостаточности. Экстракардиальные миокардиодистрофии являются, в сущности, симптоматическими и объясняют механизм нарушения сердечной деятельности при первично некардиальном патологическом процессе.
ЭТИОЛОГИЯ. Наиболее часто миокардиодистрофии имеют интоксикационное, эндокринное, дисметаболическое или токсическое происхождение. У детей миокардиодистрофия чаше всего возникает в результате хронического декомпенсированного тонзиллита. Кроме того, миокардиодистрофии развиваются при анемических состояниях; в результате острых и хронических перенапряжений; при системных нерв- но-мышечных заболеваниях (миастении, дистрофической миотонии, прогрессивной мышечной дистрофии и др.). Некоторые формы миокардиодистрофии возникают при накоплении избыточного количества нормальных метаболитов, воздействии вибрации, ионизирующего излучения и других факторов.
ПАТОГЕНЕЗ. В основе патогенеза миокардиодистрофии лежат, прежде всего, биохимические нарушения в миокарде. По механизмам нарушений обмена в миокарде можно выделить несколько аспектов.
255
Во-первых, одним из важнейших механизмов дистрофических изменений является нарушение белкового обмена с постепенным изнашиванием сократительных белков. Уменьшение сократительных белковых структур приводит к недостаточности утилизации и ресинтеза макроэргических фосфатов, т.е. к нарушению энергетического обмена.
Во-вторых, следующим важным механизмов является постепенное обеднение миокарда катехоламинами или снижение активности бетаадренергических рецепторов. Так или иначе, уменьшение влияния симпатической нервной системы на работу сердца сопровождается снижением сердечного выброса.
В-третьих, происходит значительное изменение ионного обмена с накоплением в миокарде натрия и уменьшением содержания калия и магния.
Преимущественное нарушение одного из видов метаболизма в миокарде определяет клиническую картину заболевания — нарушение ритма сердца возникает при выраженном электронном дисбалансе, сердечная недостаточность — при истощении белкового и энергетического обмена. Изменения обмена при миокардиодистрофии могут иметь разную степень выраженности — от легких, обратимых, до самых тяжелых, приводящих к резкому нарушению сердечной деятельности.
Что касается структурных изменений при миокардиодистрофии, то они могут быть выражены по-разному — от ультраструктурных на субклеточном уровне до грубых анатомических и даже некротических. Суть понятия «миокардиодистрофии» состоит в том, что оно характеризует наиболее общий универсальный тип патологических реакций миокарда при различных его поражениях. Это понятие дает ключ к пониманию патогенеза нарушений функций миокарда при самых различных патологических состояниях.
КЛАССИФИКАЦИЯ. Общепринятой классификации миокардиодистрофии у детей не существует. В клинической практике можно пользоваться классификацией, предложенной С.С. Острополец и соавторами (1991), в которой миокардиодистрофии в зависимости от основных этиологических факторов объединены в семь групп (табл. 45).
Удетей удельная значимость этиологических факторов миокардиодистрофии находится в прямой зависимости от частоты патологических процессов, присущих различным возрастным периодам. Так, в раннем возрасте особенно велика роль нарушений питания, острых респиратор- но-вирусных инфекций (ОРВИ), рахита, анемии, гипервитаминоза D и других факторов, при которых дисфункция вегетативной нервной системы, изменение нейрогуморальной регуляции, дис- и парапротеинемии, электролитные расстройства провоцируют нарушения белкового обмена в миокарде, а также развитие дисметаболических и интоксикационных миокардиодистрофии.
Удетей дошкольного и раннего школьного возраста первое место занимает хроническая очаговая инфекция, локализующаяся чаще всего в носу, полости рта и глотке (тонзиллит, аденоидит, синусит, ринит, отит
256
|
|
|
Таблица 45 |
Классификация миокардиодистрофий |
|
||
(С.С. Острополец и соавторы, 1991) |
|
||
|
|
||
Формы миокардиодистрофиь1 |
|
Функциональная |
|
|
|
|
характеристика |
|
по характеру |
|
|
по этиологии |
течения |
|
кровообращения |
|
|
|
|
Интоксикационные: |
Транзиторная |
|
|
острые инфекционные заболевания |
(до 1 месяца) |
|
СН0 |
очаги хронической инфекции |
Стойкая |
|
сн, |
отравления |
(до 1 года) |
|
сн„ |
|
|
||
Дисметаболические: |
Хроническая |
|
|
дистрофии |
(более 1 года) |
|
|
гипо- и гипервитаминозы |
|
|
|
анемии |
|
|
|
энзимопатии |
|
|
|
Нейровегетативные |
|
|
|
Гормональные: |
|
|
|
эндокринные заболевания |
|
|
|
возрастной (пубертатный) дисгормоноз |
|
|
|
Аллергические |
|
|
|
Гиперфункциогенные |
|
|
|
Смешанного генеза |
|
|
|
|
|
|
|
икариес зубов), особенно сочетание нескольких очагов хронической инфекции. Ее возникновение обусловлено сохранением криптогенных очагов в Рубцовых образованиях, спайках, грануляциях, постоянно воздействующих на рецепторный аппарат организма после любого воспалительного процесса, в том числе и широко распространенного вирусного, на фоне сниженной или извращенной иммунологической реактивности.
Неоднократно повторяющиеся острые аллергические состояния у детей, избыток или недостаток гормонов, приводящие к дисбалансу симпатической и парасимпатической частей вегетативной нервной системы, расстройству микроциркуляции и коронарного кровообращения, метаболическим и электролитным нарушениям, также могут способствовать развитию выраженных дистрофических изменений в миокарде.
Особую форму повреждения миокарда у школьников представляет дистрофия вследствие физического перенапряжения. Ее генез связан с изменениями систем, регулирующих выход ионов из мышечного волокна
ипоступление их в него, воздействием катехоламинов и других гормонов.
КЛИНИКА И ДИАГНОСТИКА. Диагностика миокардиодистрофий не представляет трудности, если достаточно очевидна их связь с основным патологическим процессом. Однако так бывает далеко не всегда. Кроме того, клиническая картина миокардиодистрофий может приобретать своеобразную окраску в зависимости от характера основного заболевания: могут часто выявляться кардиалгии, лабильность АД, ослабление тонов сердца.
257
Электролитный дисбаланс, нарушение обмена катехоламинов, мембранопатии и ферментопатии кардиомиоцитов сопровождаются изменениями на ЭКГ, появлением нарушений ритма сердца и проводимости. Изменения на ЭКГ касаются, в основном, конечной части желудочкового комплекса: смещение книзу сегмента ST, инверсия Т, иногда изменение вольтажа QRS.
И.М. Воронцов и соавторы (1982) для диагностики дистрофического поражения миокарда рекомендуют пользоваться следующими критериями:
1) развитие картины поражения миокарда: а) в непосредственной связи с острыми расстройствами жизненно важных функций — дыхания, питания, электролитного обеспечения или б) в определенной связи с заболеваниями или состояниями, вызывающими метаболические нарушения в миокарде, его функциональную перегрузку;
2) наличие положительной динамики: а) при лечении основного заболевания, восстановлении функций пораженных органов, коррекции обмена веществ, б) при уменьшении физической нагрузки, в) при проведении кардиотрофической терапии и функциональных проб с кардиотрофическими средствами.
ДИФФЕРЕНЦИАЛЬНАЯ ДИАГНОСТИКА. Клинико-инструмен- тальные признаки миокардиодистрофии малоспецифичны, что в значительной мере затрудняет проведение дифференциальной диагностики этого заболевания. Наиболее часто возникает необходимость дифференциальной диагностики миокардиодистрофии от неревматического кардита и кардиомиопатий (табл. 46).
ЛЕЧЕНИЕ. В стационарном лечении нуждаются только больные миокардиодистрофией с выраженной тяжестью основного заболевания, которая определяет степень двигательной активности ребенка. При отсутствии противопоказаний ребенок должен с первых дней заниматься лечебной гимнастикой, которая нормализует соотношение процессов возбуждения и торможения, оказывает стимулирующее и нормализующее влияние на трофику мышцы сердца. Расширение двигательной активности осуществляется под контролем проб, адекватных функциональному состоянию сердечно-сосудистой системы больного.
Лечение миокардиодистрофии должно быть направлено прежде всего на устранение вызвавших их причин. Залогом успешного патогенетического лечения является своевременное прекрашение патологических влияний на миокард (лечение основного заболевания, устранение избыточной физической нагрузки и других факторов).
Особое место в лечении больных миокардиодистрофией занимают препараты кардиотрофического действия. Назначают средства, нормализующие метаболические процессы (рибоксин, фосфаден, панангин, аспаркам). Предшественником АТФ, свободно проникающим в клетку и практически лишенным токсических свойств, является рибоксин. Он обладает положительным инотропным действием, участвует в синтезе нуклеотидов, стимулирует окислительно-вогстановительные процессы. Сократительная функция миокарда улучшается при применении препа-
258
Таблица 46
Дифференциальная диагностика воспалительных и невоспалительных поражений миокарда
Поизнэки |
Неревматиче- |
Миокардио- |
Кардио- |
|
ский кардит |
дистрофия |
миопатия |
||
г 1 yj F l W 1 1 1 Л жы 1 |
||||
|
|
|
|
|
Наличие фонового забо- |
Не характерно |
Характерно |
Не характерно |
|
левания |
|
|
|
|
Усугубление признаков |
Определенной |
Четкая зависи- |
Прямой зависи- |
|
поражения сердечно- |
зависимости |
мость |
мости нет |
|
сосудистой системы |
нет |
|
|
|
в период обострения |
|
|
|
|
основного заболевания |
|
|
|
|
Тахикардия |
Характерна ,,• |
Не характерна |
Характерна в |
|
|
|
|
фазе декомпен- |
|
|
|
|
сации |
|
Смещение границ сер- |
Характерно |
Не характерно |
Выражено |
|
дечной тупости |
|
|
|
|
Систолический шум |
Над |
Над верхушкой |
Над верхушкой |
|
|
верхушкой |
и в точке |
и в четвертом |
|
|
|
Боткина—Эрба |
межреберье сле- |
|
|
|
|
ва шумы разные |
|
|
|
|
по тембру и ха- |
|
|
|
|
рактеру (в зави- |
|
|
|
|
симости от вида |
|
|
|
|
кардиомиопатии) |
|
Стойкий диастолический |
Может быть |
Не характерен |
Выражен |
|
шум |
|
|
|
|
Стойкое нарушение ритма |
Характерно |
Не характерно |
Не характерно |
|
Нарушение функции |
Характерно |
Не характерно |
Может быть |
|
проводимости |
|
|
|
|
Желудочковая форма |
Возможна |
Не характерна |
Может быть |
|
пароксиэмальной |
|
|
|
|
тахикардии |
|
|
|
|
Мерцание и трепетание |
Может быть |
Не характерно |
Может быть |
|
предсердий |
|
|
|
|
Деформация грудной |
Может быть |
Нет |
Выражена |
|
клетки в прекардиальнои |
выражена при |
|
|
|
области |
хроническом |
|
|
|
|
течении про- |
|
|
|
|
цесса, развив- |
|
|
|
|
шегося в ран- |
|
|
|
|
нем возрасте |
|
|
|
Рентгенологические: |
|
|
|
|
увеличение тени сердца |
Характерно |
Не характерно |
Выражено |
|
конфигурация сердца |
Изменена, в |
Не изменена |
Изменена |
|
|
основном при |
|
|
|
|
подостром |
|
|
|
|
течении |
|
|
|
|
процесса |
|
|
|
характер легочного |
Усиление при |
Не изменен |
Без |
|
рисунка |
остром кар- |
|
особенностей |
|
|
дите |
« * |
|
|
|
|
|
|
2 5 9
Окончание таблицы 46
|
Неревматиче- |
Миокардио- |
Кардио- |
\ 1ризнэки |
ский кардит |
дистрофия |
миопатия |
|
|
|
|
Эхокардиографические: |
|
|
|
снижение сократитель- |
Выражено |
Может быть |
Выражено |
ной способности |
|
|
|
миокарда в покое |
|
|
|
снижение сократитель- |
Выражено |
Характерно |
Выражено |
ной способности |
|
|
|
миокарда после нагрузки |
|
|
|
увеличение размеров |
Определяется |
Не опреде- |
Выражено (в за- |
камер сердца |
|
ляется |
висимости от |
|
|
|
вида кардио- |
|
|
|
миопатии) |
Деформация клапанов |
Может быть |
Нет |
Не развивается |
сердца |
|
|
|
Нарушение гемодина- |
Характерно |
Может быть |
Нарастает |
мики |
|
только при |
постепенно |
|
|
острой мио- |
|
|
|
кардиодист- |
|
|
|
рофии с |
|
|
|
HKI-IIA |
|
Острофазовые показа- |
Характерны |
Не характерны |
Не характерны |
тели или иммунологи- |
|
|
|
ческие сдвиги при |
|
|
|
исследовании крови |
|
|
|
|
|
|
|
рата внутрь по 0,003—0,005 г на 1 кг массы тела 3 раза в день в течение 3—4 недель. Изредка наблюдаются побочные аллергические реакции в виде зуда и гиперемии кожи. Фрагментом АТФ, входящим в состав ряда коферментов, регулирующих окислительно-восстановительные процессы, является фосфаден. Он способствует увеличению силы сокращений мышцы сердца, что является следствием улучшения ее трофики и накопления энергии. В результате образования аденозина происходит также урежение ритма сердца. Назначают фосфаден внутрь по 1 мг на 1 кг массы тела детям до 6 лет 2 раза в сутки, старше 6 лет — 3 раза в сутки независимо от приема пищи или внутримышечно в виде 2%-го раствора по 0,025 г на 1 кг массы тела 2-3 раза в сутки.
При миокардиодистрофии весьма эффективным является назначение 20%-го раствора карнитина хлорида: до 6 лет — по 14 капель, старше 6 лет — по 25—40 капель 2—3 раза в сутки в течение 3—4 недель. Показано также назначение милдроната, который улучшает метаболические процессы и оказывает кардиопротективное действие. Препарат назначают внутривенно по 2—5 мл 10%-го раствора 1 раз в сутки в течение 5—7 дней, а затем продолжают принимать перорально по 250 мг 1 — 3 раза в сутки в течение 2—3 недель.
Наряду с этим проводится коррекция нарушений сердечной деятельности (лечение сердечной недостаточности, аритмии).
260
