
Руководство ЛР ТМП. Редакция 8
.pdf
После несложных преобразований, справедливых, если для всех диффузионных этапов v << vп,
приходим к следующему выражению:
Теперь его можно упрощать для отдельных частных случаев. Если в знаменателе можно пренеб-
речь всеми слагаемыми по сравнению с единицей, то реализуется кинетический режим. Уравнение связи в этом случае имеет вид:
В этом случае должна наблюдаться линейная зависимость в координатах v / [Mn] – (MnO)·[Si]0.5 / [Mn]. Если же лимитирующей стадией является диффузия марганца в металле, то в знаменателе самым большим слагаемым станет второе. В этом случае уравнение связи примет вид:
Если учесть, что предельная скорость диффузии марганца в металле пропорциональна ее концентрации: v[Mn] = k[Mn] · [Mn], то приходим к уравнению такого же вида, как для кинетического режима, но коэффициенты в нем имеют другой смысл:
В этом случае выявить режим процесса можно, меняя условия перемешивания, что не предусмот-
рено для моделируемой установки.
Наиболее сложный случай реализуется, когда наибольшим слагаемым в знаменателе формулы ()
является последнее. Здесь лимитирующей стадией может быть диффузия кремния в металле или оксида марганца в шлаке. В первом случае уравнение () может быть преобразовано к виду:
а во втором – к виду:
В зависимости от того, в каких координатах удается линеаризовать экспериментальные данные можно судить о лимитирующей стадии процесса.
Кинетическое уравнение реакции 5 имеет вид
С учетом связи объемных концентраций с поверхностными и приповерхностными приходим к со-
отношению вида:
51

Если лимитирующей стадией является диффузия оксида марганца в шлаке, то последнее уравне-
ние приводится к виду:
Для кинетического режима уравнение имеет такой же вид, но постоянные коэффициенты имеют другой смысл и, соответственно, другие обозначения.
Если лимитирующей стадией является диффузия марганца в металле, то уравнение приобретает вид:
Наконец, если затруднена доставка к межфазной границе оксида железа, то получается соотноше-
ние:
Константа равновесия реакции, выраженная через активности
(18.1)
является функцией только температуры.
Отношение равновесных концентраций марганца в шлаке и металле
(18.2)
называют коэффициентом распределения марганца, который, в отличие от 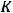 , зависит от состава фаз и служит количественной характеристикой распределения этого элемента между шлаком и металлом.
, зависит от состава фаз и служит количественной характеристикой распределения этого элемента между шлаком и металлом.
2.6.2Модель процесса
Вимитационной модели рассмотрены три электродные полуреакции, которые могут проте-
кать между оксидным расплавом CaO – MnO – FeO – SiO2 – Al2O3 и жидким железом, содержа-
щим в качестве примесей Мn и Si. Сделано допущение о диффузионном режиме их протекания.
Учтена заторможенность диффузии частиц Fe2+ в шлаке, кремния в металле, марганца в обеих фа-
зах. Общая система уравнений, описывающая модель, имеет вид
52

(18.4)
(18.5)
(18.6)
(18.7)
(18.8)
где υј – скорость электродной полуреакции, ηj – поляризация, ij – плотность предельного тока диффузии, Dj – коэффициент диффузии, β – конвективная постоянная, Cj – концентрация.
Программа имитационной модели позволяет решить систему уравнений (18.4) – (18.8), что дает возможность установить, как изменяется объемная концентрация компонентов и скорости их перехода со временем при взаимодействии металла со шлаком. Результаты расчета выводятся на дисплей. Информация, получаемая с экрана монитора, включает в себя графическое изображение изменения концентраций основных компонентов, их текущие значения, а также значения темпера-
туры и константы конвекции (рисунок 8).
Блок-схема программы имитационной модели взаимодействия металла и шлака представ-
лена на рисунке 7. Программа работает в цикле, который прекращается только после истечения заданного времени моделирования (примерно 10 мин).
53

Формирование исхо дных данных для моделирования |
Проверка наличия и реакция на команды |
пользователя |
Расчет равновесных по тенциалов в |
кислородной шкале по приповер хностным |
концентрациям |
Оценка приповер хностных концентраций |
Условие |
Вычисление объемных концентраций реагентов |
Время |
Выво д информации на экран и в файл, анимационные эффекты |
Время |
Процедуры, завершающие работу программы |
Рисунок 7 – Блок-схема программы имитационной модели
2.6.3 Порядок проведения работы
Изображение, генерируемое имитационной программой, представлено на рис 8 (правая па-
нель). В верхней части панели приводятся выборочные числовые значения измеряемых величин,
на графике отображены все значения, полученные в ходе моделирования процесса. В обозначени-
ях компонентов металлического и шлакового расплавов использованы принятые литервтуре ме-
таллургической тематики дополнительные знаки. Квадратные скобки обозначают принадлежность компонента металлическому расплаву, а круглые – шлаковому. Множители при обозначениях компонентов используются только для построения графика, их не следует учитывать при интер-
претации значений. Во время работы модели в каждый данный момент отображается только зна-
чение одной из измеряемых величин. Через 6 сек оно исчезает и появляется значение следующей величины. За этот промежуток времени надо успеть записать очередное значение. Для экономии времени рекомендуется неизменные цифры не записывать, например, ведущую единицу в значе-
нии температуры.
54

Рис 8. Изображение экрана монитора при выполнении работы № 18 на разных стадиях процессов.,
Через пять-шесть минут после начала работы установки произведите добавку предварительно прогретого оксида марганца в шлак, что реализуется при одновременном нажатии клавиши
Alt и цифровой клавиши на основной клавиатуре с номером Вашей установки.
2.6.4 Обработка и представление результатов измерений
Результаты экспериментов на промышленных установках, получение которых в работе реализуется на имитационной модели, как правило, отличаются от лабораторных испытаний одновременным изменением большого числа параметров и повышенной погрешностью результатов измерений, что затрудняет их интерпретацию и обсуждение. В этом случае приходится использовать для анализа максимально упрощенные модели и простейшие функциональные зависимости. Здесь очень важно хорошо представлять все используемые упрощения и границы их применимости. Результатом измерений в работе № 18 являются наборы дискретных значений концентраций основных реагентов в металлической ([Si], [Mn]) и шлаковой ((MnO), (FeO)) фазах, характеризующие их изменение со временем. Они дают возможность оценить численными методами скорости реакций 4 и 5, а также общую скорость перехода кремния. Реализация таких методов описана
55
во вводной части пособия. Анализ результатов становится намного проще и понятнее, когда вза-
мосвязи между всей совокупностью данных отражены на графиках. В данном случае ограничимся
4-мя графиками (диаграммами XY): 1 - зависимость температуры от времени (одна кривая), 2 - за-
висимости концентраций компонентов металла (кремния и марганца) от времени (две кривые), 3 -
зависимости концентраций компонентов шлака (оксиды марганца и железа) от времени (две кри-
вые) и 4 – зависимости скоростей перехода марганца и реакций 4 и 5, определенные по изменению содержаний кремния в металле и оксида железа в шлаке (три кривые). Методом наименьших квадратов следует оценить константы скоростей прямой и обратной реакций процесса 4 по урав-
нению (18.4) отдельно до и после увеличения содержания марганца в шлаке и погрешности опре-
деления этих величин. Учтите, что в уравнении (18.4) отсутствует свободный член.
Порядок обработки результатов
1.Ввести результаты ручной записи информации в файл электронных таблиц.
2.Вычислить скорости процессов по концентрациям кремния и марганца в металле и оксида железа в шлаке. Используйте значение массы металла 100 кг и не забудьте учесть стехиометрические множители. Площадь межфазной поверхности не учитывайте.
3.Построить на отдельных листах графики зависимостей температуры в агрегате и концентраций реагентов от времени, скоростей перехода кремния и отдельных процессов от времени.
4.Вычислить константы kf4 и kr4 процесса 4 по уравнению (18.4) до и после увеличения содержания марганца в шлаке и погрешности их определения.
5.Сделать выводы по полученным данным.
Зачетные результаты:
1.Правильно оформленные графики (четыре графика – восемь кривых) на отдельном листе электронных таблиц со всеми необходимыми подписями обозначениями.
2.Значения констант скоростей и погрешностей их определения.
3.Выводы по работе.
Контрольные вопросы
1.Почему возникает необходимость моделирования процессов производства стали?
2.Какова природа взаимодействия металла со шлаком и в чем это проявляется?
3.Какой потенциал называется стационарным?
4.Какой потенциал называется равновесным?
5.Что называется электродной поляризацией (перенапряжением)?
6.Что называется коэффициентом распределения марганца между металлом и шлаком?
7.От чего зависит константа распределения марганца между металлом и шлаком?
8.Какие факторы влияют на скорость перехода марганца из металла в шлак в диффузионном режиме?
9.Перечислите определяемые по результатам опытов физические величины.
10.Выберите комбинации величин для построения регламентированных в работе графиков (Ось Х, Ось Y)
11.Перечислите физические величины, определяемые по результатам опытов.
12.Перечислите ожидаемые наблюдения по результатам работы.
13.Укажите количество электронов в электродной полуреакции перехода марганца (кремния, железа) через границу металл-шлак.
56
14.Укажите формы существования реагентов (кремний, марганец, железо) в фазах, в которых они присутствуют.
15.Последовательно перечислите этапы восстановления марганца (железа, кремния) и механизмы их реализации.
57
Список литературы
1.Линчевский, Б.В. Техника металлургического эксперимента [Текст] / Б.В. Линчевский. –
М.: Металлургия, 1992. – 240 с.
2.Арсентьев, П.П. Физико-химические методы исследования металлургических процессов
[Текст]: учебник для вузов / П.П. Арсентьев, В.В. Яковлев, М.Г. Крашенинников,
Л.А. Пронин и др. – М.: Металлургия, 1988. – 511 с.
3.Попель, С.И. Взаимодействие расплавленного металла с газом и шлаком [Текст]: учебное пособие / С.И. Попель, Ю.П. Никитин, Л.А. Бармин и др. – Свердловск: изд. УПИ им.
С.М. Кирова, 1975, – 184 с.
4.Попель, С.И. Теория металлургических процессов [Текст]: учебное пособие / С.И. Попель,
А.И. Сотников, В.Н. Бороненков. – М.: Металлургия, 1986. – 463 с.
5.Лепинских, Б.М. Транспортные свойства металлических и шлаковых расплавов [Текст]:
Справочник / Б.М. Лепинских, А.А. Белоусов / Под. ред. Ватолина Н.А. – М.: Металлургия,
1995. – 649 с.
6.Белай, Г.Е. Организация металлургического эксперимента [Текст]: учебное пособие /
Г.Е. Белай, В.В. Дембовский, О.В. Соценко. – М.: Химия, 1982. – 228 с.
7.Панфилов, А.М. Расчет термодинамических свойств при высоких температурах [Электрон-
ный ресурс] : учебно-методическое пособие для студентов металлургического и физико-
технического факультетов всех форм обучения / А.М. Панфилов, Н.С. Семенова – Екате-
ринбург : УГТУ-УПИ, 2009. – 33 c.
8.Панфилов, А.М. Термодинамические расчеты в электронных таблицах Excel [Электронный ресурс] : методические указания для студентов металлургического и физико-технического факультетов всех форм обучения / А.М.Панфилов, Н.С. Семенова – Екатеринбург : УГТУ-
УПИ, 2009. – 31 с.
9.Краткий справочник физико-химических величин / Под. ред. А.А. Равделя и А.М. Пономаре-
ва. Л. : Химия, 1983. – 232 с.
58
