
- •4. Активность, коэффициент активности, ионная сила раствора.
- •5. Термодинамическая, концентрационная и условная константы равновесия и их взаимосвязь.
- •6. Характеристика метода титриметрического анализа. Стандартные растворы.
- •7. Виды титрования
- •8. Закон эквивалентов, расчеты в титриметрии
- •9. Теории кислот и оснований. Протолитическая теория кислот и оснований.
- •10. Автопротолиз воды. Ионное произведение воды.
- •17. Ионно-хромофорная теория индикаторов.
- •18. Индикаторные ошибки в протолитометрии.
- •19. Кривая титрования сильной кислоты сильным основанием.
- •20. Кривая титрования слабой кислоты сильным основанием.
- •21. Равновесие в растворах комплексных соединений.
- •22. Хелатометрическое титрование.
- •23. Эдта и ее комплексы с металлами.
- •24. Рабочие растворы и индикаторы в комплексонометрическом титровании
- •25. Равновесный окислительно-восстановительный потенциал и константа равновесия реакции. Уравнение Нернста.
- •26. Расчет электродного потенциала полуреакции.
- •27. Виды окислительно-восстановительного титрования.
- •28. Кривая окислительно-восстановительного титрования.
- •29. Способы определения точки эквивалентности в окислительно-восстановительном титровании.
- •30. Гравиметрия. Характеристика метода.
- •31. Понятие константы растворимости.
- •32. Связь между константой растворимости и растворимостью.
- •33. Факторы, влияющие на процесс образования осадка.
- •34. Загрязнение осадков.
- •35. Этапы гравиметрии.
- •36. Осаждаемая и гравиметрические формы.
- •37. Гравиметрический фактор.
- •38. Факторы, влияющие на полноту осаждения.
- •39. Условия образования кристаллических и аморфных осадков.
- •40. Классификация физико-химических методов анализа.
- •41. Классификация спектральных методов. Электромагнитный спектр.
- •42. Основной закон светопоглощения. Ограничения и условия его применимости.
- •43. Причины отклонения от закона Бугера-Ламберта-Бера.
- •44. Фотометрия. Преимущества и недостатки метода.
- •45. Характеристики светопоглощения в фотометрии.
- •46. Оптимальные условия для проведения количественного фотометрического анализа (выбор длины волны и концентрации).
- •47. Аддитивность оптической плотности.
- •48. Приемы количественного фотометрического анализа.
- •49. Количественный фотометрический анализ смеси светопоглощающих веществ.
- •50. Метод дифференциальной фотометрии.
- •51. Метод эмиссионной фотометрии пламени.
- •52. Пламя и его характеристики.
- •53. Метод градуировочного графика при пламенно-эмиссионном анализе. Самоионизация и самопоглощение.
- •54. Классификация электрохимических методов анализа.
- •55. Прямая ионометрия. Методы градуировочного графика и добавок.
- •56. Потенциометрическое титрование. Способы нахождения точки эквивалентности.
- •57. Классификация электродов в потенциометрии.
- •58. Стеклянный электрод.
- •59. Хлоридсеребряный электрод.
- •60. Законы электролиза.
- •61. Кулонометрия при постоянном потенциале и постоянной силе тока.
- •62. Классификация хроматографических методов анализа.
- •63. Фронтальная, вытеснительная и элюентная хроматография.
- •64. Основные характеристики хроматографического пика.
- •65. Эффективность хроматографической системы. Концепция теоретических тарелок.
- •66. Кинетическая теория хроматографии. Уравнение Ван-Деемтера.
- •67. Критерии разделения в газовой хроматографии.
- •68. Газовая хроматография. Общая характеристика метода.
- •69. Детекторы в газовой хроматографии.
- •70. Качественный анализ в газовой хроматографии.
- •71. Методы количественного анализа в газовой хроматографии.
- •73. Характеристика ионитов и реакций в ионообменной хроматографии.
- •74. Плоскостная хроматография. Принципы и характеристики.
54. Классификация электрохимических методов анализа.
Методы без наложения внешнего (постороннего) потенциала. Источником электрической энергии служит сама электрохимическая система, представляющая собой гальванический элемент (гальваническую цепь).
- потенциометрические методы; электродвижущая сила (ЭДС) и электродные потенциалы в такой системе зависят от содержания определяемого вещества в растворе.
Методы с наложением внешнего (постороннего) потенциала. К таким методам относятся:
о кондуктометрический анализ - основан на измерении электрической проводимости растворов как функции их концентрации;
о вольтамперометрический анализ - основан на измерении тока как функции приложенной известной разности потенциалов и концентрации раствора;
о кулонометрический анализ - основан на измерении количества электричества, прошедшего через раствор, как функции его концентрации;
о электрогравиметрический анализ - основан на измерении массы продукта электрохимической реакции.
Классификация по способу применения электрохимических методов. Различают прямые и косвенные методы.
- Прямые методы. Измеряют электрохимический параметр как известную функцию концентрации раствора и по показанию соответствующего измерительного прибора находят содержание определяемого вещества в растворе.
- Косвенные методы. Методы титрования, в которых окончание титрования фиксируют на основании измерения электрических параметров системы.
55. Прямая ионометрия. Методы градуировочного графика и добавок.
- метод основан на определении концентр в-ва
В основе метода лежит зависимость равновесного потенциала индикаторного электрода от концентрации тока в анализируемом растворе, выражу р-ем Нернста:
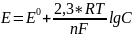
Метод градуировочного графика
Готовят серию из 5-7 эталонных р-ов. Концентрация и ионная сила в-ва не должны сильно отличаться от анализируемого в-ва – уменьш ошибки определения
Ионную силу поддерж. Постоянной, введением индифферентного электролита.
Эталонные р-ры последовательно вводят в электрохим. Ячейку. Измеряют ЭДС, строят градуировочный график в координатах ЭДС – lgC
Вносим анализ р-р и измеряем ЭДС, находим lgC, где С – концентр в-ва
Метод добавок стандарта
электрохимическую ячейку вносят известный объем V(X) анализируемого раствора с концентрацией с(Х) и измеряют ЭДС ячейки. Затем в тот же раствор прибавляют точно измеренный небольшой объем стандартного раствора V(ст) с известной, достаточно большой, концентрацией с(ст) определяемого вещества и снова определяют ЭДС ячейки.
Рассчитывают концентрацию с(Х) определяемого вещества в анализируемом растворе по формуле :

56. Потенциометрическое титрование. Способы нахождения точки эквивалентности.
- способ определения объема титранта, затраченного на титрование определяемого ве-ва, путем измерения ЭДС с помощью гальванической цепи, составленной из индикаторного электрода и электрода стравнения.
Анализируемый р-р, находящийся в электрохим. ячейке, титруют подходящим титрантом, фиксируя конец титрования по резкому измернию ЭДС – потенциала индикаторного электрода, который зависит от концентрации соотв ионов и разко изменяется в тэ
Кривые потенциометрического титрования:

