- •Самостоятельная работа студентов во внеурочное время
- •2. Консультации преподавателей (еженедельно по индивидуальному графику).
- •Теоретический материал по теме занятия
- •Взаимодействие квантов света с биологическими соединениями.
- •Люминесценция.
- •Фотобиологические процессы
- •Основы фотомедицины.
- •Контрольные вопросы
- •Примеры заданий для компьютерного тестирования
- •План занятия
Государственное образовательное учреждение
Высшего профессионального образования
"ВОРОНЕЖСКАЯ ГОСУДАРСТВЕННАЯ МЕДИЦИНСКАЯ АКАДЕМИЯ
им. Н.Н. БУРДЕНКО"
|
|
КАФЕДРА МЕДИЦИНСКОЙ ФИЗИКИ
Методические указания
студентам по теме практического занятия
КВАНТОВАЯ БИОФИЗИКА
Воронеж 2009
|
УДК |
53 (071) |
|
ББК |
22.314я73 |
|
|
Д532 |
|
Рецензенты: |
Зав. кафедрой нормальной физиологии ВГМА им. Н.Н. Бурденко, д.м.н., профессор Яковлев В.Н. |
|
|
Зав. кафедрой медико-биологических дисциплин ВГИФК, к.б.н. Попова И.Е. |
|
Д532 |
Дмитриев Е.В. Квантовая биофизика: метод. указания / Е.В. Дмитриев, И.Е. Савостина. – Воронеж: ВГМА, 2009. – 16 с.: ил. |
Методические указания разработаны на основании примерных рабочих программ по медицинской и биологической физике (специальности: лечебное дело, педиатрия, медико-профилактическое дело), физике и биофизике (специальности: фармация, сестринское дело), рекомендованных Центральным методическим советом ВГМА. Содержат основные теоретические вопросы по данной теме и дидактические единицы для подготовки к занятию и самоконтроля. Предназначены для студентов I и II курсов лечебного, педиатрического, медико-профилактического, фармацевтического факультетов, МИМОС (лечебное дело), ИСО.
Печатается по решению Центрального методического совета ВГМА
(протокол №6 от 16.04.2009 г.).
|
|
УДК 53 (071) |
|
|
ББК 22.314я73 |
|
|
© ВГМА, 2009 |
ТЕМА: Квантовая биофизика
ЦЕЛЬ ЗАНЯТИЯ:
1. Овладеть необходимыми теоретическими знаниями в области квантовой биофизики.
2. Выработать умения применять полученные знания для анализа конкретных физических явлений, наблюдаемых в биологических системах.
После изучения темы студент должен знать:
а) основные закономерности взаимодействия света с веществом;
б) пути дезактивации возбужденного состояния молекулы;
в) природу люминесценции и применение этого явления в медицине;
г) сущность фотобиологических процессов и основы квантовой медицины.
УМЕТЬ:
а) проводить расчет концентрации вещества на основе данных спектральных и фотометрических методов;
б) проводить анализ, количественную и качественную оценку спектров поглощения биологически значимых соединений.
МОТИВАЦИЯ ТЕМЫ
Фотобиологические процессы лежат в основе многих физиологических реакций организма. Закономерности миграции энергии возбужденной молекулы находят отражение в реализации биоэнергетических процессов в живой системе. Основы квантовой биофизики необходимы для понимания принципов фототерапии. Спектральные, фотометрические методы анализа, метод хемилюминесценции, люминесцентные зонды широко используются в диагностике заболеваний и являются адекватным инструментом при решении большого круга научных задач в современной биологии и медицине. Поэтому тема "Квантовая биофизика" в рамках дисциплины "Медицинская и биологическая физика" необходима студентам для прохождения профессиональных дисциплин и дисциплин специальности, приобретения навыков научно-исследовательской работы.
Самостоятельная работа студентов во внеурочное время
Задание 1.
Изучить теоретический материал занятия, используя рекомендуемую литературу по следующей логической структуре учебного материала:
1. Электронные переходы в молекулах
а) понятие о синглетном и триплетном уровнях возбужденного состояния;
б) пути миграции энергии.
2. Поглощение света веществом
а) закон Бугера–Ламберта–Бера;
в) спектры поглощения биологических соединений;
г) принципы работы спектрофотометров и фотоэлектроколориметров.
3. Природа люминесценции и ее применение в медицине.
4. Фотобиологические процессы
а) стадии фотобиологических процессов;
б) биологические эффекты оптического диапазона электромагнитных излучений;
в) спектр фотобиологического действия.
5. Основы фотомедицины
а) роль фотосенсибилизаторов в формировании ответной реакции организма;
б) фотогемотерапия.
Задание 2.
Подготовить реферативные сообщения на темы, полученные у преподавателя на предыдущем занятии.
Средства для самоподготовки студентов
во внеаудиторное время
1. Учебная и методическая литература
а) основная
– Ремизов А.Н. Медицинская и биологическая физика / А.Н. Ремизов, А.Г. Максина, А.Я. Потапенко. – М.: Дрофа, 2007. – С. 446-487.
– Физика и биофизика / Под ред. В.Ф. Антонова. – М.: ГЭОТАР-Медиа, 2008. – С. 90-115.
– Лекционный материал по теме "Квантовая биофизика".
– Ремизов А.Н. Сборник задач по медицинской и биологической физике / А.Н. Ремизов, А.Г. Максина. – М.: Дрофа, 2001. – С. 136-139.
б) дополнительная
– Владимиров Ю.А. Лекции по медицинской биофизике / Ю.А. Владимиров, Е.В. Проскурина. – М.: Изд-во МГУ; ИКЦ "Академкнига", 2007. – С. 19-113, 136-170.
– Артюхов В.Г. Биофизика / В.Г. Артюхов, Т.А. Ковалева, В.П. Шмелев. – Воронеж: Изд-во ВГУ, 1994. – С.229-259, 282-302.
2. Консультации преподавателей (еженедельно по индивидуальному графику).
Теоретический материал по теме занятия
Взаимодействие квантов света с биологическими соединениями.
Квантовая биофизика изучает электронную структуру биологически важных молекул, электронные переходы в этих молекулах и пути превращения энергии возбужденного состояния молекул в энергию продуктов.
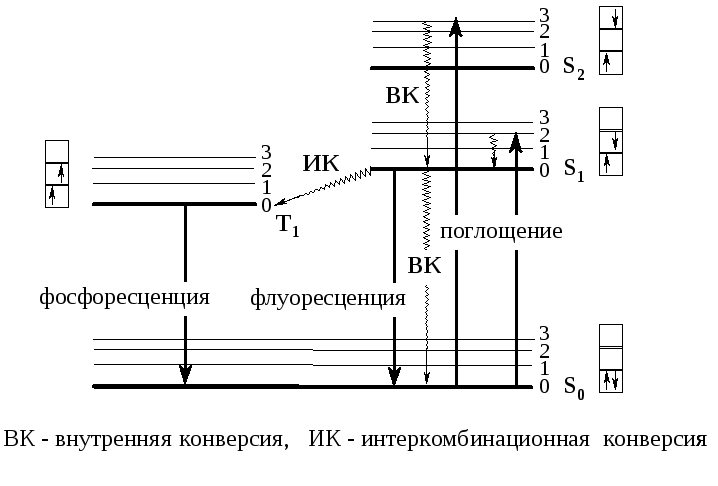
Каждый электрон в молекуле находится на определенной орбитали и обладает определенной энергией. Если молекуле сообщить энергию, например, в форме кванта света, может произойти переход с заполненного основного уровня (S0) на один из незаполненных (рис. 1). При этом молекула оказывается в синглетном (S1, S2, …, Sn) электронно-возбужденном состоянии.
|
|
|
Рис. 1. Электронные переходы в молекулах.
|
За счет внутренней конверсии (безизлучательная отдача энергии) электроны всегда оказываются на низшем колебательном подуровне синглетного возбужденного состояния (S1). Спины электронов не изменяются (антипараллельны), время жизни молекул в состоянии составляет 10–8–10–9 с. Далее, с определенной вероятностью, могут реализовываться следующие пути превращения энергии состояния S1:
1. В тепло: S1 → S0 (внутренняя конверсия).
2. Испускание кванта флюоресценции: S1 → S0 + hфл
3. Фотохимическая реакция: S1 → продукт.
4. Передача энергии возбуждения другой молекуле.
5. Обращение спина электрона и переход молекулы в триплетное возбужденное состояние: S1 → Т1 (интеркомбинационная конверсия). Спины электронов в состоянии Т1 и S0 одинаковы, поэтому переход в основное состояние запрещен и время жизни молекулы в Т1 значительно больше – 10–4–10 с. Из триплетного состояния возможны следующие пути реализации энергии:
– безизлучательный переход с обращением спина электрона: Т1 → S0;
– испускание кванта фосфоресценции: Т1 → S0 + h;
– фотохимическая реакция: Т1 → продукт;
– передача энергии возбуждения другой молекуле.
Любые излучательные переходы в молекуле (флюоресценция, фосфоресценция) называют общим термином – люминесценция.
Для того чтобы данный раствор или вещество поглощали энергию падающего пучка света необходимо выполнение энергетического условия: частота поглощаемого излучения () должна соответствовать выражению Бора:
![]() ,
,
где h – постоянная Планка – 6,63∙10–34 Дж∙с, Е1 – энергия основного состояния молекулы, Е2 – энергия возбужденного состояния. Уравнение показывает, что энергия кванта (фотона) поглощается молекулой целиком, а не по частям.
Поглощение света внешне проявляется в ослаблении светового потока при прохождении через исследуемый объект. Это явление может быть измерено инструментально с помощью приборов: спектрофотометра, фотоэлектроколориметра:
![]() ,
,
где Т – коэффициент светопропускания; I0 – интенсивность света, падающего на образец; I – интенсивность света, прошедшего через раствор (величина 1–Т называется коэффициентом светопоглощения). Поскольку коэффициент светопропускания связан с концентрацией раствора сложной экспоненциальной зависимостью, на практике обычно используют величину оптической плотности (D).
Закон Бугера–Ламберта–Бера: поглощение света исследуемым образцом прямо пропорционально зависит от концентрации вещества (с, моль∙л–1), расстояния, которое свет проходит в растворе – длины оптического пути (l, см) и способности вещества поглощать свет данной длины волны – коэффициента молярной экстинкции (, л∙моль–1∙см–1):
![]() ,
,
Коэффициент молярной экстинкции является фундаментальной характеристикой вещества, его величина не зависит от условий измерения, а определяется лишь способностью данных молекул поглощать свет той или иной длины волны. Значения для многих веществ определены и внесены в соответствующие справочные издания.
Закон Бугера-Ламберта-Бера иногда выражают в виде
![]()
Коэффициент молярной экстинкции может
быть выражен через натуральный молярный
показатель поглощения ():![]() .
Величина
отражает суммарное эффективное сечение
поглощения всех молекул одного моля
(=sNA).
Поэтому закон Бугера-Ламберта-Бера
может иметь вид
.
Величина
отражает суммарное эффективное сечение
поглощения всех молекул одного моля
(=sNA).
Поэтому закон Бугера-Ламберта-Бера
может иметь вид
![]()
Графики, выражающие зависимость D (реже ) от длины волны падающего света, называют спектрами поглощения вещества.
За поглощение света в ультрафиолетовой и видимой областях спектра ответственны определенные группы, входящие в состав сложных молекул и называемые хромофорными группами. Обычно они имеют систему сопряженных двойных связей (часто циклические, ароматические системы).
Наиболее значимые полосы поглощения биологических макромолекул:
1. λ ≈ 190 нм – пептидные связи белковой молекулы (интенсивность полосы увеличивается при нарушении пространственной организации молекулы);
2. λ ≈ 255-280 нм – серосодержащие аминокислоты (цистин, цистеин, метионин);
3. λ ≈ 260 нм – пуриновые и пиримидиновые основания нуклеотидов;
4. λ ≈ 280 нм – ароматические аминокислоты (триптофан, фенилаланин, тирозин);
5. λ ≈ 412 нм (полоса Соре) – порфиринсодержащие соединения (гемоглобин);
6. λ ≈ 500 нм – комплекс ретиналя и опсина (зрительный пигмент родопсин).
Регистрация спектров поглощения – широко используемый диагностический и научно-исследовательский метод. Он позволяет:
1. Идентифицировать вещество в исследуемой пробе.
2. Определить концентрацию вещества в растворе.
3. Оценить конформационные перестройки макромолекул, которые приводят к изменению соотношения хромофоров на их поверхности.