
- •Биология
- •В двух книгах
- •В.Н. Ярыгин, в.И. Васильева, и.Н. Волков, в.В. Синелыцикова
- •Предисловие
- •Введение
- •Раздел I
- •1.2. Стратегия жизни. Приспособление, прогресс, энергетическое и информационное обеспечение
- •1.3. Свойства жизни
- •1.4. Происхождение жизни
- •1.5. Происхождение эукариотической клетки
- •1.6. Возникновение многоклеточности
- •1.7. Иерархическая система. Уровни организации жизни
- •1.8. Проявление главных свойств жизни на разных уровнях ее организации
- •1.9. Особенности проявления биологических закономерностей у людей. Биосоциальная природа человека
- •Раздел II
- •Клеточный и молекулярно-генетический уровни организации жизни — основа жизнедеятельности организмов
- •Глава 2
- •Клетка —элементарная единица живого
- •2.1. Клеточная теория
- •2.2. Типы клеточной организации
- •2.3. Структурно-функциональная организация эукариотической клетки
- •2.3.1. Принцип компартментации. Биологическая мембрана
- •2.3.2.Строение типичной клетки многоклеточного организма
- •2.3.3.Поток информации
- •2.3.4.Внутриклеточный поток энергии
- •2.3.5.Внутриклеточный поток веществ
- •2.3.6.Другие внутриклеточные механизмы общего значения
- •2.3.7.Клетка как целостная структура. Коллоидная система протоплазмы
- •2.4. Закономерности существования клетки во времени
- •2.4.1.Жизненный цикл клетки
- •2.4.2.Изменения клетки в митотическом цикле
- •Глава 3 структурно-функциональная организация генетического материала
- •3.1. Наследственность и изменчивость — фундаментальные свойства живого
- •3.2. История формирования представлений об организации материального субстрата наследственности и изменчивости
- •3.3. Общие свойства генетического материала и уровни организации генетического аппарата
- •3.4. Генный уровень организации генетического аппарата
- •3.4.1.Химическая организация гена
- •3.4.1.1. Структура днк. Модель Дж. Уотсона и ф. Крика
- •3.4.1.2. Способ записи генетической информации в молекуле днк. Биологический код и его свойства
- •3.4.2Свойства днк как вещества наследственности и изменчивости
- •3.4.2.1. Самовоспроизведение наследственного материала. Репликация днк
- •3.4.2.2. Механизмы сохранения нуклеогидной последовательности днк. Химическая стабильность. Репликация. Репарация
- •3.4.2.3. Изменения нуклеотидных последовательностей днк. Генные мутации
- •3.4.2.4. Элементарные единицы изменчивости генетического материала. Мутон. Рекон.
- •3.4.2.5. Функциональная классификация генных мутаций
- •3.4.2.6. Механизмы, снижающие неблагоприятный эффект генных мутаций
- •3.4.3.Использование генетической информации в процессах жизнедеятельности
- •3.4.3.1. Роль рнк в реализации наследственной информации
- •3.4.3.2. Особенности организации и экспрессии генетической информации у про- и эукариот
- •3.4.4.Функциональная характеристика гена
- •3.4.5.Биологическое значение генного уровня организации наследственного материала
- •3.5. Хромосомный уровень организации генетического материала
- •3.5.1.Некоторые положения хромосомной теории наследственности
- •3.5.2.Физико-химическая организация хромосом эукариотической клетки
- •3.5.2.1. Химический состав хромосом
- •3.5.2.2. Структурная организация хроматина
- •3.5.2.3. Морфология хромосом
- •3.5.2.4. Особенности пространственной организации генетического материала в прокариотической клетке
- •3.5.3.Проявление основных свойств материала наследственности и изменчивости на хромосомном уровне его организации
- •3.5.3.1. Самовоспроизведение хромосом в митотическом цикле клеток
- •3.5.3.2. Распределение материала материнских хромосом между дочерними клетками в митозе
- •3.5.3.3. Изменения структурной организации хромосом. Хромосомные мутации
- •3.5.4.Значение хромосомной организации в функционировании и наследовании генетического аппарата
- •3.5.5.Биологическое значение хромосомного уровня организации наследственного материала
- •3.6. Геномный уровень организации наследственного материала
- •3.6.1.Геном. Генотип. Кариотип
- •3.6.2.Проявление свойств наследственного материала на геномном уровне его организации
- •3.6.2.1. Самовоспроизведение и поддержание постоянства кариотипа в ряду поколений клеток
- •3.6.2.2. Механизмы поддержания постоянства кариотипа в ряду поколений организмов
- •3.6.2.3. Рекомбинация наследственного материала в генотипе. Комбинативная изменчивость
- •3.6.2.4. Изменения геномной организации наследственного материала. Геномные мутации
- •3.6.3.Особенности организации наследственного материала
- •3.6.4.Эволюция генома
- •3.6.4.1. Геном предполагаемого общего предка про- и эукариот
- •3.6.4.2. Эволюция прокариотического генома
- •3.6.4.3. Эволюция эукариотического генома
- •3.6.4.4. Подвижные генетические элементы
- •3.6.4.5. Роль горизонтального переноса генетического материала в эволюции генома
- •3.6.5.Характеристика генотипа как сбалансированной по дозам системы взаимодействующих генов
- •3.6.5.1. Значение сохранения дозового баланса генов в генотипе для формирования нормального фенотипа
- •3.6.5.2. Взаимодействия между генами в генотипе
- •3.6.6.Регуляция экспрессии генов на геномном уровне организации наследственного материала
- •3.6.6.1. Общие принципы генетического контроля экспрессии генов
- •3.6.6.2. Роль негенетических факторов в регуляции генной активности
- •3.6.6.3. Регуляция экспрессии генов у прокариот
- •3.6.6.4. Регуляция экспрессии генов у эукариот
- •3.6.7.Биологическое значение геномного уровня организации наследственного материала
- •Глава 4
- •Клеточные
- •И молекулярно-генетические механизмы обеспечения свойств наследственности
- •И изменчивости у человека
- •4.1. Молекулярно-генетические механизмы наследственности и изменчивости у человека
- •4.2. Клеточные механизмы обеспечения наследственности и изменчивости у человека
- •4.2.1.Соматические мутации
- •4.2.2.Генеративные мутации
- •Раздел III онтогенетический уровень организации живого
- •Глава 5 размножение
- •5.1. Способы и формы размножения
- •5.2. Половое размножение
- •5.2.1.Чередование поколений с бесполым и половым размножением
- •5.3. Половые клетки
- •5.3.1.Гаметогенез
- •5.3.2.Мейоз
- •5.4. Чередование гаплоидной и диплоидной фаз жизненного цикла
- •5.5. Пути приобретения организмами биологической информации
- •Глава 6
- •6.1.1.Модификационная изменчивость
- •6.1.2.Роль наследственных и средовых факторов в определении половой принадлежности организма
- •6.1.2.1. Доказательства генетического определения признаков пола
- •6.1.2.2. Доказательства роли факторов среды в развитии признаков пола
- •6.2. Реализация наследственной информации в индивидуальном развитии. Мультигенные семейства
- •6.3. Типы и варианты наследования признаков
- •6.3.1.Закономерности наследования признаков, контролируемых ядерными генами
- •6.3.1.1. Моногенное наследование признаков. Аутосомное и сцепленное с полом наследование
- •При моногенном наследовании
- •6.3.1.2. Одновременное наследование нескольких признаков. Независимое и сцепленное наследование
- •6.3.1.3. Наследование признаков, обусловленных взаимодействием неаллельных генов
- •6.3.2.Закономерности наследования внеядерных генов. Цитоплазматическое наследование
- •6.4. Роль наследственности и среды
- •В формировании нормального
- •И патологически измененного
- •Фенотипа человека
- •6.4.1.Наследственные болезни человека
- •6.4.1.1. Хромосомные болезни
- •6.4.1.2. Генные(или менделевские)болезни
- •6.4.1.3. Мультифакториальные заболевания, или болезни с наследственным предрасположением
- •6.4.1.4. Болезни с нетрадиционным типом наследования
- •Связанные с экспансией тринуклеотидных повторов
- •6.4.2.Особенности человека как объекта генетических исследований
- •6.4.3.Методы изучения генетики человека
- •6.4.3.1. Генеалогический метод
- •6.4.3.2. Близнецовый метод
- •6.4.3.3. Популяционно-статистический метод
- •6.4.3.4. Методы дерматоглифики и пальмоскопии
- •6.4.3.5. Методы генетики соматических клеток
- •6.4.3.6. Цитогенетичвский метод
- •6.4.3.7. Биохимический метод
- •6.4.3.8. Методы изучения днк в генетических исследованиях
- •6.4.4.Пренатальная диагностика наследственных заболеваний
- •6.4.5.Медико-генетическое консультирование
- •Глава 7 периодизация онтогенеза
- •7.1. Этапы. Периоды и стадии онтогенеза
- •7.2. Видоизменения периодов онтогенеза, имеющие экологическое и эволюционное значение
- •7.3. Морфофизиологические и эволюционные особенности яиц хордовых
- •7.4. Оплодотворение и партеногенез
- •7.5. Эмбриональное развитие
- •7.5.1.Дробление
- •7.5.2.Гаструляция
- •7.5.3.Образование органов и тканей
- •7.5.4.Провизорные органы зародышей позвоночных
- •7.6. Эмбриональное развитие млекопитающих и человека
- •7.6.1.Периодизация и раннее эмбриональное развитие
- •7.6.2.Примеры органогенезов человека, отражающих эволюцию вида
- •Глава 8 закономерности индивидуального развития организмов
- •8.1. Основные концепции
- •В биологии индивидуального развития
- •8.2. Механизмы онтогенеза
- •8.2.1.Деление клеток
- •8.2.2.Миграция клеток
- •8.2.3.Сортировка клеток
- •8.2.4.Гибель клеток
- •8.2.5.Дифференцировка клеток
- •8.2.6.Эмбриональная индукция
- •8.2.7.Генетический контроль развития
- •8.3. Целостность онтогенеза
- •8.3.1.Детерминация
- •8.3.2.Эмбриональная регуляция
- •8.3.3.Морфогенез
- •8.3.4.Рост
- •8.3.5.Интегрированность онтогенеза
- •8.4. Регенерация
- •8.5. Старость и старение. Смерть как биологическое явление
- •8.5.1.Изменение органов и систем органов в процессе старения
- •8.5.2.Проявление старения на молекулярном, субклеточном и клеточном уровнях
- •8.6. Зависимость проявления старения от генотипа, условий и образа жизни
- •8.6.1.Генетика старения
- •У различных видов млекопитающих животных
- •8.6.2.Влияние на процесс старения условий жизни
- •8.6.3.Влияние на процесс старения образа жизни
- •8.6.4.Влияние на процесс старения эндоэкологической ситуации
- •8.7. Гипотезы, объясняющие механизмы старения
- •8.8. Введение в биологию продолжительности жизни людей
- •8.8.1.Статистический метод изучения закономерностей продолжительности жизни
- •8.8.2.Вклад социальной и биологической компонент в общую смертность в историческом времени и в разных популяциях
- •Глава 9 роль нарушений механизмов онтогенеза в патологии человека
- •9.1. Критические периоды
- •В онтогенезе человека
- •9.2. Классификация врожденных пороков развития
- •9.3. Значение нарушения механизмов онтогенеза в формировании пороков развития
- •Рекомендуемая литература
- •Раздел I 8
- •Глава 1 8
- •Раздел II 36
- •Глава 2 36
- •Глава 3 61
- •Глава 4 187
- •Раздел III 207
- •Глава 5 207
- •Глава 6 227
- •Глава 7 294
- •Глава 8 351
- •Глава 9 442
4.1. Молекулярно-генетические механизмы наследственности и изменчивости у человека
Благодаря большому объему человеческого генома и более низкому давлению естественного отбора, связанному с социальной природой человека (см. § 1,9), в генофонде человечества за тысячелетия его существования в результате постоянно идущего мутационного процесса накоплено большое число аллелей многих генов. Это является причиной формирования у людей разнообразных вариантов признаков и свойств как на структурном, так и на биохимическом уровнях. В основе индивидуальных различий по многим белкам лежат изменения соответствующих генов. Изучение аминокислотного состава вариантов белков человеческого организма, интенсивности их синтеза, функциональной активности дает ценные сведения об организации и экспрессии его наследственного материала.
Удобной моделью для изучения молекулярно-генетических механизмов наследственности и изменчивости у человека является гемоглобин — специфический белок эритроцитов, легко выделяемый из организма без применения трудоемких биохимических методик. В результате длительного изучения этого белка накопилось много фактов, свидетельствующих об изменчивости его первичной структуры и свойств. В настоящее время обнаружено около 400 различных разновидностей гемоглобина, встречающихся как в нормальном развитии на разных стадиях онтогенеза, так и приводящих к различным заболеваниям.
Молекула гемоглобина состоит из четырех полипептидных цепей (двух α- и двух β-цепей), каждая из которых соединена с небелковым компонентом — гемом, содержащим железо. Две названные полипептидные цепи имеют варианты, контролируемые разными, но близкими нуклеотидными последовательностями, которые образуют два семейства генов (см. разд. 3.6.4.3). Различные нуклеотидные последовательности экспрессируются на определенных стадиях индивидуального развития — у эмбриона, плода, после рождения (см. § 6.2). При этом полипептиды, сменяющиеся в зависимости от стадии онтогенеза, незначительно различаются по аминокислотному составу. Так, Aγ и Gγ-глобины различаются по одной аминокислоте в 136-м положении (аланин или глицин). Вариант Aγ-глобина (TAγ) в 75-м положении вместо изолейцина имеет треонин. Цепь δ отличается от β-цепи лишь десятью аминокислотными остатками.
Из многочисленных мутаций гемоглобина большинство достаточно редки и лишь немногие из них встречаются чаще других, например HbS, HbC, НЬЕ. Большая часть вариантов гемоглобина (около 350) различается единичными аминокислотными заменами, причиной которых являются генные мутации, связанные с заменой оснований в нуклеотидных последовательностях α- или β-глобинового семейства. Многие аминокислотные замены существенно не влияют на функцию гемоглобина и не приводят к патологическим проявлениям. Как правило, это замены в обращенных наружу участках полипептидных цепей тетрамера.
Замены аминокислот, нарушающие нормальную спиральную структуру цепей, часто вызывают неустойчивость гемоглобина. Замена в участках, которыми α- и β-цепи контактируют друг с другом, влияют на сродство гемоглобина к кислороду. Нарушения функций гемоглобина, возникающие в результате таких изменений структуры α- и β-глобиновых генов, ведут к появлению заболеваний, которые можно разделить на четыре основные группы.
1. Гемолитические анемии. Проявляются в распаде эритроцитов, зависящем от неустойчивости гемоглобина (описано около 100 вариантов нестабильных гемоглобинов с мутациями в гене β-цепи).
2. Метгемоглобинемии. Обусловлены ускоренным окислением двухвалентного железа до трехвалентного и образованием гемоглобина М (известны пять таких мутаций в генах α- и β-цепей, состоящих в замене одного основания).
3. Эритроцитоз. Заключается в образовании большего, чем обычно, количества эритроцитов, что обусловлено повышенным сродством гемоглобина к кислороду, который с трудом высвобождается в тканях (таких мутаций известно около 30).
4. Серповидно-клеточная анемия. Заключается в замене гемоглобина НЬА на HbS, который отличается растворимостью и кристаллизацией в условиях гипоксии, что приводит к изменению формы эритроцитов, и проявляется фенотипическим многообразием симптомов (см. рис. 3.21).
Заболевания первых трех групп наследуются по доминантному типу, так что гетерозиготы по мутантному гену страдают нарушением здоровья. Наследование серповидно-клеточной анемии при обычных условиях осуществляется по рецессивному типу, но в условиях сильной гипоксии, например при нахождении на высоте свыше 3000 м над уровнем моря гетерозиготы НbА HbS также страдают анемией.
Описанные мутантные формы гемоглобина возникают в результате изменений структуры генов по типу замены оснований. Мутации иного характера приводят к появлению аллелей глобинов, обусловливающих другие виды патологии. Так, нарушение процесса рекомбинации между аллельными генами (неравноценный кроссинговер) приводит к изменению числа нуклеотидов в них. Следствием этого может быть сдвиг рамки считывания. Нередким результатом таких структурных изменений генов является подавление синтеза той или иной цепи гемоглобина, приводящее к развитию патологических состояний, известных под общим названием талассемии.
Деления одного нуклеотида в 139-м триплете α-глобинового гена, состоящего из 141 триплета, приводит к сдвигу рамки считывания и прочитыванию в новой рамке терминирующего 142-го кодона. При этом (α-глобиновая цепь удлиняется на пять дополнительных аминокислот. Такой особенностью α-цепей характеризуется гемоглобин Vayne. Когда деления располагается ближе к 5'-концу, активный продукт не синтезируется и развиваются различные формы α-, β- и γ-талассемий.
Некоторые варианты гемоглобинов возникают в результате дупли-каций. Так, гемоглобин Grady несет дупликацию 116—118 аминокислотных остатков в γ-цепи. В гемоглобине Cranston удлинение р-цепи до 158 аминокислотных остатков является результатом дупликации AG-последовательности после 144-го триплета и последующего сдвига рамки с пропитыванием терминального кодона.
Описанное выше свидетельствует о том, что различные отклонения в структуре ДНК глобиновых генов приводят к замене аминокислот или удлинению полипептидных цепей. Это является причиной образования многих вариантов гемоглобина, которые определяют развитие у человека заболеваний, наследующихся в ряду поколений.
Не меньший интерес представляют механизмы развития различных заболеваний человека, в основе которых лежат мутации генов, приводящие к синтезу белков-ферментов со сниженной активностью или к его подавлению. Это нарушает течение процессов, катализируемых данными ферментами в клетках организма. Примером наследственно детерминированных повреждений метаболизма в организме человека служит фенилкетонурия, развивающаяся вследствие нарушения процессов обмена аминокислоты фенилаланина и накопления в организме токсических промежуточных продуктов.
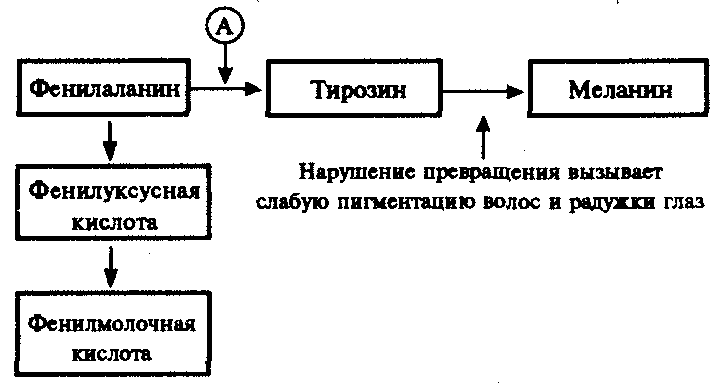
Рис. 4.1. Краткая схема обмена фенилаланина:
А — фермент фенилаланингидроксилаза, наследственный дефект которого приводит к развитию фенилкетонурии
При дефекте фермента фенилаланингидроксилазы фенилаланин не превращается в тирозин (рис. 4.1) и накапливается в крови больных в больших концентрациях (до 0,5—0,6 г/л вместо 0,003— 0,04 г/л в норме). Это приводит к частичному превращению фенилаланина в фенилуксусную и фенилмолочную кислоты, накопление которых наряду с повышенной концентрацией самого фенилаланина оказывает токсическое действие на мозг ребенка. В результате у детей наблюдается различная степень дефекта умственного развития. Нарушение метаболизма фенилаланина сопровождается также нарушением синтеза пигмента меланина, поэтому у больных наблюдается слабая пигментация волос и радужки глаз. Кроме того, высокая концентрация фенилаланина оказывает ингибирующее влияние на ряд ферментных систем, участвующих в превращении других аминокислот: у больных развивается судорожный синдром, нарастает отставание интеллектуального развития. Наследование фенилкетонурии осуществляется по рецессивному типу.
Таким образом, рассмотренные выше примеры демонстрируют весь спектр действия молекулярно-генетических механизмов, обеспечивающих образование в человеческом организме белков как нормально функционирующих, так и обусловливающих развитие различных патологических состояний. Из сказанного по поводу гемоглобина следует, что, во-первых, образование главного функционального белка эритроцитов находится под генным контролем, во-вторых, формирование тетрамерной формы этого белка, с которой связана его физиологическая активность, требует взаимодействия неаллельных генов α- и β-глобинов.
Специфический контроль небелковой части молекулы гемоглобина также имеет место и осуществляется независимо, через гены ферментов, необходимых для синтеза гема. Особенности проявления патологических признаков у носителей мутантных аллелей свидетельствуют о существовании определенных отношений между ними и нормальными аллелями. Так, аллель серповидно-клеточности в сочетании с нормальным аллелем (3-глобина (НbА HbS) проявляет себя в обычных условиях как рецессивный. Так же ведет себя мутантный аллель гена, детерминирующего синтез фермента фенилаланингидроксилазы. Проявлением взаимодействия между мутантным и нормальным аллелями по типу доминирования последнего является формирование в организме белка с нормальными свойствами у гетерозигот. Отсутствие нормального аллеля в генотипе организма, гомозиготного по мутантному аллелю, приводит к развитию патологического состояния, обусловленного нарушением функциональной активности соответствующего белка.
Особую группу наследственно обусловленных патологических состояний у человека представляют заболевания, причиной которых являются мутации митохондриальной ДНК (мгДНК).
Биосинтез митохондриальных белков находится под контролем двух генетических систем: ядерных и митохондриальных генов. Большая часть белков кодируется ядерной ДНК, синтезируется в цитоплазме, а затем транспортируется в митохондрии. Наряду с этим в кольцевой молекуле ДНК органеллы имеются гены, которые отвечают за собственный синтез белков, а также участвующих в нем тРНК и рРНК. В ядерном геноме имеется значительное количество генов, обеспечивающих функционирование митохондриальной ДНК. Предполагают, что мутации некоторых ядерных генов приводят к делениям значительных участков ДНК митохондрии. В результате нарушается синтез собственных белков, к числу которых относятся и ферменты дыхательных цепей, нарушается дыхательная функция митохондрии.
У человека описано более 100 заболеваний, причиной которых являются изменения в структуре мтДНК (см. 6.4.1.4).
