
Staraya_papka / Серия Бальмера
.docВыполнил студент 3 курса 9 группы
Грибов Денис
Серия Бальмера
Цель работы: уяснить природу серии Бальмера. Наблюдать визуально серию Бальмера с помощью монохроматора УМ-2. Проградуировать монохроматор УМ-2. Определить длины волн серии Бальмера, их частоты и энергии. Экспериментально получить значение постоянной Ридберга R.
Краткая теория
При рассматривании видимой части спектра атомов водорода в спектроскоп с невысокими разрешающей силой и обратной дисперсией, каким является монохроматор УМ-2 наблюдается совокупность отдельных узких линий разных цветов, называемая серией Бальмера. Частоты этих линий с точностью, определяемой возможностями указанного спектрального прибора, поддаются систематизации формулой Ридберга, найденной первоначально эмпирически Ридбергом в 1890 г.
![]() (1)
(1)
Здесь n=2, а m>2 -числа натурального ряда соответствуют видимой области, т.е. серии Бальмера. Формула (1) может быть получена уже в рамках теории атома Бора. Однако строго последовательно эта формула получается лишь после решения уравнения Шредингера для атома водорода.
Из формулы (1) следует, что
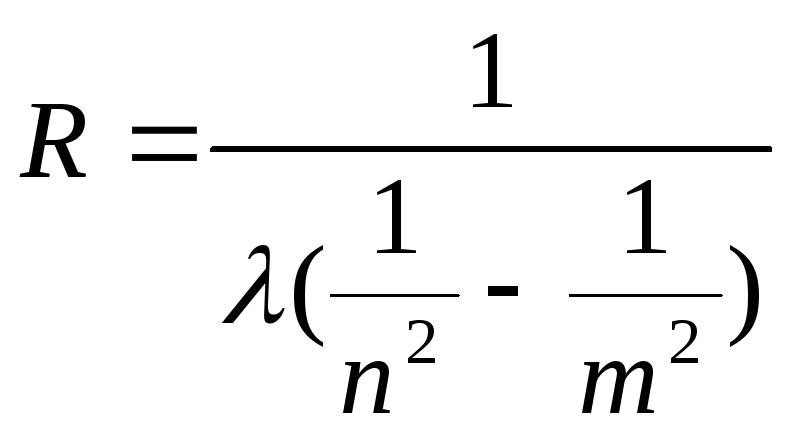 .
.
Тонкая структура линий спектра водорода может быть интерпретирована только на основе квантово-механических представлений, решение уравнения Шредингера дан уровней энергия водородоподобного атома имеет вид
![]() ,
(2)
,
(2)
где Z – заряд ядра атома, n – главное квантовое число. Формула (2) дана в атомной системе единиц для энергии, то есть в Ридбергах.
Уровень - это совокупность состояний с одним и тем же полным внутренним моментом импульса j.
Энергии уровней равны (в ед. Ry):
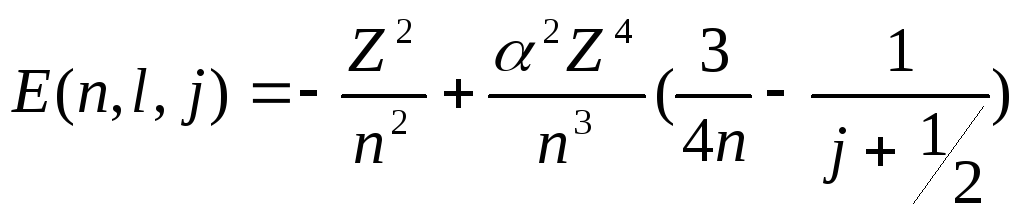 (3)
(3)
То есть
![]() ,
где
,
где
![]() -
Боровский радиус.
-
Боровский радиус.
Уровнем энергии называется одно из дискретных значений энергии, которое может иметь система. Энергия излучается или поглощается системой при переходах ее с одного уровня энергии на другое энергетический уровень.
При этом конечно должны меняться и уровни состояний!
Каждая линия серии
Бальмера состоит из пяти компонентов,
объединениях в две группы. Наибольшее
расстояние между компонентами в группах,
как это следует из формулы (3), нужно
ожидать у головной линии серии Бальмера.
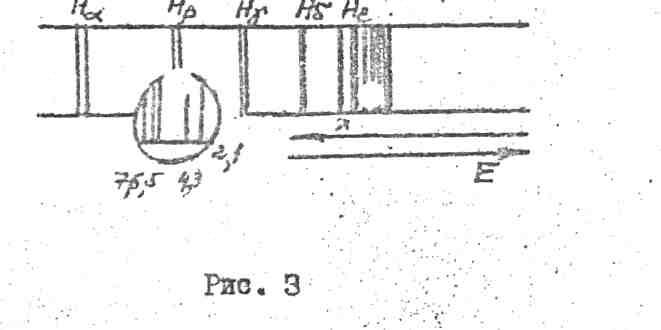
На рис. З показана
серия Бальмера атома водорода, какой
ее можно наблюдать в монохроматоре
УМ-2. Для линии
![]() приведена тонкая структура.
приведена тонкая структура.
Ход работы:
1. Таблица 1
|
Цвет |
длина волны, А |
деления барабана |
|
красная |
6234,37 |
2700 |
|
желтая |
5790,65 |
2550 |
|
желтая |
5769,59 |
2484 |
|
зеленая |
5460,74 |
1340 |
|
зелено-голубая |
4916,04 |
1890 |
|
синяя |
4358,35 |
1230 |
|
фиолетовая |
4077,81 |
742 |
|
фиолетовая |
4046,55 |
678 |
Градуировочный график
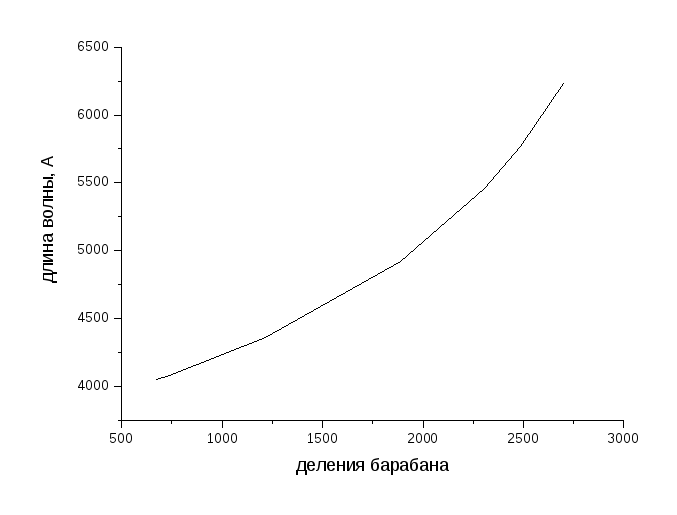
2. Таблица 2
|
цвет |
деления барабана |
интенсивность |
длина волны, А |
постоянная Ридберга |
энергия, эВ |
|
красная |
2634 |
3000 |
6300 |
114000 |
-6,047 |
|
зелено-голубая |
1838 |
500 |
4860 |
110000 |
-3,402 |
|
фиолетовая |
1202 |
200 |
4400 |
108000 |
-2,177 |
|
фиолетовая |
798 |
100 |
4090 |
110000 |
-1,512 |
