Электрохимическая коррозия
.doc
Г У А П
кафедра 15
Рейтинг за работу
Преподаватель: Кораблева А.А.
ОТЧЕТ
О ЛАБОРАТОРНОЙ РАБОТЕ
ПО КУРСУ: ОБЩАЯ ХИМИЯ
" ЭЛЕКТРОХИМИЧЕСКАЯ КОРРОЗИЯ
И МЕТОДЫ ЗАЩИТЫ ОТ НЕЁ"
Х 15 2101 04 ЛР
Работу выполнил Зуев И.А.
студент группы 3111
Санкт – Петербург
2001
Цель работы:
Проследить и обосновать как и какие реакции происходят при электрохимической коррозии.
Записать уравнения качественных реакций:
-
Налили FeSO4 + K 3[Fe (CN)6 ]
-
Налили ZnSO4 + K 3[Fe (CN)6 ]
a) Обнаружение йонов цинка:
3ZnSO4 + 2K3[Fe (CN)6] = Zn3[Fe (CN)6]2 + 3K2SO4
3Zn + 2[Fe (CN)6] = Zn3[Fe (CN)6]2
б) Обнаружение йонов железа:
3FeSO4 + 2K3[Fe (CN)6] = Fe3[Fe (CN)6]2 + 3K2SO4
3Fe + 2[Fe (CN)6] = Fe3[Fe (CN)6]2
Коррозия в нейтральной среде:
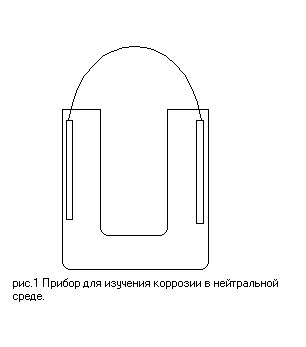
Опыт проводиться на установке, изображенной на рис.1
В U – образную трубку налить 5 – 10 мл. водного раствора NaCl. В него опускаем пластины металлов, соединенных между собой прт помощи зажимов. Пластинки металлов должны быть тщательно зачищены наждачной шкуркой, а место контакта пластинки и зажима находится вне раствора. При выполнении опыта необходимо отметить изменение окраски раствора у катода и анода.
-
Берем 1ю пару Cu и Fe, в U-образную трубку наливаем раствор NaCl, раствор фенол-фтолеина и раствор К3Fe (CN)6.
A: Zn – 2e = Zn+2
3Zn + 2[Fe (CN)6] = Zn3[Fe (CN)6]2
K: O2 + 4e + 2H2O = 4OH
Наблюдения:
На железном гвозде мы видим появление образований синего цвета, на меди – красного.
2). Берем 2ю пару Cu и Zn, добавляем растворы фенол-фтолеина, NaCl, К3Fe (CN)6
А: Fe – 2e = Fe+2
3Fe + 2[Fe (CN)6] = Fe3[Fe (CN)6]2
K: O + 4e + 2H2o = 4OH
Наблюдения:
На меди происходит образование пузырьков водорода, также мы наблюдаем ее покраснение.
Цель добавления индикаторов и иных веществ:
Целью добавления индикатора является возможность визуального наблюдения протекания реакции и результатов.
Вывод:
Коррозия в нейтральной среде идет в любом случае с кислородной деполяризацией на катоде (восстановление кислорода на катоде)
Коррозия в кислой среде:
Опыт производим на установки, изображенной на рис.2.
В фарфоровую чашечку наливаем 10% раствора HCl. В раствор опустить два металла Al и Cu, и наблюдаем за поведением металлов.
-
Берем 1ю пару Cu + HCl
Cu + HCl = Реакция не идет.
Наблюдения:
Реакция не идет.
-
Б


 ерем
2ю пару Al
+ HCl
ерем
2ю пару Al
+ HCl
A :
Al – 3e = Al+3
2
:
Al – 3e = Al+3
2
K: 2H + 2e = H2 3
2Al + 6H = 2Al +3H2
2Al + 6HCl = 2AlCl3 +3H2
Наблюдения:
Реакция идет. Появились пузырьки водорода на аллюминие.
Цель добавления индикаторов и иных веществ:
Целью добавления индикатора является возможность визуального наблюдения протекания реакции и результатов.
Вывод:
Чтобы показать, что один и тот же металл железа ведет себя по разному в зависимости от того с чем контактирует. Если контактирует с активным металлом, то является катодом и коррозией не подвергается, является только проводником электронов. Отсюда метод защиты от коррозии анодное покрытие (более активный металл).
Протекторная защита более активного металла ставится в соприкосновении с основным металлом и защищает от коррозии основной металл.