
- •176 Программа блока гетерофункциональные углеводороды.
- •Конспект лекций гетерофункциональные углеводороды
- •Углеводы
- •1.1 Моноуглеводы
- •Химическое строение моносахаридов
- •1. Реакции карбонильных форм моносахаридов
- •2.2 Реакции с участием всех гидроксильных групп
- •Олигосахариды
- •1.2.1 Дисахариды
- •1.2.3 Несахароподобные полисахариды
- •1.2.3.1 Гомополисахариды
- •1.2.3.2 Гетерополисахариды
- •2. Аминокислоты
- •(Nh2)m r(cooh)n,
- •2. Получение β-аминокислот
- •3.2.Перегруппировка оксимов (перегруппировка Бекмана):
- •1,1-Амидные группы
- •Оксикислоты
- •7. Синтез из альдегидов
- •1.3 Реакции нуклеофильного замещения α-галогенкарбоновых кислот.
- •4. Гетероциклические соединения
- •4.1 Пятичленные гетероциклы с одним гетероатомом
- •6. Реакция диенового синтеза с малеиновым ангидридом
- •2. Пиролизом:
- •1. Сухой перегонкой аммонийной соли слизевой кислоты или действием аммиака на фуран в присутствии оксида алюминия:
- •3. Получают при пропускании аммиака и паров бутиндиола-1,4 над катализатором при 300с:
- •4. При перегонке сукцинимида с цинковой пылью:
- •5. Восстановление смеси кетона с изонитрозокетона даёт гомологи или замещенные пирролы:
- •3. Реакция электрофильного замещения (механизм и ориентация замещения):
- •1. Индол обладает слабоосновными свойствами и в то же время слабокислыми, образует металлические производные – индол-калий, индол-натрий:
- •4.2 Пятичленные гетероциклы с несколькими гетероатомами
- •4.3 Шестичленные гетероциклы с одним гетероатомом
- •4.4 Шестичленные гетероциклы с несколькими гетероатомами
- •1. Основные свойства:
- •2. Свойства, обусловленные функциональными группами, в том числе групповые реакции:
- •4.4 Шестичленные гетероциклы с двумя разными гетероатомами
- •Нобелевские премии по органической химии
1. Основные свойства:
![]()
Образование солей:
растворимых в воде хлоридов, бромидов, сульфатов, нитратов, фосфатов (используются как лекарственные формы алкалоидов);
нерастворимых в воде с обще алкалоидными реактивами (используются для идентификации).
2. Свойства, обусловленные функциональными группами, в том числе групповые реакции:
мурексидная проба на пуриновые алкалоиды;
талейохинная проба на хинин и хинидин.
Мурексидная реакция:

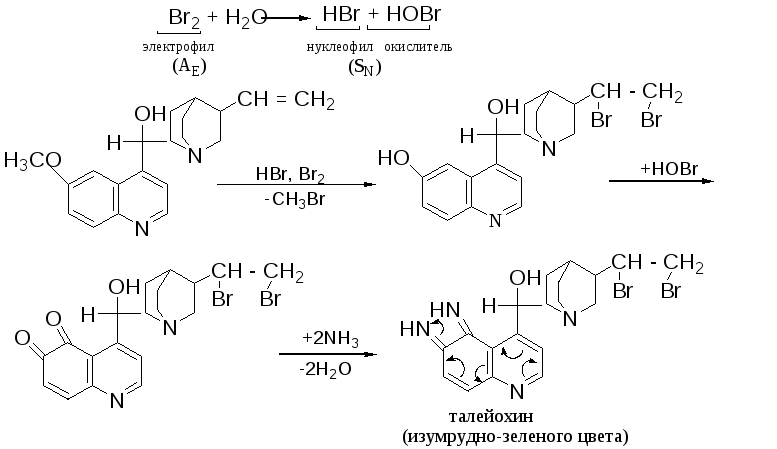
Талейохинная реакция:
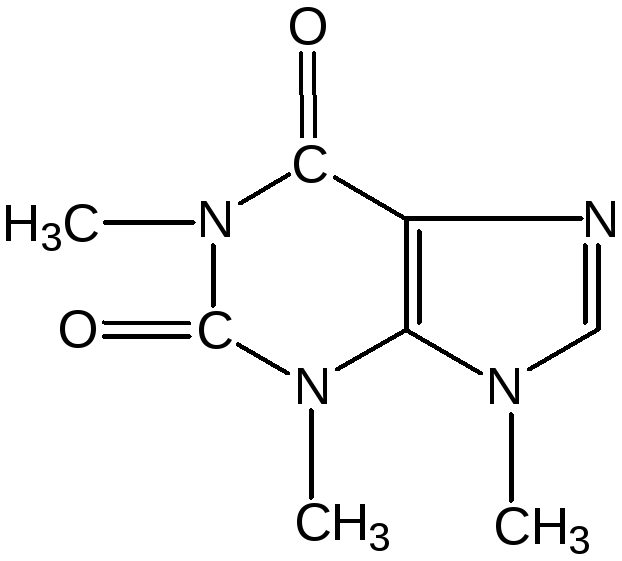
Кофеин. Химическое строение молекулы кофеина выражается формулой:
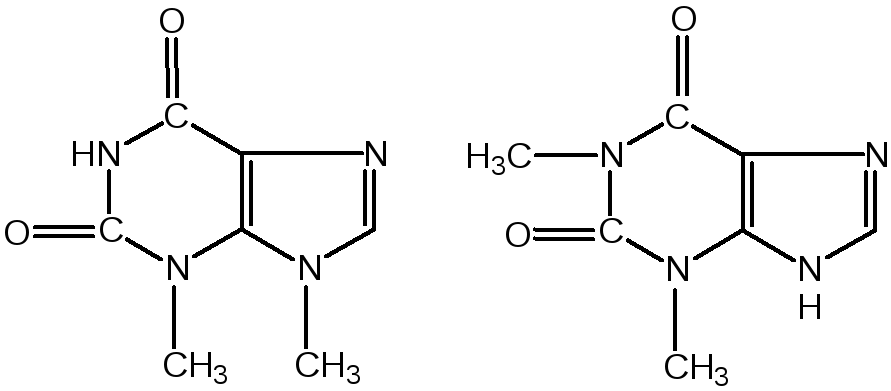
Кофеин вступает во все реакции, свойственные пуриновым соединениям. Известны два структурных аналога кофеина — теобромин и теофиллин, имеющие также важное биологическое значение:
Биологическое и медицинское значение синтетических природных пуринов. Особый интерес вызвали пуриновые соединения в связи с их возможной противоопухолевой активностью после того, как была выявленная первостепенная важность нуклеиновых кислот в процессе воспроизведения роста клеток. Если раковая опухоль есть результат патологического, ненормального роста «искаженных» клеток какой-либо биологической ткани, то естественно сделать вывод, что «главный конструктор» новых клеток – нуклеиновая кислота – сама претерпела в своей конфигурации какие-либо микроизменения, отразившиеся потом в белковом синтезе. Изменения в структуре нуклеиновой кислоты одна из основных причин возникновения злокачественных опухолей. Возможно, если измененная структура нуклеиновой кислоты вызывает нарушения в белковом синтезе, ведущие к росту необычных, возможно упрощенных клеток, то другое направленное изменение в структуре нуклеиновой кислоты может вызвать прекращение воспроизводства таких клеток. Эта мысль и привела к исследованию на противоопухолевую активность так называемых пуриновых антиметаболитов.
Пуриновые антиметаболиты – соединения со структурой похожей на структуру природных пуриновых оснований в нуклеиновых кислотах. Они могут конкурировать с последними по своей функциональной направленности и в участии в белковом синтезе. Различия в структуре природных пуринов и антиметаболитов должны быть незначительными.
Степень противоопухолевой активности сильно зависит от некоторых определенных структурных узлов в молекуле антиметаболитов. Известно также, что адениновая структура антиметаболитов придает им особо активные свойства. Люстиг и Вахтель обнаружили, что различные пурины, содержащие метальную группу в положении 7, обладают способностью продлевать жизнь подопытных животных, пораженных раковой опухолью.
Наибольшее число работ посвящено изучению противоопухолевой активности 6-меркаптопурина. Предполагается, что это соединение взаимодействует с никотинамидадениннуклеотидной коферментной системой и контролирует нормальный биосинтез пуринов. Однако более конкретные сведения о механизме действия 6-меркаптопурина на раковые опухоли пока отсутствуют. К антиметаболитам, обладающим противоопухолевой активностью, следует также отнести 6-хлор-9-метилпурин, 2-амино-6-меркаптопурин, 2-амино-6-меркапто-9-π-пропил-пурин, 9-(2'-тетрагидрофурфурил)-6-меркаптопурин. Другие производные этого соединения применялись для лечения лейкемии.
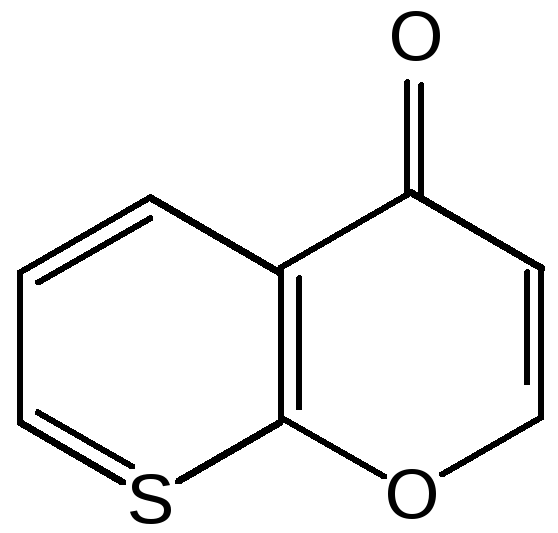
Шестичленные гетероциклы с атомом кислорода. С точки зрения обычных валентных представлений шестичленный цикл, содержащий атом кислорода, может быть представлен в виде пирановых структур или их производных – пиронов:

γ-Пиран является также очень неустойчивым соединением:
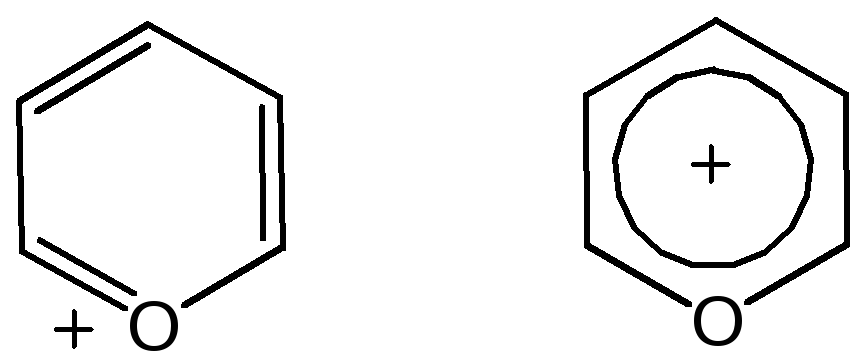
Кроме упомянутых структур известна катионная форма шестичленного гетероцикла с одним атомом кислорода – катион пирилия который входит в состав пирилиевых солей. Вывод о существовании таких солей сделали Колли и Тикле еще в 1899 г.
Производные пирана:
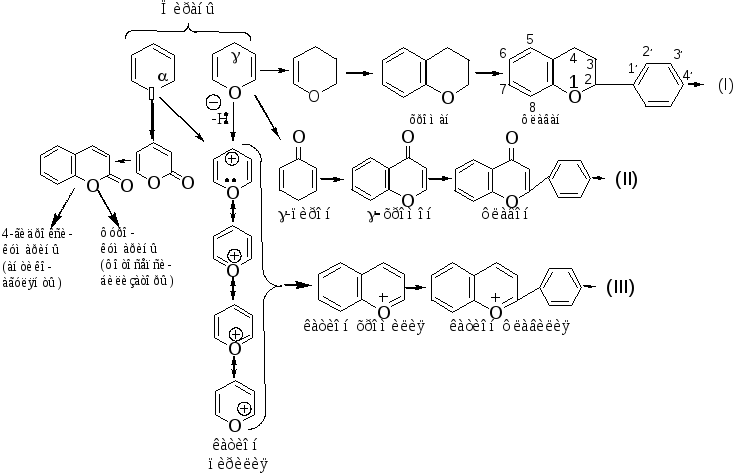
I – Катехины, гидроксипроизводные флавана.
Катехин – 3, 5, 7, 3`, 4` - пентагидроксифлаван.
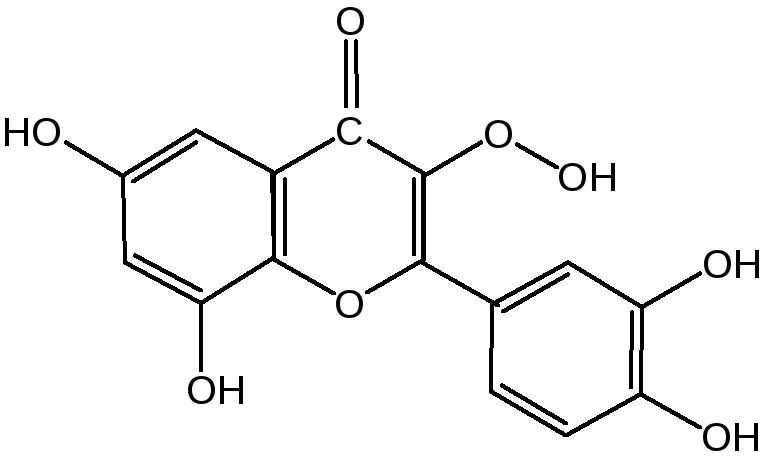
II – Флавонолы, гидроксипроизводные флавона.
Кверцетин – 3, 5, 7, 3`, 4` - пентагидроксифлавон.
III – Антоцианидины – гидроксипроизводные флавилия-катиона.
Цианидин – 3, 5, 7, 3`, 4` - пентагидроксифлавилия хлорид.
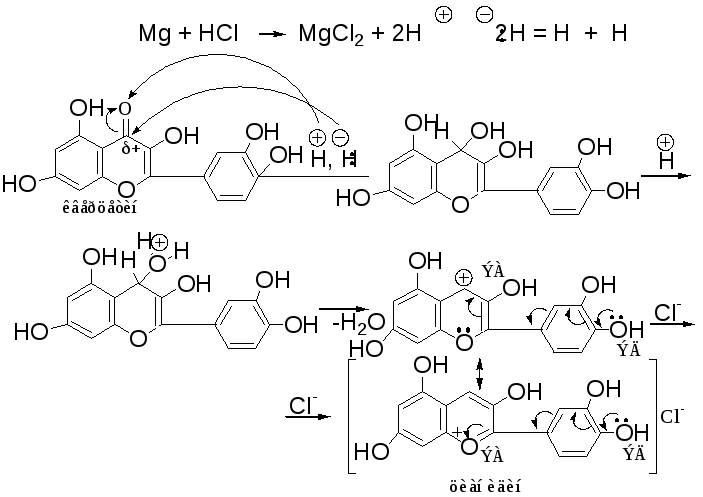
Цианидииовая проба:
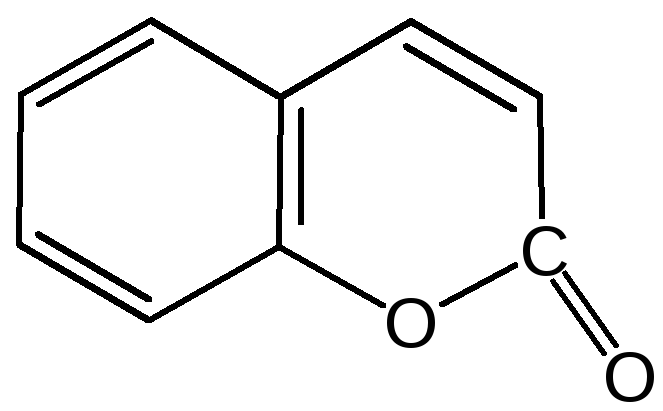
Кумарин (α-бензопирон) и его производные широко распространены в природе. Кумарин имеет запах сена, он – пахучее начало цветов донника. В растениях он находится в виде гликозида и запах кумарина появляется лишь при высыхании растений, которое сопровождается гидролизом:
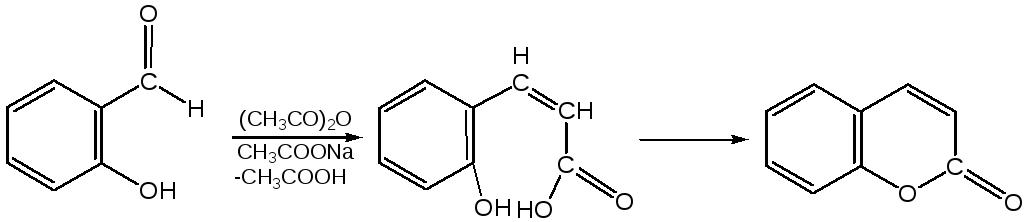
В промышленности кумарин получают по реакции Перкина – конденсацией салицилового альдегида с уксусным ангидридом в присутствии ацетата натрия:
Кумарин применяется в качестве отдушки для печенья, лимонадов, мыла и табака, а также компонента фруктовых эссенций. Оксипроизводные кумарина – 7-оксикумарин и 7,8-диоксикумарин также широко распространены в растительном мире.
Хромон (γ-бензопирон). Скелет хромона лежит в основе витаминовЕ (токоферолов), необходимых для размножения животных.
Известно семь веществ, обладающих действием изомерных друг другу.

Биологическая активность витамина Епроявляется в способности образовывать устойчивые свободные радикалы в результате отделения атома водорода от гидроксильной группы. Эти радикалы могут вступать во взаимодействие со свободными радикалами, образующимися при распаде органических пероксидов и гидропероксидов. Тем самым витаминЕпредотвращает окисление ненасыщенных липидов и предохраняет биологические мембраны от разрушения. В качестве антиоксиданта он добавляется в пищевые жировые продукты, предохраняя их от окислительного прогоркания. Из пищевых продуктов витаминомЕ наиболее богаты растительные масла, содержится он также в масле из пшеничных зародышей.
Флавоны окрашивают в желтый, красный и синий цвет цветки, почки и ягоды:

Например, природные оксипроизводные флавона лутеолин и кверцетин – это природные красители, окрашенные в желтый цвет, содержащиеся в желтых цветах:

В растениях они находятся в виде гликозидов. Один из гликозидов кверцетина с дисахаридом, состоящим из рамнозы и глюкозы, называется рутином. Это – одно из веществ, относящихся к группе витаминов Р (бифлаваноидов), при отсутствии которых в пище увеличивается проницаемость кровеносных сосудов, что ведет к «пурпуровой болезни» – множественным точечным кровоизлияниям.
Следует указать на тесную функциональную связь витаминов С (аскорбиновая кислота) и Р (рутин) в окислительно-восстановительных процессах организма, образующих единую систему. Об этом свидетельствует лечебный эффект, оказываемый комплексом аскорбиновой кислоты и бифлаваноидов, названный аскорутином. Основные источники витамина Р для человека – это растительные продукты питания (в частности, овощи и фрукты), в которых также содержится много витамина С.
При восстановлении оксифлавонов можно получить антоцианидины, содержащие оксониевый кислород, входящий в ароматический цикл. так, кверцетин дает при этом цианидин, дальнейшее гидрирование которго приводит к катехину (дубители), содержащемуся в чае и обладающем Р-витаминной активностью.
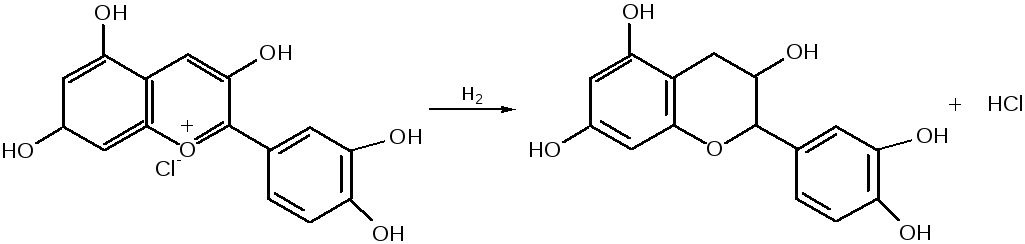
Антоцианидины – относительно прочные твердые соли, интенсивно окрашенные. В виде гликозидов они являются антоциановыми красителями, окрашивающими цветы, ягоды и овощи (по-гречески антоциан – краска цветов). Все антоцианы – кислотно-основные индикаторы, т. е. их окраска зависит от рН среды. В кислой среде их окраска сдвигается в сторону красной, в щелочной – в сторону синей (или сине-зеленой), в нейтральной она фиолетовая. Так, краситель цианидин окрашивает васильки в синий цвет (щелочная среда в лепестках), а розу – в красный цвет (кислая среда). Другие представители антоцианидинов – пеларгонидин (лежит в основе окраски цветов пеларгонии), дельфинидин (окраска синих цветов дельфиниума, а также красного винограда и вина). Первый содержит в фенильном ядре на один гидроксил меньше, а второй – на один гидрокисл больше, чем цианидин.
На этих трех антоцианидинах построено великое множество оттенков сине-красной гаммы. Отдельные антоциановые красители отличаются тем, что один или два гидроксила в фенильном ядре метилированы, а гликозиды образованы разнообразными сахарами.
