
- •Вопрос 1. Кровь. Понятие, физиологические функции.
- •Вопрос 2. Химический состав крови. Минеральные и органические вещества.
- •Вопрос 3. Особенности строения, развития и метаболизма эритроцита.
- •Вопрос 4. Гемоглобин, строение, свойства, биологическая роль.
- •Вопрос 5. Варианты первичной структуры гемоглобина человека. Гемоглобинопатии.
- •Вопрос 6. Схема связывания газов гемоглобином. Карбокси- и метгемоглобин.
- •Вопрос 7. Транспорт кровью кислорода и двуокиси углерода (схема).
- •Вопрос 8. Биосинтез гема (формулы, ферменты) и его регуляция.
- •Вопрос 9. Нарушения биосинтеза гема. Порфирии.
- •Вопрос 10. Схема распада гемоглобина. «Непрямой» (неконьюгированный) билирубин.
- •Вопрос 11. Обезвреживание билирубина печенью. Формула конъюгированного («прямого») билирубина.
- •Вопрос 12. Нарушения обмена билирубина. Гипербилирубинемия и ее причины.
- •Вопрос 13. Желтухи, причины. Типы желтух. Желтуха новорожденных.
- •Вопрос 14. Диагностическое значение определения билирубина и других желчных пигментов в крови, моче и кале при разных типах желтух.
- •Вопрос 15. Белки сыворотки крови. Общее содержание, функции. Отклонения в содержании общего белка сыворотки крови, причины.
- •Вопрос 17. Ферменты крови. Происхождение ферментов крови, диагностическое значение определения.
- •Вопрос 18. Калликреин-кеининовая система, представители, физиологическая роль кининов.
- •Вопрос 19. Белки «острой фазы», представители, диагностическое значение.
- •Вопрос 20. Ренин-ангиотензиновая система, состав, физиологическая роль.
- •Вопрос 21. Свёртывающая система крови. Общее представление о ферментном каскаде процесса свёртывания.
- •Вопрос 22. Плазменные факторы свёртывающей системы крови.
- •Вопрос 23. Внутренний и внешний пути свёртывания крови. Образование протромбиназы.
- •Вопрос 24. Принципы образования и последовательность функционирования ферментных комплексов прокоагулянтного пути. Образование геля фибрина, формирование тромба.
- •Вопрос 25. Роль витамина К в процессах свертывания крови.
- •Вопрос 26. Противосвёртывающая система крови. Основные первичные и вторичные природные антикоагулянты крови.
- •Вопрос 27. Фибринолитическая система крови. Механизм действия.
- •Вопрос 28. Нарушения процессов свёртывания крови. Тромботические и геморрагические состояния. ДВС синдром.
- •Вопрос 29. Остаточный азот крови. Понятие, компоненты, содержание в норме. Азотемия, типы, причины возникновения.
- •Вопрос 30. Обмен железа: всасывание, транспорт кровью, депонирование. Роль железа в процессах жизнедеятельности.
- •Вопрос 31. Нарушения обмена железа: железодефицитная анемия, гемохроматоз.
- •Вопрос 32. Натрий и калий, содержание в крови в норме, суточная потребность, роль в процессах жизнедеятельности. Нарушения обмена натрия и калия.
- •Вопрос 33. Кальций, содержание в сыворотке крови в норме, роль в процессах жизнедеятельности. Причины и последствия гипо- и гиперкальциемии.
- •Вопрос 34. Регуляция фосфорно-кальциевого обмена. Роль паратирина, тиреокальцитонина и витамина D в этом процессе.
- •Вопрос 35. Содержание хлоридов в крови в норме, суточная потребность, роль в процессах жизнедеятельности, нарушения обмена.
- •Вопрос 36. Распределение воды в организме. Водно-электролитные пространства организма, их состав.
- •Вопрос 37. Роль воды и минеральных веществ в процессах жизнедеятельности.
- •Вопрос 38. Регуляция водно-электролитного обмена. Строение и функции альдостерона, вазопрессина и ренин-ангиотензиновой системы, механизм регулирующего действия.
- •Вопрос 39. Механизмы поддержания объема, состава и рН жидкостей организма.
- •Вопрос 40. Гипо- и гипергидратация водно-электролитных пространств. Причины возникновения.
- •Вопрос 41. Механизмы возникновения почечной гипертензии и отеков. Восстановления объема циркулирующей крови после кровопотерь.
- •Вопрос 42. Роль почек в регуляции водно-электролитного обмена.
- •Вопрос 43. Кислотно-основное состояние организма. Механизм поддержания КОС. Основные показатели кислотно-основного состояния крови в норме.
- •Вопрос 44. Почечные механизмы поддержания кислотно-основного состояния.
- •Вопрос 45. Нарушения кислотно-основного состояния. Типы нарушений. Причины и механизмы возникновения ацидоза и алкалоза.
- •Вопрос 46. Роль печени в процессах жизнедеятельности.
- •Вопрос 47. Метаболическая функция печени (роль в обмене углеводов, липидов, аминокислот).
- •Вопрос 48. Метаболизм эндогенных и чужеродных токсических веществ в печени: микросомальное окисление, реакции конъюгации.
- •Вопрос 49. Обезвреживание шлаков, нормальных метаболитов и биологически активных веществ в печени. Обезвреживание продуктов гниения.
- •Вопрос 50. Механизм обезвреживания чужеродных веществ в печени.
- •Вопрос 51. Металлотионеин, обезвреживание ионов тяжелых металлов в печени. Белки теплового шока.
- •Вопрос 52. Токсичность кислорода. Образование активных форм кислорода.2
- •Вопрос 53. Понятие о перекисном окислении липидов, повреждение мембран в результате перекисного окисления липидов.
- •Вопрос 54. Механизмы защиты от токсического действия кислорода. Антиоксидантная система.
- •Вопрос 55. Основы химического канцерогенеза. Понятие о химических канцерогенах.
- •Вопрос 56. Биотрансформация лекарственных веществ. Влияние лекарств на ферменты, участвующие в обезвреживании ксенобиотиков.
Роль печени в липидном обмене:
Превращение экзогенных липидов с собственные (синтез собственных ТАГ и ФЛ) □ Синтез холестерина и его этерификация;
Образование желчных кислот (первичных и парных);
β-окисление жирных кислот;
Синтез жирных кислот (насыщенных и моноеновых);
Образование транспортных форм липидов – ЛПОНП и ЛПВП;
Синтез кетоновых тел.
Роль печени в белковом обмене:
Синтез собственных белков печени;
Синтез 100% альбуминов и до 90% глобулинов плазмы крови (в том числе ферментых системы гемостаза);
Синтез апобелков липопротеинов;
Синтез заменимых аминокислот;
Процессы трансаминирования, декарбоксилирования, трансметилирования;
Распад и синтез пуриновых и пиримидиновых нуклеотидов.
Вопрос 48. Метаболизм эндогенных и чужеродных токсических веществ в печени: микросомальное окисление, реакции конъюгации.
Вещества, обезвреживаемые в печени:
Собственные (эндогенные):
конечные продукты метаболизма (NH3 , продукты гниения аминокислот);
промежуточные метаболиты (билирубин);
биологически активные вещества (гормоны, биогенные амины).
Экзогенные (ксенобиотики):
яды;
лекарства.
СТАДИИ ОБЕЗВРЕЖИВАНИЯ.
1. Метаболическая (микросомальное окисление, восстановление, гидролиз; немикросомальное окисление).
Монооксигеназная система (система микросомального окисления):
Окислительные ферменты – монооксигеназы;
Промежуточные переносчики Н+ и ефлавопротеины (ФП);
Гемсодержащие белки – цитохромы с самоокисляющимся железом гема.
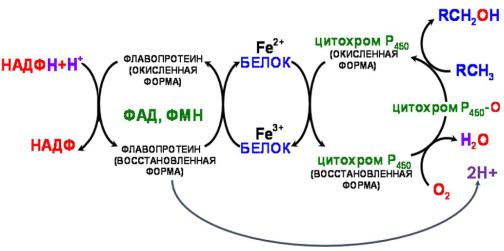
Микросомальная цепь окисления (монооксигеназное гидроксилирование):
2. Конъюгация (объединение с эндогенными молекулами или группами): Ацетильная (с ацетил-КоА);
Метильная (с SAM); Глутатионовая; Аминокислотная (с Гли или Глн); Сульфатная (с ФАФС); Глюкуронидная (с УДФГК)
Вопрос 49. Обезвреживание шлаков, нормальных метаболитов и биологически активных веществ в печени. Обезвреживание продуктов гниения.
Обезвреживание биологически активных веществ:

Гниение аминокислот в кишечнике и обезвреживание образовавшихся продуктов:
Вопрос 50. Механизм обезвреживания чужеродных веществ в печени.
Вопрос 51. Металлотионеин, обезвреживание ионов тяжелых металлов в печени. Белки теплового шока.
Белок металлотионеин – металлопротеин, его много в печени, кишечнике. Это металлопротеин содержащий цинк, органогенный нетоксичный для организма, в то время как другие ионы тяжёлых металлов токсичны для организма. При попадании солей тяжёлых металлов в организм человека, металлотионеин связывает их, выводя из своего состава цинк, тем самым устроены токсичность подступивших тяжёлых металлов в организм. Выходящий из состава металлотионеина цинк связывается с белками и выполняет много функций в организме человека. При отравлении солями тяжёлых металлов количество этого белка резко возрастает
Белки теплового шока – это класс функционально сходных белков, экспрессия которых усиливается при повышении температуры или при других стрессирующих клетку условиях.
Шапероны
Белки теплового шока действуют как внутриклеточные шапероны в отношении других белков. Белки теплового шока играют важную роль в белок-белковых взаимодействиях, например, при фолдинге и сборке сложных белков, препятствуют нежелательной агрегации белков. Белки теплового шока стабилизируют частично свернутые белки и облегчают их транспорт через мембраны внутри клетки. Некоторые белки теплового шока экспрессируются в малых или умеренных количествах во всех типах клеток всех живых организмов, так как играют ключевую роль в существовании белков.
Вопрос 52. Токсичность кислорода. Образование активных форм кислорода.2
Действие АФК на клетку:
1.Разрушение белков;
2.Повреждение ЭПС
3.Разрушение ядерной мембраны, повреждение ДНК;
4.Приводит к перикисному окислению липидов мембран;
5.Нарушает проницаемость плазматической мембраны;
6.Разрушение мембран митохондрий.
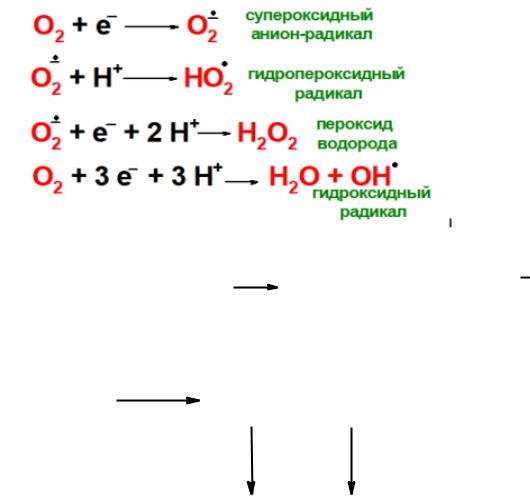
Образование активных форм кислорода:
1. Окисление железа гема:
2+ |
+ О |
3+ |
+ О |
гем-Fe |
гемин-Fe |
||
|
2 |
|
2 |
2. Радиолиз воды под действием ионизирующего излучения:
H О |
h |
ОН |
. |
+ Н |
. |
|
|
|
|
|
|
||||
2 |
|
. |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
ОН |
|
|
|
О |
|
|
|
|
|
|
|
|
2 |
|
|
Н О |
|
|
НО |
. |
|
|
|
2 |
2 |
||||
|
|
2 |
|
|
|||
Вопрос 53. Понятие о перекисном окислении липидов, повреждение мембран в результате перекисного окисления липидов.
Перекисное окисление липидов (ПОЛ) перекисное окисление липидов и представляет собой цепную реакцию, в которой образование одного свободного радикала стимулирует образование других свободных радикалов. В результате из полиеновых жирных кислот (L) образуются их гидроперекиси (L-OOH).
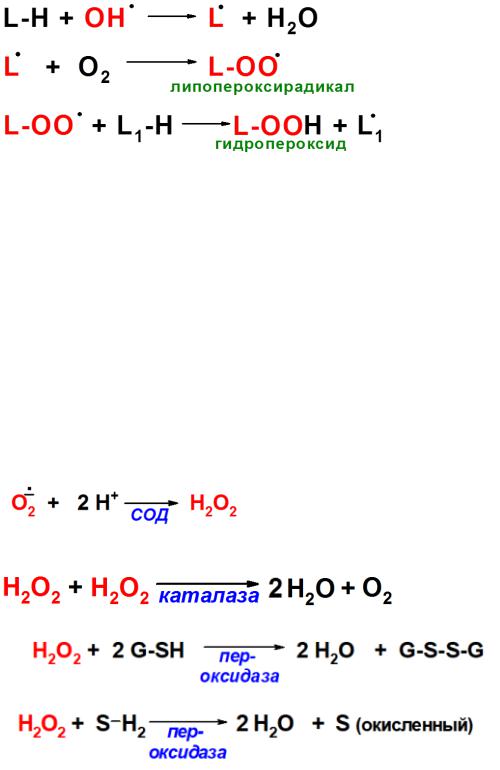
Так как липиды - компоненты мембран всех клеток организма, реакции перекисного окисления могут приводить к нарушению их структуры и повреждению клетки, что является одним из механизмов патогенеза ряда заболеваний.
Вопрос 54. Механизмы защиты от токсического действия кислорода. Антиоксидантная система.
Антиоксидантная система.
Ферментативное звено:
супероксиддисмутаза (СОД);
каталаза;
пероксидаза;
глутатионпероксидаза. Неферментативное звено:
витамины А, Е и С;
цинк, селен;
глутатион;
билирубин;
мочевая кислота;
убихинон.
Супероксиддисмутаза:
Каталаза:
Пероксидазы:
Вопрос 55. Основы химического канцерогенеза. Понятие о химических канцерогенах.
РАК – это неконтролируемая клеточная пролиферация, сопровождающаяся нарушением клеточной дифференцировки.
Химические канцерогены: полициклические ароматические углеводороды (бензопирен, бензантрацен), ароматические амины, которые используются при производстве анилиновых красителей, нитрозамины, нитриты, вторичные амины, афлотоксины как продукты плесеней. Неорганические вещества такие как хлор, свинец, кадмий, бериллий, асбест.
